食品乳狀液穩定性檢測方法研究進展
許朵霞,曹雁平,韓 富
(北京工商大學食品學院,北京工商大學食品添加劑與配料北京高校工程研究中心,北京工商大學北京市食品風味化學重點實驗室,北京100048)
食品乳狀液是在表面活性劑存在的條件下,一種液體以液滴的形式分散在另一與其互不相溶的液體中的液滴分散體系。乳狀液在食品領域中廣泛應用,如飲料、脂質替代品、蛋糕、冰激凌、巧克力等。食品乳狀液在熱力學上屬于不穩定體系,在宏觀上不穩定性現象有兩種,一種是乳狀液分散相顆粒的遷移(乳析和沉淀),另一種是分散相顆粒粒徑大小變化(團聚和絮凝)。隨著科學技術的不斷發展,實驗技術不斷完善,越來越多的精密儀器可用于食品乳狀液穩定性的檢測,但至今對乳狀液穩定性的檢測仍沒有普遍統一的方法。根據文獻報道和研究實踐,本文結合實例就常見的食品乳狀液穩定性測定方法進行綜述。
1 光學法
1.1 激光粒度儀法
激光粒度儀法是通過粒徑分析儀,對體系中肉眼不能分辨的粒子粒徑特性進行表征的一種方法。乳狀液液滴粒度分布是乳狀液的重要特性之一,粒度特征的參數主要包括粒徑大小及分布。乳狀液液滴大小及其分布對乳狀液的穩定性有很大的影響,根據stockes規律,顆粒越細小,沉淀速度越慢,乳狀液也就越穩定。液滴尺寸范圍越窄越穩定,單分散比多分散的乳狀液穩定[1]。
粒度特征既可以從微觀上確定乳狀液分散相的組成特點,又可以從宏觀上描述食品乳狀液絮凝和聚結等過程。同時,乳狀液的其他性質,如黏度、粘彈性等,也與其粒徑密切相關。乳狀液液滴粒徑分布測定可采用顯微統計法、激光散射法和超聲波法,其中應用最廣泛的是激光散射法(如Mastersizer2000,Zetasizer Nano ZS90)。
粒徑分布具有不同的表達方式,常見的有表面積加權平均值 D[3,2],體積加權平均值 D[4,3],其中D[4,3]對樣品中大顆粒的存在敏感,D[3,2]對樣品中小顆粒的存在敏感,D[4,3]對絮凝/聚結更敏感。因此,如果評價食品乳狀液的團聚現象,主要考察 D[4,3]變化值[2]。可通過粒徑大小的變化來分析乳狀液的穩定性。
豐雋莉等以Tween 80為表面活性劑,正丁醇為助表面活性劑制備VE微乳液,通過考察貯藏1個月過程中的粒徑變化,研究該微乳液的穩定性[3]。結果表明,在貯藏期內VE微乳液粒徑變化不大,分布在10nm以下,該納米級VE微乳液具有較好的穩定性。
1.2 Turbiscan法
Turbiscan是檢測乳狀液穩定性的一種新方法,儀器采用脈沖近紅外光源(λ=880nm)自下而上掃描樣品,兩個同步光學探測器分別搜集透射光和背散射光。在一定時間內連續掃描樣品,獲得透射光與背散射光信號對樣品高度的函數曲線圖,即可反映出樣品中顆粒運動趨勢,進而預測出乳狀液的穩定性。因此,Turbiscan可直觀獲得沉淀層、乳析層或澄清層隨時間的變化關系曲線。
大多數乳狀液屬于濃縮體系,而且不透明,分析時需要對其進行稀釋,而稀釋會破壞絮凝等結構,這將嚴重降低了評價的準確性。Turbiscan法的特點是:無需對乳狀液樣品進行稀釋,不接觸樣品直接進行掃描,分析乳狀液的穩定性。樣品的分析濃度最高可達95%,粒徑大小范圍50nm~1000μm。
通過Turbiscan圖譜分析不同乳化劑制備乳狀液的穩定性差異(圖 1)[4]。
采用Turbiscan Lab Expert濃縮體系穩定性分析儀,對β-胡蘿卜素納米乳狀液的穩定性進行分析。實驗中,將裝有20mL的β-胡蘿卜素納米乳狀液的儀器專用測試瓶放入檢測池中,每30min掃描一次,連續掃描4h。由于樣品濁度高,透射光量小,實驗選用背散射光值(Backscattering,BS)來分析乳狀液的穩定性。在樣品中部,BS值增大,表明乳狀液中顆粒有團聚現象發生;而樣品頂部BS值顯著增大,則表明大量分散相顆粒上浮,表現為乳析。
由圖1可知,以 TW、DML、OSS、WPI為乳化劑的四種乳狀液樣品的中部BS均有不同程度升高,表明乳狀液粒徑均有增大趨勢。DML乳狀液的BS值升高幅度最大,達到26%,表明該乳狀液聚結明顯,粒徑不斷增大,使得乳狀液發生分層現象(樣品頂部BS值顯著增大)。WPI乳狀液的BS值變化最小,表明該乳狀液穩定性較好。因此,可采用Turbiscan儀來篩選最佳乳化劑。
1.3 Lumisizer法
目前,精密穩定性分析儀主要有兩種,這兩種儀器均為非結構破壞性量測。其中一種為法國FORMULACTION公司生產的全能穩定性分析儀Turbiscan,另一種為德國LUM公司生產的LUMI穩定性分析儀。
Lumisizer穩定性分析儀,通過加速分層和量化沉淀、懸浮的方法(STEP-Technology)快速測定乳狀液的穩定性。儀器采用光學離心的分析方法,利用粒子遷移速率與光的穿透關系,記錄下隨時間改變的粒子行為。在時間和位置為參數,同步測量透射光強度。透射特征線的描繪過程反映分離過程的動力及穩定性。通過對現有的分析模式“透視度積分”(澄清的速度)和“相界面層跟蹤”進行考察,判斷乳狀液的失穩過程。在離心的過程中,平行的近紅外或藍色光照射在樣品試管上,通過記錄樣品不同位置的透射率分布的變化,確定乳狀液粒子的遷移過程[5]。

圖1 含有不同乳化劑的β-胡蘿卜素納米乳狀液(10%,w/w)Turbiscan掃描圖譜Fig.1 Turbiscan profiles of β-carotene nanoemulsions stabilized by four emulsifiers scanned every 30 minutes for 4 hours at 55℃,where Y axis represents delta backscattering intensity and X axis represents sample height.
應用Lumisizer考察大豆多糖穩定乳狀液(10%MCT,0.15% β-胡蘿卜素)的最佳濃度[6]。實驗過程中,取乳狀液約1.8mL,均勻注射至樣品試管底部,溫度設定為60℃,離心轉數為4000r/min,每30s記錄一次樣品的透射率特征曲線,共255次。
圖2表明,隨著大豆多糖濃度的增加,乳狀液的透光率變化程度逐漸減小。當大豆多糖濃度較低時,樣品頂部的透光率明顯變大,表明乳狀液在離心過程中不穩定,出現比較顯著的乳狀液乳析現象,此時大豆多糖濃度不足以覆蓋乳狀液液滴表面。當大豆多糖濃度高于4wt%時,乳狀液的透光率變化明顯減小,乳狀液能夠保持較好的物理穩定性。

圖2 不同大豆多糖濃度制備β-胡蘿卜素乳狀液的LUMiSizer分析圖Fig.2 LUMiSizer analysis of β-carotene emulsions prepared by different soybean polysaccharide concentrations
1.4 透射光濁度法
透射光濁度法主要是利用光透過乳狀液時,透光率變化確定乳狀液內部顆粒大小的變化。該方法結合濁度與比色測定,具有和顯微鏡觀察法同樣的特點。最常見的測定乳狀液穩定性的方法是:取一定量的乳狀液加入帶蓋的貯藏瓶中,在37℃條件下貯存,不同貯藏時間取出樣品,采用濁度儀測定透光率變化,分析樣品的穩定性。
Klein等人利用濁度儀,研究阿拉伯膠與乳清分離蛋白對乳狀液體系穩定性的影響。采用濁度法測定乳狀液的穩定性,而后將該乳狀液應用于飲料生產中[7]。
2 電荷分布法
乳狀液的電荷分布通常用zeta-電位(zetapotential)表征。目前測定zeta-電位的方法主要有電泳法、電滲法、流動電位法及超聲波法,其中以電泳法應用最廣。最常用且操作便利的儀器是馬爾文公司生產的Zetasizer Nano設備。Zetasizer儀基于動態光散射原理,帶電顆粒在外加電場作用下發生定向移動,當光束照到顆粒上時,會引起光束頻率或相位發生變化,且顆粒運動速度越快,光的頻率和相位變化得也快。因此可以通過測量光的頻率或相位變化來間接測出顆粒的電泳速度,從而求出zeta-電位[8]。
Zeta-電位不僅取決于液滴表面,也受分散相組成,如pH、介質離子強度的影響。Zeta-電位與體系穩定性之間的關系如表1所示。如果液滴有較大的負zeta-電位或正zeta-電位,它們將因為靜電排斥作用而穩定分散。一般而言,zeta-電位越高,乳狀液越穩定;∣zeta-電位∣≥30mV時,乳狀液較穩定。但乳狀液的穩定性不能完全靠zeta-電位值是否大于30mV來判斷,因為乳狀液的穩定性不僅取決于靜電排斥作用力,還取決于界面膜厚及空間位阻作用[9]。

表1 Zeta-電位大小與乳狀液穩定性之間的關系Table 1 The relationship between zeta-potential and emulsion stability
利用zeta-電位分布變化,考察殼聚糖分子對大豆多糖制備的β-胡蘿卜素雙層乳狀液的吸附作用,獲得殼聚糖穩定該乳狀液的最佳添加量(圖3)[6]。研究發現:在未添加殼聚糖時,大豆多糖穩定的β-胡蘿卜素乳狀液的zeta-電位約為-34mV,隨著殼聚糖濃度的增加,zeta-電位由負變正,當殼聚糖濃度為2wt%時,乳狀液電位為+58mV。通過zeta-電位分析表明,帶正電荷的殼聚糖分子能夠吸附到帶負電荷的液滴表面,乳狀液的穩定性得到提高。
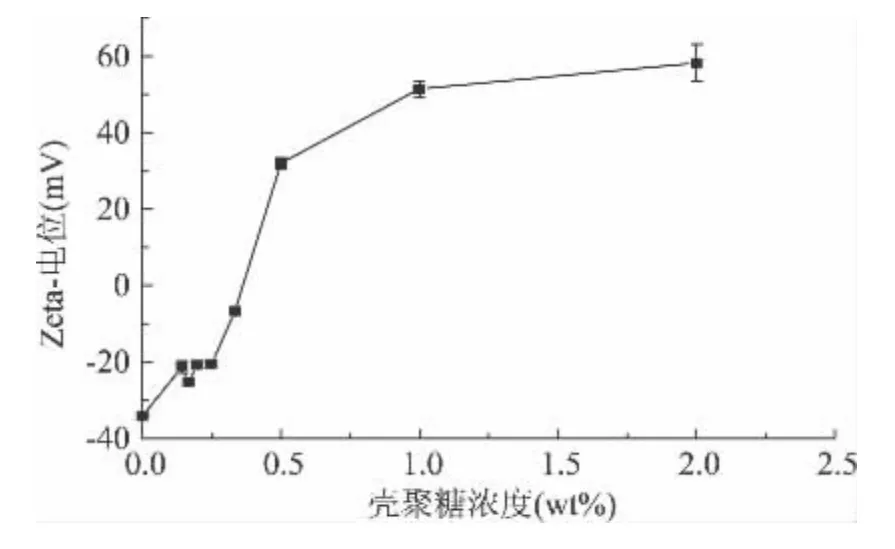
圖3 殼聚糖濃度對β-胡蘿卜素雙層乳狀液電位的影響Fig.3 Dependence of electrical charge(ζ-potential)on the chitosan concentration for SSPS stabilized β-carotene emulsions
3 流變法
乳狀液的穩定性與流變特性取決于乳狀液液滴間的相互作用,這種相互作用與油水界面結構與組成相關。在食品乳狀液體系中,界面吸附層相對較復雜。其中,最宏觀特征為乳狀液的流變學特性。食品乳狀液流體包括牛頓流體(如牛奶)和非牛頓流體(如蛋黃醬)兩種類型。
乳狀液遵守stockes沉淀作用規律,粘度高可減少乳狀液分離的趨勢。在乳狀液中添加增稠劑以增加粘度,常用低分子增調劑如甘油、山梨醇等,高分子增調劑如阿拉伯膠、海藻膠等[10-11],可提高乳狀液的穩定性。
添加不同濃度的阿拉伯膠至1%乳清蛋白制備的10%正己烷乳狀液中,考察不同阿拉伯膠濃度對乳狀液在不同剪切速率下黏度的影響。結合乳狀液的穩定性分析,得到阿拉伯膠的最佳添加濃度。結果表明,隨著阿拉伯膠濃度的增加,乳狀液的黏度增大,乳狀液流體特性符合power方程,表現為假塑性流體,n值由0.4(未添加阿拉伯膠的乳狀液)增加為0.55(添加15%阿拉伯膠的乳狀液)。因此,隨著阿拉伯膠含量的增加,乳狀液的流變學特性接近牛頓流體,穩定性得到提高[12]。
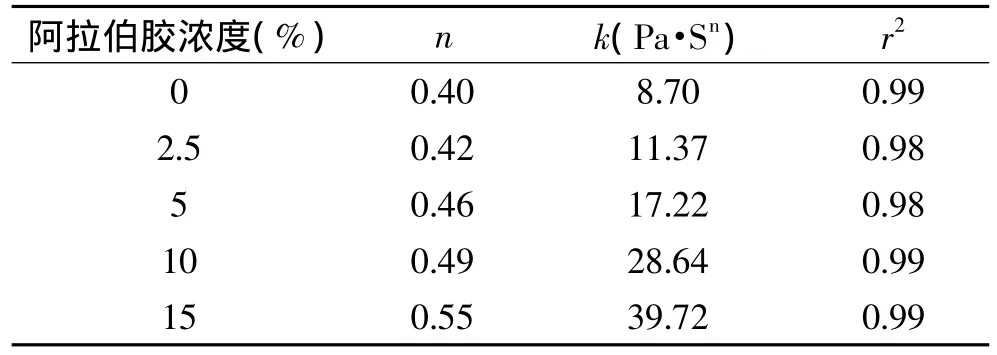
表2 不同阿拉伯膠濃度對WPI-乳狀液流變學參數的影響(n為流變行為指數,k為稠度系數)Table 2 Flow behaviour indices(n),consistency coefficients(k)and regression coefficients for emulsions having different gum arabic ratios
4 界面吸附法
乳化劑在油水界面上的動態特性對乳狀液的穩定性具有重要影響。在吸附作用下,乳化劑通過分子間非共價作用及共價鍵交聯,不僅可以降低界面張力,還可以在油滴周圍形成具有一定粘彈性的薄膜,該薄膜是影響乳狀液分散體系穩定性的重要因素。因此,乳狀液的穩定性也取決于界面上吸附的乳化劑流變學特性與界面吸附層厚度[13]。
通過界面層吸附含量表征乳清蛋白/殼聚糖混合比、pH對乳狀液穩定性的影響(圖4)。結果表明隨著乳清蛋白/殼聚糖混合比的增加,界面吸附量呈先增大后減小的趨勢。pH5.5與pH6.0相比,界面吸附量較多[14]。因此,二者混合比為 5∶1,pH5.5 時,乳狀液的穩定性較好
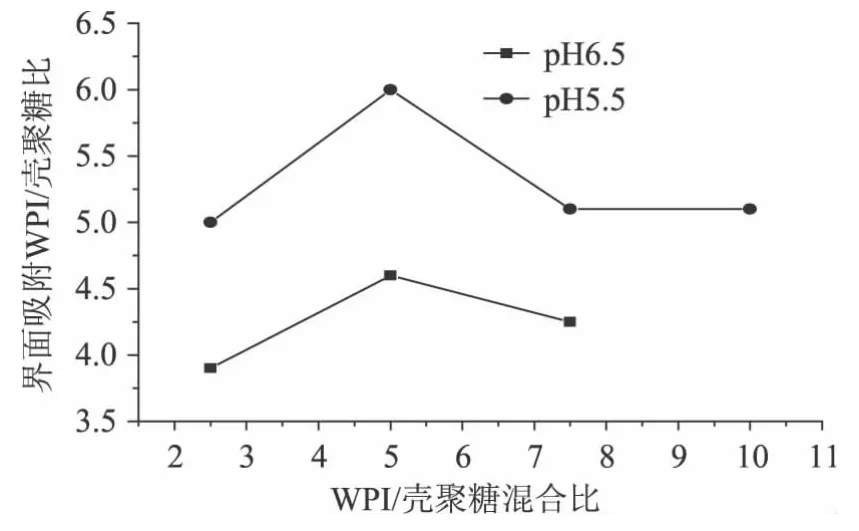
圖4 WPI/殼聚糖混合比及pH對乳狀液界面吸附量的影響Fig.4 Effect of WPI/CNI on interfacial protein-chitosan load ratio
5 微觀結構法
乳狀液的穩定性可通過微觀結構來考察,利用光學顯微鏡/原子力顯微鏡(AFM)/透射電鏡(TEM)-攝像-錄像-計算機圖像采集、處理集成系統,可實現對乳狀液界面結構、液滴大小及其分布、液滴運動和團聚的動態過程進行實時觀測、錄像、圖像采集和處理。微觀結構分析不破壞乳狀液體系的原有組成與分布,因此,在乳狀液穩定性研究領域具有廣闊的應用前景。
5.1 顯微鏡觀察法
顯微鏡觀察法是通過顯微鏡觀察微粒在整個乳狀液體系中的分散情況,從而預測體系的穩定性。該法只檢測相對較少的顆粒,采樣有可能不具有代表性,誤差較大;同時對觀察者的經驗要求較高,主觀性也比較強;因此該方法常只用于作為質量或生產控制的簡單判斷。
最簡單的可視顯微鏡觀察乳狀液的微觀結構變化,是通過取一滴乳狀液,將其置于載玻片上,調節顯微鏡焦距,放大一定倍數至形成清晰的畫面后,將顯微鏡信息轉至CCD軟件進行拍照。
采用共聚焦顯微鏡,可直觀觀測乳狀液的微觀結構,分析乳狀液的穩定性和界面組成。將1mL乳狀液樣品中加入40μL混合染料,混合均勻。選擇488nm的Ar離子和633nm的He/Ne離子激光預掃描,采集熒光圖像。常用的“油”溶性染料是“蘇丹Ⅲ”、油溶綠;常用的水溶性燃料是“亮藍FCF”、酸性紅 GG 等[15]。
利用共聚焦顯微鏡,觀察不同制備方法對多重乳狀液穩定性的影響。通過染色,可以觀察多重乳狀液內層與外層組成。由圖5可知,經過21d貯藏后,傳統兩步法制備的多重乳狀液,粒徑分布均勻,穩定性較好;而雙向進料法制備的多重乳狀液,液滴發生團聚現象[16]。

圖5 不同制備方法對PGPR-WPI(5wt%)多重乳狀液(W/O/W)貯藏21d后微觀結構的影響Fig.5 Photomicrographs of W/O/W double emulsion stabilized with 5wt.%WPI as an external emulsifier prepared by‘two-step’method
5.2 原子力顯微鏡(AFM)法
原子力顯微鏡(AFM)法是取少量樣品,加入超純水稀釋一定倍數,經過超聲波震蕩5min后,使樣品分散,然后直接將樣品滴到新鮮云母表面,自然風干。采用Agilent 5500原子力顯微鏡,輕敲(AAC)模式,Si3N4探針觀察乳狀液的微觀結構。為了客觀的分析樣品的形貌和尺寸,可選擇不同區域不同掃描范圍進行成像,結果以樣品表面形貌的平面圖和立體圖表征。
通過AFM觀察乳狀液的微觀結構,圖6是TW 20乳狀液和乳清分離蛋白(WPI)乳狀液的AFM圖。仔細觀察可以發現,乳狀液中大部分顆粒呈球形,粒徑主要集中在100~200nm間。另外,在TW 20乳狀液中,部分顆粒發生團聚,乳狀液不穩定。相比之下,WPI乳狀液的顆粒分布更為均勻[17],穩定性較好。
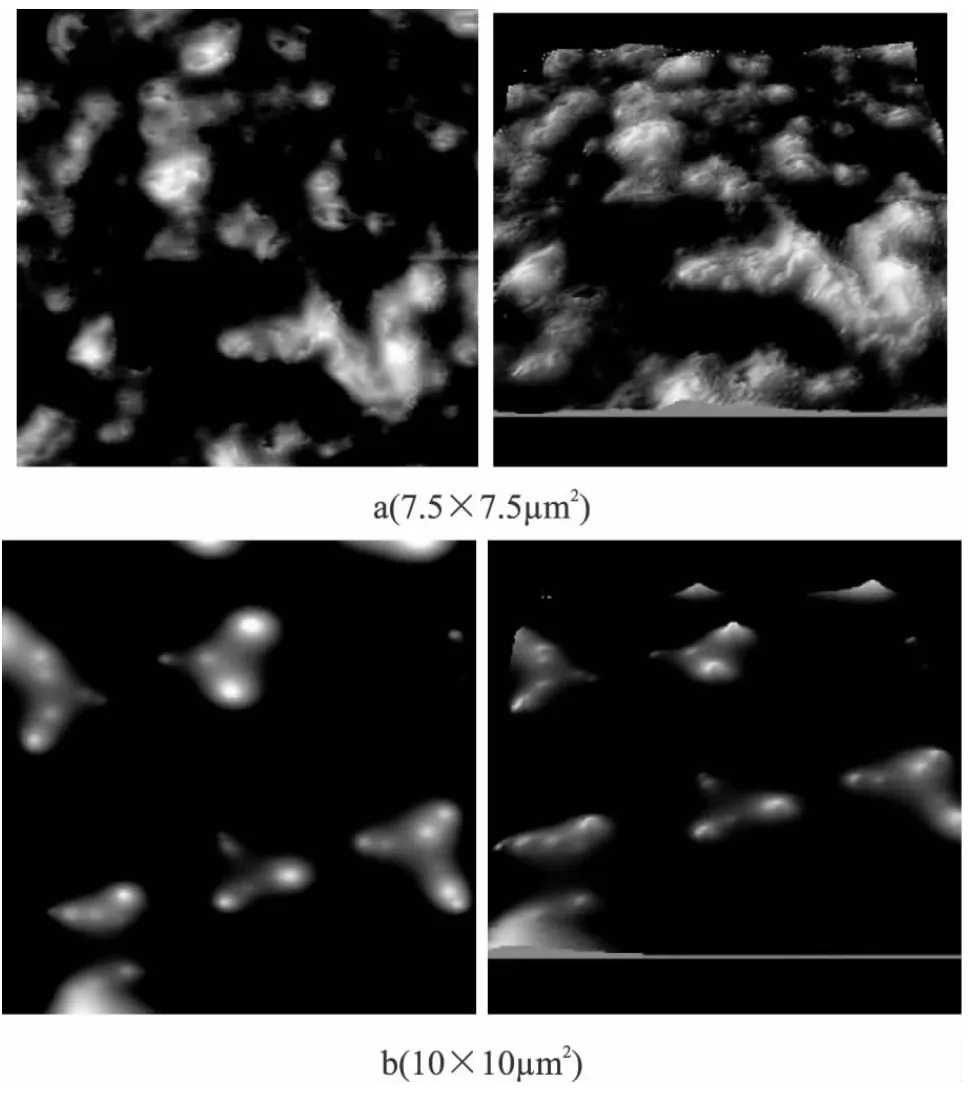
圖6 納米乳狀液AFM圖Fig.6 Representative AFM images of β-carotene nanoemulsions(prepared at 80MPa and 55℃):
5.3 透射電子顯微鏡(TEM)法
透射電子顯微鏡(簡稱透射電鏡,縮寫TEM),是將經加速和聚集的電子束投射到非常薄的樣品上,電子與樣品中的原子碰撞而改變方向,從而產生立體角散射。散射角的大小與樣品的密度、厚度相關,因此可以形成明暗不同的影像,影像將在放大、聚焦后在成像器件(如熒光屏、膠片以及感光耦合組件)上顯示出來。
通過TEM觀察TW 20和純膠納米乳狀液的微觀結構(圖7),顯示乳狀液顆粒以球形為主,部分呈棒狀,其中有的顆粒因為團聚呈現不規則形狀,尤其是TW 20乳狀液的團聚現象較為明顯[4]。

圖7 納米乳液TEM圖Fig.7 Representative TEM images of β-carotene nanoemulsions prepared at 10 MPa for three cycles.
6 高速離心分析法
高速離心分析法利用高速離心作用,加快體系中油滴的上浮和下降,達到快速分析乳狀液穩定性的目的[18]。該方法因需設備較為簡單,在食品企業中普遍使用。
實例:利用離心分析法研究大豆分離蛋白乳狀液穩定性[19]。具體方法為:在2mL離心管中準確加入2mL乳狀液,經高速離心10min,在距離心管底部1cm處取樣,測定吸光度值(A500nm)。乳狀液穩定性系數用如下公式計算。
乳狀液穩定性系數=At/A0
式中:A0為離心前乳狀液的吸光度;At為離心后乳狀液的吸光度。
7 直觀觀察法
直觀觀察法是將乳狀液灌裝于一定容器內,貯藏在一定溫度(通常為 4、25、37、55℃)下,在靜置過程中,用肉眼定期觀察體系的分層情況。該方法直觀、簡便,但耗時較長,不能滿足現代食品產品研發的需要。
直觀觀察法的具體操作為:將一定量的乳狀液放置于試管中,乳狀液的不穩定性表現為,上層為乳析層,下層為相對透明層。不穩定指數通過以下公式計算。
不穩定指數(%)=100×(樣品乳析層高度/樣品總高度)
8 結論
我國乳狀液技術在食品科學領域還處于基礎研究階段,但是它已滲透到食品工業的多個領域。因此,亟待加快發展食品乳狀液檢測技術。總之,僅使用以上一種方法,往往有一定的局限性(表3)。故應結合多種方法監測乳狀液的穩定性,互相印證,才能得到正確的、可靠的結果,以期加深乳化技術在我國食品領域的深入研究與利用。

表3 不同食品乳狀液穩定性檢測方法的優缺點Table 3 The advantanges and disadvantanges of different measurement methods of food emulsions stabilities
[1]McClements DJ.Emulsion design to improve the delivery of functional lipophilic components[J].In M.P.K.T.R.Doyle(Ed.),Annual Review of Food Science and Technology,2010,1(1):241-269.
[2]Lesmes U,McClements DJ.Structure-function relationships to guide rational design and fabrication of particulate food delivery systems[J].Trends in Food Science & Technology,2009,20(10):448-457.
[3]豐雋莉,王正武,俞惠新,等 .VE 的微乳化研究[J].食品與機械,2006,22(5):36-38.
[4]Mao L,Yang J,Xu D,et al.Effects of homogenization models and emulsifiers on the physicochemical properties of β-carotene nanoemulsions[J].Journal of Dispersion Science and Technology,2010,31:986-993.
[5]Sobisch T,Lerche D.Thickener performance traced by multisample analytical centrifugation[J].Colloids and Surface A:Physicochemical and Engineering Aspects,2008,331(1-2),114-118.
[6]Hou Z,Gao Y,Yuan F,et al.Investigation into the physicochemical stability and rheological properties of β-carotene emulsion stabilized bysoybean solublepolysaccharidesand chitosan[J].Journal of Agricultural and Food Chemistry,2010,58:8604-8611.
[7]Klein M,Aserin A,Svirov I,et al.Enhanced stabilization of cloudy emulsions with gum Arabic and whey protein isolate[J].Colloids and Surfaces B:Biointerfaces,2010,77:75-81.
[8]Dickinson E.Mixed biopolymers at interfaces:Competitive adsorption and multilayer structures[J].Food Hydrocolloids,2011,25(8):1966-1983.
[9]Dickinson E.Hydrocolloids as emulsifiers and emulsion stabilizers[J].Food Hydrocolloids,2009,23(6):1473-1482.
[10]Dickinson E.Hydrocolloids at interfaces and the influence on the properties of dispersed systems[J].Food Hydrocolloids,2003,17(1):25-39.
[11]Diftis NG,Pirzas TA,Kiosseoglou VD.Emulsifying properties of gelatin conjugated to pectin under alkaline conditions[J].Journal of the Science of Food and Agriculture.2005,85:804-808.
[12]Ibanoglu E.Rheological behaviour of whey protein stabilized emulsions in the presence of gum arabic[J].Journal of Food Engineering,2002,52:273-277.
[13]Gancz K,Alexander M,Corredig M.Interactions of high methoxyl pectin with whey proteins at oil/water interfaces at acid pH[J].Journal of Agricultural and Food Chemistry,2005,53(6):2236-2241.
[14]Laplante S,Turgeon SL,Paquin P.Emulsion-stabilizing properties of chitosan in the presence of whey protein isolate:Effect of the mixture ratio,ionic strength and pH[J].Carbohydrate Polymers,2006,65:479-487.
[15]McClements DJ,Li Y.Structured emulsion-based delivery systems:Controlling the digestion and release of lipophilic food components[J].Advances in Colloid and Interface Science,2010,159(2):213-228.
[16]Benichou A,Aserin A,Garti N.W/O/W double emulsions stabilized with WPI-polysaccharide complexes[J].Colloids and Surfaces A:Physicochem Eng Aspects,2007,294:20-32.
[17]Mao L,Xu D,Yang J,et al.Effects of small and large molecule emulsifiers on thecharacteristicsofβ-carotene nanoemulsions prepared by high pressure homogenization[J].Food Technology Biotechnology,2009,47(3):336-342.
[18]王春玲,孟祥晨.乳狀液成分對O/W乳狀液性質的影響[J].食品工業科技,2012,33(7)36-40.
[19]張芬芬,曾茂茂,何志勇,等.大豆分離蛋白乳狀液穩定性的幾種分析方法比較[J].食品科學,2012,33(17):44-47.

