骨質疏松腎陽虛病證結合模型構建的實驗研究*
陳劍磨 張勝軍 夏炳江
(浙江省紹興市中醫(yī)院,浙江 紹興 312000)
·研究報告·
骨質疏松腎陽虛病證結合模型構建的實驗研究*
陳劍磨 張勝軍 夏炳江△
(浙江省紹興市中醫(yī)院,浙江 紹興 312000)
目的研究建立骨質疏松腎陽虛病證結合模型的方法。方法雌性昆明小鼠隨機分為對照組(A組)、證型模型組(B組)、疾病模型組(C組)、疾病證型模型組(D組)。分別應用去雙側卵巢法構建骨質疏松模型,氫化可的松皮下注射誘導腎陽虛證模型。通過觀察小鼠癥狀體征、促腎上腺皮質激素、促甲狀腺激素、環(huán)磷酸腺苷、環(huán)磷酸鳥苷、骨密度、骨組織形態(tài)學等評價模型。結果與A組比較,D組小鼠出現(xiàn)毛發(fā)干枯,畏寒倦臥,肛溫降低等腎陽虛癥狀,促腎上腺皮質激素及促甲狀腺激素含量降低(P<0.01),環(huán)磷酸腺苷/環(huán)磷酸鳥苷降低(P<0.01),股骨近端、腰椎骨密度下降(P<0.01),HE染色及骨組織形態(tài)計量學分析顯示骨小梁排列稀疏、變細,破骨細胞數增多等。結論采取雙側卵巢切除結合氫化可的松皮下注射的方法,能成功構建骨質疏松腎陽虛病證結合模型。
骨質疏松 腎陽虛 病證結合 動物模型
研究人類或動物的疾病,應在獲得相應疾病動物模型基礎上,開展探索致病機制的基礎研究,根據獲得的相關信息確定最終診治方案[1]。建立合理、規(guī)范的疾病模型能有效地研究疾病的發(fā)生、發(fā)展,研究病因和尋求治療方案。病證結合動物模型融合中醫(yī)證候模型和現(xiàn)代醫(yī)學病理學模型的共同因素和特點,使動物模型同時具有疾病與證候特征[2],該類模型是闡明中醫(yī)學基礎理論和辨證論治較為理想的載體。根據病證結合的理念,本研究擬采用疾病模型復合證候模型的方法構建腎陽虛證骨質疏松癥模型,為進一步研究中醫(yī)藥防治骨質疏松奠定良好的實驗基礎。現(xiàn)報告如下。
1 材料與方法
1.1 儀器、藥物與試劑 全自動組織脫水機(日本櫻花),輪轉式切片機(德國Leica),顯微鏡及顯微拍攝系統(tǒng)(德國Leica),高速冷凍離心機(德國Eppendorf),全自動酶標儀(美國Thermo),多光譜小動物活體成像儀(美國Carestream Health),BI-2000醫(yī)學圖像分析系統(tǒng)(成都泰盟科技有限公司);氫化可的松注射液(天津金耀氨基酸有限公司,生產批號1112231);促腎上腺皮質激素(ACTH)、促甲狀腺激素(TSH)、環(huán)磷酸腺苷(cAMP)、環(huán)磷酸鳥苷(cGMP)ELISA試劑盒(南京建成生物工程研究所提供)。
1.2 動物 清潔級雌性昆明小鼠60只,體質量(20± 2)g,所有小鼠均由浙江中醫(yī)藥大學實驗動物中心提供(實驗動物號SYXK-浙-2008-0115),每籠5只,喂食普通顆粒飼料,室溫(20±2)℃,自然光照,保持良好通風,自由進水進食。
1.3 分組與造模 60只昆明小鼠隨機分為2大組,分別進行假手術和去雙側卵巢手術。假手術后存活小鼠隨機分為對照組(A組)和證型模型組(B組);去雙側卵巢手術后存活小鼠隨機分為疾病模型組(C組)和疾病證型模型組(D組),每組15只。A組:行假手術,以作對照。B組:假手術后間隔7周,皮下注射氫化可的松1周。C組:行雙側卵巢去除術。D組:去雙側卵巢術后間隔7周,皮下注射氫化可的松1周。骨質疏松癥模型采用去勢法制作:10%水合氯醛溶液(0.3 mL/100 g)腹腔注射,麻醉滿意后,小鼠俯臥位,在第3腰椎處備皮消毒,正中縱形切開皮膚約1 cm,鈍性分離一側肌肉,剪開腹膜,找到梅花狀的卵巢,0號無菌絲線結扎并用眼科剪剪斷輸卵管,分離切除卵巢,分層縫合肌肉筋膜,滴入少量青霉素水溶液后縫合皮膚,同法切除對側卵巢。A組手術同上,發(fā)現(xiàn)卵巢后僅切除與卵巢等量的脂肪后縫合皮膚。腎陽虛模型按25 mg/kg劑量,皮下注射氫化可的松來誘導,約1周[3]。腎陽虛型骨質疏松癥模型由上述2種造模方法復合而成,即在骨質疏松癥模型的基礎上復合腎陽虛模型,當骨質疏松造模至7周時,開始腎陽虛造模,至8周時骨質疏松癥及腎陽虛造模同時結束。實驗過程中各組小鼠均無死亡情況出現(xiàn)。
1.4 觀測指標 (1)動物癥狀、體征觀察。采用量化分級方法連續(xù)觀察造模后小鼠毛發(fā)光澤度、精神、活動狀態(tài)、飲食、睡眠、二便等情況。根據以下10個癥狀和體征:毛發(fā)干枯、畏寒喜暖、大便稀溏、小便清長、卷縮弓背、精神萎頓、怠倦嗜睡、自主活動次數減少、抓取時抵抗性減弱、食欲不振。對各組小鼠進行評分,依據嚴重程度不同,分別記為正常(0~1分),輕(2~4分),中(5~ 7分),重(8~10分)4個等級,評分有2個非實驗組的中醫(yī)專業(yè)人士完成[7]。(2)動物體質量及肛溫變化。采用電子天平稱量動物體質量,每3日1次,每次稱量時間為下午14:00~16:00。在每次稱量前,利用專用肛溫計測量小鼠肛溫并記錄。(3)血液學檢測。10%水合氯醛將小鼠麻醉后,采用摘除眼球的方法取血,提取血漿和血清后,-20℃冰箱內保存。按Elisa試劑盒說明的檢測方法,分別測定血漿環(huán)核苷酸cAMP、cGMP含量和血清ACTH、TSH的濃度。(4)骨密度測定。用10%水合氯醛將小鼠麻醉后,利用多光譜小動物活體成像儀對脊柱及股骨進行X線攝片,利用自帶軟件進行股骨近端及第2腰椎骨密度(bone density)測定。(5)骨組織形態(tài)學觀察。將小鼠股骨、腰椎用4%多聚甲醛液固定2 d,14%EDTA液脫鈣14 d,按常規(guī)脫水、透明、包埋、石蠟切片,厚約3~4 μm,常規(guī)HE染色,用顯微鏡在40、200倍鏡下觀察組織形態(tài)學變化情況,并利用BI-2000醫(yī)學圖像分析系統(tǒng)進行骨組織形態(tài)學計量分析,包括骨小梁平均寬度,骨小梁面積,成骨細胞數及破骨細胞數。
1.5 統(tǒng)計學處理 應用SPSS13.0統(tǒng)計軟件。組間比較采用單因素方差分析。P<0.05為差異有統(tǒng)計學意義。
2 結 果
2.1 癥狀、體征量化評分 見圖1。A組和B組評分高于C組和D組。而且與A組比較,D組小鼠出現(xiàn)毛發(fā)干枯,畏寒倦臥,肛溫降低等腎陽虛癥狀。
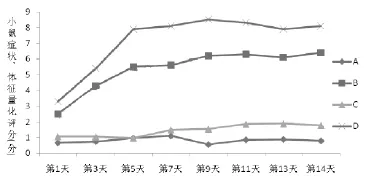
圖1 各組癥狀、體征量化評分趨勢圖
2.2 小鼠體質量及肛溫比較 見表1。與A組比較,B、D組體質量周平均增長量、平均肛溫均降低(均P<0.01)。與B組比較,D組體質量周平均增長量、平均肛溫均降低(P<0.01或P<0.05)。與C組比較,D組體質量周平均增長量、平均肛溫均低于降低(P<0.01)。
表1 各組實驗體質量及肛溫比較(±s)

表1 各組實驗體質量及肛溫比較(±s)
與A組比較,*P<0.01;與B組比較,△P<0.05,△△P<0.01;與C組比較,#P<0.01。下同。
組別 n 造模后第1日(g)造模后2周(g)周平均增長量(g / w)平均肛溫(℃)A組 1 5 B組 1 5 C組 1 5 4 4 . 2 8 ± 3 . 7 1 4 7 . 4 9 ± 3 . 4 5 1 . 6 0 ± 0 . 8 8 3 7 . 0 8 ± 0 . 2 4 4 4 . 4 3 ± 3 . 3 8 4 3 . 4 0 ± 3 . 3 9 -0 . 5 1 ± 0 . 6 3* 3 6 . 4 4 ± 0 . 3 3*4 5 . 0 8 ± 1 . 7 2 4 8 . 3 4 ± 2 . 1 3 1 . 6 3 ± 0 . 2 6 3 6 . 9 6 ± 0 . 2 6 D組 1 5 4 6 . 2 2 ± 2 . 2 2 4 2 . 5 4 ± 3 . 0 6 -1 . 8 4 ± 0 . 6 3*△△# 3 6 . 0 4 ± 0 . 1 7*△#
2.3 小鼠血清ACTH、TSH及血漿cAMP、cGMP含量比較 見表2,表3。與A組比較,B、D組促腎上腺皮質激素及促甲狀腺激素含量、cAMP、cAMP/cGMP降低(均P<0.01)。與B組比較,C組促腎上腺皮質激素及促甲狀腺激素含量降低 (均P<0.01),cAMP、cAMP/ cGMP升高 (均P<0.01);D組TSH含量、cAMP降低(均P<0.01),cAMP/cGMP升高(均P<0.01)。與C組比較,D組促腎上腺皮質激素及促甲狀腺激素含量、cAMP、cAMP/cGMP均降低(均P<0.01)。
2.4 小鼠股骨、腰椎骨密度變化比較 見表4。與A組比較,C、D組股骨近端、腰椎骨密度均下降(均P<0.01),B組腰椎骨密度下降(P<0.01)。與B組比較,C、D組股骨近端、腰椎骨密度均下降 (P<0.01或P<0.05)。與C組比較,D組股骨近端、腰椎骨密度均下降(均P<0.05)。
表2 各組血清ACTH及TSH含量比較(±s)
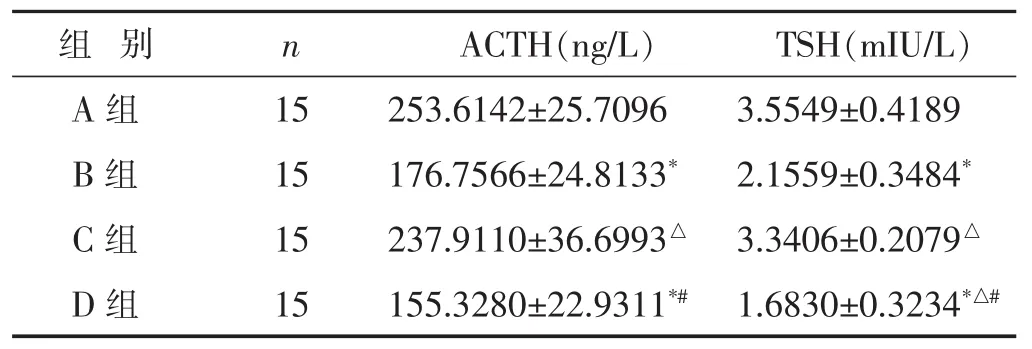
表2 各組血清ACTH及TSH含量比較(±s)
組 別 n A C T H(n g / L) T S H(m I U / L)A組 1 5 2 5 3 . 6 1 4 2 ± 2 5 . 7 0 9 6 3 . 5 5 4 9 ± 0 . 4 1 8 9 B組 1 5 1 7 6 . 7 5 6 6 ± 2 4 . 8 1 3 3* 2 . 1 5 5 9 ± 0 . 3 4 8 4*C組 1 5 2 3 7 . 9 1 1 0 ± 3 6 . 6 9 9 3△ 3 . 3 4 0 6 ± 0 . 2 0 7 9△D組 1 5 1 5 5 . 3 2 8 0 ± 2 2 . 9 3 1 1*# 1 . 6 8 3 0 ± 0 . 3 2 3 4*△#
表3 各組血清ACTH及TSH含量比較(±s)
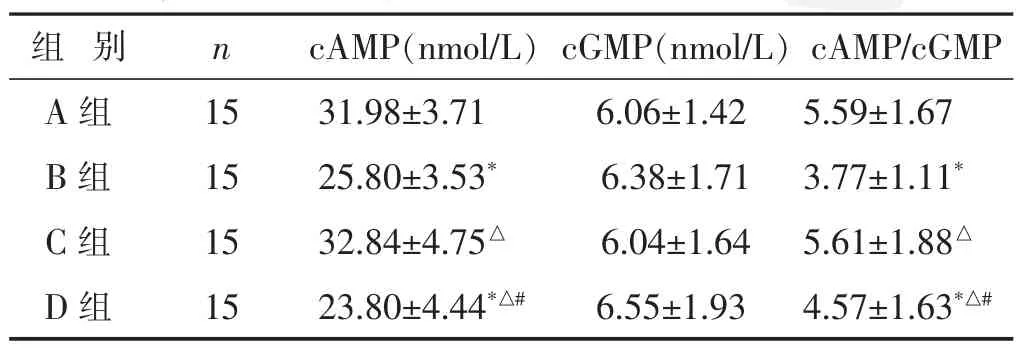
表3 各組血清ACTH及TSH含量比較(±s)
組別 n c A M P / c G M P c A M P(n m o l / L)c G M P(n m o l / L)A組 1 5 5 . 5 9 ± 1 . 6 7 B組 1 5 3 . 7 7 ± 1 . 1 1*C組 1 5 5 . 6 1 ± 1 . 8 8△3 1 . 9 8 ± 3 . 7 1 6 . 0 6 ± 1 . 4 2 2 5 . 8 0 ± 3 . 5 3* 6 . 3 8 ± 1 . 7 1 3 2 . 8 4 ± 4 . 7 5△ 6 . 0 4 ± 1 . 6 4 D組 1 5 4 . 5 7 ± 1 . 6 3*△#2 3 . 8 0 ± 4 . 4 4*△# 6 . 5 5 ± 1 . 9 3
表4 各組股骨及腰椎骨密度比較(g/cm3,±s)
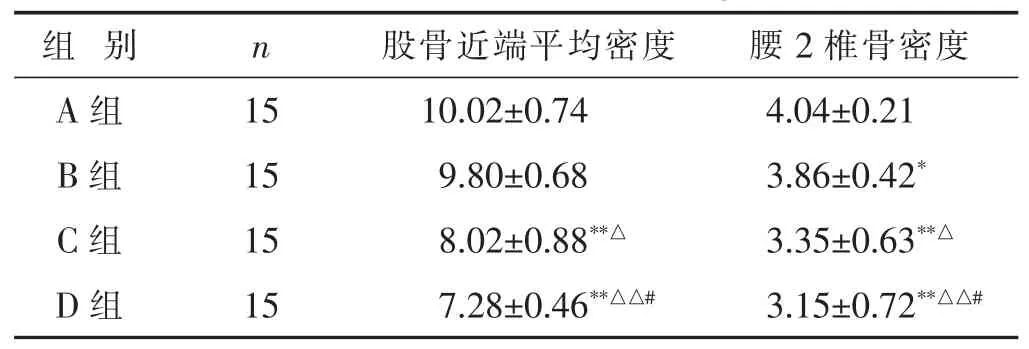
表4 各組股骨及腰椎骨密度比較(g/cm3,±s)
與A組比較,**P<0.01,*P<0.05;與B組比較,△△P<0.01,△P<0.05;與C組比較,#P<0.05。下同。
組 別 n 股骨近端平均密度 腰2椎骨密度A組 1 5 1 0 . 0 2 ± 0 . 7 4 4 . 0 4 ± 0 . 2 1 B組 1 5 9 . 8 0 ± 0 . 6 8 3 . 8 6 ± 0 . 4 2*C組 1 5 8 . 0 2 ± 0 . 8 8**△ 3 . 3 5 ± 0 . 6 3**△D組 1 5 7 . 2 8 ± 0 . 4 6**△△# 3 . 1 5 ± 0 . 7 2**△△#
2.5 骨組織形態(tài)學改變比較 見表5。與A組比較,C、D組HE染色及骨組織形態(tài)計量學分析顯示骨小梁排列稀疏、變細,成骨細胞、破骨細胞數增多等(P<0.01或P<0.05),B組骨小梁面積變小,成骨細胞數增多(P<0.05)。與B組比較,C、D組HE染色及骨組織形態(tài)計量學分析顯示骨小梁排列稀疏、變細,破骨細胞數增多等(P<0.01或P<0.05)。與C組比較,D組HE染色及骨組織形態(tài)計量學分析顯示骨小梁排列稀疏、變細,破骨細胞數增多等(P<0.05)。
表5 各組小鼠股骨骨組織形態(tài)計量學指標比較(±s)
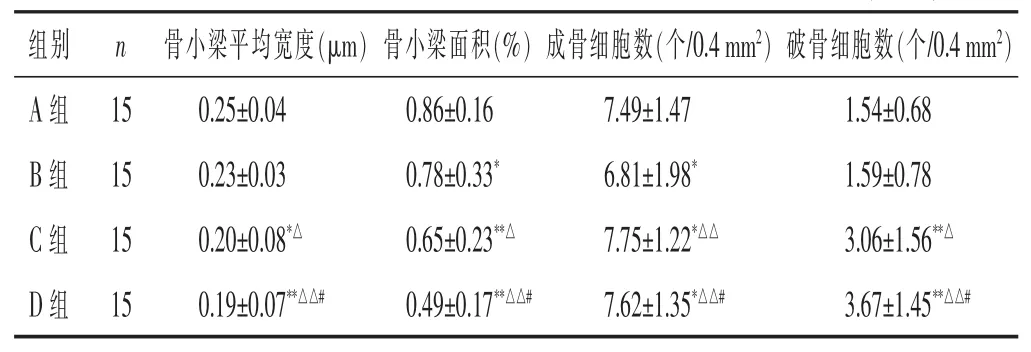
表5 各組小鼠股骨骨組織形態(tài)計量學指標比較(±s)
組別 n 骨小梁平均寬度(μ m)骨小梁面積(%)成骨細胞數(個/ 0 . 4 m m2)破骨細胞數(個/ 0 . 4 m m2)A組 1 5 B組 1 5 C組 1 5 0 . 2 5 ± 0 . 0 4 0 . 8 6 ± 0 . 1 6 7 . 4 9 ± 1 . 4 7 1 . 5 4 ± 0 . 6 8 0 . 2 3 ± 0 . 0 3 0 . 7 8 ± 0 . 3 3* 6 . 8 1 ± 1 . 9 8* 1 . 5 9 ± 0 . 7 8 0 . 2 0 ± 0 . 0 8*△ 0 . 6 5 ± 0 . 2 3**△ 7 . 7 5 ± 1 . 2 2*△△ 3 . 0 6 ± 1 . 5 6**△D組 1 5 0 . 1 9 ± 0 . 0 7**△△# 0 . 4 9 ± 0 . 1 7**△△# 7 . 6 2 ± 1 . 3 5*△△# 3 . 6 7 ± 1 . 4 5**△△#
3 討 論
病證結合動物模型是在中醫(yī)學理論指導下,適當結合現(xiàn)代醫(yī)學理論與實驗動物科學知識,分別或同時采用傳統(tǒng)中醫(yī)學病因復制證候動物模型和采用現(xiàn)代醫(yī)學病因復制疾病動物模型,使動物模型同時具有疾病與證候特征[2]。該模型以疾病模型為基礎,具有較好的可靠性及穩(wěn)定性[4]。目前病證結合模型常用的構建模式是現(xiàn)代醫(yī)學“疾病”模型復合中醫(yī)“證候”模型[5-6]。該類模式既注重中醫(yī)的思路,又注重現(xiàn)代醫(yī)學對疾病的認識,具有較強的可操作性。故本實驗將骨質疏松癥模型與腎陽虛模型復合以復制更符合中醫(yī)臨床要求的動物模型。
體內雌激素水平的降低是絕經后骨質疏松癥的發(fā)生及發(fā)展的主要原因,骨代謝發(fā)生改變,骨組織形態(tài)學及超微結構遭到破壞,最終導致骨生物力學性能下降及骨折發(fā)生[7-8]。Saville于1969年首先采用雌鼠雙側卵巢切除誘導骨質疏松模型來模擬該類骨質疏松癥,目前該模型已成為標準化的公認的絕經后骨質疏松癥經典病理模型。本研究結果示,骨質疏松組及骨質疏松腎陽虛組模型均出現(xiàn)典型的骨質疏松病理學征象:骨小梁排列稀疏,變細,數目減少,間距加寬,可見微骨折等;骨組織形態(tài)計量學能進行骨組織和細胞結構的定量分析,為骨結構、骨形成及骨吸收提供客觀數據[9]。本結果示,模型小鼠骨小梁平均寬度、骨小梁面積百分率有明顯下降,說明骨量和骨的內部結構均都有一定程度的破壞。成骨細胞是骨形成的主要細胞,負責骨基質合成、分泌和礦化,而破骨細胞貼附在舊骨區(qū)域,分泌酸性物質溶解骨礦質,分泌蛋白酶消化骨基質,促進骨吸收。本結果示,成骨細胞與破骨細胞均增多,表明骨組織處于高代謝狀態(tài),即該類骨質疏松為高轉換型。骨密度檢測能為骨質疏松診斷提供重要的輔助信息,在本研究結果示,去骨質疏松組及骨質疏松腎陽虛組骨密度明顯降低。上述數據表明我們利用昆明小鼠去勢建立骨質疏松癥模型取得成功。
腎陽虛證動物模型是最早建立的中醫(yī)證候動物模型,自20世紀60年代初,鄺安堃教授等首次建立了“氫化考的松腎陽虛”動物模型以來,此后各種“腎陽虛”動物模型相繼建立,包括“恐傷腎”性、甲狀腺素性、腺嘌呤性、羥基脲性腎陽虛動物模型等[10],并被用于多種補腎助陽方藥藥效的研究[11]。利用大劑量腎上腺皮質激素誘導的腎陽虛證動物模型目前最常用,該類動物表現(xiàn)出系列類似腎陽虛癥狀,如拱背蜷曲、畏寒喜暖、肛溫降低、反應遲鈍、呼吸深遲、毛發(fā)干枯、消瘦、尿液清長等。下丘腦-垂體-靶腺軸的功能改變是腎陽虛的主要病理變化之一[12-14]。有學者利用分子生物學技術RT-PCR化學發(fā)光定量法研究腎陽虛大鼠表明其HPA軸受抑,且下丘腦室旁核CRH mRNA的表達量明顯比正常對照組減少[15]。垂體在神經內分泌網絡系統(tǒng)中具有重要的作用,腎陽虛大鼠垂體ACTH細胞內質網擴張,線粒體空化,ACTH合成分泌受抑[16],ACTH mRNA表達下調[17]。甲狀腺功能生理范圍內或病理性降低是腎陽虛的主要病理之一。有研究報道,以醋酸考的松制作的腎陽虛模型,其血中T3、T4濃度和TSH濃度明顯降低[18],且甲狀腺濾泡上皮細胞出現(xiàn)內質網、高爾基體擴張、線粒體空化等[19]。本研究結果示,證候模型組與骨質疏松腎陽虛組小鼠血清ACTH、TSH含量均降低,與先前激素性腎陽虛動物模型研究結果類似。同時也證實骨質疏松腎陽虛組小鼠血清ACTH、TSH含量比單純腎陽虛模型小鼠降得更低,由此我們推測下丘腦-垂體-靶腺軸可能是“骨病及腎”與“腎病及骨”的中間調控通路,通過反饋機制,以使“腎”與“骨”達到相對平衡狀態(tài)。環(huán)磷酸腺苷(cAMP)、環(huán)磷酸鳥苷(cGMP)是細胞功能的重要調節(jié)物質,cAMP、cGMP的平衡失調,會引起細胞功能發(fā)生明顯變化。先前研究表明,cAMP降低、cGMP升高及cAMP/cGMP降低為陽虛,是目前反映陰陽虛較特異的指標之一[10]。本研究結果示,腎陽虛組及骨質疏松腎陽虛組小鼠血漿cAMP及cAMP/cGMP比對照組明顯降低,與cAMP降低為陽的陰陽學說相一致。由上述的癥狀體征結合實驗室指標表明復制腎陽虛小鼠模型成功。
綜上,通過將去勢小鼠骨質疏松模型與氫化可的松小鼠腎陽虛模型有機地結合起來,筆者成功研制了腎陽虛證骨質疏松模型。造模后動物出現(xiàn)了腎陽虛證的特征如畏寒倦臥、精神萎靡、反應遲鈍、體質量下降、HPA軸功能紊亂,同時出現(xiàn)了骨質疏松組織病理學改變如骨小梁排列稀疏,變細,微骨折等,成功的建立了骨質疏松腎陽虛模型。
[1] 李欣志,劉建勛,任建勛,等.痰瘀互結證冠心病小型豬模型的建立[J].中國中西醫(yī)結合雜志,2009,29(3):228-232.
[2] 康潔,高碧珍.病證結合動物模型研究概況[J].中華中醫(yī)藥學刊,2009,27(11):2357-2360.
[3] 王燕燕,張錦文,郭潔茹,等.虎尾輪根提取物對腎陽虛模型小鼠的影響[J].醫(yī)藥導報,2011,30(3):292-294.
[4] 趙慧輝,王偉.病證結合證候模型研究基本思路[J].中華中醫(yī)藥雜志,2006,21(12):762-764.
[5] 江建春,黃敏,卞琴,等.大鼠氣虛型頸椎病模型的建立[J].上海中醫(yī)藥大學學報,2009,23(3):33-37.
[6] 韓清民,王躍輝,程慧,等.腎虛型骨性關節(jié)炎造模方法研究[J].新中醫(yī),2008,40(3):90-92.
[7] 章曉霜,高順生,屈菊蘭,等.不同強度運動與雌激素聯(lián)合作用對去卵巢大鼠腰椎超微結構影響的掃描電鏡觀察[J].中國運動醫(yī)學雜志,2003,22(2):156-158.
[8] Pederson L,Kremer M.Evidence of a correlation of estrogen receptor level and avian osteoclast estrogen responsiveness[J]. J Bone Miner Res,1997,12(5):742-752.
[9] 榮杰生,陶天遵,陶樹清.N-脫硫酸肝素對ICR雌性小鼠骨形態(tài)計量學的影響[J].中國骨質疏松雜志,2006,12(6):620-622.
[10]楊裕華,李震.腎陽虛動物模型及其診斷指標研究近況[J].遼寧中醫(yī)藥大學學報,2007,9(5):40-42.
[11]楊裕華,李震.補腎中藥對腎陽虛動物模型影響的實驗研究進展[J].時珍國醫(yī)國藥,2008,19(1):231-233.
[12]杜江,李楠,王和鳴.腎虛模型造模方法及相關指標[J].中國組織工程研究與臨床康復,2010,14(50):9433-9436.
[13]陳燕清,張俊龍,郭蕾,等.腎氣丸對腎陽虛證大鼠模型T細胞亞群影響的實驗研究[J].中國中醫(yī)急癥,2014,23(3):380-384.
[14]岳仁宋,吳施國,譚毅明,等.參附注射液對甲狀腺機能減退癥腎陽虛型小鼠血清甲狀腺激素的影響[J].中國中醫(yī)急癥,2005,14(11):1094-1095.
[15]鐘歷勇,沈自尹,鄭仲承,等.下丘腦-垂體-腎上腺軸大鼠下丘腦CRH mRNA表達[J].上海鐵道大學學報,1998,19:8.
[16]宋春風,尹桂山,候潔,等.補腎中藥對腎陽虛大鼠垂體-腎上腺超微結構的影響[J].中醫(yī)藥研究,2001,17(2):41.
[17]鄭小偉,包素珍,劉明哲,等.金匱腎氣丸對腎陽虛大鼠垂體ACTH基因表達的影響[J].中國中西醫(yī)結合雜志,2004,24(3):238.
[18]王建紅,伍慶華,劉海云,等.腎陽虛大鼠垂體-甲狀腺軸功能動態(tài)分析[J].遼寧中醫(yī)雜志,2006,33(6):751.
[19]宋春風,尹桂山,李恩,等.補腎中藥對腎陽虛大鼠垂體-甲狀腺超微結構的影響[J].中國中醫(yī)基礎醫(yī)學雜志,1999,5(9):22.
Study on Osteoporosis Mice Model with Syndrome of Deficiency of Kidney-Yang
CHEN Jianmo,ZHANG Shengjun,XIA Bingjiang. Shaoxing Hospital of TCM,Zhejiang Province,Zhengjiang,Shaoxing 312000,China
Objective:To establish the osteoporosis model with syndrome of deficiency of Kidney-Yang.Methods:Female Kunming mice were randomly divided into control group(group A),syndrome group(group B),disease group(group C),disease with syndrome group(group D).The model was established by injecting hydrocortisone and resecting bilateral ovaries.Signs and symptoms,level of adrenocorticotropic hormone(ACTH),thyroid stimulating hormone(TSH),cyclic adenosine monophosphate(cAMP),cyclic guanosine phosphate(cGMP),bone density bone,and tissue morphology were observed to evaluate the model.Results:Compared with group A,mice in model group appeared obvious kidney-Yang deficiency symptoms,including hair dry,chill and frail state,low anal temperature.The levels of ACTH and TSH decreased(P<0.01),and the ratio of cAMP/cGMP decreased(P<0.01).Bone density of lumbar vertebra and femur decreased significantly(P<0.01).HE staining revealed osteoporosis of mice in group D.Conclusion:The model of osteoporosis with type of deficiency of Kidney-Yang can be established successfully by injecting hydrocortisone and resecting bilateral ovaries.
Osteoporosis;Deficiency of Kidney-Yang;Integration of disease and syndrome;Animal model
R285.5
A
1004-745X(2015)02-0201-04
10.3969/j.issn.1004-745X.2015.02.005
2014-11-27)
浙江省中醫(yī)藥科技計劃項目(2011ZB153)
△通信作者(電子郵箱:xiabj2006@sina.com)

