SiO2-CaO-Al2O3-MgO-FeO熔渣的電解還原行為
高運明, 阮 棟, 楊映斌, 段 超
(武漢科技大學 鋼鐵冶金及資源利用省部共建教育部重點實驗室,武漢 430081)
鋼鐵冶金行業是主要溫室氣體CO2排放的重要來源之一[1,2].使用惰性電極直接電解含有鐵氧化物的熔渣制取金屬鐵是一個可供選擇的減少甚至消除CO2排放的綠色短流程新工藝[3~5].但存在難以找到合適的高溫惰性陽極以及電解效率低、副反應不易控制等問題[4~6].“可控氧流還原[7]”采用只對氧離子有很強選擇透過性的氧化鋯基固體電解質膜作為控制氧定向流動的介質,能實現電解時熔渣內的陽極和陰極物理及電子隔離,既防止陽極反應參與物對陰極的不利影響,又能阻塞電子和其他非氧離子通過,消除漏電電流或熔渣中其他非氧離子的干擾,提高電解時的電流效率;氧化鋯基固體電解質良好的抗渣性也為制備出抗氧化且耐渣侵蝕的固體電解質基惰性陽極提供了更大可能.一些研究者已利用類似原理方法從溶解有所要提取金屬的氧化物電解質熔體(熔渣、熔鹽)中提取了Fe、Mg、Ti、Ta等金屬[8~13],也有一些研究者以熔鹽作為介質電解所要提取金屬的固態氧化物陰極直接制備金屬[14~16].最近Sadoway等[3,4]的研究表明SiO2-CaO-MgO-Al2O3渣系有可能是電解提鐵的潛在介質.本文采用MgO或Y2O3穩定的氧化鋯管作為氧離子膜[17],構建可控氧流電解池,外加電壓研究SiO2-CaO-Al2O3-MgO-FeO熔渣的電解還原行為,以期為綠色電解提鐵新工藝的基礎研究提供一些參考.目前,直接電解時實用化的高溫惰性陽極材料的選擇仍較為困難,為簡單起見,本文電解采用裝在氧化鋯管內的碳飽和鐵熔體做陽極.
1 實 驗
1.1 渣料制備
實驗渣料由在箱式電阻爐內 1 223 K 下保溫6 h烘干的CaCO3、SiO2、Al2O3、MgO試劑(均為分析純)制備,FeO以FeC2O4·2H2O(分析純)粉末形式配入[18].設定渣的組成(質量分數)為42.3% SiO2-25.2% CaO-8.1% Al2O3-14.4% MgO-10% FeO[19],熔渣二元堿度R(定義為渣中CaO與SiO2質量分數之比)為0.6,混勻后分別裝入已連接鐵棒的大或小鐵坩堝,將鐵坩堝置于立式硅鉬棒管式電阻爐恒溫區的剛玉坩堝(高100 mm)內.爐內通入經過銅絲和鎂屑二級凈化后的干燥Ar氣保護.高溫爐升溫至1 673 K,保溫1 h,使渣料熔化均勻后,取出鐵坩堝在水中急冷,獲得裝在鐵坩堝內的預熔渣料,備用.
1.2 實驗方法
電化學實驗裝置示意如圖1所示.將裝有預熔渣的鐵坩堝(加裝中心開孔的致密氧化鋁蓋)置于爐內恒溫區,并直接以鐵坩堝做陰極,與鐵坩堝連接的鐵棒作為陰極引線,鐵棒外套剛玉絕緣保護通管;采用一端封閉的ZrO2(Y2O3)管[20]或ZrO2(MgO)管(外購)內裝適量碳飽和鐵作陽極,在碳飽和鐵液中插入高純石墨棒(直徑4 mm,長度460 mm)并連接銅絲作陽極引線.為方便操作,將ZrO2管與剛玉通管通過高溫水泥黏結.高溫爐內通凈化Ar氣保護,Ar氣流量為400 mL/min.升溫至實驗溫度1 723 K后,保溫30 min,使鐵坩堝中的熔渣再次充分熔清.將CHI1140A型電化學分析儀的輔助電極和參比電極同時與陰極引線(鐵棒)相連接,工作電極與陽極引線(與石墨棒相連的銅絲)相連接.啟動電化學分析儀,將內裝有碳飽和鐵液的ZrO2管通過鐵坩堝上氧化鋁蓋中心孔緩慢插入熔渣中,構建可控氧流電池:
鐵棒|Fe+FeO(slag)|ZrO2(MgO或Y2O3)
|[O](Fe+C飽和)|石墨棒
同時自動記錄電池的開路電壓-時間曲線.待開路電壓穩定后,進行線性掃描實驗測定.實驗參數設定:掃描初始電壓為實驗過程中測得的開路電壓,終止電壓為4 V,掃描速率為10 mV/s,記錄實驗過程中的電流隨掃描電壓變化關系.最后外加恒電壓電解,記錄電解電流I-時間t曲線.各實驗條件如表1所示.
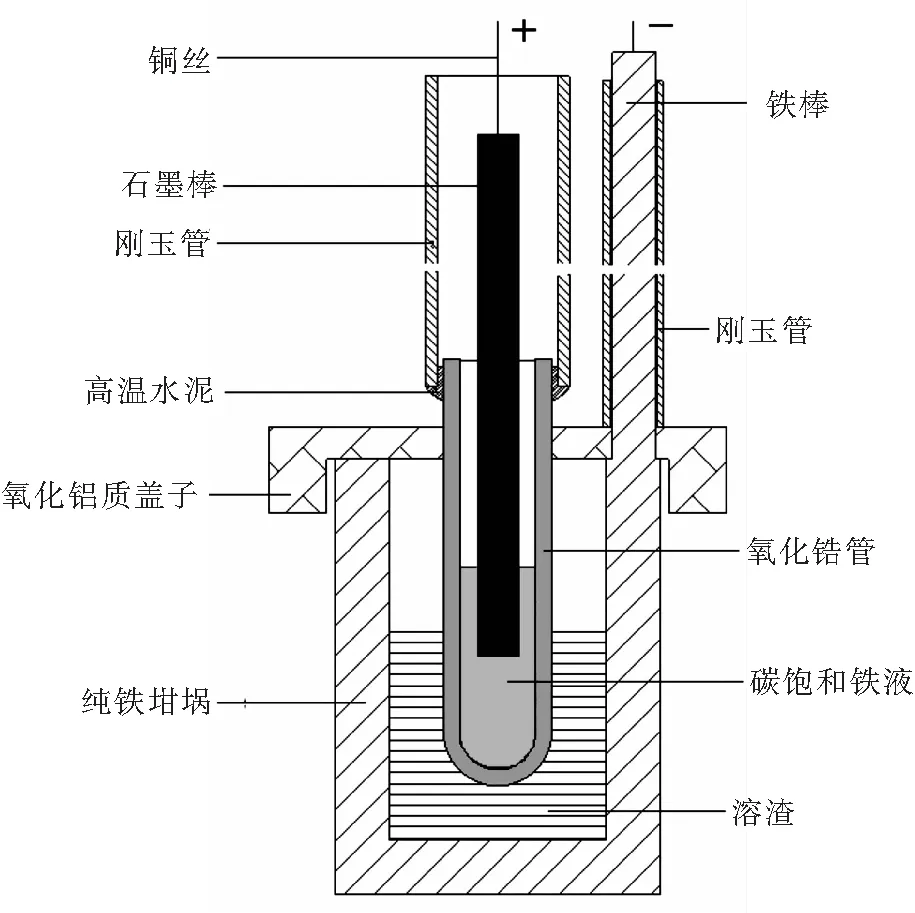
圖1 電解實驗裝置示意圖Fig.1 Schema of the electrolytic cell
實驗完畢后,冷卻到室溫,觀察到各實驗中氧化鋯管外形均完好,解剖電池,通過比較殘渣顏色大體判斷渣中FeO的還原效果.制樣拋光,通過掃描電鏡(Nova 400 Nano SEM)結合能譜儀(INCAIE 350 Penta FET X-3 EDS)分析殘樣的組織形貌及有關成分.
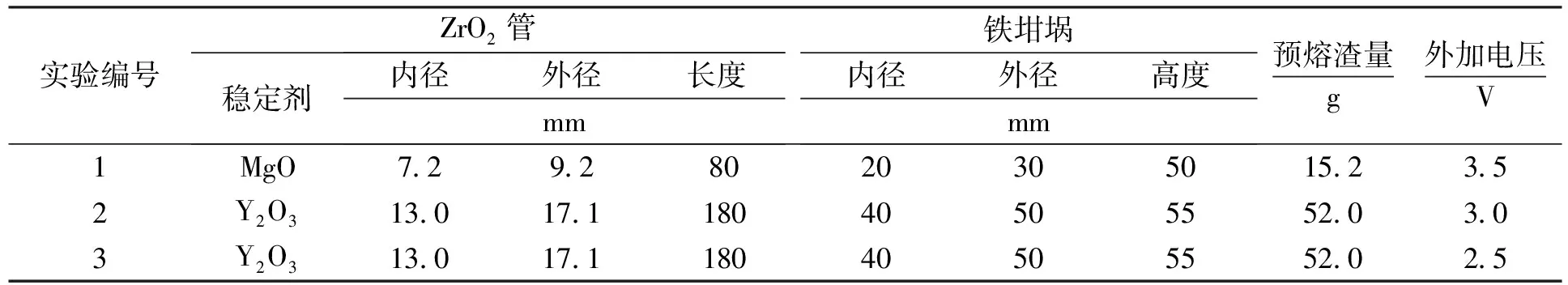
表1 實驗條件安排
2 結果與討論
2.1 開路電位-時間曲線
鐵氧化物分解電壓是電解過程中確定外加電壓大小、探索電極過程機理的一個重要依據,一般采用線性掃描伏安法測定.為了確定線性掃描曲線測定時初始外加電壓的大小,本文先進行電池開路電壓隨時間的曲線測定.開路電壓反映了氧化鋯管內外兩側(固體電解質原電池)氧濃度差的大小.由于氧化鋯管外為含FeO的熔渣,而管內為碳飽和鐵熔體,在氧化鋯管內外側存在氧勢差.熔渣側氧勢較高,鐵棒為原電池正極引線;鐵碳側氧勢較低,石墨棒為原電池負極引線.圖2為1 723 K下采用 ZrO2(MgO)管的電池開路電壓隨時間變化的典型曲線.在實驗初始階段,石墨棒并未插入碳飽和鐵熔體,所顯示的波動的開路電壓并不是正常的原電池兩端的開路電壓.在石墨棒下降的過程中,可以觀察到在50 s時電壓值突變,表明石墨棒與碳飽和鐵熔體剛好接觸,電池體系接通,最后趨于穩定,通過曲線可以觀察到測定的開路電壓約為-0.25 V.此處由于與石墨棒(原電池負極引線)相連的工作電極為電化學分析儀測定電壓的正極,故測得的開路電壓值為負.考慮到電極引線Fe棒(+)與石墨棒(-)之間的熱電勢約為0.05V[8],修正后可確定平衡時電池的開路電壓實際約為-0.20 V.
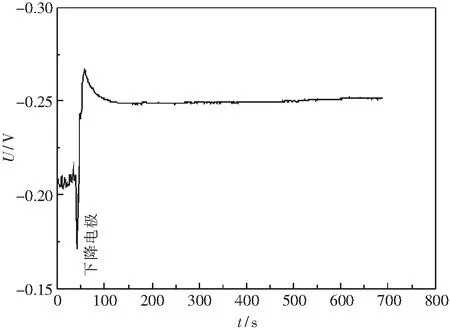
圖2 ZrO2(MgO)管實驗的開路電位-時間曲線Fig.2 Open circuit potential-time curve for the experiment with ZrO2(MgO) tube
理想情況下測定的開路電壓與固體電解質電池的理論電動勢應相等.針對本電池體系,設下述電池反應達到平衡:
(FeO)+[C]=Fe(s)+CO
(1)
此時鐵液中飽和[C]及產物Fe(s)的活度均為1.利用FactSage熱力學軟件[21]計算的 1 723 K 溫度下本文熔渣中FeO活度約為0.17,當氣體產物為CO(設其壓力為100 kPa)時,得到電池的理論電動勢為0.43 V,電動勢為正表明上述反應可自發進行.考慮到電化學分析儀的極性,與開路電壓值符號對應的電池的電動勢理論值應為-0.43 V,但該值與上述開路電壓測定值存在較大差別.分析其原因主要有二:一是碳飽和鐵熔體還原性強,此時ZrO2(MgO)管存在較大電子導電性,導致上述實驗測定值(絕對值)偏低.文獻[9~11]在短路還原以及外加電壓電解實驗中,均發現在熔渣/氧化鋯管界面附近發現有細小鐵珠生成,這是電池內部電子短路還原電流的結果,證明氧化鋯管在碳飽和鐵熔體條件下存在電子導電性.另外一個原因是實驗測定過程中氣體產物可能還有CO2生成,CO2的生成也會導致開路電壓測定值偏低.
2.2 線性掃描曲線分析
利用ZrO2(MgO)管內裝碳飽和鐵液做電解陽極(此時石墨棒為電解池陽極引線),測定鐵坩堝內熔渣中氧化物分解電壓的線性掃描伏安曲線如圖3所示.為便于對比,圖中還繪出了文獻[22]針對52.2% SiO2-22.5% CaO-9% Al2O3-6.3% MgO-10% FeO熔渣(R=0.43)的線性掃描曲線.外加電壓條件下熔渣中的O2-通過ZrO2(MgO)管在陽極氧化為O2,O2溶解在鐵碳熔體中并與[C]發生反應,非均相形核生成CO等氣泡,氣體產物的排出使氧化鋯管內壁與陽極熔體接觸的表面積不穩定,導致掃描電流波動較大,且外加電壓越大,反應越激烈,排出氣體量也越大,電流波動也越大,如圖3所示.本工作與文獻[22]中曲線的反應規律基本相同,但顯然本實驗工作中的反應較激烈.這可能與熔渣組成(或堿度)、掃描速率不同有關.本工作中,熔渣堿度高,黏度小,離子擴散快,反應激烈;掃描速率大,外加電壓增加較快,反應也加快.另外,文獻[22]中熔渣堿度低,SiO2含量高,在氧化鋯管/渣界面發現有高熔點ZrSiO4生成,而本工作中在SEM下觀察并未發現有新相生成.ZrSiO4的生成阻擋了熔渣中氧離子向氧化鋯管內的遷移,顯著降低了反應速度.
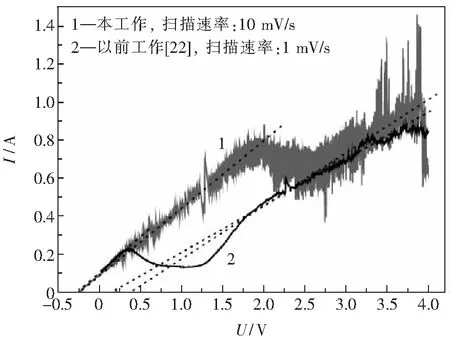
圖3 采用ZrO2(MgO)管實驗的線性掃描曲線 Fig.3 Linear scanning curves for the experiment with the ZrO2(MgO) tube
高溫下鐵坩堝與熔渣保持平衡,熔渣中的鐵氧化物只有FeO.熱力學分析表明,熔渣中最易還原的氧化物為FeO,其次為SiO2.因此,在圖3所示的線性掃描伏安曲線中出現的一個還原峰(峰電壓約1.9 V,峰電流約0.7 A),對應FeO到Fe的還原,其起峰段電流隨外加電壓幾乎呈直線增加,但達到還原峰值電流以后,FeO電解過程將受擴散步驟控制,電流下降[23].隨后又出現電流隨外加電壓增加而增加的另一直線段,對應SiO2的還原.通過直線外推法可以獲得本工作中與橫軸的第一個交點電壓(對應熔渣中FeO的分解電壓)、第二個交點電壓(對應熔渣中SiO2的分解電壓)分別約為-0.25、0.4 V.FeO與SiO2的分解電壓值符號不同,表明二者電解還原難易程度存在較大差別.本實驗條件下FeO分解電壓為負值,表明在無外加電壓甚至外加反向電壓的情況下,熔渣中FeO的電解還原也能進行,文獻[8~10]已證明在類似實驗條件下無需外加電壓(短路)即可還原熔渣中FeO;SiO2的分解電壓值為正,表明熔渣中SiO2必須外加電壓才能電解還原.在實驗溫度下,碳飽和鐵液做陽極,且氣體產物為CO+CO2時,通過FactSage熱力學軟件[21]計算FeO的理論分解電壓(產物Fe活度為1)在-0.43 V 到-0.09 V之間,而SiO2理論分解電壓(設產物Si活度為1)在0.29 V到0.62 V之間.本工作的測定結果處于FactSage熱力學軟件[21]理論計算值范圍內,表明分解電壓的測定是合理的.依據文獻[22]中的掃描曲線,可確定FeO還原峰電壓僅約0.4 V,且FeO、SiO2分解電壓分別為-0.255 V和0.15 V(如圖3所示),其中FeO的分解電壓值與本工作基本相同,而SiO2分解電壓比本工作小.考慮到文獻中熔渣的SiO2較高、堿度較低、產物Si活度小于1以及掃描速率的不同,結果與本工作(或理論計算結果)相比有一定差別是可以理解的.以上分析也表明,與文獻[22]比較,采用本工作的渣系組成, FeO還原的峰電壓、峰電流均較高,能在較寬的外加電壓范圍內提高電解電流,因而本工作渣系組成對提高渣中FeO電解還原速率更有利.
在線性掃描過程中達到各自分解電壓后,熔渣中FeO、SiO2分別按(1)~(4)式被電解,一般認為高溫下生成CO的(1)、(3)是主要電池反應:
2(FeO)+[C]=2Fe(s)+CO2
(2)
(SiO2)+2[C]=[Si]+2CO
(3)
(SiO2)+[C]=[Si]+CO2
(4)
2.3 恒電壓下電解電流-時間曲線
在本實驗條件下,盡管熔渣中的FeO無需外加電壓也可自發還原,但為加快電解反應速率,同時考慮到電極反應的超電勢和電路電阻的電壓降等因素,對可控氧流電池外加2.5~3.5 V的恒電壓U,考察熔渣的電解還原行為.分別采用MgO和Y2O3穩定的氧化鋯管內裝碳飽和鐵做陽極進行實驗,得到外加不同恒電壓U下電流隨時間的變化曲線,如圖4所示.
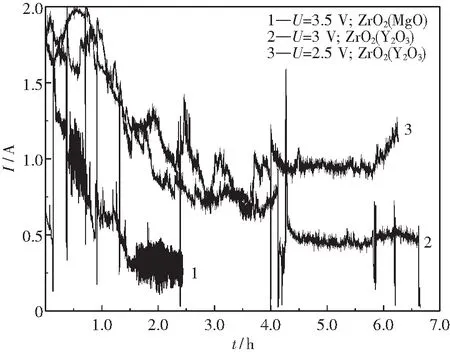
圖4 恒電壓電解電流-時間曲線Fig.4 Current-time curves of potentiostatic electrolysis
圖4中電流I-時間t曲線波動較大,正如前面所分析,這是鐵碳熔體中排出氣體產物的結果.總體上看,各外加恒電壓下電流隨時間變化逐漸減小,這是電解還原導致熔渣中FeO含量不斷下降的結果.從還原后殘渣顏色的明顯差別可比較三個實驗中渣中FeO的還原效果.眾所周知,含10%的FeO原始預熔渣是黑色的.但采用ZrO2(Y2O3)管的實驗后殘渣顏色是無色或淺綠色,表明殘渣中FeO量很低;而采用ZrO2(MgO)管的實驗后殘渣顏色顯墨綠色,表明殘渣中FeO量較高,FeO還原不完全.因此,采用ZrO2(Y2O3)管構建的可控氧流電池中FeO的還原效果明顯高于采用ZrO2(MgO)管的.
對于不同外加電壓下相同穩定劑的ZrO2(Y2O3)管實驗,在電解初始階段,外加電壓為2.5 V時的最大電流值甚至大于3 V時的電流,主要是由于ZrO2(Y2O3)管插入熔渣中的深度不同所致.實驗結束后取出樣品,發現外加電壓為3 V時ZrO2(Y2O3)管插入渣中僅2 mm,幾乎只有ZrO2(Y2O3)管底部與渣面接觸,而2.5 V時ZrO2(Y2O3)管插入渣中超過5 mm.ZrO2(Y2O3)管插入深,與熔渣接觸的表面積大,相當于增大了電極有效面積,一方面減小電路中渣、ZrO2(Y2O3)管引入的電阻,另一方面可加快電極反應.因此,熔渣中FeO的還原效果較好.這與通過殘渣顏色變化判斷的FeO還原效果是一致的.在外加電壓為2.5 V時電解的后期,熔渣中的FeO含量已經降到很低,但電流又有所升高,這可能與電極附近熔渣中SiO2的還原有關.
相同溫度下ZrO2(Y2O3)固體電解質的離子電導率一般大于ZrO2(MgO)固體電解質[17].外加電壓為3 V時ZrO2(Y2O3)管插入渣中僅2 mm,其陽極面積明顯小于ZrO2(MgO)管時的陽極面積,盡管采用ZrO2(Y2O3)管的實驗的外加電壓(3 V)小于采用ZrO2(MgO )管的實驗的外加電壓(3.5 V),且渣量也較大,但前者的還原電流遠大于后者,且從殘渣顏色判斷前者中FeO的還原效果明顯好于后者.這表明可控氧流還原效果與氧化鋯管的穩定劑種類有關.另外,采用ZrO2(MgO)管做實驗的還原時間較短,也是其FeO還原效果差的一個原因.
2.4 顯微觀察與能譜分析
采用ZrO2(Y2O3)管外加3V電壓和ZrO2(MgO)管外加3.5 V電壓電解后陰極鐵坩堝/渣界面的掃描電鏡圖及能譜分析分別如圖5和表2所示.

圖5 鐵坩堝/渣界面SEM圖Fig.5 SEM images in the iron crucible /slag interface (a)—ZrO2(Y2O3)管電解實驗(U=3 V); (b)—ZrO2(MgO)管電解實驗(U=3.5 V)
從圖5可以看出,在鐵坩堝壁與熔渣接觸處,熔渣中有發亮且呈枝晶狀的物質析出,經能譜分析(如表2所示)證明該物質為純鐵.實驗結果表明,在外加電壓的條件下,熔渣中的Fe2+向陰極鐵坩堝表面移動,在陰極得到電子而析出固態金屬鐵,新析出的鐵與鐵坩堝結合在一起構成新的陰極.隨著電解的進行,陰極的電極面積與初始狀態相比逐漸增大,且由于電解新析出的鐵活性較強,Fe2+更容易在剛析出的鐵上析出,并以此為基礎,不斷的向渣中延伸,最后形成樹枝狀的鐵枝晶結構.觀察還可以發現,距離陰極鐵坩堝壁越近,析出的鐵枝晶狀物質越多,而在遠離鐵坩堝壁的熔渣中幾乎沒有鐵析出.熔渣冷卻結晶后組織成分雖有一定偏析,但一般在距離鐵坩堝壁或鐵枝晶(陰極)較近的渣中FeO很低,甚至不含FeO,而在遠離陰極的渣中含有FeO,表明在陰極Fe2+的電極反應很快,一般不會是電解還原過程的控速環節.
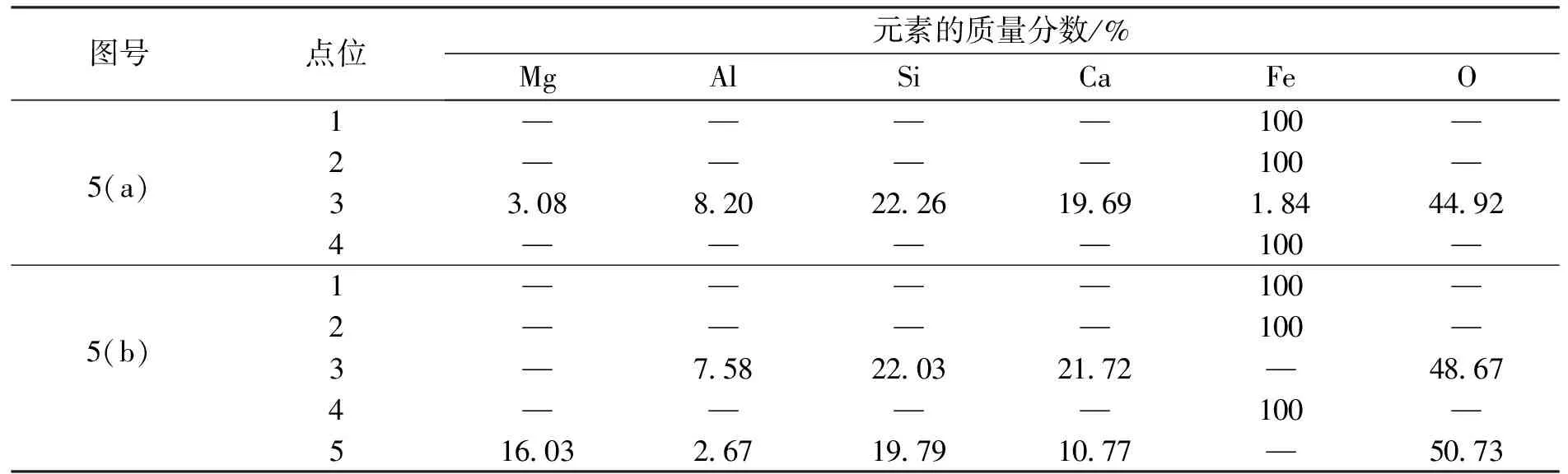
表2 鐵坩堝/渣界面附近EDS分析
采用ZrO2(Y2O3)管電解熔渣,當外加電壓為3 V時,可以觀察到渣內部不僅在鐵坩堝壁析出較多枝晶狀的鐵(圖5(a)),且有些枝晶延伸到鐵坩堝壁與 ZrO2(Y2O3) 管外壁之間的渣表面上,并匯集成較大鐵片;但外加電壓為2.5 V時,出乎意料的是在鐵坩堝內壁面沒有觀察到明顯的鐵枝晶,而僅在鐵坩堝內壁與 ZrO2(Y2O3) 管外壁之間的渣面上觀察到匯集形成的較大鐵片,如圖6所示.較大鐵片的形成實際上有利后續渣鐵的磁選或熔融分離.能譜分析(表3)結果表明,外加電壓為3 V時,在渣表面形成的較大鐵片為純Fe,殘渣中含有少量的FeO,這可能與 ZrO2(Y2O3) 管插入渣中深度不夠,導致FeO還原不完全有關.但在外加電壓為2.5 V時,在渣表面形成的較大鐵片為Fe-Si合金(Si量較低),殘渣中不含FeO,表明熔渣中FeO完全被還原,并存在SiO2的還原.依據Fe-Si相圖[24],Si與Fe可形成低熔點合金.外加電壓為2.5 V時鐵坩堝壁面沒有觀察到明顯的鐵枝晶可能是由于后期Si的析出導致先前析出的鐵枝晶破碎而脫落.
由于熔渣中存在FeO與SiO2的還原,且電解中不能直接確定電子電流的大小(電子電流可以影響電流效率[11]),因此本文未能通過外電路電流的大小計算熔渣電解過程中FeO的還原率.為獲得較大電解速率,外加電壓較大時,如需電解獲得純鐵,應在FeO基本還原完畢后及時結束電解.

圖6 ZrO2(Y2O3)管實驗中渣表面金屬片的SEM圖Fig.6 SEM images of metal sheet on the surface of slag after electrolysis with ZrO2(Y2O3) tube(a)—外加電壓U=2.5 V; (b)—外加電壓U=3 V
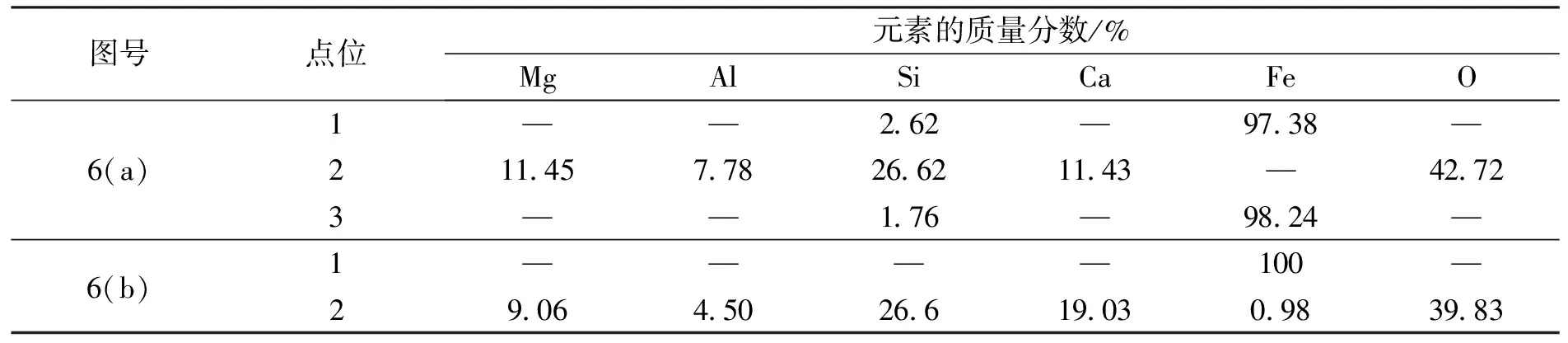
圖號點位元素的質量分數/%MgAlSiCaFeO1——262—9738—6(a)2114577826621143—42723——176—9824—6(b)1————100—290645026619030983983
3 結 論
(1) 利用構建的可控氧流電池,采用線性掃描技術測定,得到本實驗條件下SiO2-CaO-Al2O3-MgO-FeO熔渣中FeO、SiO2分解電壓分別約為-0.25 V、0.4 V,實驗測定結果位于FactSage熱力學軟件理論計算值范圍內,表明了本實驗裝置測定熔渣中氧化物組元分解電壓的可行性.同時掃描曲線也表明本文所選熔渣組成對外加電壓電解FeO是有利的.
(2) 采用MgO或Y2O3穩定的ZrO2管內裝碳飽和鐵作陽極,構建可控氧流電池,外加電壓均可以從SiO2-CaO-Al2O3-MgO-FeO熔渣中電解還原獲得金屬鐵(或鐵合金).外加電壓過大,易導致熔渣中SiO2的還原.
(3) 在相同的實驗條件下,可控氧流電解電流的大小以及熔渣中FeO的還原效果與外加電壓、ZrO2穩定劑的種類和ZrO2管(陽極)插入熔渣中的深度、電子電流等有關.對于不同穩定劑的ZrO2管,ZrO2(Y2O3)管比ZrO2(MgO)管似乎更利于熔渣中FeO電解還原反應的進行.
[1] Sun Wenqiang, Cai Jiuju, Mao Hujun,etal. Change in carbon dioxide (CO2) emissions from energy use in China's iron and steel industry[J]. Journal of Iron and Steel Research, International, 2011, 18(6): 31-36.
[2] Tian Yihui, Zhu Qinghua, Geng Yong. An analysis of energy-related greenhouse gas emissions in the Chinese iron and steel industry[J]. Energy Policy, 2013, 56: 352-361.
[3] Wang D H, Gmitter A J, Sadoway D R. Production of oxgen gas and liquid metal by electrochemical decomposition of molten iron oxide[J]. Journal of the Electrochemical Society , 2011, 158(6): E51-E54.
[4] Kim H J, Paramore J, Allanore A,etal. Electrolysis of molten iron oxide with an iridium anode:The role of electrolyte basicity[J]. Journal of The Electrochemical Society, 2011,158 (10): E101-E105.
[5] Sirk A H C, Sadoway D R,Sibille L. Direct electrolysis of molten lunar regolith for the production of oxygen and metals on the moon[J]. ECS Transactions, 2010,28 (6): 367-373.
[6] Allanore A, Yin L, Sadoway D R. A new anode material for oxygen evolution in molten oxide electrolysis[J]. Nature, 2013, 497(7449):353-356.
[7] 高運明, 姜英, 張華, 等.可控氧流冶金[J]. 武漢科技大學學報, 2007, 30(5): 449-453.
(Gao Yunming, Jiang Ying, Zhang Hua,etal. Metallurgy with controlled oxygen flow[J]. Journal of Wuhan University of Science and Technology, 2007, 30(5): 449-453.)
[8] 高運明. 無污染短路還原法提鐵的基礎研究[D]. 北京: 北京科技大學, 2004, 9.
(Gao Yunming. Study on extraction of iron by the short circuit reduction method with no pollution [D]. Beijing: Beijing University of Science and Technology, 2004, 9.)
[9] 高運明, 郭興敏, 周國治. 熔渣無污染短路電化學還原分析[J]. 中國有色金屬學報, 2006, 16(3): 530-535.
(Gao Yunming, Guo Xingmin, Zhou Guozhi. Unpolluted short circuit electrochemical reduction analysis for molten oxide slags[J]. The Chinese Journal of Nonferrous Metals, 2006,16(3):530-535.)
[10] 高運明, 郭興敏, 周國治.短路還原法提取鐵的研究[J]. 金屬學報, 2006, 42(1): 87-92.
(Gao Yunming, Guo Xingmin, Zhou Guozhi. Study on extraction of iron by the short circuit reduction method[J]. Acta Metallurgica Sinica, 2006, 42(1): 87-92.)
[11] Gao Y M, Wang B, Wang S B,etal. Study on electrolytic reduction with controlled oxygen flow for iron from molten oxide slag containing FeO[J]. Journal of Mining and Metallurgy Section B Metallurgy, 2013, 49 (1) B: 49-55.
[12] Pal U B, Powell A C. The use of solid-oxide-membrane technology for electrometallurgy[J]. JOM, 2007, 59(5): 44-49.
[13] Krishnan A, Pal U B, Lu X G. Solid oxide membrane process for magnesium production directly from magnesium oxide[J]. Metallurgical and Materials Transactions B, 2005, 36(4): 463-497.
[14] Lu X, Zou X, Li C,etal. Green electrochemical process solid-oxide oxygen-ion-conducting membrane(SOM):Direct extraction of Ti-Fe alloys from natural ilmenite[J]. Metallurgical and Materials Transactions B, 2012, 43(3): 503-512.
[15] 陳朝軼, 魯雄剛, 李謙, 等. SOM法金屬氧化物制取金屬新技術[J]. 材料與冶金學報, 2007,6(3):204-208.
(Chen Chaoyi, Lu Xionggang, Li Qian,etal. A new technique study of metal preparation by SOM method[J]. Journal of Materials and Metallurgy, 2007, 6(3):204-208.)
[16] Zou Xingli, Lu Xionggang, Zhou Zhongfu,etal. Direct selective extraction of titanium silicide Ti5Si3from multi-component Ti-bearing compounds in molten salt by an electrochemical process[J]. Electrochimica Acta, 2011, 56(24): 8430-8437.
[17] 王常珍. 固體電解質和化學傳感器[M]. 北京: 冶金工業出版社, 2000.
(Wang Changzhen. Solid electrolyte and chemical sensors[M]. Beijing: Metallurgical Industry Press,2000.)
[18] Franks E. Electroanalysis of iron in molten slags[J]. Journal of Applied Electrochemistry, 1977, 7(2): 147-151.
[19] 王少博, 高運明, 王兵, 等. 電解提鐵酸性熔渣介質的組成及熔化性能研究[J]. 中國稀土學報, 2012,30(專輯): 334-339.
(Wang Shaobo, Gao Yunming, Wang Bing,etal. Study on compositions and melting property of acid slag medium by electrolysis for iron[J]. Journal of Chinese Society of Rare Earths, 2012, 30(Spec. Issue):334-339.)
[20] 石亮, 謝光遠, 高運明, 等. 凝膠注模制備氧化鋯管工藝研究[J]. 武漢科技大學學報, 2013, 36(5): 366-369.
(Shi Liang, Xie Guangyuan,Gao Yunming,etal. Preparation of zirconia tube with gel-casting method[J]. Journal of Wuhan University of Science and Technology, 2013,36(5):366-369.)
[21] Bale C W, Bélisle E, Chartrand P,etal. FactSage thermochemical software and databases: Recent developments[J]. Calphad, 2009, 33(2): 295-311.
[22] 高運明, 王兵, 王少博, 等. 含FeO熔渣對ZrO2固體電解質侵蝕性研究[J]. 武漢科技大學學報, 2012, 35(5): 330-337.
(Gao Yunming, Wang Bing, Wang Shaobo,etal. Study on the corrosion of ZrO2solid electrolyte by molten slag containing FeO[J]. Journal of Wuhan University of Science and Technology, 2012,35(5):330-337)
[23] 張圣弼. 冶金物理化學實驗[M]. 北京: 冶金工業出版社,1994: 232.
(Zhang Shengbi. Experiments in physical chemistry of metallurgy[M]. Beijing: Metallurgical Industry Press, 1994:232.)
[24] 虞覺奇, 易文質, 陳邦迪, 等. 二元合金狀態圖集[M]. 上海: 上海科學技術出版社, 1987: 375.
(Yu Jueqi, Yi Wenzhi, Chen Bangdi,etal. Binary alloy phase atlases[M]. Shanghai: Shanghai Science and Technology Publishing House, 1987:375.)

