鋅-鎳合金鍍層的稀土電解轉化膜工藝
李亨特, 李明仙, 安茂忠
(哈爾濱工業大學 化工學院,黑龍江 哈爾濱150006)
0 前言
稀土鈍化是一種很有前途的金屬防腐蝕處理技術。目前研究較多的稀土轉化膜方法主要有化學浸漬法[1]、復合轉化法[2]和陰極電解法[3]等。
本實驗采用陰極電解法,在鋅-鎳合金鍍層表面生成稀土轉化膜。這種處理方法不僅能明顯提高鍍層的耐蝕性,而且轉化膜和鍍層結合牢固,是一種良好的無鉻鈍化技術。
1 實驗
1.1 電鍍鋅-鎳合金流程及鈍化工藝
陽極采用的是鋅、鎳聯合陽極(鋅陽極和鎳陽極交替使用,每用兩次鋅陽極板更換一次鎳陽極板);陰極是低碳鋼片。電源為YJ92/5型數字直流穩流電源。

鍍液組成及工藝條件為:氯化鋅100g/L,氯化鎳120g/L,氯化鉀200g/L,十二烷基硫酸鈉0.06 g/L,添加劑3~4 mL/L,pH值5.0~5.5,電流密度3A/dm2,溫度38~42℃。電鍍得到的鋅-鎳合金鍍層的厚度為5μm,其中鎳的質量分數為9%~13%。
稀土鈍化工藝規范:硝酸鈰20g/L,硝酸銨1.5 mol/L,硝酸鈉0.5 mol/L,硼酸2g/L,電流密度300mA/dm2,pH值5.5,鈍化溫度60℃,陰極沉積90s,陽極采用不溶性不銹鋼網。鈍化后,取出試樣,用蒸餾水沖洗干凈并用熱風吹干,放置一段時間后即可獲得彩虹色或黃色稀土轉化膜。
對部分試樣進行鉻酸鈍化處理以提供耐蝕性對比試樣,處理條件為:重鉻酸鉀20g/L,濃硫酸8~10mL/L,硫酸亞鐵8g/L,室溫下在溶液中浸漬8~10s,在空氣中成膜15~20s,洗凈吹干。
1.2 測試方法
1.2.1 耐蝕性測試
(1)點滴法
在室溫下,用滴管將5%的硫酸銅溶液滴一滴在試樣表面,觀察該處的顏色變化情況,并用秒表記錄其變黑所經歷的時間。耐黑變時間可大致反映稀土轉化膜的耐蝕性。
(2)浸泡法
將鈍化試樣置于3.5%的氯化鈉溶液中,在室溫下浸泡不同的時間,之后用硬毛刷和去污粉洗凈試樣表面的腐蝕產物,在電子天平上測量其質量損失,求得其腐蝕速率。用顯微鏡觀測鈍化層的腐蝕狀況,并測量鈍化前后的自腐蝕電位和自腐蝕電流密度。
(3)極化曲線和電化學交流阻抗法
對試樣進行電化學測試。采用三電極體系,工作電極為研究試樣,輔助電極為鉑片,參比電極為飽和甘汞電極(SCE),測試面積為1cm2。測試介質為3.5%的氯化鈉溶液。極化曲線由CHI630B型電化學工作站測得,掃描速率為1mV/s。測試后用計算機軟件擬合,求出自腐蝕電位和自腐蝕電流密度等電化學參數。電化學交流阻抗測試在2273型電化學工作站上完成,正弦波激勵信號幅值為10 mV,頻率范圍為105~10-2Hz,測試電位為工作電極的開路電位。
1.2.2 表面分析
電鍍鋅-鎳合金板經過稀土鈍化后,先在光學顯微鏡下觀察其表面形貌。將試樣鋸成0.5cm×0.5 cm 的小片進行SEM 測試。使用S-4800型掃描電子顯微鏡(SEM)對轉化膜的表面形貌進行觀察。采用PHI5700型光電子能譜儀分析轉化膜的表面組成及化學形態。X 射線源采用AlKa(1 486.71 eV)射線,采用污染碳的C1s(284.9eV)進行能量校正,分峰擬合采用高斯/勞倫特斯方程最小均方差Shirley消背底方法,分析轉化膜表層的元素含量。
2 結果與討論
2.1 鈍化液組成及工藝條件優化
2.1.1 鈍化液組成
鈍化液的主要成分為硝酸鈉、硝酸銨、硼酸、硝酸鈰。固定鈍化液的部分組成,鈍化溫度定為50℃。采用L9(33)正交試驗表優化各組分的用量。
從極差的大小順序可以看出:鈍化層的耐蝕性和形貌主要受硝酸鈰的影響,電流密度主要影響轉化膜的覆蓋面積,鈍化時間主要影響轉化膜的耐蝕性和外觀。通過正交試驗,確定硝酸鈰的質量濃度為20g/L。由于本正交試驗范圍較窄,所以其他參數由后面的單因素試驗得出。
2.1.2 電流密度
電流密度的研究選取如下體系:硝酸鈰20 g/L,硝酸銨1.5mol/L,硝酸鈉0.5mol/L,硼酸2 g/L,溫度50℃,pH值5.5,機械攪拌,鈍化90s。對不同電流密度下得到的鈍化件進行硫酸銅點滴試驗,結果如表1所示。
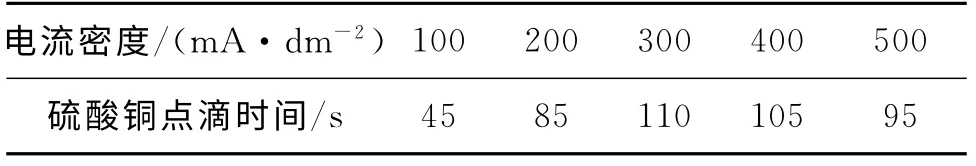
表1 電流密度對轉化膜耐蝕性的影響
由表1可知:在一定范圍內,隨著電流密度的增加,鈍化層的耐蝕性逐漸變好。這是因為電流密度增加會使鈍化層更致密,覆蓋更完整,形成的轉化膜更厚。電流密度較大時,析出的氣體破壞了鈍化層的結構,導致鈍化層的耐蝕性變差。為此,選擇最佳電流密度為300mA/dm2。
2.1.3 鈍化時間
選取硝酸鈰20g/L,硝酸銨1.5mol/L,硝酸鈉0.5mol/L,硼酸2g/L,電流密度300mA/dm2,pH值5.5,溫度50℃,機械攪拌。對不同鈍化時間下得到的鈍化件進行硫酸銅點滴試驗,結果如表2所示。沉淀量用0~10來衡量,0表示沒有,1~3表示少量沉淀且以吸附在鍍件表面的形式存在,4~6表示有明顯沉淀而且部分沉淀進入溶液,7~8表示進入溶液的沉淀較多,9~10表示沉淀量很大。
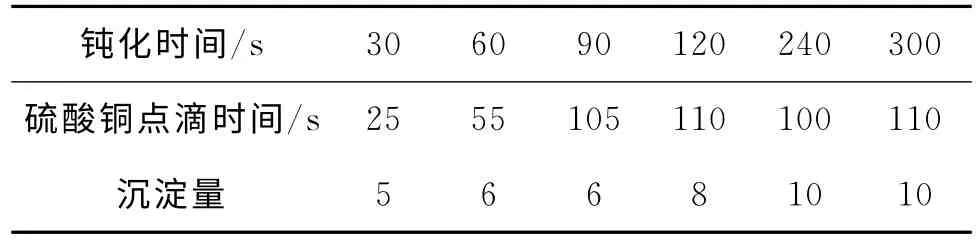
表2 鈍化時間對轉化膜性能及鈍化液中沉淀量的影響
由表2可知:隨著鈍化時間的延長,鈍化層的耐蝕性逐漸變好。這是因為鈍化時間越長,鈍化層越完整、致密。鈍化時間過長,轉化膜的耐蝕性并沒有明顯提升,且沉淀量明顯增大。其原因為鈍化層形成一定厚度后,無法均勻致密沉積,而是以沉淀的形式進入鈍化液中,所以耐蝕性沒有明顯提升。因此,鈍化時間確定為90s。
2.1.4 鈍化溫度
選取硝酸鈰20g/L,硝酸銨1.5mol/L,硝酸鈉0.5mol/L,硼酸2g/L,電流密度300mA/dm2,pH值5.5,鈍化時間90s,機械攪拌。鈍化后進行硫酸銅點滴試驗。表3為鈍化溫度對轉化膜性能及鈍化液中沉淀量的影響。
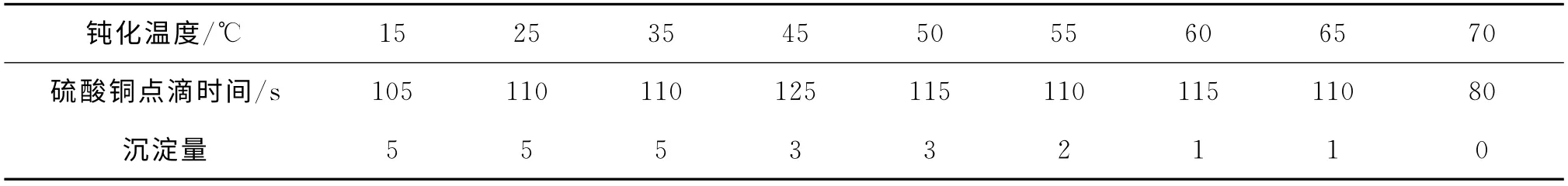
表3 鈍化溫度對轉化膜性能及鈍化液中沉淀量的影響
由表3可知:隨著鈍化溫度的升高,轉化膜的耐蝕性沒有明顯提升。這可能是因為在一定溫度范圍內,鈍化層的形成與溫度沒有明顯關系。溫度過高會造成耐蝕性降低。這是由于溫度過高時鈍化層溶解較快,形成的轉化膜較薄。另外,沉淀量隨溫度升高而降低。所以,鈍化溫度確定為55~65℃。
經以上分析討論,得出鈍化液組成及工藝條件的優化結果為:硝酸鈰20g/L,硝酸銨1.5mol/L,硝酸鈉0.5mol/L,硼酸2g/L,pH值5.5,電流密度300mA/dm2,溫度55~65℃,機械攪拌,鈍化時間90s。
2.2 稀土轉化膜的微觀形貌及組成
鋅-鎳合金鍍層試樣經過稀土電解鈍化后,其鈍化層的微觀形貌,如圖1所示。由圖1可知:鍍層表面覆蓋了一層均勻、平整的轉化膜。與鋅-鎳合金鍍層相比,鈍化層更加致密。在高倍下能觀測到鈍化層的層狀結構,但觀測不到晶粒結構。分析認為,陰極極化作用下稀土沉積均勻,晶粒較為細致。
圖2和圖3分別為稀土轉化膜表面XPS全掃描能譜圖和Ce元素的窄幅掃描譜圖。經分析,鈍化層主要含有O、Ce、Zn三種元素。鋅-鎳合金鍍層經過稀土電解鈍化后,轉化膜表面的元素主要是CeO2,也含有一定量的Ce2O3;Zn元素則主要以Zn和ZnO 的形式存在。
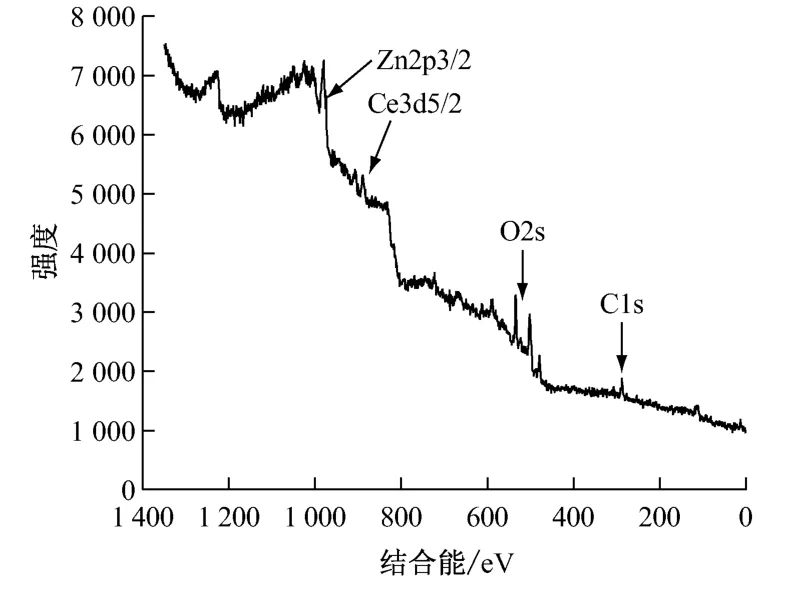
圖2 稀土轉化膜表面XPS全掃描能譜圖
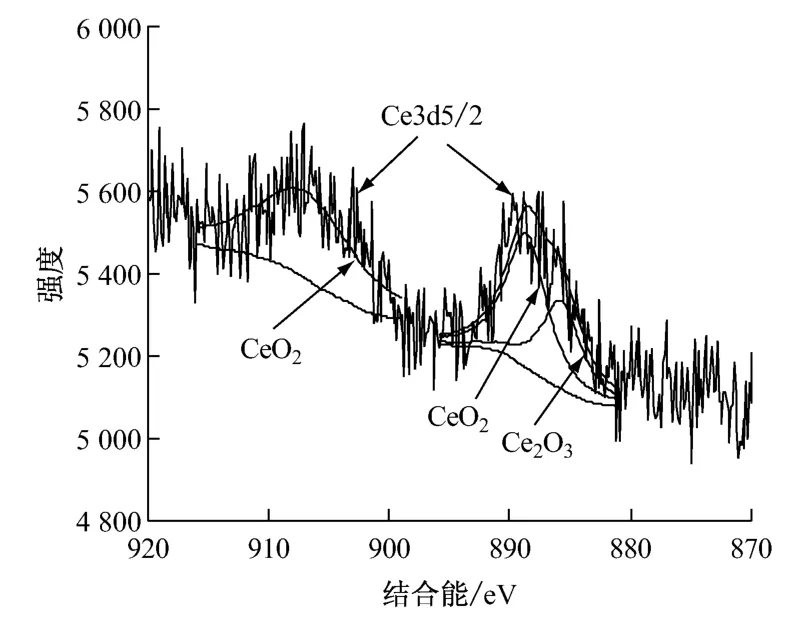
圖3 稀土轉化膜表面Ce元素的窄幅掃描能譜圖
2.3 稀土轉化膜的耐蝕性
(1)將不同鈍化工藝處理后的鍍件用3.5%的氯化鈉溶液浸泡96h后,將鍍件洗凈吹干,稱量其質量損失,求出腐蝕速率。表4給出了其腐蝕試驗結果。
由表4可知:稀土鈍化后的試樣的腐蝕速率明顯減緩;相對于未鈍化的試樣,其腐蝕速率大幅降低,與六價鉻鈍化的接近。
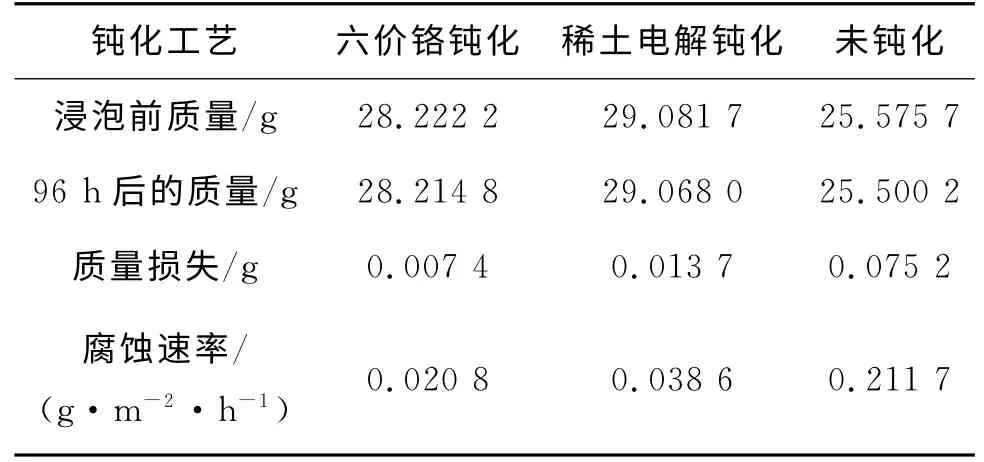
表4 腐蝕試驗結果
(2)圖4為不同轉化膜在3.5%的氯化鈉溶液中的Tafel曲線。表5為Tafel曲線的擬合結果。
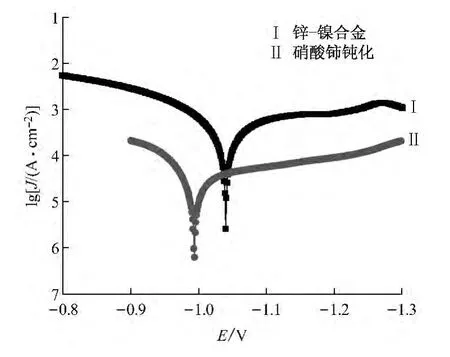
圖4 Tafel曲線
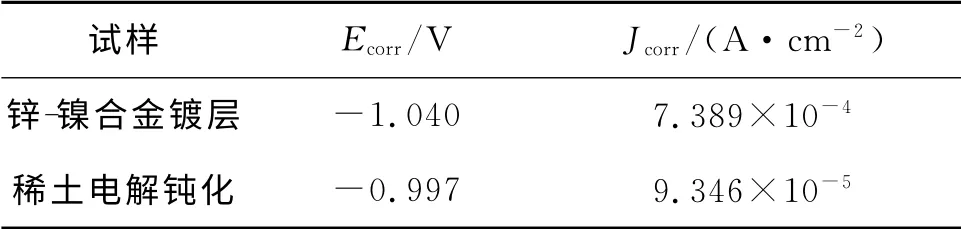
表5 Tafel曲線擬合結果
對比發現:鈍化后試樣的自腐蝕電位明顯正移,自腐蝕電流密度變小。這說明鈍化試樣的耐蝕性得到明顯提高。
(3)圖5為不同鈍化工藝下所得轉化膜和未鈍化鍍層在3.5%的氯化鈉溶液中的EIS譜圖。
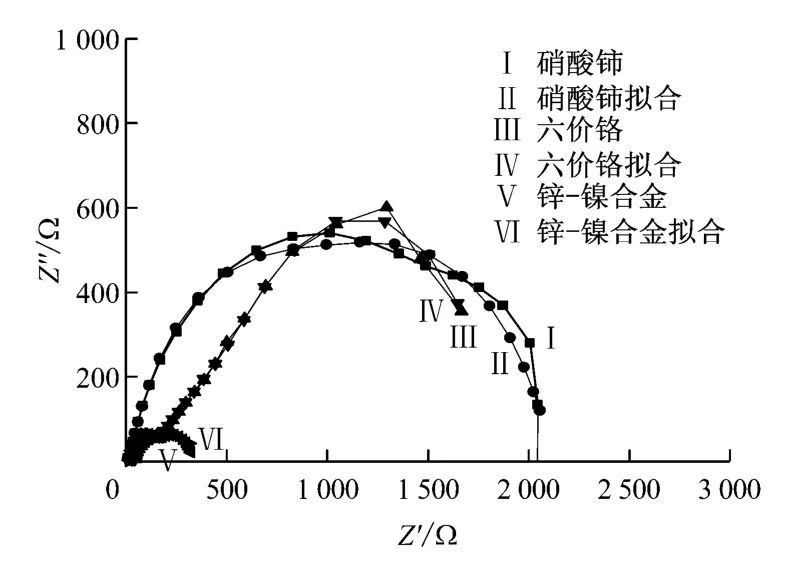
圖5 Nyquist圖
由圖5可知:有轉化膜的試樣的容抗弧半徑都明顯大于未鈍化試樣的,說明鈍化后腐蝕電阻增大,阻礙了腐蝕的進行。
(4)圖6 為交流阻抗的擬合模擬電路圖。其中:R1對應溶液電阻;Q1對應電化學腐蝕時雙電層的容抗型常相位元件;R2對應電化學腐蝕時的電化學反應電阻;Q2對應第一層轉化膜的容抗型常相位元件;R3對應第一層轉化膜的腐蝕反應電阻;Q3對應第二層轉化膜的容抗;R4對應第二層轉化膜的腐蝕反應電阻。
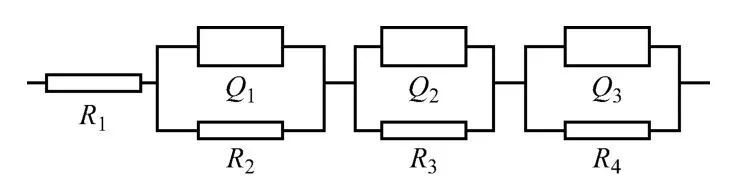
圖6 交流阻抗模擬電路
從擬合得到的各個參數可以看出:鉻酸鹽轉化膜的腐蝕電阻為1 713.5Ω/cm2,稀土電解轉化膜的腐蝕電阻為2 175.7Ω/cm2,鋅-鎳合金的腐蝕電阻為325.0Ω/cm2。對比可知,稀土鈍化明顯提高了鋅-鎳合金鍍層的耐蝕性,而且稀土電解鈍化的效果略優于鉻酸鹽鈍化的。
3 結論
(1)確定了較優的稀土無鉻陰極電解鈍化液配方:硝酸鑭20g/L,硝酸銨1.5 mol/L,硝酸鈉0.5 mol/L,硼酸2g/L,電流密度300 mA/dm2,pH值5.5,鈍化時間90s,鈍化溫度55~65℃,機械攪拌。該工藝簡單,操作靈活,成本較低,具有一定的實用價值和推廣前景。
(2)稀土轉化膜的主要成分為CeO2和Ce2O3,并含有部分Zn和ZnO 的混合物。
(3)稀土陰極電解鈍化能使鍍層表面更平整,提高了鍍層的耐蝕性,其耐蝕效果可與六價鉻鈍化的相媲美。
[1]MONTEMOR M F,SIMOES A M,FERREIRA M G S.Composition and behavior of cerium films on galvanised steel[J].Progress in Organic Coatings,2001,43(4):274-281.
[2]MANSFELD F, WANY V,SHIH H.Development of“stainless aluminum”[J].Journal of the Electrochemical Society,1991,138(12):74-75.
[3]石鐵.陰極電沉積稀土轉化膜工藝與耐蝕性研究[D].北京:北京化工大學,2005.

