腫瘤對小鼠腎上腺皮質細胞膽固醇穩態分子表達的影響
潘志強,方肇勤,盧文麗,劉小美,張園園
(上海中醫藥大學基礎醫學院,上海 201203)
細胞內膽固醇穩態機制在肝臟、主動脈研究很深入[1,2],而膽固醇作為類固醇激素合成的前體物質,如何被腎上腺細胞用于合成皮質激素以適應各種應激尚缺乏深入研究。現有研究表明[3],腎上腺皮質細胞通過3 種方式獲得類固醇激素合成的原料:①攝取血液膽固醇(人主要是低密度脂蛋白膽固醇,嚙齒類動物主要是高密度脂蛋白膽固醇),②在內質網中從頭合成膽固醇,③將脂滴中酯化膽固醇酶解為游離膽固醇。一旦細胞內膽固醇積聚過量,則通過細胞膜上三磷酸腺苷結合盒轉運蛋白體A1 和G1 將膽固醇逆轉運至細胞外。此外,肝X 受體、固醇調節元件結合蛋白、過氧化物酶體增殖物激活受體等信號分子還參與細胞內膽固醇進出與轉運調節[4,5],腎上腺皮質細胞正是通過這一精密調控機制以確保胞內膽固醇的穩態。
然而,在腫瘤狀態下,機體為適應腫瘤的慢性應激,腎上腺分泌皮質激素以抵御應激反應,那么,腫瘤大小是否對腎上腺皮質細胞膽固醇穩態有影響,尚未發現相關研究報道。本文在課題組對H22 肝癌小鼠腎上腺皮質酮合成與分泌的研究基礎上[6],重點比較了不同腫瘤大小的肝癌小鼠腎上腺皮質細胞內膽固醇穩態分子的表達差異,發現腫瘤越大者,小鼠腎上腺皮質細胞對膽固醇需求越高,用于皮質激素的合成以抵御腫瘤的慢性應激。
1 材料和方法
1.1 材料
1.1.1 實驗動物
SPF 級KM 雄性小鼠250 只,7 周齡,體重(21±1)g,購自上海斯萊克實驗動物有限責任公司【SCXK(滬)2007-0005】;實驗在上海中醫藥大學動物實驗中心設施內進行【SYXK(滬)2009-0069】。
1.1.2 試劑
乙二胺四乙酸二鉀鹽(EDTA-2K)抗凝劑購自國藥集團;總膽固醇、甘油三酯、高密度脂蛋白膽固醇檢測試劑盒購自南京建成生物工程研究所。Trizol 購自Invitrogen,反轉錄試劑盒PrimeScript? RT Reagent Kit 和PCR 試劑盒SYBR? Premix Ex TaqTM(Tli RNaseH Plus)II 購自TaKaRa 公司。SRB1、ApoA1、GAPDH 抗體購自Abcam 公司,BCA 蛋白質定量檢測試劑盒購自上海碧云天生物技術有限公司,免疫印跡化學發光試劑ECL 試劑盒購自Pierce公司。
1.1.3 儀器
Elx800 型酶標儀(美國Bio-TEK 公司),Elx50型自動洗板機(美國Bio-TEK 公司)。5417R 型冷凍臺式離心機(德國Eppendorf 公司),Eco-Illumina實時熒光定量PCR 儀(美國Illumina 公司),GBOX CheMI 凝膠掃描與分析系統。
1.2 方法
1.2.1 H22 肝癌小鼠模型建立
隨機取30 只小鼠作正常對照組,另220 只小鼠腋下接種H22 肝癌腹水癌細胞(課題組前期采用并保種凍存于-196℃液氮中),每只0.2 mL(細胞濃度1 ×107個/mL)。
1.2.2 小鼠分組、處死、取材與組織濕重
采用游標卡尺精確測量小鼠腋下腫瘤最長直徑(a)和最短橫徑(b),通過腫瘤體積預測公式V =0.5ab2,估算腫瘤大小,按照腫瘤體積大小排序,選擇瘤體最大者18 只,瘤體最小者18 只,同時選擇體重居中的18 只正常小鼠作為正常對照組,于接種腫瘤細胞后第11 天處死瘤體大組、瘤體小組和正常組小鼠,摘眼球取血,常規分離血漿,剝離腫瘤并稱重,多余小鼠用于后續實驗。
1.2.3 血脂含量檢測
按照試劑盒及所提供的方法進行操作,檢測血漿總膽固醇、甘油三酯、高密度脂蛋白膽固醇含量。
1.2.4 實時熒光定量PCR 檢測基因表達
上下游引物序列采用Primer3 (v.0.4.0)在線軟件合成(參見表1),委托Life Technologies 公司上海合成部完成。按照Trizol 試劑盒說明書抽提腎上腺總RNA;逆轉錄反應體系20 μL,反應條件為37℃×15 min,85℃×5 s,4℃(逆轉錄反應程序結束,可以取出,也可以過任意時間后取出);PCR 擴增反應體系為20 μL,反應程序為95℃×3 min,95℃×30 s,60℃×30 s,40 cycles。基因相對表達量分析方法:采用2-ΔΔCT法分析[7],以正常組作為對照組,以GAPDH 和β-actin 基因Ct 均值作為內參組,ΔCt=Ct目的基因- Ct內參基因(其中,Ct 值為擴增n 個循環基因的熒光數值),ΔΔCt=ΔCT 腫瘤組- ΔCT 對照組,目的基因相對表達量=2-ΔΔCT。

表1 小鼠上、下游引物序列Tab.1 Sequences of the mose primers
1.2.5 Western blot 檢測蛋白表達
采用RIPA 裂解液裂解腎上腺組織,依據BCA蛋白質定量試劑方法進行蛋白定量,采用10% SDSPAGE 凝膠電泳分離蛋白,并進行PVDF 轉膜與5%脫脂奶粉封閉,加入一抗(SRB1 抗體1∶1000 稀釋、ApoA1 抗體1 ∶2000 稀釋、GAPDH 抗體1 ∶2000 稀釋)4℃過夜,用TBST 洗滌,再加入相應辣根過氧化物酶標記的山羊抗兔IgG 二抗(1∶2000 稀釋)孵育,TBST 洗滌,ECL 化學發光顯影,最后用GBOX Che-MI 凝膠掃描與分析系統進行半定量分析。
1.2.6 統計學方法
應用SPSS 15.0 統計軟件,兩組比較采用t 檢驗,三組比較采用單因素方差分析對實驗指標進行統計。P≤0.05 為差異有統計學意義。
2 結果
2.1 小鼠去瘤體重與腫瘤質量比較
與正常組比較,兩組肝癌小鼠去瘤體重差異無顯著性;與瘤體小組比較,瘤體大組小鼠腫瘤質量明顯增大(P <0.05)(見表2)。
2.2 血脂含量比較
與正常組比較,兩組肝癌小鼠血漿TC 和TG 差異均無顯著性,而HDL-C 顯著下降(P <0.05),提示肝癌小鼠膽固醇逆向轉運至肝臟的代謝能力下降(見表3)。
表2 各組小鼠去瘤體重與腫瘤質量比較(±s,n =18)Tab.2 Comparison of body weight and tumor weight among the mice of all groups
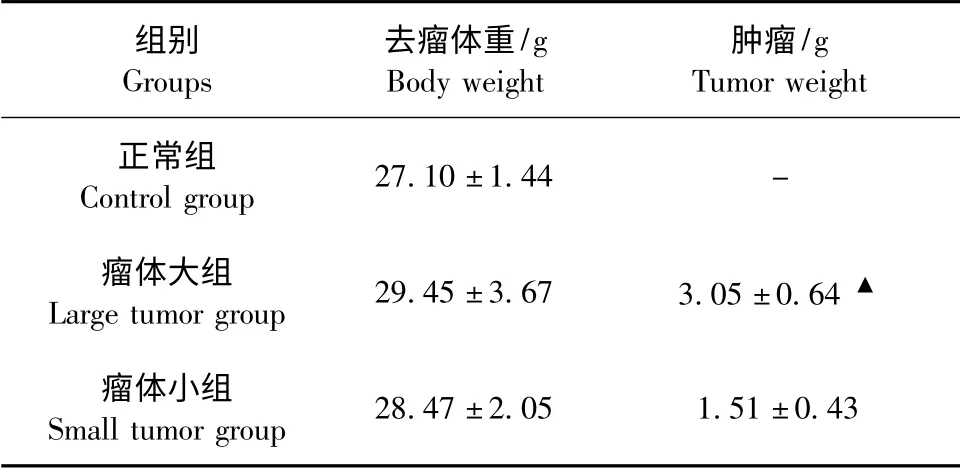
表2 各組小鼠去瘤體重與腫瘤質量比較(±s,n =18)Tab.2 Comparison of body weight and tumor weight among the mice of all groups
注:與瘤體小組比較,▲P <0.05。Note.▲P <0.05 compared with the small tumor group.
組別Groups去瘤體重/g Body weight腫瘤/g Tumor weight正常組Control group 27.10±1.44 -瘤體大組Large tumor group 29.45±3.67 3.05±0.64 ▲瘤體小組Small tumor group 28.47±2.05 1.51±0.43
2.3 腎上腺皮質細胞膽固醇攝取與轉運相關基因表達
與正常組比較,瘤體大組肝癌小鼠腎上腺膽固醇攝取分子高密度脂蛋白受體(Srb1)和低密度脂蛋白受體(Ldlr)基因表達顯著升高(P <0.05),且瘤體大組肝癌小鼠Ldlr 基因表達顯著高于瘤體小組(P <0.05)。Ldlr 通過質膜內吞進入胞內體,釋放膽固醇并通過含START 結合域蛋白3(Stard3)、C型尼曼-匹克病基因(Npc1 和Npc2)等蛋白轉運至內質網,然而這幾個膽固醇轉運分子基因表達在各組間差異無顯著性(見表4)。
表3 各組小鼠血脂含量比較(±s,mmol/L)Tab.3 Comparison of blood TC,TG and HDL-C among the mice of all groups
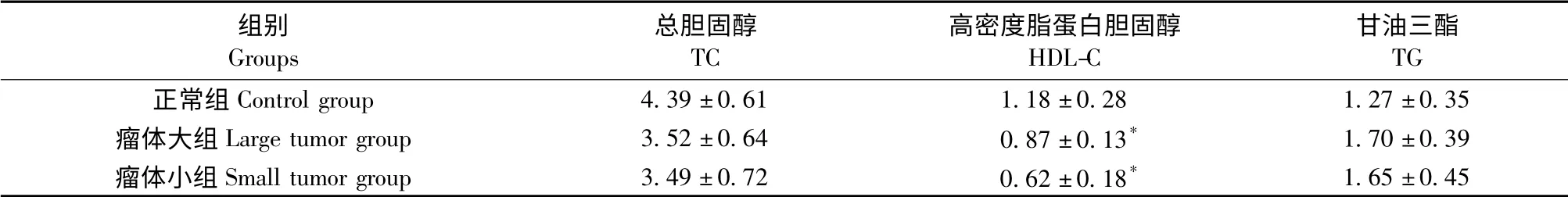
表3 各組小鼠血脂含量比較(±s,mmol/L)Tab.3 Comparison of blood TC,TG and HDL-C among the mice of all groups
注:與正常組比較,* P <0.05。Note.* P <0.05 compared with the control group.
組別Groups總膽固醇TC高密度脂蛋白膽固醇HDL-C甘油三酯TG正常組Control group 4.39±0.61 1.18±0.28 1.27±0.35瘤體大組Large tumor group 3.52±0.64 0.87±0.13* 1.70±0.39瘤體小組Small tumor group 3.49±0.72 0.62±0.18*1.65±0.45
表4 各組小鼠腎上腺細胞膽固醇攝取與轉運相關基因表達(±s)Tab.4 Comparison of the expression of cholesterol uptake and transport-related genes among all groups
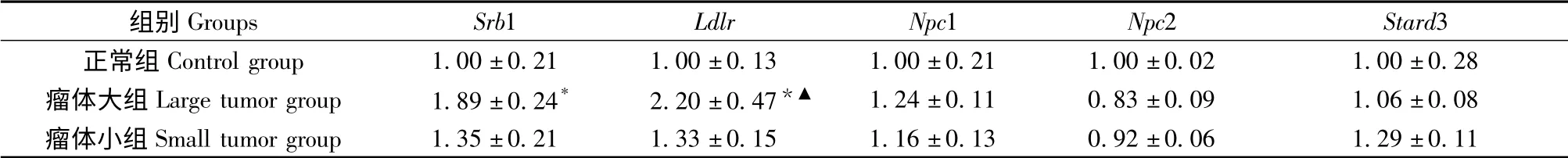
表4 各組小鼠腎上腺細胞膽固醇攝取與轉運相關基因表達(±s)Tab.4 Comparison of the expression of cholesterol uptake and transport-related genes among all groups
注:與正常組比較,* P <0.05;與瘤體小組比較,▲P <0.05;Stard3 又名Mln64,Npc1 又名Nmf164。Note.* P <0.05,compared with the control group;▲P <0.05,compared with the small tumor group.Stard3 also known as Mln64.Npc1 also known as Nmf164.
組別Groups Srb1 Ldlr Npc1 Npc2 Stard3正常組Control group 1.00±0.21 1.00±0.13 1.00±0.21 1.00±0.02 1.00±0.28瘤體大組Large tumor group 1.89±0.24* 2.20±0.47*▲ 1.24±0.11 0.83±0.09 1.06±0.08瘤體小組Small tumor group 1.35±0.21 1.33±0.15 1.16±0.13 0.92±0.06 1.29±0.11
2.4 腎上腺皮質細胞膽固醇合成、轉化與流出相關基因表達
與正常組比較,瘤體大組肝癌小鼠酰基輔酶A:膽固醇酰基轉移酶(Acat1)與膽固醇逆向流出胞外的三磷酸腺苷結合盒轉運蛋白體G1(Abcg1)基因表達顯著下降(P <0.05);與瘤體小組比較,瘤體大組肝癌小鼠酯化膽固醇的激素敏感脂肪酶(Lipe)、Acat1、Abca1 基因表達顯著下調(P <0.05);然而,內質網膽固醇合成的3-羥基-3-甲基戊二酰輔酶A還原酶(Hmgcr)各組間差異無顯著性(見表5)。
2.5 調節膽固醇穩態分子的基因表達
與正常組比較,瘤體大組肝癌小鼠肝X 受體β(Lxrβ)與載脂蛋白a1(Apoa1)基因表達顯著升高(P<0.05),瘤體小組肝癌小鼠固醇調節元件結合蛋白-1c(Srebp-1c)、Lxrβ 基因 表達明 顯升高(P <0.05),而Apoa1 表達顯著下調(P <0.05);與瘤體小組比較,瘤體大組肝癌小鼠Srebp-1c 和Apoa1 顯著升高(P <0.05),而肝X 受體α(Lxrα)與載脂蛋白e(Apoe)基因表達各組間差異無顯著性(見表6)。
2.6 腎上腺SRB1 與ApoA1 蛋白表達
與正常組比較,瘤體大組肝癌小鼠腎上腺SRB1蛋白表達顯著升高(P <0.05),而瘤體小組ApoA1蛋白表達顯著下降(P <0.05);且瘤體大組肝癌小鼠ApoA1 蛋白表達顯著高于瘤體小組(P <0.05)(見圖1A、B)。
表5 各組小鼠腎上腺細胞膽固醇合成、轉化、流出相關基因表達(±s)Tab.5 Comparison of expression of cholesterol synthesis,transform and efflux-related genes in all groups
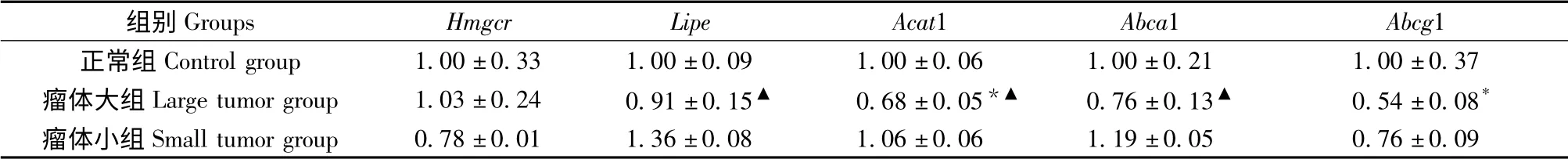
表5 各組小鼠腎上腺細胞膽固醇合成、轉化、流出相關基因表達(±s)Tab.5 Comparison of expression of cholesterol synthesis,transform and efflux-related genes in all groups
注:與正常組比較,* P <0.05;與瘤體小組比較,▲P <0.05;Lipe 又名Hsl。Note.* P <0.05,compared with the control group;▲P <0.05,compared with the small tumor group.Lipe also known as Hsl.
組別Groups Hmgcr Lipe Acat1 Abca1 Abcg1正常組Control group 1.00±0.33 1.00±0.09 1.00±0.06 1.00±0.21 1.00±0.37瘤體大組Large tumor group 1.03±0.24 0.91±0.15▲ 0.68±0.05*▲ 0.76±0.13▲ 0.54±0.08*瘤體小組Small tumor group 0.78±0.01 1.36±0.08 1.06±0.06 1.19±0.05 0.76±0.09
表6 各組小鼠腎上腺細胞膽固醇穩態調節分子基因表達(±s)Tab.6 Comparison of the expression of cholesterol homeostasis-related genes in the mice of all groups

表6 各組小鼠腎上腺細胞膽固醇穩態調節分子基因表達(±s)Tab.6 Comparison of the expression of cholesterol homeostasis-related genes in the mice of all groups
注:與正常組比較,* P <0.05;與瘤體小組比較,▲P <0.05。Note.* P <0.05,compared with the control group;▲P <0.05,compared with the small tumor group.
組別Groups Srebp-1c Lxrα Lxrβ Rxrα Apoa1 Apoe正常組Control group 1.00±0.12 1.00±0.25 1.00±0.09 1.00±0.10 1.00±0.21 1.00±0.09瘤體大組Large tumor group 1.06±0.19▲ 0.81±0.13 1.52±0.32* 1.30±0.28 1.79±0.16*▲ 1.11±0.08瘤體小組Small tumor group 1.88±0.21* 1.12±0.12 1.40±0.06* 1.38±0.06* 0.18±0.01*1.24±0.03
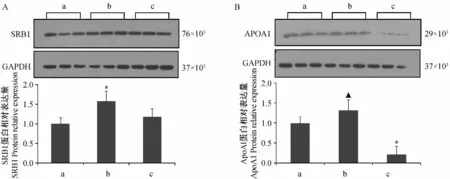
圖1 SRB1(A)、ApoA1(B)蛋白相對表達量Fig.1 SRB1 (A)and ApoA1 (B )protein relative expression in the mice
3 討論
膽固醇是腎上腺皮質細胞合成類固醇激素的重要前體物質,在肝癌疾病狀態下,機體為適應腫瘤的慢性反復應激,腎上腺皮質需合成糖皮質激素以抵御應激反應,因此,維持腎上腺皮質細胞充裕的膽固醇是必需的。課題組對各組小鼠血漿激素檢測結果表明[6],腫瘤形成后,小鼠血漿皮質酮水平均高于正常對照組,且瘤體越大者,血漿促腎上腺皮質激素含量顯著升高,并存在垂體-腎上腺皮質軸的負反饋機制。那么,對于皮質激素合成前期過程而言,與肝細胞、主動脈內皮細胞、巨噬細胞類似,腎上腺皮質細胞也存在一套精密的調控膽固醇穩態機制,既可通過質膜上高密度脂蛋白受體和低密度脂蛋白受體攝入血液中的膽固醇并儲存于脂滴中備用,又可在內質網中從頭合成膽固醇,此外,胞內過量的膽固醇還將通過三磷酸腺苷結合盒轉運蛋白體相關蛋白逆向流出胞外,而且,肝X 受體、固醇調節元件結合蛋白、過氧化物酶體增殖物激活受體等信號分子還參與細胞內膽固醇的維穩過程[8,9]。因此,生理狀態下,腎上腺皮質細胞能充分協調有效利用各種途徑的膽固醇并轉運至線粒體內合成類固醇激素,在腫瘤病理狀態下,有報道顯示膽固醇代謝、血清膽固醇水平及膽固醇合成抑制劑與結直腸癌的關系密切[10],那么,在腫瘤慢性應激過程中,腎上腺皮質細胞對膽固醇的利用如何?我們以H22 肝癌小鼠為觀察對象,深入研究不同大小肝癌的小鼠腎上腺皮質細胞膽固醇攝入、運輸、轉化、合成、流出及其參與維穩的調控分子表達差異,以闡明腫瘤對腎上腺皮質激素合成前膽固醇利用與穩態的影響。
基于Srb1 與Apoa1 協同作用是小鼠腎上腺皮質細胞攝取血漿膽固醇的主要方式,而Ldlr 對膽固醇的內吞作用也很重要,結果表明腫瘤越大,肝癌小鼠腎上腺Srb1、Apoa1、Ldlr 基因表達升高越顯著(P<0.05),相應的蛋白表達檢測顯示腫瘤大組腎上腺SRB1 蛋白表達顯著升高(P <0.05)、而ApoA1蛋白表達在腫瘤大組明顯高于腫瘤小組(P <0.05),提示腫瘤越大,肝癌小鼠為適應腫瘤慢性反復的應激,需要攝取更多的膽固醇用于合成皮質激素以抵御應激。Lipe 主要將脂滴中酯化膽固醇分解為游離膽固醇,而Acat1 則是將攝入的膽固醇通過酯化形式儲存于脂滴中,結果顯示腫瘤大組肝癌小鼠腎上腺Lipe 和Acat1 基因表達顯著低于腫瘤小組(P <0.05),提示腫瘤大的肝癌小鼠為適應腫瘤慢性反復的應激,隨時啟動fight or flight response、相比脂滴中膽固醇的儲備量減少。然而,Abca1 和Abcg1主要負責將胞內過量的膽固醇逆向轉出胞外,結果顯示腫瘤大組肝癌小鼠腎上腺Abca1 和Abcg1 基因表達顯著低于腫瘤小組(P <0.05),提示腫瘤大的肝癌小鼠腎上腺皮質細胞內膽固醇流程減少,主要用于線粒體內合成皮質激素。然而內質網自身合成膽固醇的關鍵酶Hmgcr 在各組間無顯著性變化。
細胞主要通過調節膽固醇的胞內合成、胞外攝取、酯化及外流等途徑之間的平衡以維持正常的胞內膽固醇濃度,其中,Lxr 和Srebps 對維持細胞內膽固醇平衡發揮重要作用。結果顯示腫瘤大組肝癌小鼠腎上腺Srebp-1c、Lxrα 與Rxrα 基因表達無明顯變化,而腫瘤小組Srebp-1c、Lxrβ 與Rxrα 基因表達顯著升高(P <0.05),提示腫瘤越大,因膽固醇更多用于運輸至線粒體內合成皮質激素、流出胞外減少,相應地調節腎上腺皮質細胞內膽固醇穩態的能力減弱。
綜上,本研究發現,在肝癌狀態下,小鼠血漿HDL-C 含量下降,提示肝臟膽固醇代謝能力減弱,為適應腫瘤慢性反復的應激,瘤體越大者,維持胞內膽固醇穩態能力越弱,即儲存于脂滴和流出胞外的膽固醇減少,相反,腎上腺皮質細胞通過攝取血膽固醇并即刻轉運至線粒體內合成糖皮質激素,而以適應機體的各種應激反應。結合課題組張園園等研究結果[11],化療藥物局部介入治療聯合索拉非尼灌胃治療對H22 肝癌小鼠抑瘤作用好,且對中醫氣血陰陽證候有影響,本研究結果將有助于從內分泌角度拓展認識腫瘤對機體的影響。
[1]Yang T,Espenshade PJ,Wright ME,et al.Crucial step in cholesterol homeostasis:sterols promote binding of SCAP to INSIG-1,a membrane protein that facilitates retention of SREBPs in ER[J].Cell,2002,110:489 -500.
[2]Kalaany NY,Gauthier KC,Zavacki AM,e t al.LXRs regulate the balance between fat storage and oxidation[J].Cell Metab,2005,1:231 -244.
[3]Miller WL,Auchus RJ.The molecular biology,biochemistry,and physiology of human steroidogenesis and its disorders[J].Endocr Rev,2011,32:81 -151.
[4]Cummins CL,Mangelsdorf DJ.Liver X receptors and cholesterol homeostasis:spotlight on the adrenal gland[J].Biochem Soc Trans,2006,34:1110 -1113.
[5]Xia X,Jung D,Webb P,et al.Liver X receptor β and peroxisome proliferator-activated receptor δ regulate cholesterol transport in murine cholangiocytes[J].Hepatology,2012,56:2288-2296.
[6]潘志強,方肇勤,盧文麗,等.不同程度邪毒證H22 肝癌小鼠血液激素含量動態變化分析[J].中國中西醫結合雜志,2012,32:1361 -1365.
[7]Livak KJ,Schmittgen TD.Analysis of relative gene expression data using real-time quantitative PCR and the 2(-Delta Delta C(T))method[J].Methods,2001,25:402 -408.
[8]Yang F,Vought BW,Satterlee JS,et al.An ARC/mediator subunit required for SREBP control of cholesterol and lipid homeostasis[J].Nature,2006,442:700 -704.
[9]Zelcer N,Hong C,Boyadjian R,et al.LXR regulates cholesterol uptake through Idol-dependent ubiquitination of the LDL receptor[J].Science,2009,325:100 -104.
[10]楊永濤,盛華,李志文,等.膽固醇代謝與結直腸癌的關系及其機制[J].中華內分泌代謝雜志,2014,30(3):254-257.
[11]張園園,方肇勤,王艷明.不同治療方案對H22 肝癌荷瘤小鼠的療效比較[J].中國實驗動物學報,2014,22(3):67 -71,77.

