兩種方法檢測血紅蛋白H百分比一致性比較*
王阿慧,凌艷英,莊秋容,鄧家德
(廣東省廣州市第一人民醫院檢驗科 510180)
?
·臨床研究·
兩種方法檢測血紅蛋白H百分比一致性比較*
王阿慧,凌艷英,莊秋容,鄧家德
(廣東省廣州市第一人民醫院檢驗科 510180)
目的 比較高效液相色譜方法(HPLC)和醋酸纖維素薄膜堿性電泳(CAFE)方法對血紅蛋白(Hb)H定量的一致性。方法 采用HPLC和CAFE對廣州市第一人民醫院已行基因確診的50例缺失型Hb H病患者標本進行檢測,詳細記錄和分析其相關血液學指標。結果 缺失型HbH病患者經HPLC檢測可出現特異HbH異常峰,出峰時間為(0.42±0.05)s,CAFE可得到特異的HbH帶。兩種方法得到的HbH百分比經配對t檢驗差異無統計學意義(P>0.05)。結論 HPLC是一種高效快速檢測HbH的方法,是能滿足臨床快速檢測缺失型HbH病的有效手段。
缺失型血紅蛋白H病; 高效液相色譜方法; 醋酸纖維素薄膜堿性電泳
海洋性珠蛋白生成障礙性貧血是我國華南地區常見的以慢性進行性溶血為特點的一組遺傳病。根據臨床表現的嚴重程度,α珠蛋白生成障礙性貧血可分為靜止型、輕型、中間型和重型。血紅蛋白(Hb)H病屬于α珠蛋白生成障礙性貧血的中間型,由于4個α基因中有3個缺失或缺陷,α鏈嚴重合成不足,相對過剩的β鏈自行聚合為4聚體即HbH。HbH性質不穩定,易形成包涵體沉積在紅細胞內,使紅細胞在通過脾臟時易于被破壞,出現貧血等癥狀[1]。由于珠蛋白生成障礙性貧血除干細胞移植外,尚無有效治療手段,因此采用相應技術方法,篩查出高風險夫婦,并采取孕期產前診斷以阻止重癥患兒出生,是國內外公認的首選預防措施[2]。缺失型HbH病在外周血中可檢測出HbH。傳統的檢測HbH的常用方法有醋酸纖維素膜堿性電泳(CAFE)、Hb電泳、包涵體試驗等。本試驗中采用堿性CAFE及高效液相色譜方法(HPLC)檢測HbH百分比,以比較二者之間的一致性。
1 資料與方法
1.1 一般資料 全部病例為2012~2013年在廣州市第一人民醫院診治的患者,經基因檢測為α珠蛋白生成障礙性貧血缺失型HbH病50例。抽取患者4 mL肝素鋰抗凝血備用。
1.2 儀器與試劑 美國Bio-Rad公司Variant Ⅱ Hb HPLC分析系統及配套β-thalassemia試劑;北京市六一儀器廠生產的DYY-2C型電泳儀及電泳槽。其他試劑為一般分析純。
1.3 Hb HPLC分析 取肝素鋰抗凝全血4 mL,無需制備溶血液直接進行高效液相色譜分析。按儀器說明書操作,Hb各成分定量約7 min后由HPLC分析儀自動分析計算。
1.4 CAFE HbH定量肝素鋰抗凝血,用四氯化碳抽提制備Hb液,取20 μL加樣于已浸透Tris緩沖液的醋酸纖維素薄膜上,置于pH8.6的硼酸緩沖液中電泳約30 min,分別剪取HbA2、HbA、HbH,加蒸餾水浸泡,待Hb完全洗脫后,用723分光光度計以415 nm波長比色,計算HbH百分比。
1.5 統計學處理 采用SPSS19.0統計軟件進行分析,兩種方法得到的HbH百分比比較采用配對t檢驗,以P<0.05為差異有統計學意義。
2 結 果
2.1 分離HbH條帶 將抗凝血球用生理鹽水洗滌,四氯化碳萃取Hb液,以20 μL量點樣于醋酸纖維素薄膜上,經pH8.6的堿性緩沖液電泳可獲得HbH條帶。圖1示自負極向正極泳動條帶依次為HbA2(HbH患者標本中HbA2降低顯著,電泳時HbA2帶隱約可見)、HbA、HbH。將條帶依次剪下,洗脫于相應體積蒸餾水中并用723分光光度計以415 nm波長處比色,經計算即可獲得HbH占Hb的百分含量,計算公式為:HbH(%)=2×AHbH/(5×AHbA+2×AHbH+AHbA2)%。
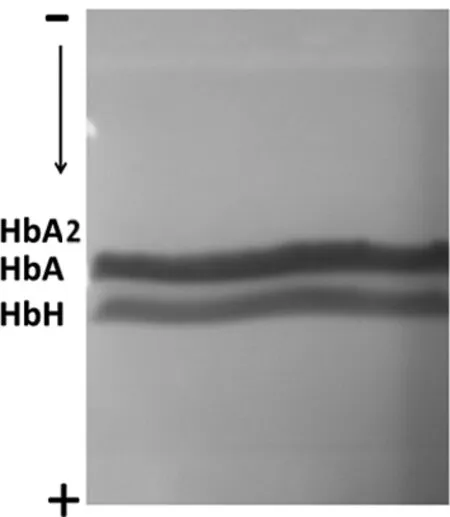
圖1 Hb經CAFE分離出HbH條帶(pH 8.6)
2.2 HPLC檢測HbH 取肝素鋰抗凝全血4 mL,無需前處理直接上樣于Variant Ⅱ HPLC分析儀,約7 min后得到分析圖譜,相應出峰時間范圍可見一明顯的異常洗脫峰,見圖2、3。在設置中將START TIME由0.55 s改為0.00 s,顯示按出峰時間(0.42±0.05)s對應異常峰的峰面積即是HbH百分比。
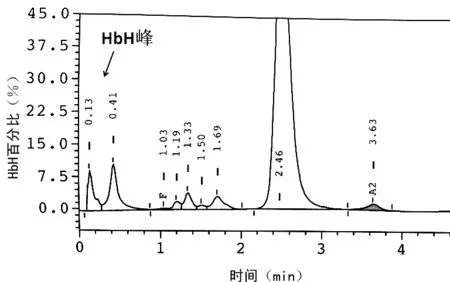
圖2 HPLC檢測HbH可見HbH異常峰
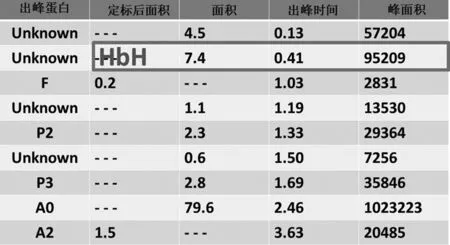
圖3 HbH患者HPLC圖分析結果
2.3 兩種方法檢出HbH百分比的一致性比較 CAFE測得HbH百分比為(7.96±3.01)%,HPLC為(8.06±3.04)%。兩種方法測得的HbH百分比采用配對t檢驗,其差異無統計學意義(P>0.05)。
3 討 論
臨床上篩查常用檢測Hb的方法有Hb電泳、紅細胞指數、紅細胞脆性試驗等。這些方法雖操作要求低,成本低廉,但又因其敏感性和特異性較低,人為影響因素較大,存在較多漏診和誤診現象。目前臨床上對珠蛋白生成障礙性貧血的診斷和鑒別主要依靠Hb分析,該方法所用標本無需前處理,容易操作,并進行質控,準確性和重復性也比較好[3]。
近年來發展起來的基于陽離子交換的HPLC是以物理化學原理為主的分離分析方法,特別適合于生物大分子,如各種蛋白組分的分離,已實現高通量全自動化分析,操作簡單,人為因素影響少。在分離的同時,根據出峰位置可以定性;根據峰面積可以定量,選擇性、靈敏度、準確性高,適合目前珠蛋白生成障礙性貧血大規模篩查與常規診斷[4]。HPLC已成為目前對于珠蛋白生成障礙性貧血非基因檢測手段中最經典的方法,廣泛應用于臨床。尤其在對于β-珠蛋白生成障礙性貧血的檢測,HPLC是介于篩查和確診之間的一種理想方法,已被國際珠蛋白生成障礙性貧血協會推薦為β-珠蛋白生成障礙性貧血的常規篩查方法[5]。
Variant Ⅱ β-thalassemia Short program HPLC分析系統專用于檢測β-珠蛋白生成障礙性貧血且可同時檢測各種異常Hb。盡管對于α-珠蛋白生成障礙性貧血的檢測存在一定的漏檢,但是對于缺失型HbH病患者,異常HbH的檢出還是有優勢的[6]。本文比較應用CAFE和HPLC Hb分析儀在定量HbH方面是否存在一致性,以本院已行基因確診的50例缺失型HbH病患者標本進行檢測,經HPLC檢測出現異常峰標本,CAFE均能發現HbH帶。有研究顯示,CAFE對于HbH的分離能力要優于瓊脂糖凝膠電泳,可清楚地分離出HbH帶及HbBart′s帶[7-8]。但是作為手工法,CAFE存在很多不足,分辨率較差僅能分辨出HbH、HbBartS、HbA、HbA2條帶,操作較繁瑣費時且影響因素多,重復性差。醋酸纖維素薄膜脆而易碎,區帶顏色易掉,不易保存。而HPLC可快速高效地分離出Hb各組分,重復性高[9]。本次研究使用的全自動Hb分析儀采用HPLC對人Hb、HbA2及HbF進行自動化定量測定,可將珠蛋白生成障礙性貧血初步分類為α珠蛋白生成障礙性貧血和β珠蛋白生成障礙性貧血,同時還可檢出HbH、HbS、HbE、HbQ、HbJ等異常Hb,具有高效快速,自動化程序高,準確性和重復性良好等優點,是介于篩查和確診的試驗。
但在實踐工作中,必須根據特定儀器及配套試劑的適應范圍,總結經驗,并結合受檢者家族史,血液學表型紅細胞指數等其他實驗室檢查結果,進行綜合分析,以避免誤診和漏檢。
[1]鄧家棟,揚崇禮,揚天楹,等.臨床血液學[M].上海:上海科學技術出版社,1985:623-624.
[2]Chen FE,Ooi C,Ha SY,et al.Genetic and clinical features of hemoglobin H disease in Chinese patients[J].N Engl J Med,2000,343(8):544-550.
[3]馬升俊,肖永君,韋子斌,等.全自動血紅蛋白分析儀在地中海貧血篩查診斷中的應用[J].中國醫藥導報,2013,10(9):92-93.
[4]Colah RB,Surve R,Sawant P,et al.HPLC studies in hemoglobinopathies[J].Indian J Pediatrics,2007,74(7):657-662.
[5]鄭琳,黃海龍,范向群,等.高效液相色譜技術檢測β-地中海貧血的臨床價值探討[J].中國婦幼保健,2011,26(11):1665-1666.
[6]彭建宏,劉運科,肖春燕.離子交換高效液相色譜法血紅蛋白分析篩查地中海貧血的研究[J].國際醫藥衛生導報,2012,18(4):539-543.
[7]Liao C,Zhou JY,Xie XM,et al.Screening for Hb constant spring in the Guangdong province,South China,using the sebia capillary electrophoresis system[J].Hemoglobin,2011,35(1):87-90.
[8]陳永秀,周云珍,陳錦宏,等.兩種電泳方法血紅蛋白分析一致性的比較[J].檢驗醫學,2013,28(3):229-232.
[9]謝建紅,張永良,肖奇志,等.應用高效液相色譜法檢測β-地中海貧血及異常血紅蛋白[J].廣東醫學,2011,32(11):1473-1476.
醫學統計工作的基本內容
按工作性質及其先后順序,可將醫學統計工作分為實驗設計、收集資料、整理資料、分析資料。實驗設計是開展某項醫學研究工作的關鍵,包括醫學專業設計和統計學設計,醫學專業設計的內容包括研究對象納入和排除標準、樣本含量、獲取樣本的方法、分組原則、觀察(檢測)指標、統計方法等。收集資料的方法包括各種試驗、檢測或調查,要求資料完整、準確、及時、有足夠數量、具有代表性和可比性等。整理資料包括原始資料的檢查與核對、對資料進行分組與匯總等。分析資料即對資料進行統計學分析,包括進行統計描述和統計推斷。
廣東省廣州市醫藥衛生科技項目(20131A011013)。
10.3969/j.issn.1672-9455.2015.03.040
A
1672-9455(2015)03-0385-02
2014-08-07
2014-10-28)

