煤焦油中芳烴(萘)的加氫飽和試驗
夏良燕,夏芝香,方夢祥,唐 巍,王勤輝,駱仲泱
(浙江大學 能源清潔利用國家重點實驗室,浙江 杭州310027)
世界原油供應日益緊張,煤、焦油等非常規能源的利用受到了越來越多的關注.《2012—2016年煤焦油行業投資分析及投資前景預測報告》指出,2011年中國煤焦油的總產能約為2 200萬噸,其中低溫煤焦油產能接近1 000萬噸.由于煤炭氣化、液化、煤基多聯產技術的發展[1],煤焦油產量仍將呈現增加的趨勢,因此,在我國發展煤焦油加氫制取燃料油技術具有廣闊的前景.
煤焦油作為煤熱解的副產物,其組成成分非常復雜,主要為碳氫化合物,且以芳烴類為主,并有一些含硫、氮和氧等雜原子的芳香族化合物[2].與石油相比,煤焦油中的S質量分數較低,N、O和芳烴的質量分數較高.大量的芳烴不易燃燒充分,不僅降低了油品的質量,還會增加空氣中固體顆粒物含量[3].因此,脫芳烴已經成為煤焦油加氫精制工藝中的重要環節.
優化加氫工藝和研制高性能催化劑是促進煤焦油中芳烴加氫的重要措施.朱紅英等[4]用 Ni/γ-Al2O3加氫催化劑,在固定床反應器中考察了萘的飽和加氫反應,得出在體積空速0.6~6.0 h-1,反應溫度210~250℃,壓力不低于5.4 MPa的條件下,萘的轉化率能達到100%,且十氫萘的選擇性較高.Zhang等[5]考察了萘在Ni2P/SiO2催化劑上的加氫反應,萘的轉化率約為65%,但是添加質量分數為0.1%的喹啉(約0.01%N)和0.3%的喹啉(約0.03%N)時,萘的轉化率分別下降了10%和15%.添加質量分數為0.03%的二苯并噻吩(dibenzothiophene,DBT)(約0.005%S)和0.05%的DBT(約0.009%S)時,萘的轉化率分別下降了2%和4%.這些實驗室自行開發的催化劑用于煤焦油中的芳烴加氫,往往存在反應條件和實際煤焦油加氫工業不符,反應液中雜原子明顯抑制芳烴加氫等問題,距離大規模工業應用還有一段距離.傳統石油加氫工業的催化劑具有成熟的技術,如能直接用于煤焦油加氫工程,可避免催化劑開發的問題,但是需要提出合適的煤焦油加氫工藝.
為了優化煤焦油脫芳烴的工藝,本研究使用石油工業中的Mo NiWP/γ-Al2O3催化劑,選取煤焦油中含量較高的雙環化合物萘作為模型化合物,考察反應溫度、壓力、體積空速和氫油體積比對芳烴加氫飽和反應的影響.分別根據煤焦油原料油、經過一次脫硫脫氮后的煤焦油以及合格燃料油[6-7]中硫、氮、氧等雜原子的濃度,選取DBT、喹啉和鄰甲酚作為模型化合物,研究不同質量分數的S、N、O對芳烴加氫飽和反應的影響.同時,根據低溫煤焦油中芳烴的種類[8],初步考察多種芳烴混合物加氫飽和的效果.
1 實驗部分
1.1 實驗儀器與試劑
萘的加氫反應在自制的固定床加氫試驗臺上進行,其工藝流程如圖1所示.該系統主要由3部分組成,包括進料單元、加氫反應單元和產品收集單元.進料單元包含進氣系統和進液系統,分別由加壓氣路和高壓恒流泵控制.加氫反應單元由預熱器和固定床反應器構成,其中不銹鋼反應管內徑為8 mm.產品收集單元包括冷凝器和氣液分離器.
氣相色譜儀為安捷倫科技有限公司生產的7890A型,采用氫火焰離子化檢測器(FID),HP-5毛細柱,N2為載氣.氣相色譜-質譜聯用儀為美國賽默飛世爾集團生產的CDS5200/DSQII型.
試驗所用試劑萘、環己烷、四氫萘、二硫化碳(均為分析純)以及鄰甲酚(化學純)從國藥集團化學試劑有限公司購買;二苯并噻吩(98%)、喹啉(分析純)從阿拉丁試劑有限公司購買,H2從杭州今工特種氣體有限公司購買,體積分數為99.99%.Mo NiWP/γ-Al2O3催化劑由齊魯石油化工有限公司提供,其比表面積大于130 m2/g,活性組分為 WO3、MoO3和NiO,對應的質量分數依次為20.0%±2.0%、10.0%±1.0%以及2.5%±0.5%.
1.2 實驗方法
將Mo NiWP/γ-Al2O3加氫精制催化劑研磨篩分至20~40目后,取1 m L裝填在不銹鋼反應管中部,上、下部分分別裝填4 m L石英砂作為緩沖劑.通入一定量N2保壓8 h,檢查裝置的氣密性.用w(CS2)=5%的環己烷溶液作為硫化液,通入流量為100 m L/min的H2,從20℃以4℃/min的升溫速率升溫至100℃,再以5℃/min的升溫速率升溫至360℃,并保留4 h.預硫化結束后,持續通入H2半小時,吹掃后備用.反應液經高壓恒流泵增壓后送至反應器頂部,與H2混合后進入反應器反應.反應后的產物經冷凝器冷卻后,進入氣液分離器氣液分離.每個反應進行6 h,前3 h保證反應的穩定性,后3 h中每小時收集一次液相產物.產物分別用氣相色譜-質譜聯用儀和氣相色譜儀進行定性、定量分析.每次試驗結束后,用酒精清洗整個裝置.
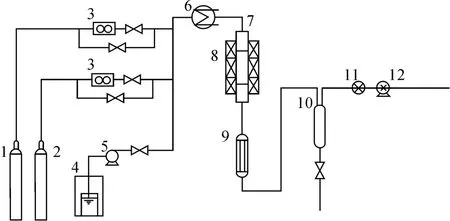
圖1 固定床加氫試驗臺工藝流程圖Fig.1 Schematic diagram of fixed bed reactor for hydrogenation
1.3 計算方法
為了對比加氫反應的效果,選取反應物的轉化率與產物的選擇性作為評價指標.反應物轉化率表示反應物的反應程度,是指某一反應物參加反應的量占加入量的百分率;產物選擇性是指目標產物的摩爾濃度占參加反應的反應物質量分數的百分率,其定義式如下:
轉化率為
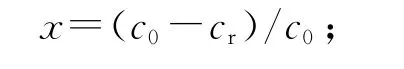
選擇性為
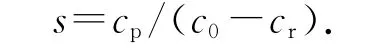
式中:w0為反應物的摩爾濃度,wr為產物中反應物的摩爾濃度,wp為產物中目標產物的摩爾濃度.
2 結果與討論
2.1 萘的加氫產物分析
萘的加氫反應主要產物是四氫萘和十氫萘,根據催化劑以及反應條件的不同,四氫萘與十氫萘的選擇性存在很大差別[9-10].對 Mo NiWP/γ-Al2O3催化劑上萘的加氫產物進行氣質聯用分析,表1為不同停留時間(t1)所對應的物質,由表可發現萘的加氫主要是經逐環加氫反應生成四氫萘和十氫萘,同時發生開環以及異構化反應[11],生成微量乙苯、丁基環己烷、丁基環己烯等.

表1 萘加氫的產物分析_Tab.1 Product analysis of naphthalene hydrogenation
2.2 萘的加氫飽和工藝優化
2.2.1 溫度的影響 圖2為當反應壓力為4 MPa,體積空速為2 h-1,氫油體積比為600:1時,萘的轉化率以及產物分布隨溫度(θ)的變化情況.由圖2可知,在300~340℃,萘的轉化率χNa=100%,四氫萘的選擇性(ste)低于5%,十氫萘的選擇性Sde始終保持90%以上.當溫度高于340℃時,萘的轉化率開始下降,且十氫萘的含量明顯減少.這說明在一定反應條件下,高溫不利于萘的加氫飽和[12].這是因為芳烴加氫飽和反應是可逆強放熱反應,受熱力學平衡控制[13],溫度過高時,平衡向脫氫反應方向移動[14],反而抑制了萘的加氫.
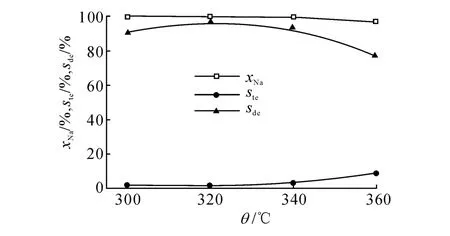
圖2 溫度對萘轉化率及四氫萘和十氫萘選擇性的影響Fig.2 Influence of temperature on naphthalene conversion,tetraline and decalin selectivity
2.2.2 壓力的影響 圖3為當反應溫度320℃,體積空速為2 h-1,氫油體積比為600:1時,萘的轉化率以及產物分布隨壓力(p)變化的情況.由圖3可知,在此反應條件下,萘的轉化率始終保持100%,不受反應壓力的影響.四氫萘的生成量不斷減少,十氫萘的生成量不斷增多.這是由于萘加氫是體積縮小的反應,壓力升高有利于十氫萘的生成.
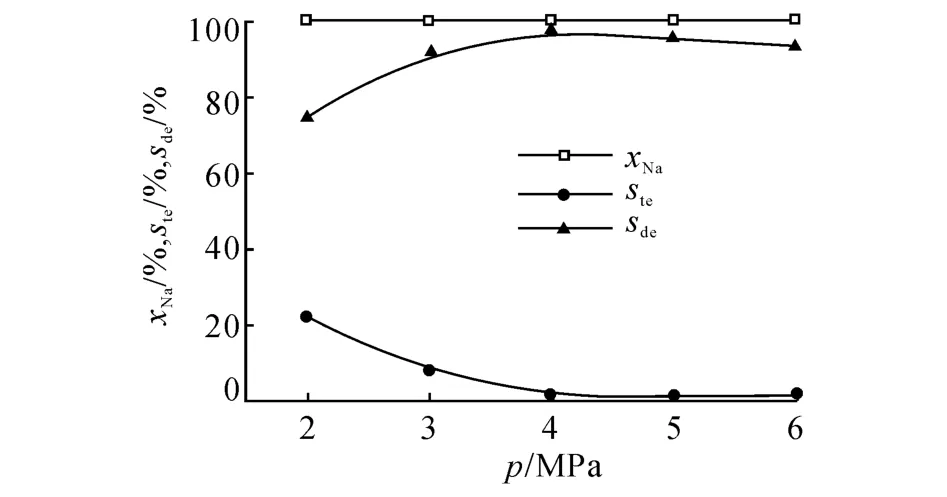
圖3 壓力對萘轉化率及四氫萘和十氫萘選擇性的影響Fig.3 Influence of pressure on naphthalene conversion,tetraline and decalin selectivity
2.2.3 體積空速的影響 圖4為當反應溫度為320℃,反應壓力為4 MPa,氫油體積比為600:1時,萘的轉化率以及產物分布隨液時體積空速(v)變化的情況.當體積空速在1~5 h-1范圍內時,萘在Mo NiWP/γ-Al2O3的加氫轉化率達到100%,且十氫萘具有較高選擇性.當體積空速高于5 h-1時,萘的轉化率開始下降,且十氫萘的量大幅減少.為進一步探究體積空速對萘加氫飽和反應的影響,在相同反應條件下,以四氫萘為反應物進行試驗.當體積空速從6 h-1增加到20 h-1時,萘的轉化率由97.1%下降到94.2%,而對應的四氫萘的轉化率由93.3%下降到54.8%.這是因為隨著體積空速的增大,反應物與催化劑的接觸時間減少,第1步加氫飽和反應(萘轉化為四氫萘)只受到較小的影響,第2步加氫飽和反應(四氫萘轉化為十氫萘)沒有足夠的反應時間.較小的體積空速雖然會大大提高萘的加氫效果,但是在實際工業應用中,會增加反應的氫耗,使催化劑床層溫度升高,不利于工業生產,因此需要選擇合理的體積空速.
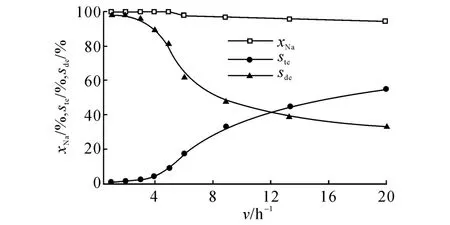
圖4 體積空速對萘轉化率及四氫萘和十氫萘選擇性的影響Fig.4 Influence of space velocity on naphthalene conversion,tetraline and decalin selectivity
2.2.4 氫油體積比的影響 圖5為當反應溫度為320℃,反應壓力為4 MPa,體積空速為2 h-1時,萘的轉化率以及產物分布隨氫油體積比(R)變化的情況.由圖5可知,隨著氫油體積比的增加,萘始終保持100%的轉化率,四氫萘的選擇性基本保持穩定,十氫萘的選擇性隨著氫油體積比的增大而增加.這說明氫油體積比的增加有利于十氫萘的生成.在氫油體積比為800時,十氫萘選擇性出現微小的下降.這可能是由于過高的氫油體積比引起氫分壓的增大,雖然對萘的加氫有促進作用,但是也會稀釋反應物,抑制萘向催化反應活性中心的擴散[15].在工業應用中,過高的氫油體積比也會增加設備投入和操作費用.
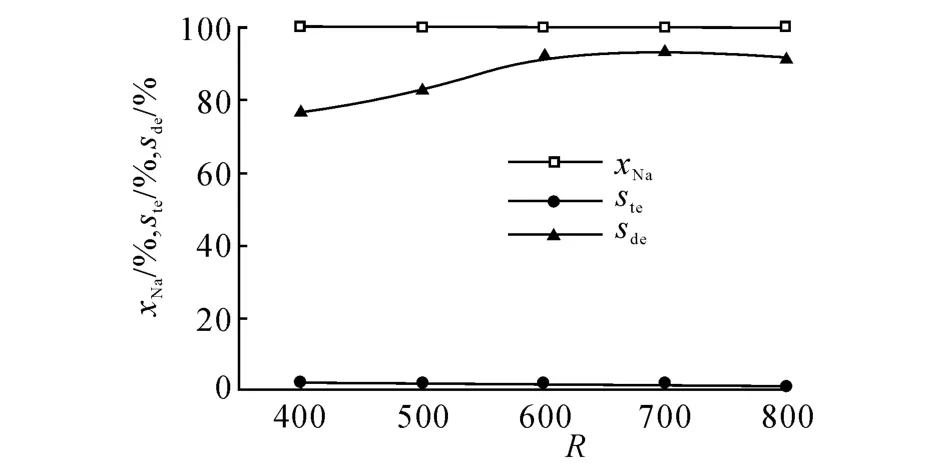
圖5 氫油體積比對萘轉化率及四氫萘和十氫萘選擇性的影響Fig.5 Influence of hydrogen to oil ratio on naphthalene conversion,tetraline and decalin selectivity
通過考察反應條件對萘在 MoNiWP/γ-Al2O3催化劑上加氫飽和反應的影響,可得出如下結果:Mo NiWP/γ-Al2O3催化劑具有很好的芳烴加氫活性,且當反應溫度為320℃,反應壓力為4 MPa,氫油體積比為600:1,體積空速為2 h-1時,具有最佳的加氫效果.
2.3 雜原子對萘加氫飽和的影響
在壓力為4 MPa,溫度為320℃,氫油體積比為600:1的反應條件下,考察DBT、喹啉和鄰甲酚的存在對芳烴加氫反應的影響.
2.3.1 S存在的影響 圖6為不同質量分數的S存在的情況下,反應過程中萘的轉化率及產物分布隨接觸時間的變化.結果表明:添加0.01%S后,萘的轉化率基本沒有下降.當添加0.15%S時,萘的轉化率減小,隨著接觸時間的增加,基本趨于平緩.當少量S(≤0.15%)存在時,四氫萘選擇性下降,十氫萘選擇性呈現增大的趨勢.當添加0.70%S時,萘的轉化率出現了較為明顯的下降,且十氫萘的產量減少.在萘加氫飽和和DBT加氫脫硫反應中,硫物種的存在對催化劑的活性位有競爭吸附,且一部分吸附在催化劑表面的硫化物是不可逆的[16],不利于萘的加氫飽和.當S的質量分數較小時,這種抑制作用表現不明顯;當S的質量分數增加時,芳烴的加氫飽和反應受到明顯的抑制.為了達到較好的芳烴飽和效果,需要選擇具有良好脫硫效果的催化劑,預先脫除原料中的大部分S.
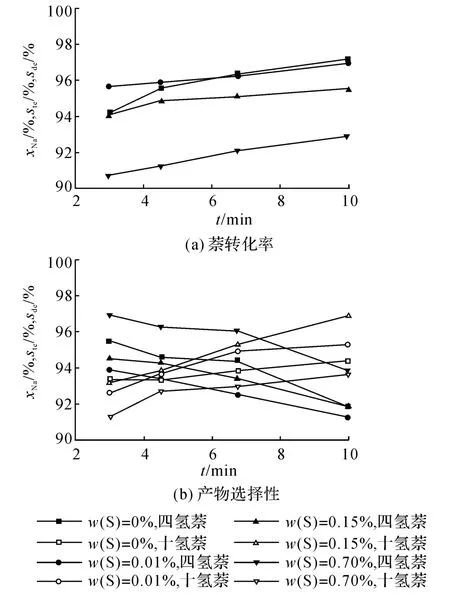
圖6 不同質量分數S的存在隨接觸時間對萘轉化率和產物選擇性的影響Fig.6 Naphthalene conversion,tetraline and decalin selectivity with addition of different mass fraction of DBT as a function of contact time
2.3.2 N的存在的影響 圖7為不同質量分數的N存在的情況下,反應過程中萘的轉化率及產物分布隨接觸時間的變化.當含w(N)=0.01%時,當接觸時間較短時,萘的轉化率有小幅的下降,四氫萘與十氫萘的選擇性有明顯的變化,隨著接觸時間的增加,這種變化均減小.這是由于反應開始時喹啉與萘爭奪催化劑的活性位,隨著接觸時間的增加,少量吸附在活性位上的喹啉開始轉化為吸附性較弱的物質并離開活性位,使得萘能夠更容易吸附于加氫活性位上[17].當接觸時間為10 min時,萘的加氫效果已恢復到不含N的水平,甚至生成了更多的十氫萘.當含w(N)=0.15%時,萘的轉化率大幅下降,且接觸時間從10 min減少到3 min時,萘的轉化率由75%下降為50%.這表明大量的喹啉或者喹啉的加氫產物吸附在催化劑活性點位,使其無法催化萘的加氫反應.當接觸時間減少時,吸附物無法脫附下來.因此當含w(N)=0.15%時,萘轉化率隨接觸時間減小而降低,且下降的幅度遠大于含0.01%的N和不含N時.當含w(N)=0.15%時,十氫萘選擇性非常低,四氫萘選擇性則明顯大于不含N和含有0.01%N時.可見,萘加氫生成四氫萘反應的平衡在N的質量分數較高時容易實現,但是四氫萘進一步加氫為十氫萘則受到了嚴重抑制.諸多研究[18-20]指出,N的存在對加氫脫硫也有一定的負面影響,因此,想要獲得更好的芳烴加氫飽和和脫硫效果,必須選擇一類優質的催化劑,盡可能地脫除其中的含氮化合物.
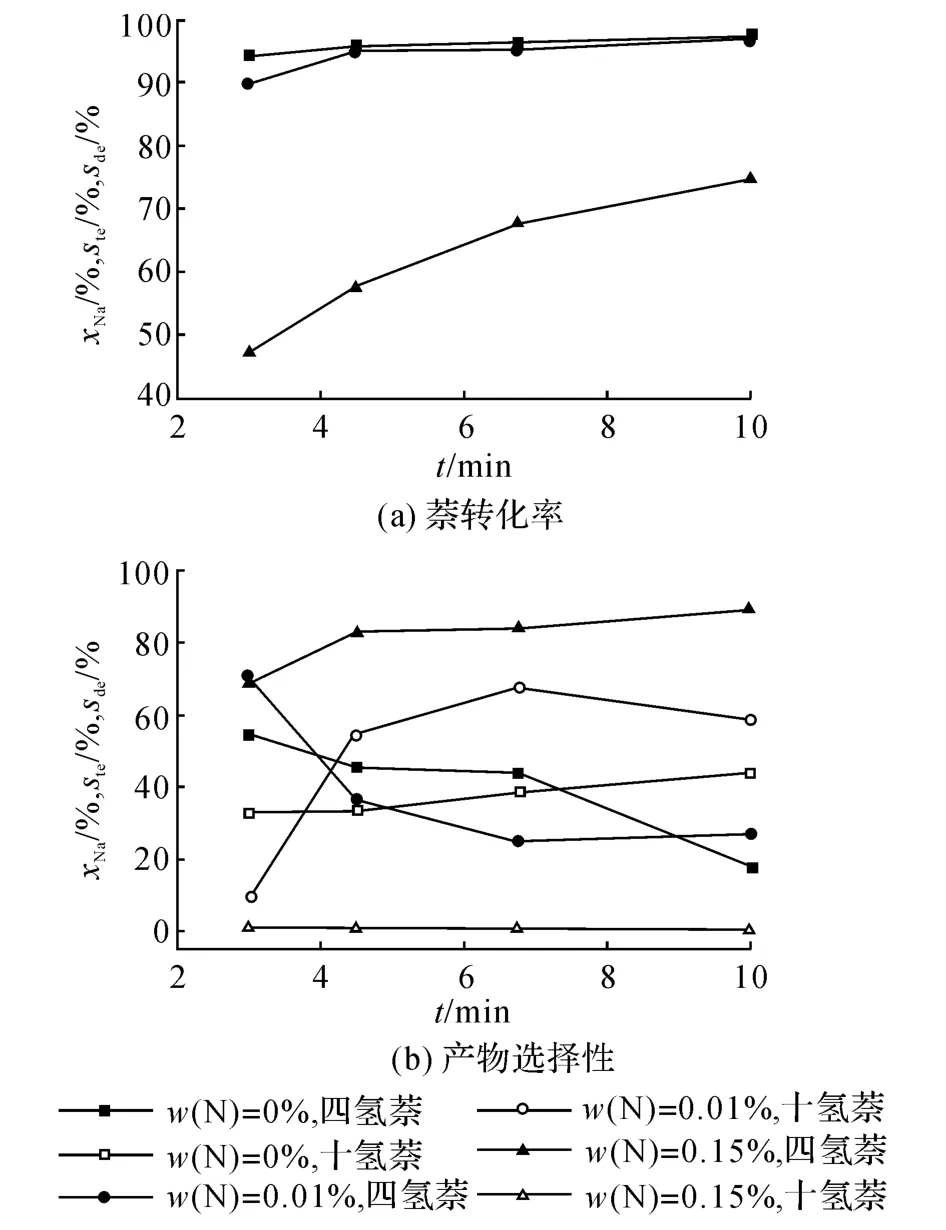
圖7 不同質量分數N的存在隨接觸時間對萘轉化率和產物選擇性的影響Fig.7 Naphthalene conversion,tetraline and decalin selectivity with the addition of different mass fraction of quinoline as a function of contact time
2.3.3 O存在的影響 圖8為不同質量分數的O存在的情況下,反應過程中萘的轉化率及產物分布隨接觸時間的變化.當含w(O)=0.30%時,萘的轉化率有微小的下降,均小于2%,四氫萘與十氫萘的量基本維持原趨勢.當含w(O)=3%時,萘的轉化率下降了8%~10%,特別是接觸時間為3 min時,萘的轉化率甚至低于85%.反應產物中,四氫萘的量有所上升,十氫萘的選擇性基本不變.
鄰甲酚的加氫脫氧主要是2條路徑[21]:一是先直接脫氧生成甲苯,再加氫飽和生成甲基環己烷;二是先發生加氫反應依次生成鄰甲醛和2-甲基環己醇,再經過脫氧反應最終生成甲基環己烷.產物中主要有甲苯和甲基環己烷2種不含O的化合物.表2為當添加不同質量分數的O時,鄰甲酚的轉化率和不含氧化合物的選擇性.當含w(O)=0.30%時,鄰甲酚保持超過99%的轉化率,且表現出良好的脫氧效果.隨著含氧量的增加,鄰甲酚的轉化率大幅下降,且不含氧產物選擇性明顯降低.
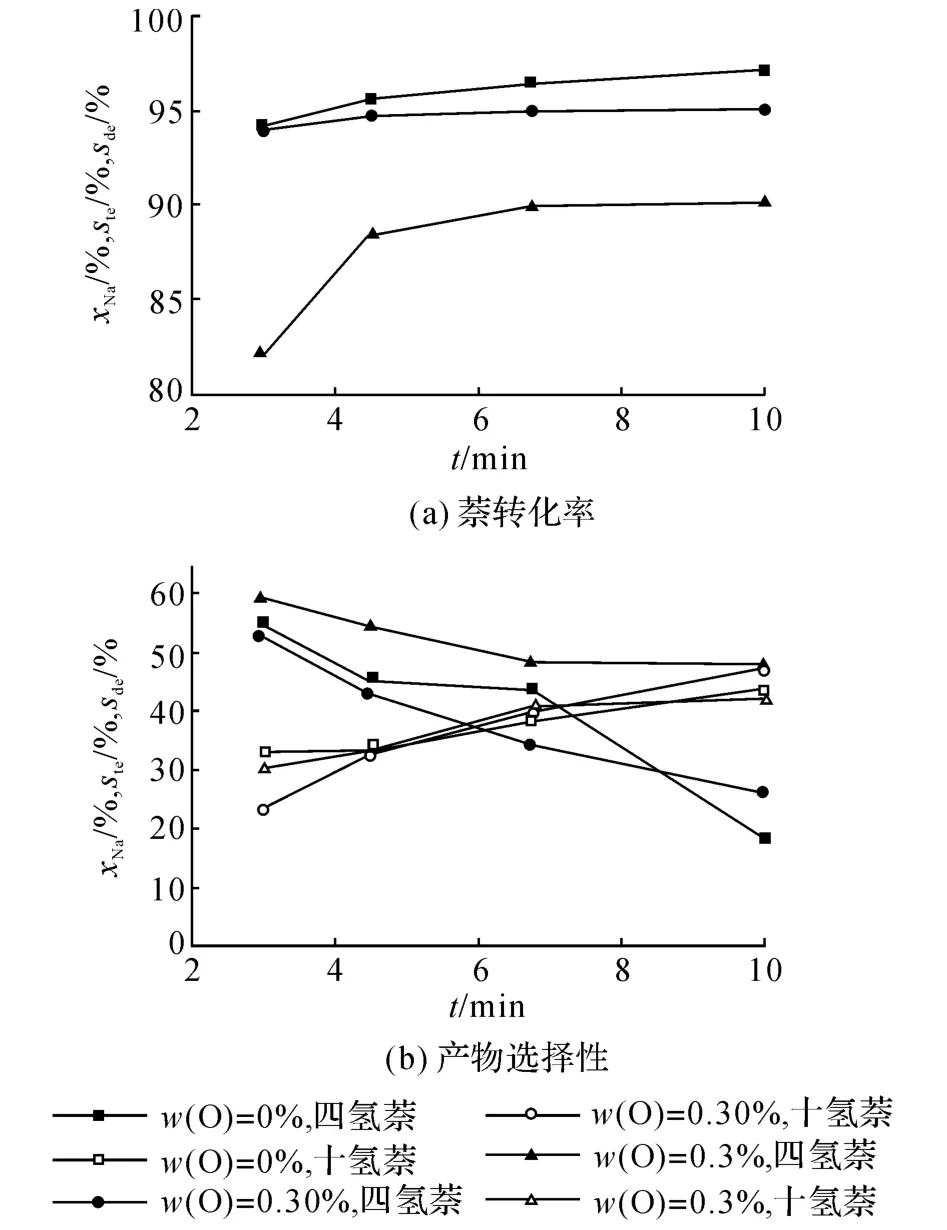
圖8 不同質量分數O的存在隨接觸時間對萘轉化率和產物選擇性的影響Fig.8 Naphthalene conversion,tetraline and decalin selectivity with addition of different mass fraction of o-cresol as a function of contact time
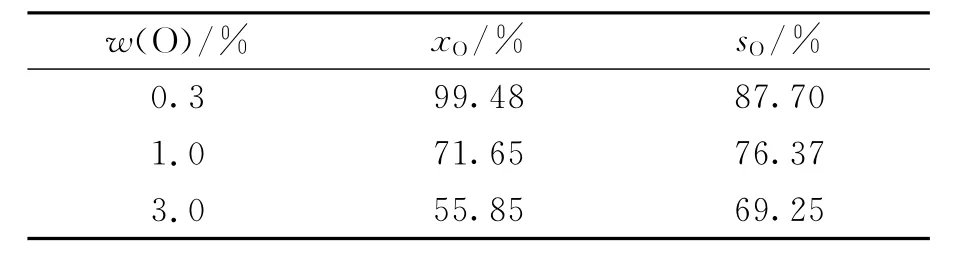
表2 不同氧質量分數O下鄰甲酚轉化率與產物選擇性Tab.2 O-cresol conversion and product selectivity with different mass fractions of O
實驗結果表明:當O的質量分數過高時,C-O鍵的斷裂會更加困難,苯環的加氫飽和也受到抑制,特別是萘中第2個苯環加氫反應.針對煤焦油中含有較多的含氧化合物,需要對煤焦油進行加氫脫氧或預先提酚處理,才能保證芳烴加氫飽和的良好效果.
2.4 低溫煤焦油中多種芳烴混合物的加氫飽和
選取低溫煤焦油中典型的各類化合物,配制煤焦油模擬混合物,在壓力為6 MPa,溫度為360℃,體積空速為0.8 h-1,氫油體積比為1 250:1的反應條件下,考察其中的芳烴加氫飽和效果.煤焦油模擬混合物包含一定質量分數的芳烴類(鄰二甲苯10%、萘20%、菲15%),酚類(鄰甲酚25%),鏈烴類(正十六烷27%),雜原子類(DBT 1%、喹啉2%).表3為反應前后芳烴類的含量變化.單環類芳烴鄰二甲苯很難加氫飽和,隨著芳烴中苯環數目的增加,轉化率大幅提高.混合其他種類芳烴后,萘的主要加氫產物由十氫萘變為四氫萘,這主要是因為菲對十氫萘的生成產生了抑制作用[22].
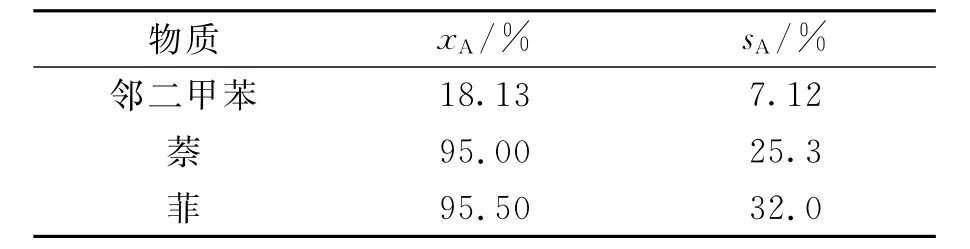
表3 煤焦油模擬混合物中芳烴類轉化率與產物選擇性Tab.3 Aromatic hydrocarbons conversion and product se-______lectivity in simulative mixture of coal tar
實驗結果表明:煤焦油中的芳烴類化合物加氫飽和反應遵循多環化合物(菲)>雙環化合物(萘)>單環化合物(鄰二甲苯),且芳烴類物質之間存在相互影響.
3 結 論
本文以萘為煤焦油中芳烴的模型化合物,從反應工藝的角度對萘催化加氫反應進行了研究,得出了以下結論:
(1)Mo NiWP/γ-Al2O3催化劑對萘的加氫飽和反應具有很好的活性,最佳的反應條件是壓力為4 MPa,溫度為320℃,氫油體積比為600:1,體積空速為2 h-1,適合實際的煤焦油加氫工程.
(2)不同質量分數雜原子的存在對萘的加氫反應有不同的影響.0.01%的S和N幾乎對萘的轉化率沒有影響;隨著S、N質量分數的增加,萘的飽和受到抑制,特別是N的抑制作用更加明顯;O存在會抑制萘的加氫反應.
(3)芳烴類化合物加氫飽和反應存在相互影響,其中萘的完全飽和反應受到明顯的抑制.
在煤焦油加氫精制工程中,為了達到較好的脫芳烴效果,提出以下建議:
(1)采用兩步加氫精制工藝,其中第一步使用商用催化劑中具有良好脫硫、脫氮和脫氧效果的催化劑,減少原料中的S、N和O,第二步使用目前已廣泛應用的商用加氫精制類催化劑進行芳烴的飽和反應.
(2)在煤焦油加氫工程中,考慮預先提取原料中的主要含氧化合物(酚類),可以提高芳烴脫除的效果,同時具有一定的經濟性.
(
):
[1]國家能源局.國家能源科技“十二五”規劃(2011-2015)[R].北京:國家能源局,2011.
[2]肖瑞華.煤焦油化工學[M].2版.北京:冶金工業出版社,2009:8.
[3]SIDHPURIA K B,PATEL H A,PARIKH P A,et al.Rhodium nanoparticles intercalated into montmorillonite for hydrogenation of aromatic compounds in the presence of thiophene[J].Applied Clay Science,2009,42(3):386- 390.
[4]朱紅英,張曄,邱澤剛,等.反應條件對萘飽和加氫的影響 [J].精細化工,2009,26(5):512- 516.ZHU Hong-ying,ZHANG Ye,QIU Ze-gang,et al.Effects of reaction conditions on saturated hydrogenation of naphthalene[J].Fine Chemicals,2009,26(5):512- 516.
[5]ZHANG X F,ZHANG Q M,ZHAO A Q,et al.Naphthalene hydrogenation over silica supported nickel phosphide in the absence and presence of N-containing compounds[J].Energy and Fuels,2010,24(7):3796- 3803.
[6]中華人民共和國國家標準.車用汽油,GB17930-2011[S].北京:中國標準出版社,2011.
[7]中華人民共和國國家標準.車用柴油,GB19147-2013[S].北京:中國標準出版社,2013.
[8]余盼龍.多聯產煤焦油的蒸餾和加氫研究[D].杭州:浙江大學,2013:41- 44.YU Pan-long.Studies for distilling and hydroprocessing on coal tar from polygeneration system[D].Hangzhou:Zhejiang University,2013:41- 44.
[9]殷長龍,劉歡,張勝,等.非負載型NiMoW催化劑催化萘一步加氫合成十氫萘[J].石油煉制與化工,2013,44(10):53- 58.YIN Chang-long,LIU Huan,ZHANG Sheng,et al.Synthesis of decalin by one step hydrogenation of naphthalene on unsupported NiMoW catalyst[J].Petroleum Processing and chemicals,2013,44(10):53- 58.
[10]李望良,柳云騏,劉春英,等.MCM-41負載 Mo-Ni-P催化劑的加氫性能[J].石油學報:石油加工,2004,20(2):69- 74.LI Wang-liang,LIU Yun-qi,LIU Chun-ying,et al.Hydrogenation properties of Mo-Ni-P catalyst on MCM-41 supported[J].Acta Petrolei Sinica:Petroleum Processing Section,2004,20(2):69- 74.
[11]LYLYKANGAS M S,RAUTANEN P A,KRAUSE A O I.Liquid-phase hydrogenation kinetics of multicomponent aromatic mixtures on Ni/Al2O3[J].Industrial and Engineering Chemistry Research,2002,41(23):5632- 5639.
[12]任曉乾,余夕志,李凱,等.高溫下工業NiW/Al2O3催化劑上萘的加氫飽和反應[J].化學工程,2007,35(3):30- 33.REN Xiao-qian,YU Xi-zhi,LI Kai,et al.Reactivity of saturated hydrogenation of naphthalene over the commercial NiW/Al2O3catalyst at high reaction temperature[J].Chemical Engineering,2007,35(3):30- 33.
[13]鞠雪艷,張毓瑩,胡志海,等.Ni-Mo加氫催化劑上1-甲基萘的飽和反應規律[J].石油學報:石油加工,2012,28(4):538.JU Xue-yan,ZHANG Yu-ying,HU Zhi-hai,et al.Hydrogenation saturation discipline of 1-methyl naphthalene over Ni-Mo catalyst[J].Acta Petrolei sinica:Petroleum Processing Section,2012,28(4):538.
[14]DEMIREL B,WISER W H,OBLAD A G,et al.Production of high octane gasoline components by hydroprocessing of coal-derived aromatic hydrocarbons[J].Fuel,1998,77(4):301- 311.
[15]NAGY G,POLCZMANN G,KALLO D,et al.Investigation of hydrodearomatization of gas oils on noble metal/support catalysts [J].Chemical Engineering Journal,2009,154(1):307- 314.
[16]EGOROVA M,PRINS R.Competitive hydrodesulfurization of 4,6-dimethyldibenzothiophene,hydrodenitrogenation of 2-methylpyridine,and hydrogenation of naphthalene over sulfided NiMo/γ-Al2O3[J].Journal of Catalysis,2004,224(2):278- 287.
[17]梁宇通.萘在Ni2P/AC上的加氫飽和及硫氮化合物對其影響[D].大連:大連理工大學,2013:54- 55.LIANG Yu-tong.Hydrogenation of naphthalene on Ni2P/AC catalyst and influences of nitride and sulfide [D].Dalian:Dalian University of Technology,2013:54- 55.
[18]DING L H,ZHENG Y,ZHANG Z S,et al.HDS,HDN,HDA,and hydrocracking of model compounds over Mo-Ni catalysts with various acidities [J].Applied Catalysis A:General,2007,319:25- 37.
[19]LU M H,WANG A J,LI X,et al.Hydrodenitrogenation of quinoline catalyzed by MCM-41-supported nickel phosphides[J].Energy and Fuels,2007,21(2):554- 560.
[20]DUAN X P,TENG Y,WANG A J,et al.Role of sulfur in hydrotreating catalysis over nickel phosphide[J].Journal of Catalysis,2009,261(2):232- 240.
[21]XIA L Y,XIA Z X,TANG W,et al.Hydrogenation of model compounds catalyzed by MCM-41-supported nickel phosphide [J].Advanced Materials Research,2014,864:366- 372.
[22]BELTRAMONE A R,RESASCO D E,ALVAREZ W E,et al.Simultaneous hydrogenation of multiring aromatic compounds over NiMo catalyst [J].Industrial and Engineering Chemistry Research,2008,47(19):7161- 7166.

