白藜蘆醇順反異構體及第一三重激發態結構的理論研究
何云清,胡啟山,胡 文,劉柳斜
(1.四川文理學院化學化工學院,達州 635000; 2.特色植物開發研究四川省高校重點實驗室,達州 635000; 3.四川師范大學化學與材料科學學院,成都 610066)
白藜蘆醇順反異構體及第一三重激發態結構的理論研究
何云清1,2,胡啟山1,2,胡 文1,劉柳斜3
(1.四川文理學院化學化工學院,達州 635000; 2.特色植物開發研究四川省高校重點實驗室,達州 635000; 3.四川師范大學化學與材料科學學院,成都 610066)
在B3LYP/6-311++G(d,p)水平對白藜蘆醇順反異構體及第一三重激發態進行了結構優化、頻率計算和自然鍵軌道(Natural Bond Orbital,NBO)分析.在MP2/6-311++G(d,p)//B3LYP/6-311++G(d,p)水平比較了白藜蘆醇順反異構體的能量.反式白藜蘆醇整個分子呈平面結構,順式白藜蘆醇兩苯環之間存在約30o扭角.第一三重激發態中兩苯環幾乎處于互相垂直的關系,C7-H5與C8-H6鍵也是幾乎互相垂直的關系.順式和反式白藜蘆醇C7-C8的σ鍵成鍵情況分別為sp1.53-sp1.53和sp1.59-sp1.60,C7與C8各自提供p軌道形成π鍵,即形成C7=C8雙鍵.三重態中,C7-C8的成鍵情況為sp1.92-sp1.89,沒有p-p π鍵,C7、C8均還有一個2p軌道未參與雜化,NBO分析證實C7、C8的各自剩下的2p軌道均幾乎獨立形成了高能量的反鍵軌道,分別垂直于單羥基和雙羥基苯環,C7-C8鍵長明顯長于白藜蘆醇順反異構體.順式白藜蘆醇比反式白藜蘆醇的自由能高約1.3-2.5 kcal/mol,反式構型是熱力學穩定構型.含時密度泛函方法(Time-Dependent Density Functional Theory,TD-DFT)方法,B3LYP/6-311++G(d,p)水平計算得反式和順式白藜蘆醇最強紫外吸收峰分別在330 nm和319 nm.
白藜蘆醇; 異構體; 三重態; 自然鍵軌道; 前線軌道; UV
1 引 言
白藜蘆醇(resveratrol)是一種非黃酮類天然活性多酚化合物,廣泛存在于分布于葡萄科(Vitis)、桑科木波羅屬(Artocarpus)、桑屬(Morus)、山毛櫸科假山毛櫸屬(Nothofagus)、松科松屬(Pinus)等植物體內.在自然條件下,它主要以反式構型存在,有抗細菌及真菌、降低血脂、抗血小板凝聚等作用,對動脈粥樣硬化、冠心病具有保護作用,對癌變及細胞組織變異都有抑制作用,對癌癥有化學預防作用,通過抑制cAMP磷酸二酯酶(PDEs)改善由衰老引起的代謝疾病[1-10].白藜蘆醇的功效主要來自于它的反式結構,反式白藜蘆醇在物理及化學因素的誘導下可生成順式異構體[7-9],白藜蘆醇順反異構體結構見圖1.Forster在Muliken研究基礎上,提出烯烴光致異構化反應是在同一個三重態上發生的,順反異構體從各自的最低激發單重態經過系間竄躍到達相應的三重態.Hammond等從實驗上證實烯烴順反異構化反應可以通過三重態有效發生[11,12].劉宇平等對反式白藜蘆醇熱穩定性與光致異構化進行了研究,在4~40℃條件下反式白藜蘆醇溶液避光保存600h濃度沒有明顯下降,在254 nm和365 nm紫外光照射下則迅速發生異構化反應[13].史先敏等的研究則證實反式白藜蘆醇具有光不穩定和熱不穩定性,在光照和/或加熱下有部分轉變為順式白藜蘆醇,反式白藜蘆醇溶液在太陽光照射下其含量迅速減少,溫度的升高對其穩定性影響增加,白藜蘆醇熱穩定性高于光穩定性,樣品在-20、4、30、40、60 ℃放置白藜蘆醇溶液60h,-20和4℃處理的溶液在306 nm的吸光度幾乎沒有變化,31℃處理的溶液306 nm吸光度有少量降低,60℃處理的溶液306 nm處吸光度下降32%[14].文獻[13]報道反式和順式白藜蘆醇最大吸收波長分別為306 nm和286 nm,吳波等[15]的研究表明反式白藜蘆醇在304 nm和325 nm處有較強吸收,從戴蘊青等[9]研究報道的紫外光譜圖可以看出,反式白藜蘆醇在302~322 nm范圍有較強吸收,順式白藜蘆醇在288 nm左右有較強吸收.對白藜蘆醇順反異構體及第一三重激發態的結構進行詳細的理論研究是非常有必要的.本研究采用密度泛函B3LYP[16,17]方法對白藜蘆醇順反異構體及第一三重激發態進行了幾何結構、電子結構的理論研究,采用導體極化連續模型(Conductor-like Polarizable Continuum Model,CPCM)[18,19]方法和考慮相關效應的MP2方法對各結構進行了溶劑化效應和相關效應計算.采用含時密度泛函方法(Time-Dependent Density Functional Theory,TD-DFT)在B3LYP/6-311++G(d,p)水平計算了白藜蘆醇順反異構體的紫外光譜.
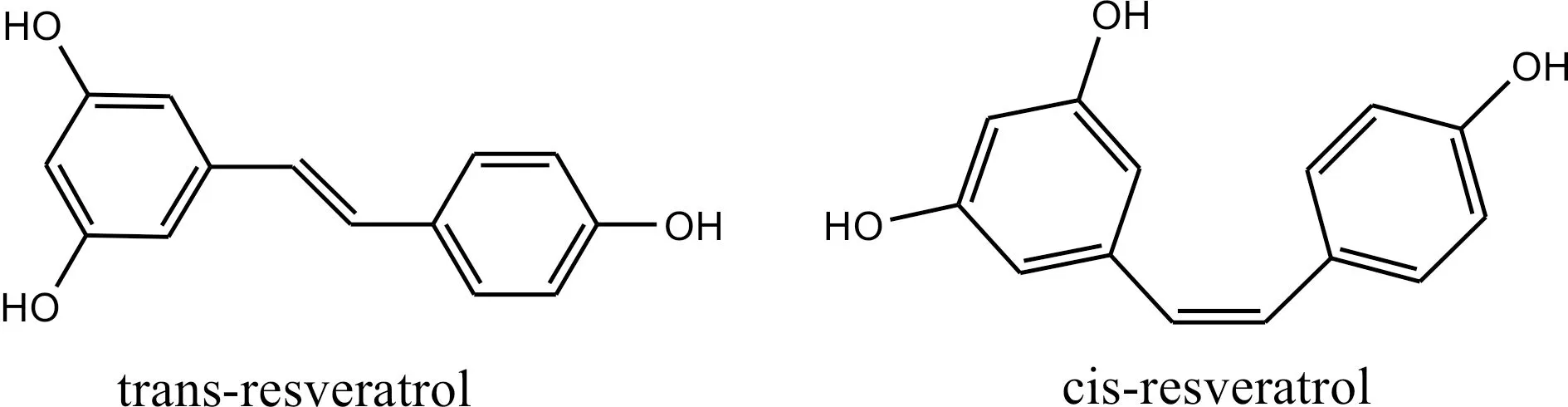
圖1 白藜蘆醇順反異構體Fig. 1 Resveratrol isomers
2 計算方法
在B3LYP/6-311++G(d,p)水平對白藜蘆醇順反異構體及第一三重激發態進行了結構優化、頻率計算和自然鍵軌道(Natural Bond Orbital,NBO)分析.B3LYP/6-311++G(d,p)水平下反式白藜蘆醇優化結構中C4-C7、C7-C8、C8-C9的鍵長分別為1.463、1.346和1.467 ?,C7C8C9C10和C5C4C7C8二面角分別為 -4.00和-3.61度(見表1),對應的晶體X-射線衍射結構參數[20]則分別為1.460、1.333、1.468 ?和-3.0、8.0度,可以看出計算結果與實驗結果吻合得很好,說明B3LYP/6-311++G(d,p)水平計算結果是可靠的.同時,采用上述水平優化結構,在MP2/6-311++G(d,p)水平上計算了白藜蘆醇順反異構體在氣相、乙醇溶液、水溶液條件下的單點能,進行電子相關效應和溶劑化效應校正,采用的溶劑化模型是CPCM模型,該計算水平記為MP2/6-311++G(d,p)//B3LYP/6-311++G(d,p).我們也在MP2/6-311++G(d,p)優化了白藜蘆醇的結構,并沒有獲得跟實驗結果更接近的結構,認為采用考慮電子相關效應的MP2方法優化白藜蘆醇的結構是沒有必要的.所有計算在GAUSSIAN 09程序包[21]上進行.
3 結果與討論
3.1 優化構型
圖2是B3LYP/6-311++G(d,p) 水平優化得到的白藜蘆醇順反異構體和三重態的結構,部分鍵長、鍵角和二面角參數列于表1.
從白藜蘆醇順反異構體結構參數分析:白藜蘆醇順反異構體的各鍵長、鍵角數據很接近,C7-C8鍵長均為1.346 ?,與乙烯的C=C鍵長(1.337 ?)[22]一致;分子的兩苯環中C-C鍵長在1.37-1.41 ?,鍵長介于C=C與C-C單鍵之間,證實苯環的共軛結構;順式白藜蘆醇中C4-C7和C8-C9鍵長分別為1.472和1.477 ?,反式白藜蘆醇中C4-C7和C8-C9鍵長分別為1.463和1.467 ?,均為分子體系中最長C-C鍵,但比C-C單鍵(1.54 ?)短,與C-C單鍵的差小于與C=C的差,表明在白藜蘆醇中C4-C7和C8-C9主要表現為單鍵性質,具有一定的雙鍵性質;反式白藜蘆醇的C7C8C9C10、C9C8C7H5、C5C4C7C8、C4C7C8H6二面角分別為-4.00、-0.64、-3.61和-0.72度,表明C4、C5、C7、C8、C9、C10、H5和H6幾乎在同一平面內,又由于苯環的平面結構,反式白藜蘆醇的所有原子幾乎都在同一平面內;順式白藜蘆醇的C9C8C7H5和C4C7C8H6二面角分別為-174.58和-173.93度,表明C4、C7、C8、C9、H5和H6仍然幾乎在同一平面內,而C7C8C9C10和C5C4C7C8二面角分別為39.36和31.71度,表明C9、C10和C4、C5所在的兩苯環與C4、C7、C8、C9、H5和H6所在平面并不重合,而是存在約30°的扭角.順式白藜蘆醇中C8C9C10C11和C2C3C4C7二面角分別為177.34和-178.41度,表明C8、C9、C10、C11共平面,C2、C3、C4、C7共平面,即C7、C8分別與相連的苯環共平面;而C10C9C8H6和C5C4C7H5二面角分別為-139.88和-146.89度,表明H5、H6偏離了兩平面,而反式白藜蘆醇中H5、H6與其它原子共平面.
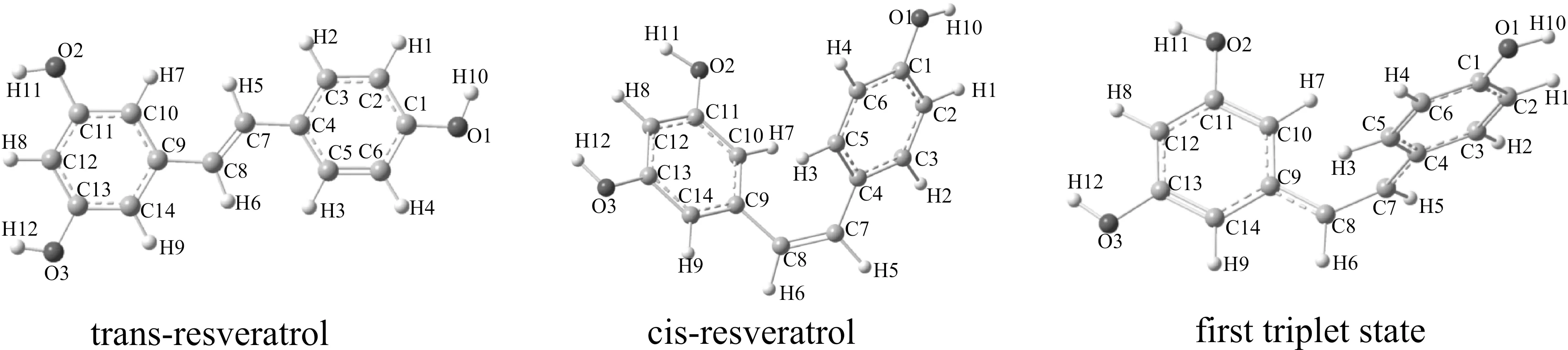
圖2 B3LYP/6-311++G(d,p) 水平優化的白藜蘆醇順反異構體及第一三重激發態的結構Fig. 2 Molecular structures of cis/trans-resveratrol and first triplet state opted at B3LYP/6-311++G(d,p) level
表1 B3LYP/6-311++G(d,p)水平下白藜蘆醇順反異構體及第一三重激發態優化結構的鍵長、鍵角和二面角參數
Table 1 Bond distances,bond angles and dihedral angles for trans/cis-resveratrol (trans-Res and cis-Res) and first triplet state obtained at B3LYP/6-311++G(d,p) level
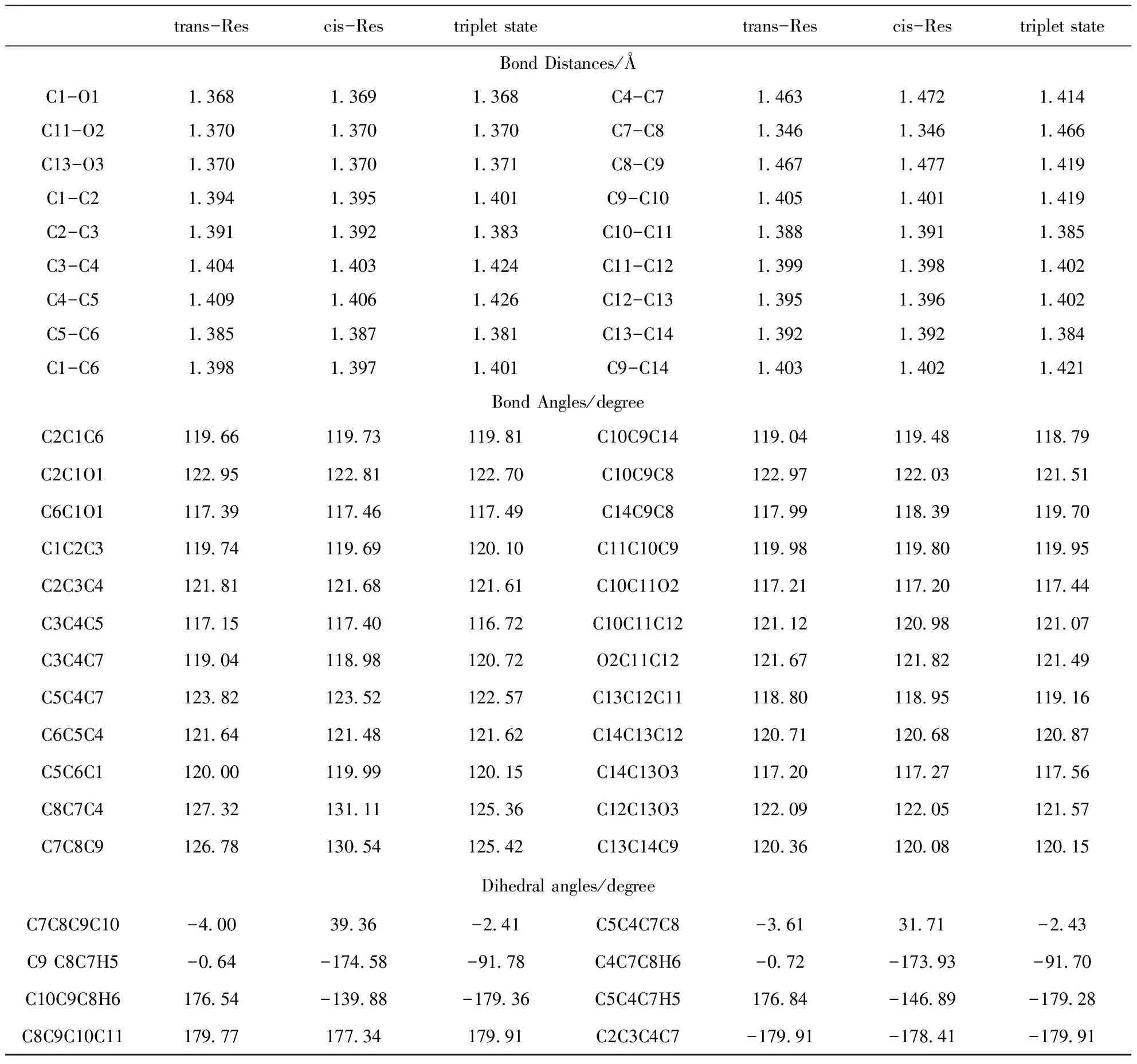
trans-Rescis-Restripletstatetrans-Rescis-RestripletstateBondDistances/?C1-O11 3681 3691 368C4-C71 4631 4721 414C11-O21 3701 3701 370C7-C81 3461 3461 466C13-O31 3701 3701 371C8-C91 4671 4771 419C1-C21 3941 3951 401C9-C101 4051 4011 419C2-C31 3911 3921 383C10-C111 3881 3911 385C3-C41 4041 4031 424C11-C121 3991 3981 402C4-C51 4091 4061 426C12-C131 3951 3961 402C5-C61 3851 3871 381C13-C141 3921 3921 384C1-C61 3981 3971 401C9-C141 4031 4021 421BondAngles/degreeC2C1C6119 66119 73119 81C10C9C14119 04119 48118 79C2C1O1122 95122 81122 70C10C9C8122 97122 03121 51C6C1O1117 39117 46117 49C14C9C8117 99118 39119 70C1C2C3119 74119 69120 10C11C10C9119 98119 80119 95C2C3C4121 81121 68121 61C10C11O2117 21117 20117 44C3C4C5117 15117 40116 72C10C11C12121 12120 98121 07C3C4C7119 04118 98120 72O2C11C12121 67121 82121 49C5C4C7123 82123 52122 57C13C12C11118 80118 95119 16C6C5C4121 64121 48121 62C14C13C12120 71120 68120 87C5C6C1120 00119 99120 15C14C13O3117 20117 27117 56C8C7C4127 32131 11125 36C12C13O3122 09122 05121 57C7C8C9126 78130 54125 42C13C14C9120 36120 08120 15Dihedralangles/degreeC7C8C9C10-4 0039 36-2 41C5C4C7C8-3 6131 71-2 43C9C8C7H5-0 64-174 58-91 78C4C7C8H6-0 72-173 93-91 70C10C9C8H6176 54-139 88-179 36C5C4C7H5176 84-146 89-179 28C8C9C10C11179 77177 34179 91C2C3C4C7-179 91-178 41-179 91
從白藜蘆醇三重態結構參數分析:C7-C8、C4-C7和C8-C9鍵長分別為1.466、1.414和1.419 ?,相對白藜蘆醇順反異構體基態來說,C7-C8明顯的變長,而C4-C7和C8-C9則較明顯的縮短了,但三個鍵均介于單雙鍵之間,C7-C8鍵與白藜蘆醇順反異構體中C4-C7和C8-C9鍵長很相近,C4-C7和C8-C9則更接近于苯環中C-C鍵長,表明三重態中的C7-C8鍵主要表現為單鍵性質,C4-C7和C8-C9則類似于苯環中的C-C鍵;C7C8C9C10、C10C9C8H6、C5C4C7C8、C5C4C7H5二面角分別為-2.41、-179.36、-2.43和-179.28度,表明C7、C8、C9、C10、H6幾乎在一個平面內,C4、C5、C7、C8、H5也幾乎在一平面內;而C9C8C7H5、C4C7C8H6二面角分別為-91.78和-91.70度,表明C7-H5鍵幾乎垂直于C7、C8、C9、H6所在平面,C8-H6鍵幾乎垂直于C4、C7、C8、H5所在平面,即兩苯環幾乎處于互相垂直的關系,C7-H5與C8-H6鍵也是幾乎互相垂直的關系.
3.2 電子結構
3.2.1 NBO構成分析
表2列出了白藜蘆醇順反異構體及第一三重激發態的占據鍵軌道構成情況.
反式白藜蘆醇中C1以sp1.63雜化軌道與C2的sp1.89雜化軌道形成σ鍵,記作sp1.63-sp1.89,C1與C2各自提供p軌道形成π鍵,記作p-p,即形成C1=C2雙鍵.其它在C3-C4、C5-C6、C7-C8、C9-C14、C10-C11、C12-C13成鍵情況與C1=C2類似,順式白藜蘆醇的NBO構成情況與反式結構類似,詳見表2.三重態中,帶有兩個羥基的苯環成鍵情況與白藜蘆醇順反異構體比較沒有明顯差異,C1-C2、C3-C4、C7-C8之間沒有了p-p π鍵,而C2-C3增加了p-p π鍵,形成了C2=C3 雙鍵.C7-C8的成鍵情況為sp1.92-sp1.89,C7、C8雜化軌道的p成分都增加了(沒有了p-p π鍵,C7-C8鍵長明顯長于白藜蘆醇順反異構體.這樣的C7-C8有利于鍵的旋轉,從三重態回到基態的白藜蘆醇順反異構體,實現白藜蘆醇的光致異構化.C7分別以sp1.92、sp1.66和sp2.55與C8、C4、H5成鍵,C8分別以sp1.89、sp1.68和sp2.55與C7、C9、H6成鍵,C7、C8的平均雜化情況均為sp2,那么C7、C8均還有一個2p軌道未參與雜化,NBO分析證實C7、C8的各自剩下的2p軌道均幾乎獨立地形成了高能量的反鍵軌道,那么來自C7的p軌道垂直于單羥基苯環,來自C8的p軌道垂直于雙羥基苯環.這正是文獻中的p-幾何狀態[13,23].
3.2.2 前線軌道(Frontier Orbital)分析
圖3是白藜蘆醇順反異構體及第一三重激發態的最高占據軌道(Highest Occupied Molecular Orbital,HOMO)和最低空軌道(Lowest Unoccupied Molecular Orbital,LUMO).從HOMO看,反式白藜蘆醇的HOMO是一個涵蓋整個分子體系的共軛分子軌道,而順式白藜蘆醇的HOMO分子軌道主要分布區域為C7、C8和含2個羥基的苯環,所以反式結構的能量應該低于順式結構,為熱力學穩定結構.三重態的HOMO則主要分布于C7、C8和含1個羥基的苯環.三者的LUMO的軌道分布區域與對應的HOMO分布區域類似,只是截面更多,能量更高.
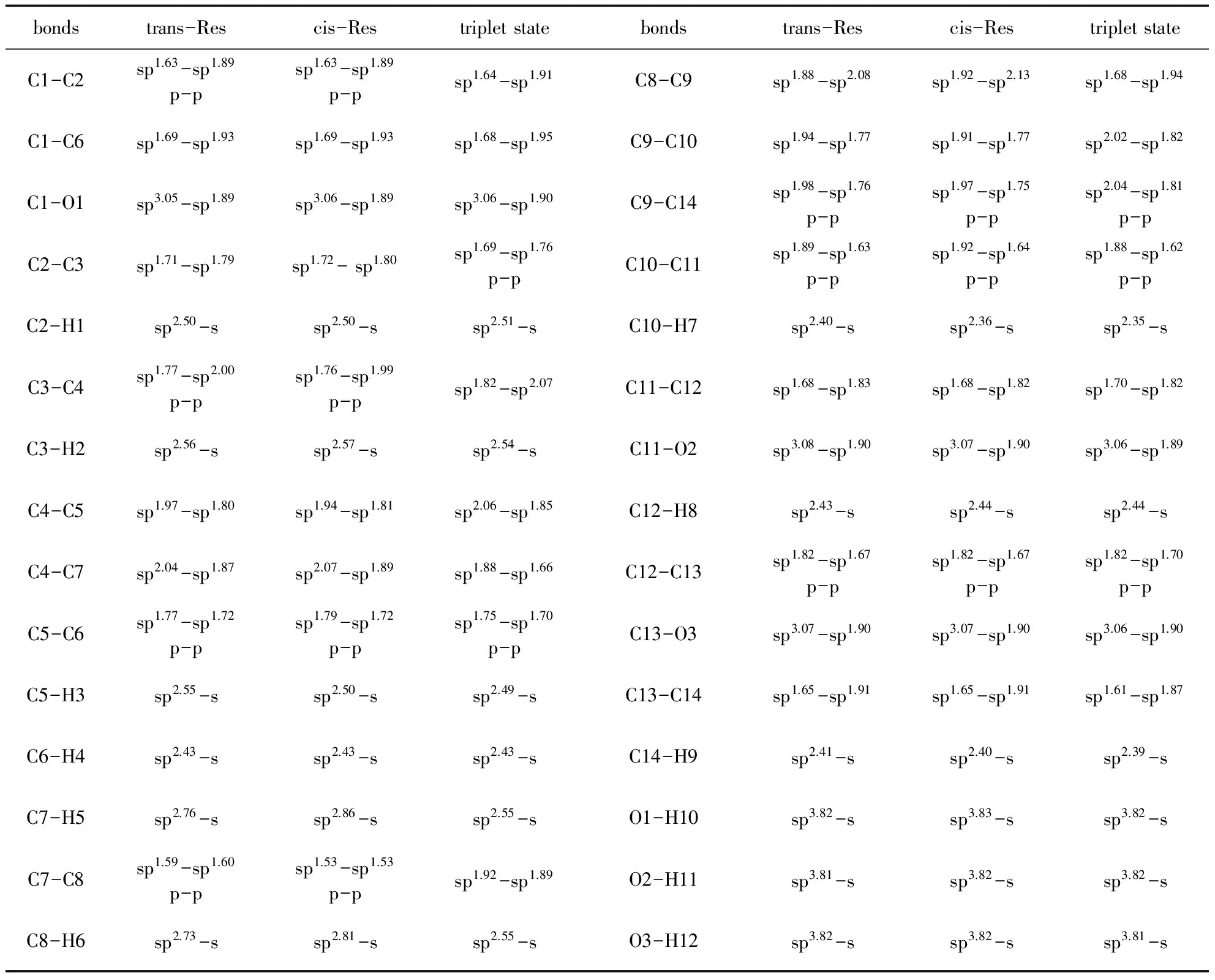
表2 順/反式白藜蘆醇及第一三重激發態的鍵軌道構成
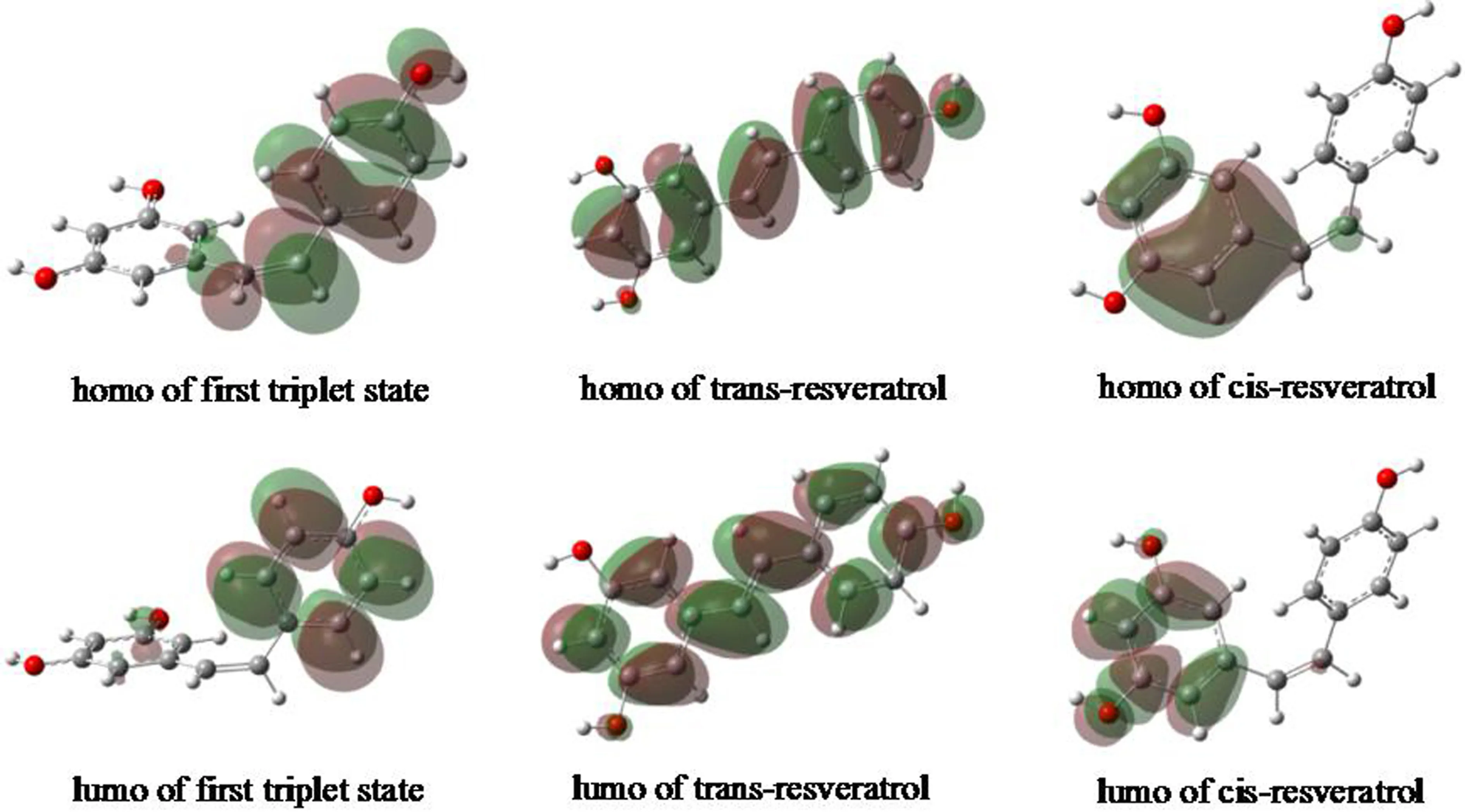
圖3 白藜蘆醇順反異構體及第一三重激發態的HOMO和LUMOFig. 3 HOMOs and LUMOs of cis/trans-resveratrol and first triplet state
4 白藜蘆醇順反異構體的相對自由能
采用B3LYP/6-311++G(d,p)水平進行構型優化和振動頻率計算,采用B3LYP/6-311++G(d,p)水平優化構型在MP2/6-311++G(d,p)水平在氣相、乙醇溶液、水溶液條件下分別進行單點能計算,計算溫度為298.15 K.各點自由能由頻率計算得到的自由能校正項加上MP2單點能得到.表3列出了在氣相、乙醇溶液、水溶液中白藜蘆醇順反異構體的自由能相對值,白藜蘆醇順式構型和反式構型的能量差別不大,考慮電子相關效應的計算結果顯示順式比反式的自由能高約1.3-2.5 kcal/mol,說明反式構型是熱力學穩定構型,這有利于反式白藜蘆醇制品中反式有效成分的保存.如前所述,順反式白藜蘆醇C7-C8鍵長均為1.346 ?,與乙烯的C=C鍵長(1.337 ?)一致,即為雙鍵C7=C8,不能自由旋轉,反式白藜蘆醇的熱穩定性應該比較良好,常溫或低溫避光儲存不會快速的異構化.這一結論與劉宇平、史先敏等的實驗研究[13,14]的結果是一致的.

表3 白藜蘆醇順反異構體的自由能相對值(kcal/mol)
5 紫外光譜
順式白藜蘆醇相對于反式白藜蘆醇的相對電子能量為4.993 kcal/mol,即順式能量高于反式,而烯烴光致異構化反應是在同一個三重態上發生的[11,12],故順式白藜蘆醇形成三重激發態需要更高能量.采用TD-DFT方法在B3LYP/6-311++G(d,p)水平進行了激發態能量計算,反式白藜蘆醇在286 nm、314 nm和330 nm處有吸收峰,330 nm為最強吸收峰;順式白藜蘆醇在在277 nm、301 nm和319 nm處有吸收峰,319 nm為最強吸收峰.最強吸收均產生于60到61分子軌道能級之間的躍遷.我們的計算與戴蘊青及吳波等[9,15]的實驗結論較吻合.而實驗吸收峰展寬,是由于C7=C8鍵軌道是強成鍵軌道,需要紫外精細光譜.
6 結 論
白藜蘆醇順反異構體的各鍵長、鍵角數據很接近,C7-C8為典型的雙鍵,C4-C7和C8-C9主要表現為單鍵性質,具有一定的雙鍵性質.反式白藜蘆醇整個分子呈平面結構,順式白藜蘆醇兩苯環不共面.三重態中兩苯環幾乎處于互相垂直的關系,C7-H5與C8-H6鍵也是幾乎互相垂直的關系.白藜蘆醇順反異構體中C7-C8的σ鍵成鍵情況分別為sp1.53-sp1.53和sp1.59-sp1.60,C7與C8各自提供p軌道形成p-p π鍵,形成C7=C8雙鍵.三重態中,C7-C8為sp1.92-sp1.89σ鍵,無p-p π鍵,C7-C8鍵長明顯長于白藜蘆醇順反異構體;C7分別以sp1.92、sp1.66和sp2.55與C8、C4、H5成鍵,C8分別以sp1.89、sp1.68和sp2.55與C7、C9、H6成鍵,C7、C8的平均雜化情況均為sp2,C7、C8各自剩下的2p軌道均幾乎獨立形成了高能量的反鍵軌道,分別垂直于單羥基和雙羥基苯環,即文獻中所說的p-幾何狀態的三重態.反式白藜蘆醇的HOMO是一個涵蓋整個分子體系的共軛分子軌道,而順式白藜蘆醇的HOMO分子軌道主要分布區域為C7、C8和含2個羥基的苯環,順式比反式的自由能高約1.3-2.5 kcal/mol,反式構型是熱力學穩定構型,常溫或低溫避光儲存反式白藜蘆醇不會快速異構化.TD-DFT方法在B3LYP/6-311++G(d,p)水平進行了激發態能量計算,反式白藜蘆醇在286 nm、314 nm和330 nm處有吸收峰,330 nm為最強吸收峰;順式白藜蘆醇在在277 nm、301 nm和319 nm處有吸收峰,319 nm為最強吸收峰.最強吸收均產生于60到61分子軌道能級之間的躍遷.
[1] Sun W,Sheng J.Ahandbookofbioactivecompoundsfromplants[M]. Beijing: China Medical-Pharmacological Science and Technology Publishing House,1998: 481 (in Chinese)[孫文基,繩金房. 天然活性成分簡明手冊[M]. 北京:中國醫藥科技出版社,1998: 481]
[2] Ganini S,etal.Kinase inhibitors from polygonum cuspidatum[J].NaturalProduct,1993,56: l805.
[3] Siemann E H,Creasy L L,etal.Concentration of the phyeoalexin resveratrol in wine[J].Am.J.Enol.Vitic,1992,43: 49.
[4] Bertelli A A E,Giovannini L,Giannessi D,etal.Antiplatelet activity of synthetic and natured resveratrol in red wine[J].OfficeInternationaldelaVigneetduVin,1995,17: 1.
[5] Jang M,Cai L,Udeani G O,etal.Cancer chemopreventive activity of resveratrol,a natural product derived from grapes[J].Science,1997,275: 218.
[6] Pace-Asciad C R,Hahn S E,etal.The red wine phenolics trans-resveratrol and quercetin block human platelet aggregation and eicosanoid synthesis:Implications for protection against coronary heart disease[J].Clin.ChimicaActa,1995,235: 207.
[7] Deak M,Falk H. On the chemistry of the resveratrol diastereomers[J].MonatsheftefürChemie/ChemicalMonthly,2003,134: 883.
[8] Brent C. Resveratrol isomericmolar absorptivities and stability[J].J.Agric.FoodChem.,1996,44: 1253.
[9] Dai Y Q,Han Y S,Hui B D,etal. Analysis of the geometrical isomers of resveratrol and resveratrol glucoside from red wines produced in China by HPLC[J].JournalofChinaAgriculturalUniversity,2002,7: 14 (in Chinese)[戴蘊青,韓雅珊,惠柏棣,等. 紅葡萄酒中白藜蘆醇及其糖苷異構體的反相HPLC分析[J]. 中國農業大學學報,2002,7: 14]
[10] Park S J,Ahmad F,Philp A,etal. Resveratrol ameliorates aging-related metabolic phenotypes by inhibiting cAMP phosphodiesterases[J].Cell,2012,148: 421.
[11] Willam M H,Pill-Soon Song.CRChandbookoforganicphotochemistryandphotobiology[M]. Florida: CRC Press Inc.,1995: 3.
[12] Hammond G S,Saltiel J,Lamola A A,etal. Mechanisms of photochemical reactions solution. XXII. Photochemical cis-trans isomerization[J].J.Am.Chem.Soc.,1964,86: 3197.
[13] Liu Y,Wen D,Chen Z,etal. Study on thermostability and photo-isomerization of trans-resveratrol by high performance liquid chromatography and liquid chromatography-electrospray ionization-mass spectrometry[J].ChineseJournalofChromatography,2004,22: 583(in Chinese)
[14] Shi X M,Yan Z M,Xie J H,etal. Study of photo-stability and thermo-stability of resveratrol[J].ChinaSurfactantDetergent&Cosmetics, 2011,41: 204(in Chinese)
[15] Wu B,Zhang H J. Quantitative determination of the (E)- and (Z)-diastereomers of resveratrol and resveratrol glucoside in the roots of Polygonum cuspidatum by HPLC and elementary study on their fluorescence[J].ActaPharmaceuticaSinica.,2006,41: 522(in Chinese)
[16] Beck A D. Densityfunctional thermochemistry. III. the role of exact exchange[J].J.Chem.Phys.,1993,98: 5648.
[17] Parr R G,Yang W.Densityfunctionaltheoryofatomsandmolecules[M]. Oxford: Oxford University Press, 1989.
[18] Barone V,Cossi M. Quantum calculation of molecular energies and energy gradients in solution by a conductor solvent model[J].J.Phys.Chem. A,1998,102: 1995.
[19] Cossi M,Rega N,Scalmani G,etal. Energies,structures,and electronic properties of molecules in solution with the C-PCM solvation model[J].J.Comput.Chem.,2003,24: 669.
[20] Francesco C,Joseph T,Adriel V-E,etal. Structural basis for antioxidant activity of trans-resveratrol: ab initio calculations and crystal and molecular structure[J].J.Agric.FoodChem.,2004,52: 7279.
[21] Frisch M J,Trucks G W,Schlegel H B. Gaussian Inc.,Wallingford CT,2009.
[22] Allen F H,Watson D G,Brammer L,etal. Chapter 9,Sec 5.Typicalinteratomicdistances:organiccompounds.Ininternationaltablesforcrystallography,Vol.C:mathematical,physicalandchemicaltables[M]. 3rd ed.,Prince E,Ed.,Kluwer Academic Publishers: Boston,MA,2004: 790.
[23] Xing Q,Xu R,Zhou Z,etal.Fundamentalorganicchemistry[M]. 2nd ed. Beijing: Higher Education Press, 1994: 813 (in Chinese)
A theoretical study on the structures of cis/trans-resveratrol and the first triplet state
HE Yun-Qing1,2,HU Qi-Shan1,2,HU Wen1,LIU Liu-Xie3
(1. College of Chemistry and Chemical Engineering,Sichuan University of Arts and Science,Dazhou 635000,China;2. Key Laboratory of Exploitation and Study of Distinctive Plants in Education Department of Sichuan Province,Dazhou 635000,China; 3. College of Chemistry and Materials Science,Sichuan Normal University,Chengdu 610066,China)
The geometry optimizations,vibration frequencies,and natural bond orbital (NBO) analysis of cis/trans-resveratrol and the first triplet state were performed at B3LYP/6-311++G(d,p) level,free energies of two isomers were obtained at B3LYP /6-311++G(d,p)//B3LYP/6-311++G(d,p) level. Trans-resveratrol is a planar structure,a torsional angle of benzene rings of cis-resveratrol is about 30o. One benzene ring of the first triplet state is perpendicular to the other,and C7-H5 bond is perpendicular to C8-H6. C7-C8 σ bonds in cis/trans-resveratrol are sp1.53-sp1.53and sp1.59-sp1.60,respectively,and a π bond is formed using p orbital from C7 and C8. C7-C8 in the triplet state is sp1.92-sp1.89σ bond,2p orbital of C7 or C8 forms one high energy antibonding orbital independently,and similar to C8,and is perpendicular to the benzene ring with one hydroxy and two hydroxies,respectively,with its C7-C8 bond length longer than that in cis/trans-resveratrol. Trans-resveratrol is the thermodynamic stable structure because its free energy is lower than that of cis-resveratrol 1.3-2.5 kcal/mol. The strongest ultraviolet absorption peaks of trans- and cis-resveratrol are at 330 nm and 319 nm,respectively,achieved at B3LYP/6-311++G(d,p) level using TD-DFT method.
Resveratrol; Isomers; Triplet state; Natural bond orbital (NBO); Frontier orbital; UV
2014-12-04
特色植物開發研究四川省高校重點實驗室開放課題重點項目(sctz201302);四川省大學生創新創業訓練項目(201310644016);四川文理學院化學化工學院大學生應用創新能力訓練計劃項目(hg2014xly03)
103969/j.issn.1000-0364.2015.08.008
O561.1
A
1000-0364(2015)08-0572-07
作者介紹: 何云清(1971—), 女,博士,副教授,主要從事天然產物和量子化學研究. E-mail: heyunqing625@126.com

