穩定期慢性阻塞性肺疾病患者認知功能的相關因素研究
楊莉蓉,李賤,魏慧梅
(峨眉山市人民醫院,四川 峨眉山614200)
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)是一種以不完全可逆的氣流受限為特征的慢性呼吸道疾病,常呈進行性發展,可分為急性加重期和穩定期。隨著環境污染的加重以及人口老齡化,我國COPD的發病率呈逐年上升的趨勢。隨著對COPD的研究不斷深入,目前認為COPD不僅累及呼吸系統,引起肺功能降低,還累及中樞神經系統,影響患者的認知功能、心理健康等[1]。既往研究[2]證實COPD急性期可合并肺性腦病,引起精神障礙,但較少研究關注穩定期COPD患者的認知功能損害及其相關因素,對其機制也不完全明確。本研究通過蒙特利爾認知評估量表(montreal cognitiveassessment,MoCA)評價穩定期COPD患者的認知功能,并分析MoCA評分與其各臨床指標的關系,旨在探討影響患者認知功能的相關因素,為臨床早期診治提供參考依據。現將結果報道如下:
1 資料與方法
1.1 一般資料
選取2013年1月-2014年11月期間峨眉山市人民醫院收治的128例穩定期COPD患者為病例組。納入標準:①根據患者的臨床表現、肺功能、血氣分析及影響學結果確診為COPD,符合其診斷標準;②處于COPD穩定期,距離上次急性加重時間≥3個月;③文化程度為小學及以上,意識清楚,視聽功能正常,能配合完成神經心理測試;④同意納入本研究,并簽署知情同意書。排除標準:①既往有阿爾茨海默病(AD)、腦卒中、腦腫瘤、一氧化碳中毒等其他引起腦功能的疾病;②服藥不穩定、濫用藥物或吸毒者;③合并有嚴重的心、肝、腎功能不全或惡性腫瘤者;④合并有肺炎、哮喘、阻塞性睡眠呼吸暫停綜合征等其他呼吸系統疾病;⑤合并糖尿病,并出現血管并發癥;⑥與調查者交流障礙者。病例組128例,其中,男78例,女50例,年齡42~75歲,平均(62.3±7.6)歲,體重指數(BMI)為(22.5±2.0)kg/m2,受教育時間(9.2±3.3)年,吸煙指數(610±130)支/年。并選取同期來該院進行體檢的75名健康成人為對照組。納入標準:①肺功能、胸部X線片檢查均正常;②能配合完成神經心理測試;③同意入組,并簽署知情同意書。排除標準同病例組。對照組75例,其中男42例,女33例,年齡40~73歲,平均(60.9±6.8)歲,體重指數(BMI)為(22.2±1.8)kg/m2,受教育時間(9.7±3.0)年,吸煙指數(590±120)支/年。兩組一般資料比較,差異無統計學意義(P>0.05)。
1.2 方法
1.2.1 問卷調查 采用本研究自擬的一般情況調查表調查所有患者的性別、年齡、吸煙史、身高、體重、臨床癥狀、體征、病程等一般情況,并計算BMI及標準體重,BMI=體重(Kg)/身高2(m2),然后據此分成2個亞組(>22 kg/m2及≤22 kg/m2)。采用MoCA量表中文版進行評價所有受試者的認知功能,MoCA量表包括視空間、執行功能、命名等8個認知領域,總分30分,若受教育年限≤12年則需在得分上加1分,≥26分視為正常[3]。并全程進行質量控制,調查前對調查員進行培訓,使其熟練掌握問卷內容,明確調查的目的及意義;調查員在每次調查結束后都要核對簽字并將問卷交給研究人員,研究人員對每份問卷都要進行檢查,對明顯邏輯不合理以及內容有缺漏的問卷要及時糾正,對調查對象重新進行核實;調查后,由雙人對問卷進行數據錄入,如果有問題應及時返回查找原因,確定數據輸入無誤。
1.2.2 輔助檢查 在進行MoCA評分的當日對所有受試者進行肺功能檢測,測定其FEV1、FVC,然后進行支氣管舒張試驗,讓受試者吸入硫酸沙丁胺醇400μg,休息20min后再次檢測肺功能。根據第1秒用力呼氣量(FEV1)/用力肺活量(FVC)是否<70%診斷COPD,然后根據FEV1/預計值進行COPD嚴重程度分級,分為GOLDⅠ級(FEV1≥80%預計值)、GOLDⅡ級(50%≤FEV1<80%預計值)、GOLDⅢ級(30%≤FEV1<50%預計值)、Ⅳ級(FEV1<30%預計值)。對穩定期COPD患者在未吸氧的情況下,經橈動脈取血后采用羅氏Cobasb123血氣分析儀進行血氣分析,檢測動脈血PaO2、Pa-CO2、SO2。采用焦慮自評量表(SAS)、抑郁自評量表(SDS)分別評價患者的焦慮、抑郁狀況,兩個量表均有20個條目(1~4分),總分乘以1.25后取整為標準分,正常人的標準分應≤50分,>50分的表示有焦慮和抑郁傾向,分數越高,傾向越重。
1.3 統計學處理
采用SPSS 17.0統計軟件進行處理,定性資料采用χ2檢驗,定量資料以均數±標準差(±s)表示,兩組比較采用t檢驗,多組比較先采用方差分析,然后采用SNK q檢驗進行兩兩比較,采用簡單線性相關和多重線性回歸探討25(OH)D降低的危險因素及其與IR的關系,以P<0.05視為差異具有統計學意義。
2 結果
2.1 病例組和對照組的MoCA評分比較
病例組與對照組的MoCA評分分別為(23.7±4.7)分、(26.8±3.8)分,病例組的評分明顯低于對照組,差異有統計學意義(t=4.856,P<0.05)。
2.2 病例組中各亞組的MoCA評分比較結果
年齡、吸煙指數、受教育時間、COPD嚴重程度、病程、PaO2、PaCO2、SO2、SAS及SDS評分的各亞組的MoCA評分比較,差異有統計學意義(P<0.05)。在COPD嚴重程度方面,GOLDⅠ級的MoCA評分與GOLDⅡ級相比,差異無統計學意義(P>0.05),GOLDⅡ級的MoCA評分顯著高于GOLDⅢ級,Ⅲ級的MoCA評分顯著高于GOLDⅣ級,差異有統計學意義(P<0.05)。詳見表1。
表1 病例組中各亞組的MoCA評分比較結果 (±s)
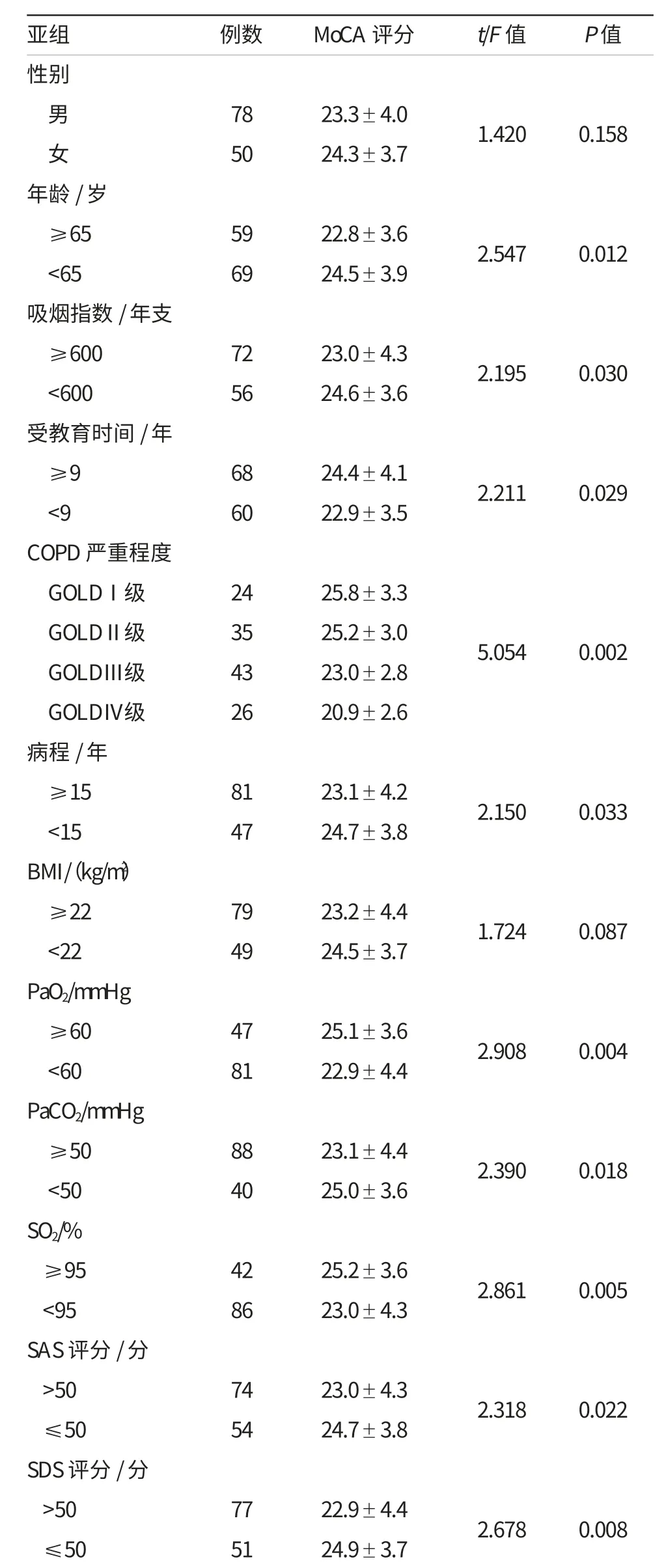
表1 病例組中各亞組的MoCA評分比較結果 (±s)
亞組 例數 MoCA評分 t/F值 P值性別男78 23.3±4.0 1.420 0.158女50 24.3±3.7年齡/歲≥65 59 22.8±3.6 2.547 0.012<65 69 24.5±3.9吸煙指數/年支≥600 72 23.0±4.3 2.195 0.030<600 56 24.6±3.6受教育時間/年≥9 68 24.4±4.1 2.211 0.029<9 60 22.9±3.5 COPD嚴重程度GOLDⅠ級 24 25.8±3.3 GOLDⅡ級 35 25.2±3.0 GOLDⅢ級 43 23.0±2.8 GOLDⅣ級 26 20.9±2.6病程/年≥15 81 23.1±4.2 2.150 0.033<15 47 24.7±3.8 BMI/(kg/m2)≥22 79 23.2±4.4 1.724 0.087<22 49 24.5±3.7 PaO2/mmHg≥60 47 25.1±3.6 2.908 0.004<60 81 22.9±4.4 PaCO2/mmHg≥50 88 23.1±4.4 2.390 0.018<50 40 25.0±3.6 SO2/%≥95 42 25.2±3.6 2.861 0.005<95 86 23.0±4.3 SAS評分/分>50 74 23.0±4.3 2.318 0.022≤50 54 24.7±3.8 SDS評分/分>50 77 22.9±4.4 2.678 0.008≤50 51 24.9±3.7 5.054 0.002
2.3 病例組中MoCA評分與各因素的簡單線性相關分析結果
將男性=0,女性=1進行賦值,GOLDⅠ級、GOLDⅡ級、GOLDⅢ級、GOLDⅣ級分別賦值為1、2、3、4分,進行簡單線性相關分析。結果表明,MoCA評分與患者的受教育時間、PaO2、SO2成正相關,與年齡、吸煙指數、COPD嚴重程度、病程、PaCO2、SAS及SDS分成負相關(P<0.05)。詳見表2。
2.4 病例組中MoCA評分與各因素的多重線性回歸結果
采用逐步回歸法進行多重線性回歸,結果表明,年齡、COPD嚴重程度、PaO2、SO2及SDS評分最終進入模型,與MoCA評分有線性回歸關系,其中MoCA評分與PaO2、SO2成正相關,與年齡、COPD嚴重程度、SDS評分負相關(P<0.05)。詳見表3。
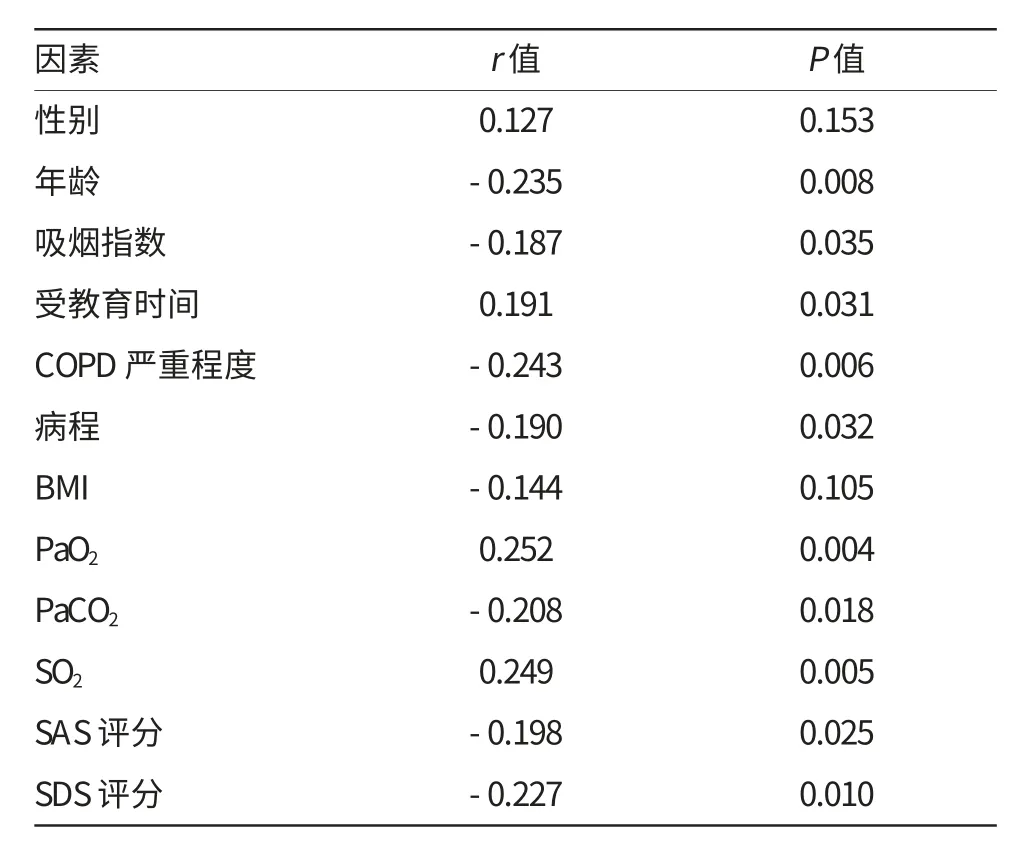
表2 病例組中MoCA評分與各因素的簡單線性相關分析結果

表3 病例組中MoCA評分與各因素的多重線性回歸結果
3 討論
近年來的多個研究均證實COPD不僅是呼吸系統疾病,也是能累及中樞神經系統的疾病,既往已有研究證實COPD急性加重期可導致嚴重缺氧和CO2潴留,引起肺性腦病,造成精神障礙,甚至危及生命。穩定期COPD同樣可造成腦功能損害,引起認知功能降低,包括感知、記憶力、學習、運動、注意力、執行功能等方面的異常。目前機制尚不完全清楚,可能與下列因素有關:①COPD常因影響肺功能而引起低氧血癥,慢性缺氧可降低腦血流灌注,常導致前額葉和頂葉的低血流灌注[4],國內有研究[5]報道COPD合并認知功能障礙患者的海馬體積顯著降低,海馬結構的萎縮可能是引起認知受損的原因之一;②慢性缺氧可引起神經元損傷,影響神經遞質合成中重要的氧依賴酶,降低了乙酰膽堿等神經遞質的合成,從而影響了腦功能;③COPD患者的氣道中IL-6、IL-8、TNF-α 等炎癥介質進入血液循環中,引起全身的炎癥反應,長期的炎癥刺激可引起患者認知功能和精神情緒的變化[6-7]。由于穩定期COPD可導致患者出現輕度認知功能障礙(MCI),部分患者甚至發展為AD,嚴重影響患者的生活質量,故有必要研究COPD患者發生認知功能障礙的影響因素,對高危患者進行認知功能測試,早期發現MCI,并進行積極的診治,改善其預后。
本研究采用MoCA量表評估穩定期COPD患者的認知功能,MoCA量表是加拿大NASREDDINE等學者參考簡易精神智能評定量表(MMSE)的認知測評項目,并結合臨床經驗制定的,該量表較全面覆蓋了執行功能、記憶、注意、計算力等多個認知領域,總分30分,<26分者視為異常,分數越低提示認知功能越差,并且該量表僅需10min左右即可完成測試,可對認知功能異常進行快速篩查,臨床實用性較高。本研究選取了128例穩定COPD患者為病例組,并選擇同期75例健康成人為對照組,兩組一般資料方面差異無統計學意義(P>0.05),神經測試結果表明,病例組的MoCA評分為(23.7±4.7)分,高于錢紅玉等人[8]報道的(20.6±2.3)分,這可能與本研究所納入患者的年齡較低、COPD嚴重程度較低有關,本研究中病例組的MoCA評分明顯低于對照組的評分(26.8±3.8),差異有統計學意義(P<0.05),與以往的研究結果一致[8]。故穩定期COPD患者的認知功能存在不同程度的降低。多元線性回歸分析結果表明,年齡、COPD嚴重程度、PaO2、SO2及SDS評分與穩定期COPD患者MoCA評分密切相關(P<0.05)。
本研究根據年齡分為≥65歲和<65歲兩個亞組,測試結果提示老年(≥65歲)患者的MoCA評分顯著低于<65歲患者(P<0.05),MoCA評分與年齡成負相關(P<0.05),因此,年齡越大,患者的MoCA評分越低,認知功能損害越重。這可能是由于與中年患者相比,老年患者的心、肺、腦等各系統的功能均出現不同程度的降低,機體慢性缺氧的時間更長,而大腦的耐受性較差,疾病的損害更重。故臨床上對老年COPD患者應重視其認知功能的評價,早期診治MCI。本研究根據肺功能判斷COPD嚴重程度,將患者分為GOLDⅠ~Ⅳ級,多重線性回歸分析結果表明MoCA評分與COPD嚴重程度成負相關(P<0.05),故COPD患者的肺功能損傷越重,認知功能越差。因此,臨床上可采用肺功能預測患者認知功能,對重度或極重度COPD患者應進行神經心理測試。但DODD等[9]的薈萃分析結果表明,肺功能不是一個預測COPD患者認知功能障礙的理想指標,可能是由于該研究較少包括中重度的COPD患者。本研究中GOLDⅠ級患者的MoCA評分與GOLDⅡ級相當,而GOLDⅡ級患者的評分高于GOLDⅢ級,而GOLDⅢ級患者的評分高于GOLDⅣ級,故與輕中度患者相比,重度、極重度患者的肺功能與認知功能的關聯性可能更強,認知功能障礙更嚴重,建議臨床上對重度和極重度患者進行神經心理學測試,早期診治認知功能障礙。
本研究還對患者的血氣分析結果及MoCA評分的關聯性進行分析,結果表明,MoCA評分與PaO2、SO2成正相關(P<0.05),PaO2、SO2越小,認知功能損害越重,故低氧血癥是影響穩定期COPD患者認知功能的重要指標,PaO2與SO2是預測其認知功能的理想指標,與以往的研究結果一致[10]。這可能是由于低氧血癥引起腦部低血流灌注和神經元損傷,抑制乙酰膽堿的合成。雖然PaCO2≥50mmHg患者的MoCA評分明顯低于<50mmHg患者,但PaCO2未進入多重線性回歸的模型中,與以往研究[8]中結果不一致,PAREKH等[11]研究結果表明,PaCO2越低,患者的執行功能、記憶、注意力等功能越好。因此,PaCO2與認知功能的關系尚不完全清楚,不推薦臨床作為COPD患者的認知功能的預測指標。此外,本研究中患者的MoCA評分與SDS評分成負相關(P<0.05),患者的抑郁表現越重,認知功能損傷越重。既往研究[12]證實抑郁是認知功能損害的獨立危險因素及前驅癥狀,這可能是由于長期的抑郁情緒會嚴重抑制患者的精神活動,思維聯想和決斷較困難,出現不同程度的認知功能損害,甚至出現癡呆,并且抑郁情緒會顯著減少患者與外界的溝通交流,使患者出現社會交流的功能障礙,與社會出現隔離,從而也可能影響其認知功能。因此,臨床上對COPD患者除了進行常規的肺功能和血氣分析檢查外,還應該仔細采集病史,對存在抑郁表現的患者應進行認知功能的檢測及干預。
綜上所述,穩定期COPD患者存在不同程度的認知功能障礙,高齡、肺功能顯著降低、低氧血癥、抑郁表現是患者發生認知功能障礙的高危因素,應進行積極的早期診治。但是本研究仍然存在不足之處,首先,雖然MoCA量表的可信度和實用性均較高,但單獨采用一個量表不能完全、準確地判斷患者的認知功能狀況。其次,本研究為單中心研究,樣本量較少,更可信的結果有待大樣本、多中心的研究證實。
[1]王麗君,曾冬新,欒秀麗,等.慢性阻塞性肺疾病患者心理健康狀況及其影響因素的分析研究[J].中國現代醫學雜志,2014,24(29):62-66.
[2]顧新南,蔣建中.無創正壓通氣聯合呼吸興奮劑治療慢性阻塞性肺疾病急性加重期合并輕中度肺性腦病的療效分析[J].江蘇醫藥,2012,38(21):2599-2600.
[3]DALRYMPLE-ALFORD JC,MACASKILL MR,NAKAS CT,et al.The MoCA:well-suited screen for cognitive impairment in Parkinson disease[J].Neurology,2010,75(19):1717-1725.
[4]KLEIN M,GAUGGEL S,SACHS G,et al.Impact of chronic obstructive pulmonary disease(COPD)on attention functions[J].Respir Med,2010,104(1):52-60.
[5]李靜.慢性阻塞性肺疾病患者的認知功能評價及相關影響因素分析[D].安徽醫科大學,2013.
[6]KERSUL AL,IGLESIAS A,RIOS A,et al.Molecular mechanisms of inflammation during exacerbations of chronic obstructive pulmonary disease[J].Arch Bronconeumol,2011,47(4):176-183.
[7]BARNES PJ,CELLI BR.Systemic manifestations and comorbidities of COPD[J].Eur Respir J,2009,33(5):1165-1185.
[8]錢紅玉,林紅英,李毅.穩定期慢性阻塞性肺疾病患者的認知功能評價及其影響因素[J].中華結核和呼吸雜志,2014,37(10):769-773.
[9]DODD JW,GETOV SV,JONES PW.Cognitive function in COPD[J].Eur Respir J,2010,35(4):913-922.
[10]THAKUR N,BLANC PD,JULIAN LJ,et al.COPD and cognitive impairment:the role of hypoxemia and oxygen therapy[J].Int J Chron Obstruct Pulmon Dis,2010,5:263-269.
[11]PAREKH PI,BLUMENTHAL JA,Babyak MA,et al.Gas exchange and exercise capacity affect neurocognitive performance in patients with lung disease[J].Psychosom Med,2005,67(3):425-432.
[12]HASSELBALCH BJ,KNORR U,HASSELBALCH SG,et al.The cumulative load of depressive illness is associated with cognitive function in the remitted state of unipolar depressive disorder[J].Eur Psychiatry,2013,28(6):349-355.

