RASSF1A基因甲基化與肝細胞癌關系的Meta分析
葉婷,於琳,劉靳波
(瀘州醫學院附屬醫院,四川瀘州646000)
RASSF1A基因甲基化與肝細胞癌關系的Meta分析
葉婷,於琳,劉靳波
(瀘州醫學院附屬醫院,四川瀘州646000)
目的 探討RAS相關結構家庭1A基因(RASSF1A基因)異常甲基化與肝細胞癌的關系。方法 檢索國外PubMed、Embase、Ovid、Web of science、Cochrane Library數據庫和國內的中國生物醫學文獻數據庫(CBM)、中文科技期刊全文數據庫(VIP)、中國期刊全文數據庫(CNKI)、萬方數據庫2014年7月以前的相關文獻,按納入排除標準篩選文獻并提取數據。用RevMan5.2軟件進行統計分析,使用比值比(OR)及95%置信區間(95%CI)衡量RASSF1A基因啟動子區甲基化與肝癌的關系。結果 共15篇文獻1 417例患者納入研究,其中肝細胞癌組710例、對照組707例。肝細胞癌組織中RASSF1A甲基化陽性率高于正常肝組織[OR=50.23,95%CI(22.21~113.61)、P<0.05]、癌旁正常組織[OR=7.63,95%CI(3.38~17.22),P<0.05]及肝硬化組織[OR=17.18,95%CI(2.57~114.91),P<0.05]。結論 RASSF1A基因的高甲基化導致該基因的失活,與肝細胞癌的發生發展密切相關。
肝細胞癌;DNA 甲基化; RAS相關結構家庭1A基因; Meta分析
肝細胞癌是原發性肝癌的主要類型,是最常見的預后不良惡性腫瘤之一,其發生率呈上升趨勢[1]。肝癌的發生發展是一個多階段過程,由基因改變和表觀遺傳學異常共同引起原癌基因激活和抑癌基因失活或丟失。DNA甲基化是表觀遺傳學失活的主要類型,抑癌基因啟動子區CpG島高甲基化引起的表觀沉默已成為肝癌發生發展中遺傳學改變的關鍵因素之一[2]。近年有關DNA甲基化與肝細胞癌的研究較多,但結果并不完全一致。2014年8~9月,對國內外有RAS相關結構家族1A基因(RASSF1A基因)甲基化與肝細胞癌的文獻進行Meta分析,以期為臨床提供參考依據。
1 資料與方法
1.1 文獻檢索
1.1.1 檢索策略 制定檢索策略并進行系統全面的計算機檢索。檢索范圍包括國外PubMed、Embase、Ovid、Web of Science、Cochrane Library數據庫以及國內的中國生物醫學文獻數據庫(CBM)、中文科技期刊全文數據庫(VIP)、中國期刊全文數據庫(CNKI)、萬方數據庫。中文檢索詞為RASSF1A基因、肝細胞癌、甲基化;英文檢索詞為Hepatocellular Carcinoma/HCC/Liver Cancer Carcinoma, Methylation/Methylate/Hypermethylation,Ras association domain family protein 1A/RASSF1A,對研究設計類型限定為case control/incidence,檢索時間從建庫截止到2014年6月30日,無語種限制。同時輔以文獻追溯,獲取全文。
1.1.2 納入排除標準 納入標準:①國內外公開發表的關于RASSF1A基因在肝細胞癌中甲基化情況研究的一次文獻;②研究對象為人群,研究類型為病例—對照研究,病例組均由病理學確診為肝細胞癌患者,對照組為經臨床證實良性肝疾病患者或健康人群;③研究方法相似,即采用DNA甲基化特異性PCR(MSP)檢測基因甲基化情況。④能獲得全文,直接報告了有效的比值比(OR)及其95%CI,或者可以從文章報告的數據進行計算。排除標準:①重復發表的文獻;②文摘、綜述、講座或會議文章;③標本為血清、細胞或動物等非肝臟組織實驗研究;④檢測方法不明確,資料不完整或數據不全不能統計的研究;⑤無法獲得全文的文獻。
1.2 資料提取 由兩名評價者按照標準的數據提取表格,獨立提取符合要求的研究資料。包括第一作者姓名、發表年份、研究地點、腫瘤的組織學類型、對照組來源、病例組和對照組的樣本量、平均年齡及性別。通過討論解決分歧。
1.3 文獻質量評估 由兩名評價者按照Cochrane手冊推薦使用的紐卡斯爾—渥太華量表(NOS)獨立評估納入研究的方法學質量。該量表主要從研究人群即病例組與對照組的定義和選擇、組間可比性、暴露因素的測量三方面共8個條目進行評分,滿分9分。
1.4 統計學分析 采用Cochrane協作網提供的Reviews Manager 5.2(Rev Man 5.2)統計軟件。對納入文獻的研究結果通過Meta分析方法進行合并,繪制森林圖。各個被納入文獻之間的異質性大小用χ2檢驗和I2統計量來驗證。若P≤0.05、I2≥50%則采用隨機效應模型進行數據合并;若P>0.05、I2<50%則采用固定效應模型進行數據合并。進行敏感性分析以驗證每個獨立研究對總的合并結果的影響。通過Begg's測試以及繪制漏斗圖估計是否有發表偏倚。P<0.05為差異有統計學意義。
2 結果
2.1 檢索結果及納入文獻情況 初步檢索獲得相關文獻共87篇,通過Endnote X6文獻管理軟件去重后獲得文獻49篇,再通過閱讀文題和摘要排除綜述、會議文章、與主題不相關的文獻以及相同作者相似內容文獻等獲得18篇,進一步閱讀全文,未達到納入標準的3篇,最終納入文獻共15篇[3~17]。入選病例1 417例,其中肝細胞癌組710例,對照組707例(包括癌旁組354例、肝硬化111例、肝炎組39例及正常組織136例)。納入文獻基本情況見表1。
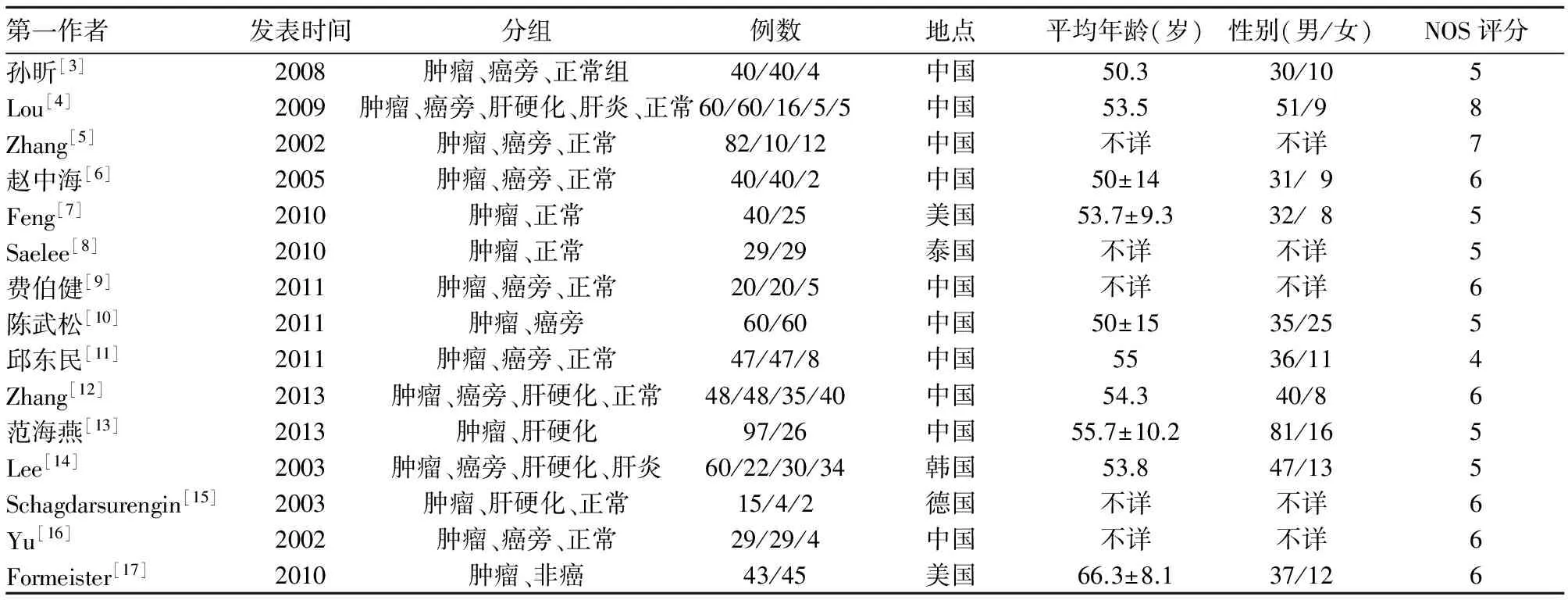
表1 RASSF1A基因納入Meta分析文獻的基本特征及質量評分
2.3 統計結果分析
2.3.1 肝細胞癌組織和正常肝組織RASSF1A基因甲基化率比較 11篇文獻[3~9,11,12,15,16]報道此內容,肝細胞癌組450例、正常肝組織對照組136例,其中分別有372例(83.7%)患者肝細胞癌組織和11例(8.1%)正常肝組織檢測到RASSF1A基因甲基化。異質性檢驗結果P=0.49、I2=0%,顯示結果無異質性,采用固定效應模型進行Meta分析。結果顯示肝細胞癌組織和正常肝組織中RASSF1A基因甲基化率差異有統計學意義[OR=50.23,95%CI(22.21~113.61),P<0.05],肝細胞癌組織中RASSF1A基因甲基化率明顯高于正常肝組織,詳見圖1。
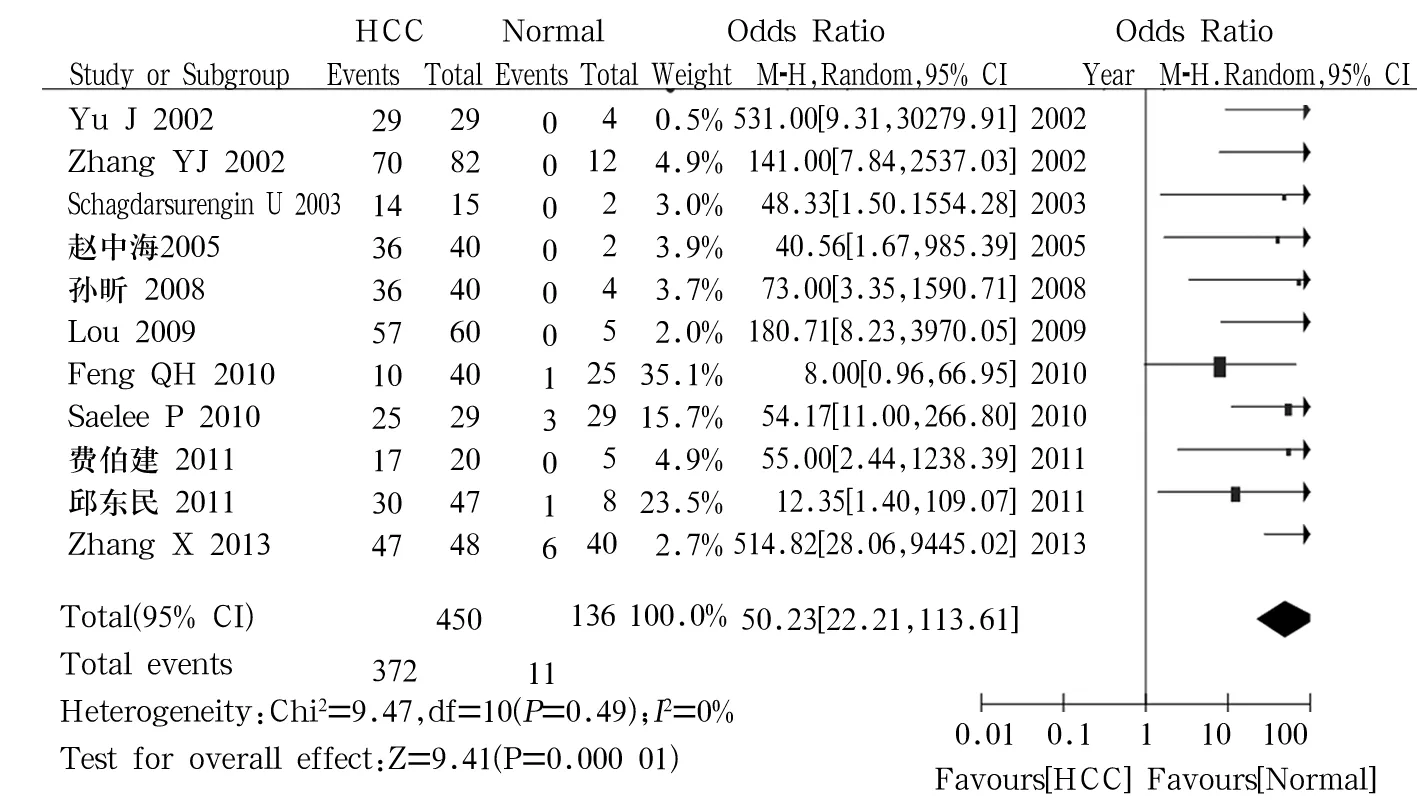
圖1 肝癌組織與正常肝組織中RASSF1A基因甲基化的Meta分析
2.3.2 肝細胞癌組織和癌旁組織RASSF1A基因甲基化率比較 10篇文獻[3~6,9~12,14,16]報道此內容,肝細胞癌426例、癌旁組織354例,其中分別有374例(87.8%)患者肝細胞癌組織和196例(55.4%)癌旁組織檢測到RASSF1A基因甲基化。異質性檢驗結果P=0.005、I2=64%,顯示結果有異質性,采用隨機效應模型進行Meta分析。結果顯示肝細胞癌組織和正常肝組織中RASSF1A基因甲基化率差異有統計學意義[OR=7.63,95%CI(3.38~17.22),P<0.05],腫瘤組織中RASSF1A基因甲基化率明顯高于癌旁組織,詳見圖2。
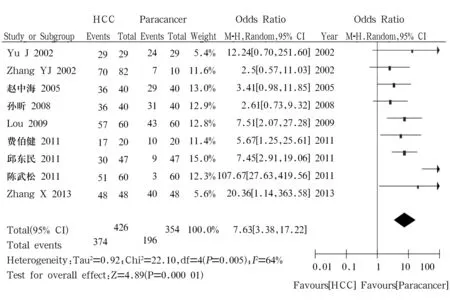
圖2 肝癌組織與癌旁組織中RASSF1A基因甲基化的Meta分析
2.3.3 RASSF1A基因在HCC腫瘤組織和肝硬化組織中的甲基化比較 5篇文獻[4,12~15]報道此內容,肝細胞癌280例、肝硬化111例,其中分別有374例(87.8%)患者肝細胞癌組織和196例(55.4%)肝硬化組織檢測到RASSF1A基因甲基化。異質性檢驗結果P=0.00 09、I2=79%,顯示結果有異質性,采用隨機效應模型進行Meta分析。結果顯示肝細胞癌組織和正常肝組織中RASSF1A基因甲基化率差異有統計學意義[OR=17.18,95%CI(2.57~114.91),P<0.05],肝細胞癌組織中RASSF1A基因甲基化率明顯高于肝硬化組織,詳見圖3。
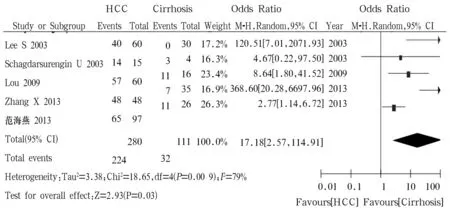
圖3 肝癌組織與肝硬化組織中RASSF1A基因甲基化的Meta分析
2.4 發表偏倚評估 漏斗圖圖形基本呈對稱倒立分布,說明發表偏倚對研究結果無影響。
2.5 敏感性分析 對I2>50%的結果行敏感性分析,每次減少一篇文獻估計單個獨立研究對Meta分析的影響。剔除后結果前后無明顯差異,提示Meta分析結論較穩定可信。
3 討論
抑癌基因啟動子區異常甲基化的表觀遺傳失活被認為是肝癌等多種癌癥發生的重要機制。RASSF1A基因定位于3p21.3,在細胞周期調控、微管穩定、細胞黏附和細胞凋亡中起著重要作用[18]。RASSF1A作為抑癌基因的功能已被體內外實驗所證實, 在腫瘤細胞中高表達可降低細胞軟瓊脂克隆形成及裸鼠的致瘤性[19]。RASSF1A基因啟動子區異常甲基化導致的基因缺失是癌癥形成的頻發事件,已在包括肝癌等多種類型的腫瘤中被證實。其作用機制是同源異位基因HOXB3與DNA甲基轉移酶DNMT3B基因結合使其高表達,同時多梳抑制復合物2與癌基因MYC相互作用促進DNMT3B結合于RASSF1A啟動子區,導致高甲基化及表達沉默促進腫瘤形成。RASSF1A基因異常甲基化與肝細胞癌的關系日益受到國內外研究者的關注,然而文獻報道的結論存在一定分歧。本研究結果顯示,肝細胞癌組織中RASSF1A基因甲基化率高于正常肝組織、肝硬化組織和癌旁組織。肝細胞癌的發生發展經過肝炎、肝硬化再到肝癌的多步驟演變,RASSF1A基因甲基化率在此過程中逐漸增高。
檢驗研究間的異質性是Meta分析的重要內容之一。本系統評價對納入研究是否具有異質性做了詳細分析,根據組間異質性存在與否選擇隨機效應或固定效應模型。為了保證結果的穩定性,另行敏感性分析,剔除單個獨立研究后觀察結果前后并無顯著性變化,說明本次Meta分析結果穩定可靠。本研究尚有不足之處,包括檢索到的文獻不夠全面,檢索范圍局限在公開發表的文獻,對于未公開發表的研究存在漏檢的可能;檢索語種僅限于中文和英文,可能漏檢其他語種的研究;納入文獻人種多為肝細胞癌多發的東亞地區等。因此,本系統評價納入研究存在選擇性偏倚、文獻收集性偏倚的可能。由于Meta分析評價方法本身的不足與納入研究間的差異,要更準確的評價抑癌基因RASSF1A甲基化與肝細胞癌的關系,尚需要納入更全面、嚴謹,更高質量的病例對照研究進一步證實結果。
總之,本系統評價表明抑癌基因RASSF1A高甲基化與肝細胞癌密切相關,基因啟動子區高甲基化誘導的表達失活在肝細胞癌的發生發展中發揮了重要作用。
[1] Siegel R, Naishadham D, Jemal A. Cancer statistics[J]. CA Cancer J Clin, 2013, 63(2):11-30.
[2] Nishida N, Nagasaka T, Nishimura T, et al. Aberrant methylation of multiple tumor suppressor genes in aging liver, chronic hepatitis, and hepatocellular carcinoma[J]. Hepatology, 2008, 47(3):908-918.
[3] 孫昕,朱立新,錢波,等.肝細胞癌中抑癌基因的甲基化現象[J].中華肝膽外科雜志,2008,14(5):318-320.
[4] Lou C, Du Z, Yang B, et al. Aberrant DNA methylation profile of hepatocellular carcinoma and surgically resected margin[J]. Cancer Sci, 2009, 100(6):996-1004.
[5] Zhang YJ, Ahsan H, Chen Y, et al. High frequency of promoter hypermethylation of RASSF1A and p16 and its relationship to aflatoxin B1-DNA adduct levels in human hepatocellular carcinoma[J]. Mol Carcinog, 2002,35:85-92.
[6] 趙中海, 耿小平, 朱立新,等. 肝細胞癌組織中Ras相關區域家族蛋白1A、腫瘤高甲基化基因1和p73基因的異常甲基化[J].中華外科雜志,2005,43(23):1528-1532.
[7] Feng QH, Stern JE, Hawes SE, et al. DNA methylation changes in normal liver tissues and hepatocellular carcinoma with different viral infection[J]. Exp Mol Pathol, 2010,88(2):287-292.
[8] Saelee P, Wongkham S, Chariyalertsak S, et al. RASSF1A promoter hypermethylation as a prognostic marker for hepatocellular carcinoma[J]. Asian Pac J Cancer Prev, 2010, 11(3):1677-1681.
[9] 費伯健,黃朝暉,華東,等. 血漿Ras相關區域家族蛋白1A基因甲基化在肝細胞癌分子診斷中的價值[J]. 腫瘤,2011,31(8):742-747.
[10] 陳武松,郭圣龍.原發性肝細胞癌RASSF1基因啟動子甲基化檢測及其臨床意義[J].中國現代醫學雜志,2011,21(15):1864-1867.
[11] 邱東民,余堅,黃朝暉.MSRE-qPCR技術分析多基因DNA甲基化對肝細胞癌的診斷價值[J]. 中國癌癥雜志, 2011, 21(8):615-620.
[12] Zhang X, Li HM, Liu Z, et al. Loss of heterozygosity and methylation of multiple tumor suppressor genes on chromosome 3 in hepatocellular carcinoma[J]. J Gastroenterol, 2013,48(3):132-143.
[13] 范海燕, 張慧景, 郭占軍,等.肝細胞癌患者癌組織中rassf1a和wif-1基因甲基化的臨床意義[J].山東大學學報,2013,51(5):89-93.
[14] Lee SLH, Kim JH, Lee HS, et al. Aberrant CpG Island Hypermethylation Along Multistep Hepatocarcinogenesis[J]. AJP, 2003,163(4):1371-1378..
[15] Schagdarsurengin U, Wilkens L, Steinemann D, et al. Frequent epigenetic inactivation of the RASSF1A gene in hepatocellular carcinoma[J]. Oncogene, 2003,22(6):1866-1871.
[16] Yu J, Ni M, Xu J, et al. Methylation profiling of twenty promoter-CpG islands of genes which may contribute to hepatocellular carcinogenesis[J]. BMC Cancer, 2002, 12(2):29.
[17] Formeister EJ, Tsuchiya M, Fujii H, et al. Comparative analysis of promoter methylation and gene expression endpoints between tumorous and non-tumorous tissues from HCV-positive patients with hepatocellular carcinoma[J]. Mutat Res, 2010,692(1-2):26-33.
[18] Agathanggelou A, Cooper WN, Latif F. Role of the Ras-association domain family 1 tumor suppressor gene in human cancers[J]. Cancer Res, 2005, 65(9):3497-3508.
[19] Donninger H, Vos MD, Clark GJ. The RASSF1A tumor suppressor[J]. J Cell Sci, 2007,120(18):3163-3172.
四川省教育廳科研項目重點項目(12ZA243)。
劉靳波
10.3969/j.issn.1002-266X.2015.06.034
R735.7
B
1002-266X(2015)06-0085-04
2014-11-12)

