人臍帶來源的間充質干細胞再次培養效果觀察
高彥琳, 張寧坤, 陳厚良, 高連如, 朱智明
(中國人民解放軍海軍總醫院,北京100000)
·基礎研究·
人臍帶來源的間充質干細胞再次培養效果觀察
高彥琳, 張寧坤, 陳厚良, 高連如, 朱智明
(中國人民解放軍海軍總醫院,北京100000)
目的 探討人臍帶來源間充質干細胞(hUC- MSCs )體外培養的最佳方法。方法 采用組織塊貼壁法分離培養hUC- MSCs,記為初次培養組。將原代培養瓶中的培養液及組織離心,重新分成再次培養組織組、再次培養混合組和再次培養純液組進行再次培養。觀察四組原代細胞的細胞形態、獲得時間和細胞得率;MTT法繪制細胞生長曲線, 流式細胞儀檢測細胞周期及免疫表型。結果 初次培養組、再次培養組織組、再次培養混合組、再次培養純液組獲取細胞的平均時間分別為(15±0.45)d、(7±0.30)d、(8±0.25)d、(8±0.25)d。每個T75培養瓶可獲取的第1代細胞數分別為(4.0±0.50)×105、(9.0±0.55)×105、(15.0±0.20)×105、(7.0±0.33)×105個。倒置顯微鏡下觀察四組細胞為形態相對均一的梭形貼壁細胞,呈平行排列生長或旋渦狀生長。四組細胞的生長曲線、增殖活性、表面標記物檢測均無明顯差異。結論 對臍帶間充質干細胞的原代培養體系進行再次培養,可在短時間內擴增出大量原代細胞。
間充質干細胞;臍帶;細胞培養
間充質干細胞(MSCs)是進行細胞療法的主要種子細胞[1], 具有較強的自我更新能力和多向分化潛能,在細胞治療領域有著極為廣闊的應用前景[2,3]。目前已從骨髓、 脂肪、 羊膜、 胎盤、 臍血以及臍帶等組織中分離出MSCs,其有向內皮細胞、成骨細胞、軟骨細胞、脂肪細胞、成肌細胞和神經細胞分化的能力[4~6]。 臍帶的來源廣泛,取材方便,易于收集、保存、冷凍,屬于醫療廢棄物,不受倫理、道德及法律方面的限制,且臍帶組織中MSCs含量豐富,是再生醫學理想的種子細胞[7]。目前分離培養臍帶血來源的間充質干細胞(hUC-MSCs )的方法很多,但是都不能快速有效地獲取原代細胞。2014年1~5月,我們觀察并比較了對hUC-MSCs原代培養體系進行再次培養所獲得hUC-MSCs的形態,獲得hUC-MSCs 時間及數目,獲得hUC-MSCs 細胞表型、增殖能力、周期分布,探討最佳的hUC- MSCs 培養方法。現報告如下。
1 材料與方法
1.1 材料
1.1.1 臍帶來源 經醫院倫理委員會的批準, 在征得產婦和家屬書面知情同意的情況下, 在海軍總醫院婦產科產房取當日剖宮產健康足月生產的新生兒臍帶 (乙型肝炎病毒、 丙肝病毒、 人類免疫缺陷病毒、 TP-SX、巨細胞病毒梅毒、艾滋病等傳染性疾病檢測陰性)。
1.1.2 主要試劑及器材 DMEM/F12培養液、胎牛血清(FBS)、0.25%trypsin-EDTA胰蛋白酶均為美國 Gibco 公司生產;MTT為Sigma公司生產;流式單抗CD45-FITC、CD44-FITC、CD90-PE、 CD105-PE、HLA-ABC-PE、HLA-DR-FITC、CD31-PE 均為美國Biolegend 公司生產;倒置相差顯微鏡下為日本Nikon公司生產;流式細胞儀為美國 BD 公司生產;紫外分光光度儀、 二氧化碳培養箱(Thermo)。
1.2 hUC-MSCs分離及培養
1.2.1 hUC-MSCs的原代培養 將無菌條件下獲取的臍帶放入無菌生理鹽水中,1 h內送至細胞培養實驗室。參照Li等[8]報道的hUC-MSLs分離、培養方法。用生理鹽水反復沖洗,洗去臍帶殘留血液,將臍帶剪成3~4 cm的小段,每段均沿臍靜脈腔剪開,平鋪后剔除靜脈,再剔除2根動脈,取出血管之間、血管與外膜之間的膠狀物——華通膠,用小剪刀將取出的華通膠反復剪切成大約1 mm3及以下小塊,接種于T75培養瓶內,每個培養瓶內加入10 mL含有10%FBS 的 DMEM/F12 培養液,使臍帶華通膠均勻分布瓶底,置于5%CO2、37 ℃的培養箱內培養。在顯微鏡下觀察細胞生長增殖情況并拍照。待細胞生長至80%~90%融合狀態時,用0.25%胰蛋白酶消化傳代細胞,為初次培養組。
1.2.2 hUC-MSCs再次培養 將原代培養瓶中的培養液及組織移入離心管中,1 500轉/min離心5 min。將此體系分成三組,并分別接種于T75培養瓶內。再次培養組織組:單純組織塊組(無原培養基)加入10 mL含有10%FBS 的 DMEM/F12 培養液;再次培養混合組:組織塊及原培養基的混合物組加入5 mL含有10%FBS 的 DMEM/F12 培養及5 mL原培養液;再次培養純液組:原培養液10 mL,分別置于5%CO2、37 ℃的培養箱內培養。在顯微鏡下觀察細胞生長增殖情況并拍照。待細胞生長至80%~90%融合狀態時,用0.25%胰蛋白酶消化傳代細胞。
1.3 觀察項目及方法
1.3.1 hUC-MSCs形態、第一代細胞獲取時間及數量 采用倒置顯微鏡觀察四組hUC-MSCs形態。統計各組獲取第一代hUC-MSCs的時間及每個培養瓶獲取hUC-MSCs的數量。
1.3.2 hUC- MSCs 表面標記物 取各組第3代細胞,0.25%胰蛋白酶消化,PBS洗兩次,調整細胞濃度為1×106/mL單細胞懸液,每個Eppembrf 管加 100 μL的細胞懸液 , 加入鼠抗人單克隆抗體 PE- CD90PE- CD105PE- CD44PE-CD73PE- HLA- ABC FITC- CD45FITC- CD34FITC- HLA- DR各 20 μL,充分混勻,避光室溫孵育30 min, PBS 洗 2 遍(250 g 離心 5 min ),重新制成細胞懸液 0.5 mL,經300目細胞篩過濾,流式細胞儀上機檢測并分析。
1.3.3 細胞增殖活性 取各組第3代細胞, 經0.25%胰蛋白酶消化計數后,分別用完全培養基調整細胞數至2.5 × 104/mL,取200 μL細胞懸液接種在96孔板中,每組設6個復孔,置于37 ℃ 5%CO2飽和濕度培養箱中培養。每隔24 h用MTT法檢測各組細胞吸光度值(激發波長490 nm),連續7 d,取6孔均值繪制生長曲線。
1.3.4 細胞周期分布 取各組第3代細胞,經0.25%胰蛋白酶消化收集后,分別用 PBS 離心洗滌 2 次,調整細胞數至 1×106/mL,離心棄上清,加入4 ℃預冷的70%乙醇1 mL重懸,4 ℃冰箱過夜; 離心棄上清,用1 mL碘化丙啶重懸,4 ℃避光孵育 30 min,流式細胞儀檢測,分析細胞周期。
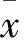
2 結果
2.1 hUC-MSCs形態、得第一代細胞獲取時間及數量 倒置顯微鏡下觀察四組原代細胞呈貼壁生長,形態均為長梭形或多角形1。初次培養組細胞以華通膠為中心呈旋渦狀或平行排列生長,獲取細胞的時間為(15.00±0.45)d,每個培養瓶可獲取(4.00±0.5)×105個第一代細胞;再次培養組織組細胞以華通膠為中心呈旋渦狀生長,獲取細胞的平均時間為(7.00±0.3)d,每個培養瓶可獲取(9.00±0.55)×105個第一代細胞;再次培養混合組部分細胞以華通膠為中心呈旋渦狀生長,部分細胞呈散在生長,得到原代細胞的時間(8.00±0.25)d,每個培養瓶可獲取(15.00±0.20)×105個第一代細胞;再次培養純液組細胞呈散在生長,得到原代細胞的平均時間(8.00±0.58)d,每個T75培養瓶可獲取(7.00±0.33)×105個第一代細胞。傳至第3 代, 細胞增殖速度加快,形態較為均一呈長梭形,折光度好。四組第一代及第3代hUC-MSCs細胞形態無明顯差異,初次培養組原代細胞獲取時間顯著長于其他三組(P均<0.05),再次培養的三組之間兩兩比較,P均>0.05。獲取原代細胞數再次培養混合組數目最多,再次培養組織組其次,再次培養純液組稍差,初次培養組最少,四組間兩兩比較P均<0.05。
2.2 hUC-MSCs免疫表型 四組第3代臍帶間充質干細胞均高表達CD90、CD105、HLA-ABC,不表達 CD31、CD34、CD45、HLA- DR。
2.3 hUC-MSCs增殖能力 四組第3代hUC- MSCs細胞生長曲線見圖1。四組hUC- MSCs 生長曲線形態相似,基本重疊。第1~2 d各組細胞處于潛伏期,增殖不明顯; 3~5 d各組細胞進入對數生長期, 細胞增殖加速; 第 6 天以后進入平臺期,細胞生長停滯。
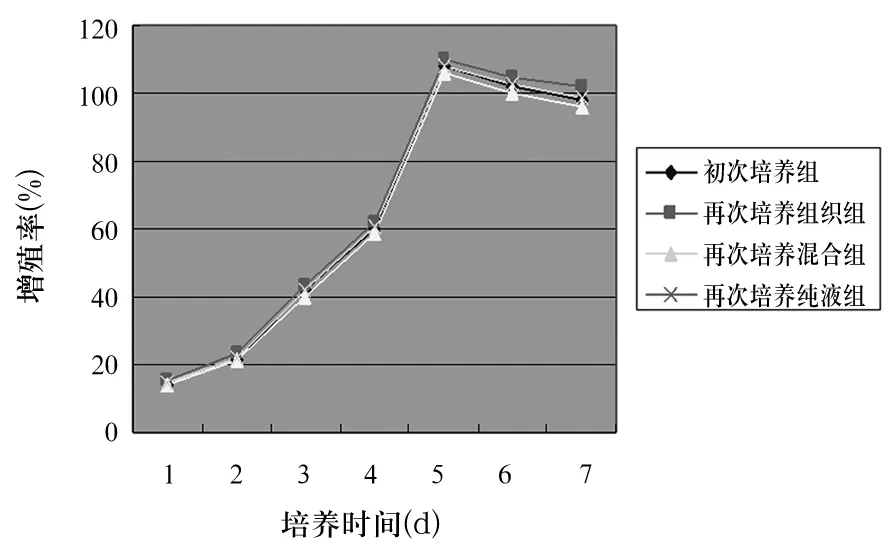
圖1 四組hUC-MSCs 生長曲線
2.4 hUC-MSCs細胞周期分布 各組細胞周期分布無統計學差異。
3 討論
最近幾年里,對成體干細胞療法的研究在不斷增加。MSCs是一個相當具有吸引力的種子細胞,可以用于治療各種疾病,包括神經系統疾病、心血管疾病、自身免疫性疾病、內分泌疾病等[9]。hUC- MSCs 是介于胚胎干細胞和成體干細胞之間的原始干細胞,分化能力強,倍增時間短,具有免疫調節作用和較低的免疫原性,且無致腫瘤性[10,11]。1976年Friedenstein等[12]首先從臍帶組織中分離培養出間充質干細胞,之后Schugar等[13]采用組織塊法和酶消化法兩種方法分別培養出臍帶間充質干細胞,這也是目前較為常用的兩種方法。這兩種方法分離培養出的臍帶間充質干細胞形態、 生長曲線、 細胞表面標記物等無明顯差異[14]。但是酶消化法成本較高;操作比較繁瑣污染概率大;消化過程時間過短,細胞很難爬出;消化時間過長易損傷細胞;長時間酶的消化對細胞損傷較大, 多次傳代后細胞易脫落死亡[15]。
本研究采用組織塊培養法提取臍帶中MSCs。通常來講組織塊貼壁法是將小的組織塊均勻鋪于培養瓶底,原代細胞從組織塊邊緣爬出。雖然組織塊貼壁法方便易行,操作簡單,但存在原代細胞收獲率低、培養周期長等問題[16],難以適應組織工程對種子細胞的需要。本研究中初次培養組獲取原代細胞的平均時間大約2周,獲取細胞數量較少,符合組織塊貼壁法培養的結果。一般傳代結束后就會將培養原代細胞的組織和培養液丟棄。本研究中筆者將廢棄的組織和培養液離心后,分成組織組、混合組和純液組進行再次培養,大約1周即可傳代,且獲取的細胞數為初次培養的2倍左右。相對于傳統組織貼壁法,這種改進的方法可在較短時間內獲得大量原代細胞,而且獲得細胞的免疫表型、增殖能力及周期分布正常。筆者推測其原因:①初次培養后組織塊內細胞并未完全爬出;②初次培養過程中可能形成了某些黏附物質和生長因子,促進組織塊貼壁和生長[17];③組織塊在經過一輪培養后,纖維組織松解,細胞易于爬出;④原代培養的培養液中可能存在一些散在細胞。
[1] Gatta V, Aurora MD, Lanuti P, et al. Gene expression modifications in Wharton's Jelly mesenchymal stem cells promoted by prolonged in vitro culturing[J]. BMC Genomics,2013,14(12):635.
[2] Mok PL, Leong CF, Cheong SK. Cellular mechanisms of emerging applications of mesenchymal stem cells[J]. Mal J Pathol, 2013,35(1):17-32.
[3] Neirinckx V, Coste C, Rogister B,et al. Concise review: adult mesenchymal stem cells, adult neural crest stem cells, and therapy of neurological pathologies: a state of play[J]. Stem Cells Trans Med, 2013,2(4):284-296.
[4] Constantinescu A, Andrei E,Iordache F, et,al.Recellularization potential assessment of Wharton's Jelly-derived endothelial progenitor cells using a human fetal vascular tissue model[J]. Develop Biol, 2014,8(3):37-39.
[5] Kang BJ, Ryul HK, Park SS, et al. Comparing the osteogenic potential of canine mesenchymal stem cells derived from adipose tissues, bone marrow, umbilical cord blood, and Wharton′s jelly for treating bone defects[J]. Korean Soc Veterin Sci, 2012,3(3):299-310.
[6] Fu YS, Shih YT, Cheng YC, et al. Transformation of human umbilical mesenchymal cells into neurons in vitro[J]. J Biomed Sci, 2004,11(5):652-660.
[7] Parvathy V,Sudha B, Majumdar AS, et al. Isolation, characterization, and gene expression analysis of Wharton′s jelly-derived mesenchymal stem cells under xeno-free culture conditions[J]. Adv App, 2011,8(5):39-50.
[8] Hsieh JY, Fu YS, Chang SJ, et al. Functional module analysis reveals differential osteogenic and stemness potentials inhuman mesenchymal stem cells from bone marrow and Wharton′s jelly of umbilical cord[J]. Stem Cells Dev, 2010,19(12):1895-1910.
[9] Bai J, Hu Y, Wang YR,et al. Comparison of human amniotic fluid-derived and umbilical cord Wharton's Jelly-derived mesenchymal stromal cells: Characterization and myocardial differentiation capacity[J]. J Geriatric Cardiol, 2012,9(5):166-171.
[10] Ribeiro J, Pereira T, Amorim I, et al. Cell therapy with human MSCs isolated from the umbilical cord Wharton jelly associated to a PVA membrane in the treatment of chronic skin wounds[J]. Inte J Med Sci, 2014,11(10):979-987.
[11] Prasajakl P, Leeanansaksiri W. Developing a new two-step protocol to generate functional hepatocytes from wharton′s jelly-derived mesenchymal stem cells under hypoxic condition[J]. Stem Cells Inter, 2013,5(10):1155-1165.
[12] Friedenstein AJ, Gorskaja JF, Kulagina NN. Fibroblast precursors in normal and irradiated mouse hematopoietic organs[J]. Exp Hematol, 1976,34(4):267-274.
[13] Schugar RC, Chirieleison SM, Wescoe KE, et al. High harvest yield, high expansion, and phenotype stability of CD146mesenchymal stromal cells from whole primitive human umbilical cord tissue[J]. J Biomed Biotechnol, 2009,2009:1-11.
[14] 李昆,于艷秋,李世正.兩種分離人胎盤間充質干細胞方法的比較[J] .中國醫科大學學報,2010,39(5):675-676.
[15] 郝白露,楊瑞峰,彭祥熾,等.改良的人臍帶間充質干細胞培養方法[J].中國計劃生育學雜志,2013,1(21):44-49.
[16] Diao Y, Ma Q, Cui F, et al.Human umbilical cord esenchymal stem cells :Osteogenesis in vivo as seed cells for bone tissue engineering[J]. J Biomed Mater Res, 2009,91(2):123-131.
[17] Conget PA , Minguell JJ. Phenotypical and functional properties of human bone marrow Mesenchymal progenit or cells[J]. J Cell Physiol, 1999,181 (1):67- 73.
國家自然科學基金面上項目(81170094)。
朱智明
10.3969/j.issn.1002-266X.2015.06.010
R318
A
1002-266X(2015)06-0028-03
2014-10-15)

