復方半邊蓮凝膠制備工藝優化
陳瓊,王海燕,余紅霞,李青青,楊俊杰
(信陽農林學院 信陽市中藥資源開發工程技術研究中心 信陽市中藥質量分析檢測重點實驗室,河南 信陽 464000)
?
復方半邊蓮凝膠制備工藝優化
陳瓊,王海燕,余紅霞,李青青,楊俊杰Δ
(信陽農林學院 信陽市中藥資源開發工程技術研究中心 信陽市中藥質量分析檢測重點實驗室,河南 信陽 464000)
目的 考察影響復方半邊蓮凝膠制備工藝的各因素,確定復方半邊蓮凝膠最佳制備工藝條件。方法 在單因素實驗基礎上,以成型性、涂展性、穩定性的綜合作用為指標,采用正交試驗設計對卡波姆-940用量、載藥量、5%羥苯乙酯乙醇溶液和三乙醇胺用量進行考察,并用高效液相色譜法測定所制凝膠中野黃芩苷的含量。結果 確定復方半邊蓮凝膠最佳處方工藝為:以0.25 g卡波姆-940為凝膠基質,2 g 10%月桂氮卓酮無水乙醇溶液為促滲劑,1.0 g三乙醇胺為pH調整劑、0.4 g甘油為保濕劑、0.3 g 5%羥苯乙酯乙醇溶液為防腐劑;載藥量為每1 g凝膠含1 g飲片。結論 復方半邊蓮凝膠制備工藝簡便,質地均勻細膩,穩定性良好。
復方半邊蓮;凝膠;工藝;正交試驗
復方半邊蓮凝膠由半邊蓮、半枝蓮、白花蛇舌草組成。現代藥理研究證實半邊蓮[1]、半枝蓮[2]、白花蛇舌草[3-5]對金黃色葡萄球菌、大腸埃希菌、銅綠假單胞菌均有明顯的抑制或殺滅作用。復方半邊蓮具有較好的α-葡萄糖苷酶抑制、抗氧化和抗菌活性[6]。復方半邊蓮注射液抗菌消炎作用明確[7]。文獻[8-10]報道含有半邊蓮、白花蛇舌草的制劑可以治療隱翅蟲皮炎。目前尚未見復方半邊蓮用于皮膚外科的報道,本實驗利用其抗菌活性對其劑型進行改革,采用超聲提取[11],通過正交試驗將其制備成外用給藥的凝膠劑,不但克服了復方半邊蓮注射液的不良反應[12-16],而且填補了國內復方半邊蓮凝膠劑型的空白,擴大了復方半邊蓮臨床應用范圍。
1 材料與方法
1.1 藥品與試劑 半邊蓮(LobeliachinensisLour.),半枝蓮(PortulacagrandifloraHook.),白花蛇舌草(HedyotisdiffusaWilld.)購于信陽市藥材站(鑒定人余運平,高級工程師,河南同源制藥有限公司),野黃芩苷標準品(含量測定用,含量>98%,中國食品藥品檢定研究所,批號110842-201106)。卡波姆940(廊坊聚通化工有限公司,批號20120116),甲醇為色譜純,乙醇、三乙醇胺、羥丙乙酯、甘油、月桂氮卓酮等均為分析純,純化水自制。
1.2 儀器 Agilent1100高效液相色譜儀,VWD紫外檢測器,Agilent化學工作站(安捷倫科技有限公司);ZSBB-712 恒溫水浴(上海智城分析儀器制造有限公司),AB-135-S型電子天平(梅特勒.托利多儀器(上海)有限公司);PB602-S電子天平(梅特勒.托利多儀器(上海)有限公司);101AS-2電熱恒溫干燥箱(上海實驗儀器有限公司),UPT-I-100L優普超純水機。
1.3 復方半邊蓮浸膏的制備 將半邊蓮、半枝蓮、白花蛇舌草挑揀淘洗后105 ℃烘干,備用。以上3味,各取50 g,加飲用水浸泡30 min,于超聲提取儀中超聲提取兩次,設定提取條件為:超聲功率400 W,料液比1:15(第1次加水10倍飲片量,第2次加水5倍飲片量),超聲時間30 min(第1次20 min,第2次10 min)[11],合并提取液,濾過,濾液濃縮至1︰1,加等量95%乙醇,靜置12 h,濾過,濾液回收乙醇并濃縮至稠膏狀(約50 g),即得。
1.4 復方半邊蓮凝膠的制備 20 g復方半邊蓮凝膠劑中,促透劑10%月桂氮卓酮無水乙醇溶液按常用量2 g、保濕劑甘油按常用量0.4 g投料。本實驗對凝膠質量較大影響因素的凝膠基質用量、pH調整劑用量、防腐劑用量及載藥量進行優選。
取卡波姆-940適量,加入甘油0.4 g攪拌均勻使其全部潤濕,加入純化水適量使完全溶脹,得空白凝膠,備用。另取適量提取物,加入含0.3 g 5%羥苯乙酯乙醇溶液和2 g 10%月桂氮卓酮無水乙醇溶液,混勻。將提取物溶液加入到空白凝膠中,攪拌使其分布均勻后,加入三乙醇胺調節pH至6.5~7.0,攪拌均勻,即得含藥凝膠。
1.4.1 復方半邊蓮凝膠基質的選擇:按凝膠制備總量為20 g,分別稱取凝膠基質卡波姆-940 0.10、0.20、0.25、0.30、0.35 g于小燒杯中,加入甘油0.4 g攪拌均勻使其全部潤濕,加入純化水適量使完全溶脹,得空白凝膠,備用。另稱取適量提取物(按每1 g凝膠含飲片1 g計),加入適量5%羥苯乙酯乙醇溶液和2 g 10%月桂氮卓酮無水乙醇溶液,混勻。將提取物溶液加入到空白凝膠中,攪拌使其分布均勻后,加入三乙醇胺調節pH至6.5~7.0,攪拌均勻,即得含藥凝膠。
以含藥凝膠的成型性、涂展性、穩定性為指標,將制得的凝膠置潔凈白色透明玻璃容器中并密封,于室溫下放置0、15、30 d后進行考察。
1.4.2 復方半邊蓮凝膠載藥量的選擇:固定卡波姆0.25 g、三乙醇胺1.0 g、甘油0.4 g、10%月桂氮卓酮無水乙醇溶液2 g、5%羥苯乙酯乙醇溶液0.3 g,按照上述凝膠制備方法制成20 g。同法制成5份,分別使載藥量為0.5、1.0、1.5、2.0、2.5 g/g,攪勻。以成型性、涂展性、穩定性為指標,將制備得到的凝膠置白色透明玻璃容器中并密封,于室溫下放置0、15、30 d后進行考察。
1.4.3 復方半邊蓮凝膠防腐劑的選擇:固定載藥量為1 g/g(每g含藥凝膠中含飲片1 g),卡波姆0.25 g、三乙醇胺1.0 g、甘油0.4 g、10%月桂氮卓酮無水乙醇溶液2 g,按照上述凝膠制備方法制成凝膠20 g,同法制成5份,分別加5%羥苯乙酯乙醇溶液0、0.2、0.3、0.4、0.5 g,攪勻。
以細菌數、霉菌數和酵母菌作為考察指標,將制得的凝膠置無菌白色透明玻璃容器中并密封,于室溫下放置0、30 d后,按薄膜過濾法[17]檢查。
1.4.4 復方半邊蓮凝膠pH調整劑的選擇:按照上述凝膠制備方法,分別加入0.6、0.7、0.8、1.0、1.2 g的三乙醇胺,攪拌均勻,得不同三乙醇胺用量的復方半邊蓮凝膠。分別取各凝膠約1.0 g置小燒杯中,加純化水適量,攪勻,轉移至10 mL量瓶中,超聲20 min,放涼后,用純化水定容。離心,濾過,取續濾液測定pH值。
1.4.5 復方半邊蓮凝膠正交試驗設計:在上述單因素試驗基礎上,選取卡波姆940用量(A)、載藥量(B)、5%羥丙乙酯乙醇溶液用量(C)和三乙醇胺用量(D)為考察因素,按L9(34)正交表進行試驗,綜合評分標準[18]見表1,正交因素水平表見表2。采用綜合評分法對正交試驗數據進行分析。

表1 凝膠綜合評分標準Tab.1 The comprehensive scoring criteria of gel
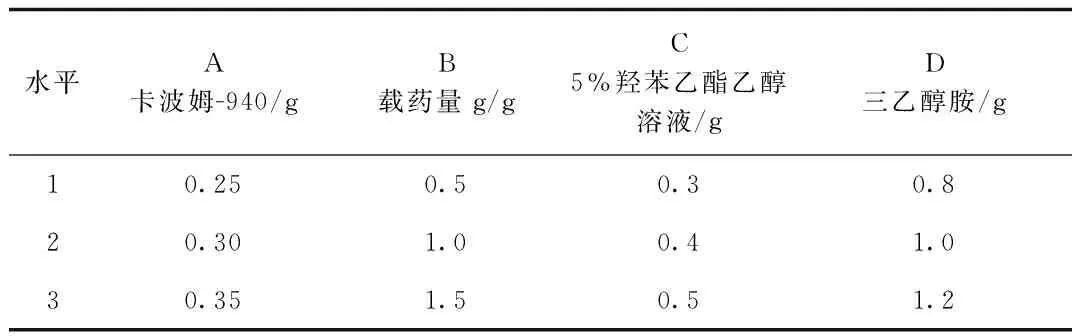
表2 正交試驗因素-水平表Tab.2 Factor-level table of orthogonal experiment
1.5 復方半邊蓮凝膠驗證試驗 按優選的制備工藝條件制備總量為20 g凝膠3批:稱取凝膠基質卡波姆-940 0.25 g置小燒杯中,加入甘油0.4 g,攪拌均勻使其全部潤濕,加入純化水適量使完全溶脹,得空白凝膠,備用。另稱取適量提取物(按每1 g凝膠含飲片1 g計),加入5%羥苯乙酯乙醇溶液0.3 g和10%月桂氮卓酮無水乙醇溶液2 g,混勻。將提取物溶液加入到空白凝膠中,攪拌使其分布均勻,加入1.0 g三乙醇胺,攪拌均勻,即得。
1.6 復方半邊蓮凝膠的質量控制
1.6.1 性狀:按照1.5項下中方法制備復方半邊蓮凝膠。
1.6.2 鑒別:取本品3 g,加稀鹽酸1 mL,用石油醚(60~90 ℃)振搖提取2次,每次10 mL,棄去石油醚液,水溶液用氨試液調節pH至9~10,用三氯甲烷振搖提取2次,每次10 mL,合并提取液,蒸干,殘渣加三氯甲烷1 mL使溶解,作為供試品溶液。另取半邊蓮對照藥材2 g,加飲用水100 mL,超聲提取20 min,濾過,濾液濃縮至10 mL,用氨試液調節pH值至9~10,同法制成對照藥材溶液。照薄層色譜法(中國藥典2010年版一部附錄VI B)試驗,吸取上述2種溶液各10 μL,分別點于同一硅膠G薄層板上,以甲苯-丙酮-乙醇-氨水(4:2:0.6:0.4)為展開劑,展開,取出,晾干,置紫外光燈(365 nm)下檢視。
1.6.3 檢查:按照凝膠劑項下的方法操作[17]。
1.6.4 含量測定:按復方半邊蓮注射液含量測定項下方法[19]測定:取本品3 g,精密稱定,置小燒杯中,加20%甲醇超聲使溶解,轉移至25 mL容量瓶中,用20%甲醇反復沖洗小燒杯,將沖洗液轉移至容量瓶中,并用20%甲醇定容,搖勻,以微孔濾膜(0.45 μm)濾過,取續濾液,測定野黃芩苷的含量。
2 結果
2.1 復方半邊蓮凝膠制備
2.1.1 復方半邊蓮凝膠基質的選擇:于室溫下放置15 d、30 d后與0 d比較,以0.25 g卡波姆為基質,所得的含藥凝膠易涂展,黏稠度適中,成型性好。見表3。

表3 凝膠基質成型性考察結果Tab.3 The formability results of gel matrix at different content
2.1.2 復方半邊蓮凝膠載藥量的選擇:于室溫下放置15 d、30 d后與0 d比較,以載藥量1.0 g/g所得的含藥凝膠易涂展,黏稠度適中,成型性好、質量穩定。見表4。

表4 載藥量考察結果Tab.4 The experiment results of different drug-loading rate
2.1.3 復方半邊蓮凝膠防腐劑的選擇:于室溫下放置30 d后與0 d比較,以0.3 g、0.4 g和0.5 g的5%羥苯乙酯乙醇溶液為防腐劑,所得的含藥凝膠穩定。見表5。
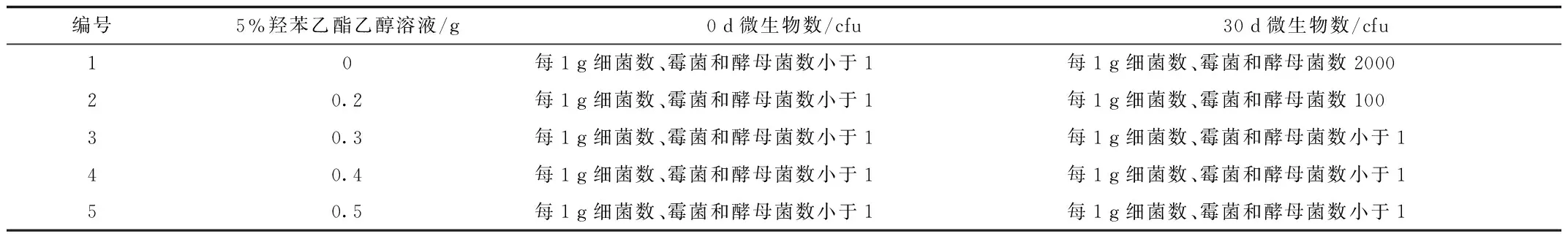
表5 防腐劑考察結果 Tab.5 The experiment results of preservatives at different content
2.1.4 復方半邊蓮凝膠pH調整劑的選擇:復方半邊蓮凝膠pH調整劑的選擇結果表明:1.0 g的三乙醇胺調節pH凝膠成型性良好,且易涂展。
2.1.5 復方半邊蓮凝膠正交試驗設計:由表6、表7分析結果可知,復方半邊蓮凝膠中各因素對復方半邊蓮凝膠影響的主次順序為:A> B>C>D,即卡波姆-940和載藥量為主要影響因素,且具有顯著性,三乙醇胺影響最小。確定的最佳工藝條件為A1B2C1D2,即以卡波姆-940 0.25 g、載藥量1 g/g(即每1 g凝膠含飲片1 g)、5%羥苯乙酯乙醇溶液0.3 g、三乙醇胺1.0 g、制備的凝膠成型性能好、易涂展、質量穩定。
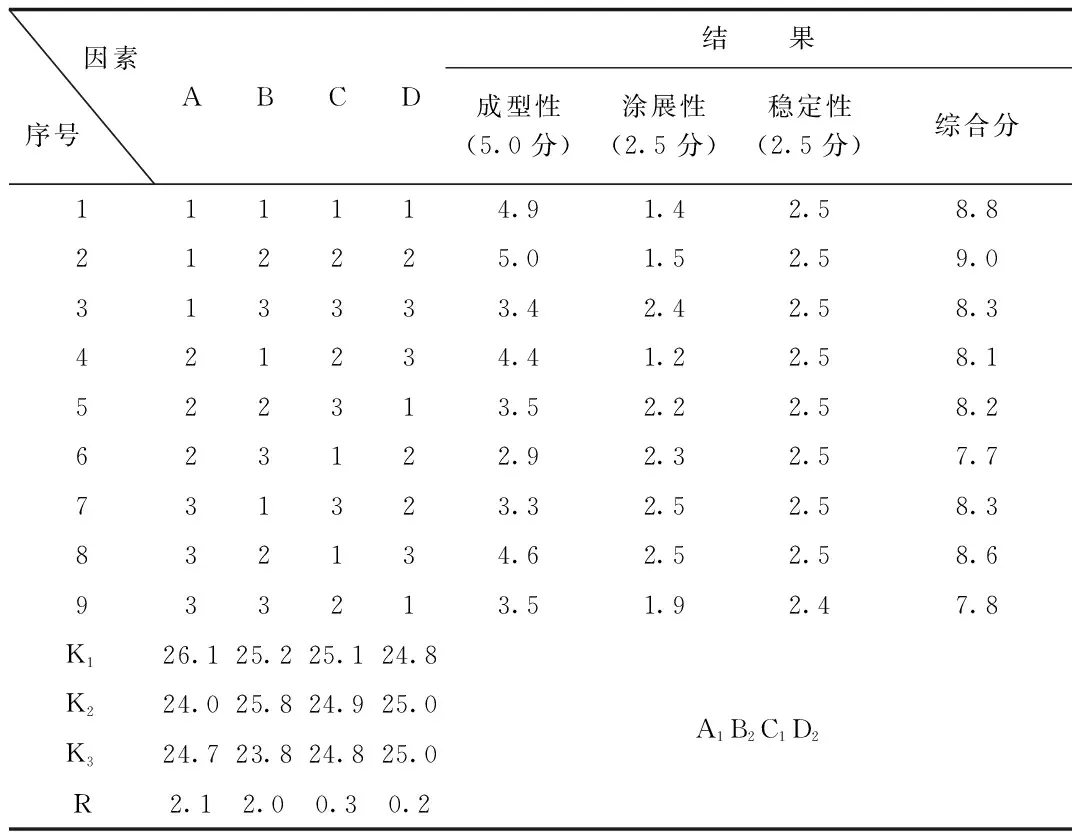
表6 正交設計試驗結果Tab.6 The results of orthogonal experiment
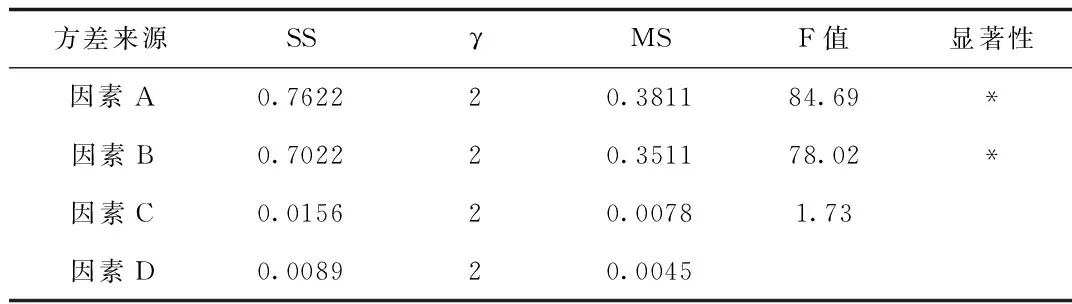
表7 方差分析表Tab.7 Analysis of variance table
F0.05(2,2)=19.00 F0.01(2,2)=99.00
按優選的工藝制備的3批凝膠,放置30 d后,其外觀均勻、細膩,易涂展,成型性良好,微生物限度檢測均符合規定。
2.2 復方半邊蓮凝膠的質量控制
2.2.1 性狀:本品為棕紅色半固體凝膠。
2.2.2 鑒別:①供試品色譜中,在與對照藥材色譜相應的位置上,顯相同顏色的熒光斑點。②在含量測定項下記錄的色譜圖中,供試品主峰的保留時間應與對照品峰的保留時間一致。
2.2.3 檢查:結果符合凝膠劑項下的有關規定[17]。
2.2.4 含量測定:按優選的工藝制備的3批凝膠野黃芩苷含量分別為8.77 mg/g,9.12 mg/g,9.02 mg/g,平均含量8.97 mg/g,每g飲片相當于野黃芩苷8.97 mg,遠遠高于復方半邊蓮注射液標準規定中的每g飲片相當于野黃芩苷0.27 mg。
3 討論
中藥凝膠劑一般由中藥提取物與基質構成制劑處方,影響凝膠劑成型的因素有載藥量、基質的用量、保濕劑的用量,以及pH調整劑的用量等。本實驗以3個指標的綜合作用進行評價,采用單因素試驗及正交試驗設計系統考察了影響凝膠質量的工藝條件,制備出復方半邊蓮凝膠。復方半邊蓮凝膠具有制備簡單,使用、攜帶方便的優點,提高了患者的依從性。
卡波姆(carbomer)為丙烯酸鍵合烯丙基蔗糖或季戊四醇烯丙醚的高分子聚合物[20]。最早由美國Goodrich公司生產,商品名為卡波普(Carbopol)[21],中國藥典2000年版開始收載[22]。卡波姆是pH型凝膠基質[23],卡波姆水溶液的pH為2.5~3.5,而卡波姆只有在pH大于5,才有一定的黏性,通常采用pH調整劑為三乙醇胺和氫氧化鈉,但氫氧化鈉為強堿,對皮膚有刺激性,所以本試驗選擇弱堿性的三乙醇胺為pH調整劑[24],且pH控制在6.8~7.0較好。卡波姆940具有易于涂展、黏附性好、易清洗、無油膩感、能吸收組織滲出液、對皮膚無刺激性等特點,常作為凝膠劑骨架材料被廣泛用于緩控釋經皮制劑的制備,其用量會直接影響凝膠黏度和藥物的釋放,一般選用質量分數0.5%~2.0%[25]。處方中選用0.4 g甘油為保濕劑、2g10%月桂氮卓酮無水乙醇溶液為促透劑。
本研究中載藥量對凝膠的成型性能影響較大,可能是藥物的有效成分影響了卡波姆的成型性且改變了凝膠系統的pH,當載藥量大于1.5 g/g時,卡波姆用量達0.35 g,三乙醇胺用量達1.2 g,成型性能仍不理想。
按優選工藝條件制備的復方半邊蓮凝膠外觀、涂展性、穩定性等均符合規定,作為新劑型,還需對其刺激性、藥物的透皮吸收、藥物的體外抗菌作用進行相關考察。
[1] 姜艷艷,石任兵,劉斌,等.半邊蓮黃酮類化學成分研究[J].北京中醫藥大學學報,2009,32(1):59-61.
[2] 王桂玲,房建強,邊書芹,等.半枝蓮中總生物堿的提取及抑菌作用的初步研究[J].中成藥,2013,35(6):1315-1319.
[3] 蔣丹,王關林.22種中草藥抑菌活性的研究[J].遼寧高職學報,2003,5(4):140-141,146.
[4] 邊才苗.白花蛇舌草提取物的抑菌作用研究[J].時珍國醫國藥,2005,16(10):991-992.
[5] 王宇翎,張艷,方明,等.白花蛇舌草總黃酮的抗炎及抗菌作用[J].中國藥理學通報,2005,21(3):348-350.
[6] 石磊,王俊霞,李園園,等.復方半邊蓮生物活性研究[J].中國實驗方劑學雜志,2010,16(16):57-61.
[7] 李枝端.復方半邊蓮注射液抗菌消炎作用明確[N].中國社區醫師,2012-9-9(12).
[8] 芩桂芹.半邊蓮外用治療隱翅蟲皮炎[J].新醫學,1987,24(2):41.
[9] 劉彥,梁瑜,曾橋,等.自制蓮黃蘇打液治療隱翅蟲皮炎394例[J].皮膚科與性病,2002,24(1):41-42.
[10] 彭國英.雙花解毒湯合季德勝蛇藥片治療隱翅蟲皮炎12例[J].實用中西醫結合臨床,2004,4(2):50.
[11] 陳瓊,李丹,周紀磊.纖維素酶協同超聲波法提取復方半邊蓮注射液的工藝優選[J].中國實驗方劑學雜志,2014,20(7):13-15.
[12] 嚴遠質.復方半邊蓮注射液靜滴致嚴重過敏2例[J].藥物不良反應雜志,2005,7(1):44.
[13] 于泳,曲廣洪.復方半邊蓮注射液致過敏反應1例[J].基層醫學論壇,2006,10(4):337.
[14] 譚曉黎,慈紅麗.復方半邊蓮注射液致過敏反應4例分析[J].齊魯藥事,2005,24(7):442.
[15] 陳美明,周敏.肌注復方半邊蓮注射液致過敏性休克1例[J].中國麻風皮膚病雜志,2004,20(1):90.
[16] 李娜,于福文.復方半邊蓮注射液致過敏性休克1例[J].中國臨床藥學雜志,2004,13(6):377.
[17] 國家藥典委員會.中華人民共和國藥典[M].北京:中國醫藥科技出版社,2010,附錄79,附錄12.
[18] 李娜,買爾丹·馬合木提.新疆紫草提取物凝膠劑的制備及質量考察[J].中國實驗方劑學雜志,2011,17(1):14-17.
[19] 國家食品藥品監督管理局.國家藥品標準[S].北京:人民衛生出版社,2002:WS-10609(ZD-0609)-2002.
[20] 國家藥典委員會.中華人民共和國藥典(第一增補本)[M].北京:中國醫藥科技出版社,2013,519.
[21] 盧毅,張彤木,陶建生.卡波姆在藥劑學中的應用[J].中國醫藥工業雜志,2007,38(6):457-460.
[22] 國家藥典委員會.中華人民共和國藥典[M].北京:化學工業出版社,2000,133.
[23] Merclin N,Bramer T,Edsman K.Iontophoretic delivery of 5-aminolevulinic acid and its methyl ester using a carbopol gel as vehicle[J].J Control Release,2004,98(1):57-65.
[24] Rathapon A,Sirivat A,Vayumhasuwan P,Viscoelastic propertycs of carbopol 940 gels and their relationships to piroxicam diffusion coefficients in gel bases[J].Pharmaleutical Research,2005,22(12):2134-2140.
[25] 徐和,戴領,沈成英,等.苦參堿凝膠劑的制備及體外釋藥特性考察[J].中國實驗方劑學雜志,2014,20(1):8-11.
(編校:王儼儼)
Optimization of compound lobelia gel in preparation process
CHEN Qiong,WANG Hai-yan,YU Hong-xia,LI Qing-qing,YANG Jun-jieΔ
(Xinyang Key Laboratory of Xinyang Engineering Research Center for the Exploitation of Chinese Medicine Resources, Detection and Analysis of Chinese Medicine, Xinyang College of Agriculture and Forestry, Xinyang 464000, China)
ObjectiveTo study the factors which affect the preparation of compound lobelia gel and establish the optimal preparation process.MethodsBased on single factor test, formability, spread performance, stability were used as comprehensive evaluation indicators to select the preparation process by orthogonal design, taking the dosage of carbopol-940, drug loading, 5% hydroxy ethyl benzene ethanol solution and triethanolamine as factors. The content of scutellarin in gel was determined by HPLC.ResultsThe best prescription of compound lobelia gel was as follows: substrat of carbopol-940 was 0.25 g, 10% Azone for promoting the permeability was 2 g, pH regulator of triethanolamine was 1.0 g, moisturizer of glycerol was 0.4 g; preservatives of 5% ethylparaben ethanol solution was 0.3 g; the drug loading was 1 g processed herbs per 1 g gel.ConclusionThe preparation process of compound lobelia gel is simple, the product is texture and delicate stable.
compound lobelia; gel; preparation process; orthogonal test
河南省科技攻關項目(132102310266)
陳瓊,女,學士,副教授,研究方向:主要為中藥制藥新技術,E-mail:599299467@qq.com;楊俊杰,通迅作者,男,碩士,副教授,研究方向:主要為中藥化學,E-mail:285385557@qq.com。
R283.6
A
1005-1678(2015)03-0162-04

