組蛋白去乙酰化酶抑制劑放射增敏作用與DNA損傷修復機制關系的研究進展
韓永濤,羅月,鳳志慧
(山東大學1.齊魯醫院藥學部,2.公共衛生學院職業衛生與職業醫學系,山東濟南250012)
組蛋白去乙酰化酶抑制劑放射增敏作用與DNA損傷修復機制關系的研究進展
韓永濤1,羅月2,鳳志慧2
(山東大學1.齊魯醫院藥學部,2.公共衛生學院職業衛生與職業醫學系,山東濟南250012)
組蛋白去乙酰化酶抑制劑(HDACIs)是抑制HDAC活性并造成組蛋白過度乙酰化作用的一類化合物,根據其化學結構的特點,HDACIs化合物被分成短鏈脂肪酸、異羥肟酸、環肽和苯甲酰胺四大類。研究表明,HDACIs能抑制多種腫瘤細胞的生長,某些具有抗腫瘤作用的HDACIs已經進入臨床試驗階段。近年來還發現,HDACIs能增加腫瘤細胞對電離輻射的敏感性,具有較強的放射增敏作用,但該類化合物的放射增敏機制目前還不十分清楚,可能與其能增強腫瘤細胞的凋亡和自噬作用,以及DNA損傷修復機制破壞等有關,其中HDACIs通過導致DNA雙鏈斷裂修復機制障礙發揮放射增敏作用已越來越引起學者們的關注。為此,本文就HDACis的放射增敏作用與DNA損傷修復機制之間關系的研究進行綜述。
組蛋白去乙酰化酶抑制劑;輻射耐受性;DNA損傷
組蛋白去乙酰化酶抑制劑(histone deacetylase inhibitors,HDACIs)是抑制HDAC活性并造成組蛋白過度乙酰化作用的一類化合物[1-2]。研究表明,組蛋白乙酰化的程度與組織細胞轉錄活性和染色質結構的重塑等功能密切相關。近年來發現,HDACIs不但能抑制多種腫瘤細胞生長,還能增加腫瘤細胞對電離輻射(ionizing radiation,IR)的敏感性[1-2],表現出較強的增敏作用。因此,這類化合物的抗腫瘤作用逐漸受到關注。本文從其化合物結構特點、抗腫瘤特性和放射增敏作用及其機制等方面進行綜述。
1 HDACIs化合物及其特點
HDACIs包括許多結構不同的化合物,目前認為是一組有特異性的抗腫瘤藥物,其最重要的特點是對腫瘤細胞具有毒性作用,對正常組織細胞卻無明顯的毒性作用,正常細胞對其呈現耐受性。由于該類化合物均具有抑制HDAC活性的作用,因而被統稱為HDACIs。乙酰化是組蛋白一種重要的共價修飾。研究表明,組蛋白乙酰化主要由組蛋白乙酰化轉移酶和HDAC共同調控并維持一個平衡狀態,這種狀態與細胞轉錄調控和染色質結構重塑,甚至基因組穩定性都有密切的關系。一般認為,組蛋白的過度乙酰化是轉錄活躍的一個標志,低乙酰化則表示轉錄活性被抑制。目前根據HDACIs的結構特點將其分為4類[1-3]。①短鏈脂肪酸類,該類化合物有丙戊酸(valproic acid,VPA)、丁酸鹽和丁酸苯酯;②異羥肟酸類,或稱為氧肟酸鹽類,曲古抑菌素A(trichostatin A,TSA)是第一個被發現具有抑制HDAC活性的天然氧肟酸;伏立諾他(vorinostat)(亦稱為N-羥基-N′-苯基辛二酰胺,SAHA)是第一個被美國食品藥物管理局(Food and Drug Administration,FDA)批準的臨床上用于治療皮膚性T淋巴細胞瘤的藥物;③環肽類,天然產物縮酚酸肽FK-228和羅米地辛(romidepsin)等;④苯甲酰胺類,包括MS-275和MGCD0103等。雖然每類HDACIs均能抑制HDAC活性,但由于其結構特征不同,每類HDACIs通常選擇性地抑制一種或幾種HDAC的活性,因而其在生物學上的效應也存在一定的區別。關于這幾類化合物在分子結構、選擇性靶向的HDAC、生物學作用及其所處臨床試驗階段等見表1。
目前已發現人類有18種HDAC,依據它們與酵母菌HDAC的同源性、亞細胞定位以及酶活性將其分為Ⅰ,Ⅱ,Ⅲ及IV類。Ⅰ類HDAC的特點是與酵母菌去乙酰化酶RPD3(histone deacetylase RPD3)蛋白同源,分布于核內,在人體多種組織和細胞中表達;Ⅱ類HDAC是與酵母菌去乙酰化酶Had(histone deacetylase Had)蛋白同源,它們能在細胞核與細胞漿之間轉運;Ⅲ類HDAC則是與酵母菌沉默信息調控子2(silent information regulator 2,Sir2)同源,在應答細胞內還原狀態變時需要煙酰胺腺嘌呤二核苷酸(NAD+)參與調控基因表達;而Ⅳ類HDAC只有1個成員,HDAC11,雖然它與Ⅰ和Ⅱ類HDAC的催化區有相似性,但是并不具備它們的其他生物學特性[4]。HDAC與不同的抑制劑之間的關系見表1。
2 HDACIs對腫瘤細胞的放射增敏作用
2.1 抗腫瘤作用
本研究集體和其他學者的許多研究結果均表明,VPA,SAHA,TSA和PCI-24781等HDACIs對多種腫瘤細胞和轉型細胞的生長有直接的抑制作用[5-8]。VPA 500 μmol·L-1對結腸癌、食管癌和乳腺癌等腫瘤細胞的生長即具有抑制作用[5-8]。MTT實驗結果表明,VPA可顯著降低食管癌鱗狀細胞的存活率,呈明顯的濃度依賴性[9]。SAHA可抑制人卵巢癌紫杉醇耐藥細胞OC3/P的存活,對肝癌細胞亦具有殺傷作用[4,9]。
2.2 對腫瘤細胞放射增敏作用
HDACIs化合物在細胞水平上對肺癌、腦膠質瘤、食管癌、前列腺癌、結腸癌和乳腺癌等腫瘤細胞均具有放射增敏作用[9-13]。與單純IR處理組比較,PCI-24781能顯著增加結腸癌HCT116、人大細胞肺癌細胞NCI-H460和人肺腺癌A549等細胞的IR敏感性,表現為細胞克隆形成率明顯下降[14]。我們研究發現,VPA 0.5 mmol·L-1還可增強乳腺癌細胞的IR敏感性[5]。而且在腸癌HCT116細胞研究中發現,VPA所致的腫瘤放射增敏作用可能與細胞的p53狀態密切相關,VPA對p53野生型細胞的作用敏感于p53缺陷型細胞[10]。但也有研究報道,HDACIs對胃腸道腺細胞的放射增敏作用并不依賴于p53的活性[15]。以上研究提示,HDACIs在增強腫瘤細胞放射敏感性方面具有不可忽視的作用。
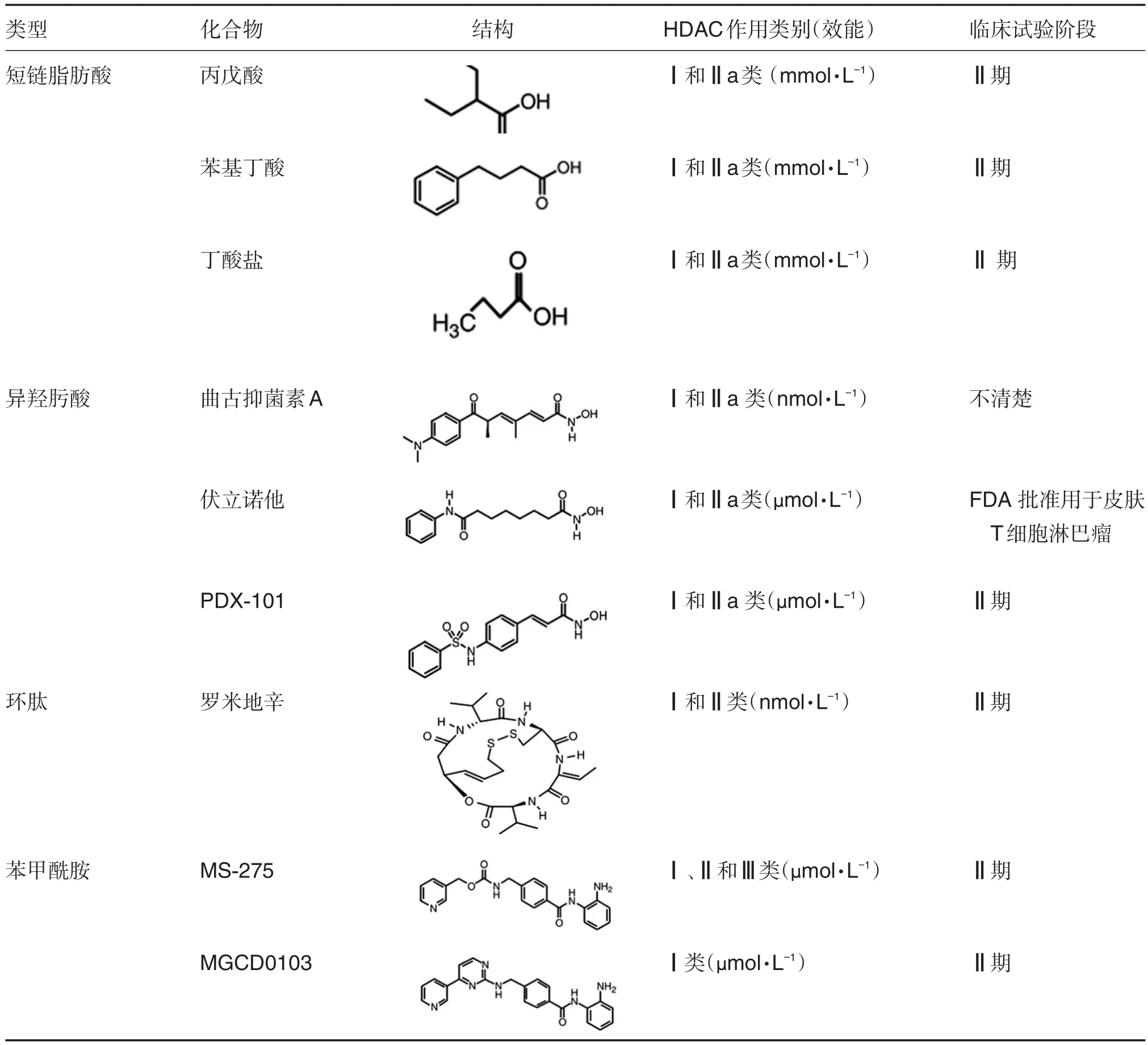
表1 主要組蛋白去乙酰化酶抑制劑(histone deacetylase inhibitors,HDACIs)分子的結構和生物學功能
深入研究還表明,HDACIs對動物實體瘤腫瘤細胞亦具有放射增敏作用。應用腦腫瘤細胞U251、前列腺癌和腸癌HCT116細胞進行裸鼠移植瘤動物實驗,與單純IR組比較,VPA與IR聯合應用使移植瘤生長得到明顯的抑制[10,15]。
3 HDACIs對腫瘤細胞放射增敏作用的DNA損傷修復機制
HDACIs增強腫瘤細胞對IR的敏感性的作用機制可能與細胞凋亡、自噬以及DNA損傷修復機制破壞等有關[1,16-17]。其中,HDACIs對DNA損傷修復機制的影響越來越引起學者們關注。目前認為,HDACIs能夠通過影響DNA損傷修復機制,造成DNA雙鏈斷裂(double-strand break,DSB)不能有效地被修復,使腫瘤細胞內DNA損傷蓄積,表現出對IR的更為敏感。在應答DNA損傷修復反應中,DSB信號能通過級聯反應激活細胞傳導通路,啟動DNA修復系統以保證遺傳信息的完整,這一信號通路包括感受器、傳導器及下游效應器等信號分子,信號通路中任何部分發生功能障礙,都將造成系統對DNA損傷修復能力的下降。
3.1 DNA雙鏈斷裂的蓄積增加
HDACIs可影響DNA損傷修復機制一個關鍵實驗依據是發現DNA DSB在腫瘤細胞核內的蓄積增加。DNA損傷后,組蛋白家族2A變異體(histone family 2A variant,H2AX)將迅速發生磷酸化,磷酸化的H2AX焦點形成(γ-H2AX foci formation)被認為是DNA DSB損傷的標志物,同時它還可作為DNA損傷的早期應答因子。在DNA損傷中,H2AX還具有促進局部DNA修復因子[如乳腺癌易感基因1(breast cancer susceptibility gene1,BRCA1)和p53結合蛋白1(p53 binding protein,53BP1)等]募集到DNA損傷區域修復損傷的DNA,維持基因組的穩定性[18]。Sha等[9]研究報道,高濃度(5 mmol·L-1)VPA能使CHO33細胞DNA DSB增加,核內γ-H2AX焦點形成蓄積顯著增加,提示VPA可能直接造成DNA損傷。進一步研究證明,VPA和TSA等HDACIs預處理的腫瘤細胞使IR誘導的γ-H2AX焦點形成進一步增加[19-20],提示HDACIs能加重IR所誘導DNA DSB的蓄積。還有,IR誘導的γ-H2AX焦點消退的時間也是反映DNA損傷修復能力的一項重要指標。研究發現,HDACIs預處理黑色素瘤細胞或者人皮膚成纖維細胞后,IR引起的γ-H2AX或53BP1焦點消退的時間明顯延長,間接推測HDACIs可致細胞對DSB修復能力降低[13]。以上研究表明,HDACIs可能造成腫瘤細胞內DSB損傷的蓄積,使其對放射更加敏感,而且也可能下調細胞修復損傷的DNA能力。
3.2 DNA損傷反應通路的激活障礙
DNA損傷應答因子毛細血管擴張性共濟失調癥突變蛋白(mutated in ataxia telangiectasia,ATM)和53BP1等被認為是DNA損傷修復通路中重要的感受器。研究表明,在DSB應答反應中,HDACIs可影響ATM和53BP1的活性。在人或纖維母細胞中,ATM和HDAC-I可相互結合,IR能增強與ATM功能相關的HDAC活性,HDACIs(如TSA)或者下調HDAC-I都可抑制與ATM相關的HDAC活性,提示HDACIs可能在ATM介導的DSB的信號傳導通路中發揮作用[21]。在應答DNA損傷時,發現HDAC-IV和53BP1均被募集到DSB區域,但HDAC-IV蛋白表達抑制后,53BP1蛋白因子的表達也被下調且不能被有效地募集到DNA損傷區參與DSB修復反應,還會造成G2/M期阻滯[22]。以上研究提示,HDACIs可引起DNA損傷反應通路中感受器ATM和53BP1活性抑制,進一步導致DSB修復機制的啟動障礙,最終引起DNA DSB在核內蓄積,增加腫瘤細胞的放射敏感性。
3.3 DNA損傷修復因子表達的下調
同源重組(homologous recombination,HR)和非同源末端連接(non-homologous end joining,NHEJ)是修復DNA DSB損傷的2種重要機制[23],重組酶Rad51(recombinase Rad51)和DNA依賴性蛋白激酶催化亞單位(catalytic sunbunit of the DNA-dependent protein kinase,DNA-PKcs)分別在調控HR和NHEJ機制中起關鍵的作用,也被認為是DNA損傷修復通路的效應器。通常IR可誘導Rad51和DNA-PKcs表達上調,在前列腺癌和膠質瘤細胞中,SAHA可抑制IR誘導的這兩種修復蛋白表達的上調[24]。VPA預處理食管癌TE11細胞,Rad51蛋白表達水平被顯著下調[8]。丁酸鈉處理黑色素瘤細胞,NHEJ中關鍵蛋白因子Ku70、Ku80和DNA-PKcs mRNA和蛋白表達水平均下降[13,25]。由此提示,HDACIs可能抑制HR和NHEJ修復中關鍵因子的表達,直接影響其參與DNA損傷修復過程,進一步提示HDACIs通過導致DSB修復機制障礙發揮放射增敏作用。
4 展望
雖然眾多研究指出,HDACIs可通過影響DNA損傷反應通路的激活以及DNA損傷修復因子表達等方式,造成DNA損傷修復機制障礙,但它們之間的密切相關性還需要更確鑿的直接實驗依據。還需指出的是,目前HDACIs中大多數化合物已進入臨床試驗階段,迫切需要闡明在臨床安全劑量條件下這類化合物的抗腫瘤作用以及其作用的特異性靶器官和靶基因等,這不但有助于闡述HDACIs致腫瘤細胞放射增敏的作用機制,而且還能更好地指導這類新型抗腫瘤藥物在臨床上的應用,從而為腫瘤患者個體化治療制定出有效的方案和對策。
[1]Bolden JE,Peart MJ,Johnstone RW.Anticancer activities of histone deacetylase inhibitors[J].Nat Rev Drug Discov,2006,5(9):769-784.
[2]Dokmanovic M,Clarke C,Marks PA.Histone deacetylase inhibitors:overview and perspectives[J].Mol Cancer Res,2007,5(10):981-989
[3]Camphausen K,Cerna D,Scott T,Sproull M,Burgan WE,Cerra MA,et al.Enhancement ofin vitroandin vivotumor cell radiosensitivity by valproic acid[J].Int J Cancer,2005,114(3):380-386.
[4]Marks PA,Xu WS.Histone deacetylase inhibitors:Potential in cancer therapy[J].J Cell Biochem,2009,107(4):600-608.
[5]Zhao XP,Luo Y,Dong C,Zhang FM,Feng ZH. Effect of valproic acid on radiosensitivity to breast cancer cells[J].Chin J Pharmacol Toxicol(中國藥理學與毒理學雜志),2015,29(2):247-252.
[6]Thurn KT,Thomas S,Moore A,Munster PN.Rational therapeutic combinations with histone deacetylase inhibitors for the treatment of cancer[J].Future Oncol,2011,7(2):263-283.
[7]Arundel CM,Glicksman AS,Leith JT.Enhancement of radiation injury in human colon tumor cells by the maturational agent sodium butyrate(NaB)[J].Radiat Res,1985,104(3):443-448.
[8]Biade S,Stobbe CC,Boyd JT,Chapman JD. Chemical agents that promote chromatin compaction radiosensitize tumour cells[J].Int J Radiat Biol,2001,77(10):1033-1042.
[9]Sha K,Winn LM.Characterization of valproic acid-initiated homologous recombination[J].Birth Defects Res B Dev Reprod Toxicol,2010,89(2):124-132.
[10]Chen X,Wong P,Radany E,Wong JY.HDAC inhibitor,valproic acid,induces p53-dependent radiosensitization of colon cancer cells[J].Cancer Biother Radiopharm,2009,24(6):689-699.
[11]Entin-Meer M,Rephaeli A,Yang X,Nudelman A,VandenBerg SR,Haas-Kogan DA.Butyric acid prodrugs are histone deacetylase inhibitors that show antineoplastic activity and radiosensitizing capacity in the treatment of malignant gliomas[J].Mol Cancer Ther,2005,4(12):1952-1961.
[12]Kim JH,Shin JH,Kim IH.Susceptibility and radiosensitization of human glioblastoma cells to trichostatinA,ahistonedeacetylaseinhibitor[J]. 2004,59(4):1174-1180.
[13]Munshi A,Kurland JF,Nishikawa T,Tanaka T,Hobbs ML,Tucker SL,et al.Histone deacetylase inhibitors radiosensitize human melanoma cells by suppressing DNA repair activity[J].Clin Cancer Res,2005,11(13):4912-4922.
[14]Feng Z,Scott SP,Bussen W,Sharma GG,Guo G,Pandita TK,Powell SN.Rad52 inactivation is synthetically lethal with BRCA2 deficiency[J].Proc Natl Acad Sci USA,2011,108(2):686-691.
[15]Zhang Y,Adachi M,Zhao X,Kawamura R,Imai K. Histone deacetylase inhibitors FK228,N-(2-aminophenyl)-4-[N-(pyridin-3-yl-methoxycarbonyl)amino-methyl]benzamide and m-carboxycinnamic acid bis-hydroxamide augment radiation-induced cell death in gastrointestinal adenocarcinoma cells[J].Int J Cancer,2004,110(2):301-308.
[16]Robert T,Vanoli F,Chiolo I,Shubassi G,Bernstein KA,Rothstein R.HDACs link the DNA damage response,processing of double-strand breaks and autophagy[J].Nature,2011,471(7336):74-9.
[17]Shubassi G,Robert T,Vanoli F,Minucci S,Foiani M.Acetylation:a novel link between doublestrand break repair and autophagy[J].Cancer Res,2012,72(6):1332-1335.
[18]Wyman C,Kanaar R.DNA double-strand breakrepair:all's well that ends well[J].Annu Rev Genet,2006,40:363-383.
[19]Harikrishnan KN,Karagiannis TC,Chow MZ,El-Osta A.Effect of valproic acid on radiationinduced DNA damage in euchromatic and heterochromatic compartments[J].Cell Cycle,2008,7(4):468-476.
[20]Karagiannis TC,Harikrishnan KN,El-Osta A.Disparity of histone deacetylase inhibition on repair of radiation-induced DNA damage on euchromatin and constitutive heterochromatin compartments[J].Oncogene,2007,26(27):3963-3971.
[21]Thurn KT,Thomas S,Raha P,Qureshi I,Munster PN.Histone deacetylase regulation of ATM-mediated DNA damage signaling[J].Mol Cancer Ther,2013,12(10):2078-2087.
[22]KaoGD,McKennaWG,GuentherMG,MuschelRJ, Lazar MA,Yen TJ.Histone deacetylase 4 interacts with 53BP1 to mediate the DNA damage response[J].J Cell Biol,2003,160(7):1017-1027.
[23]Zhao XP,Zhang FM,Feng ZH.Progress in role of breast cancer susceptibility gene 1 in DNA damage repair[J].Chin J Pharmacol Toxicol(中國藥理學與毒理學雜志),2014,28(4):606-611.
[24]Chinnaiyan P,Vallabhaneni G,Armstrong E,Huang SM,Harari PM.Modulation of radiation response by histone deacetylase inhibition[J].IntJRadiatOncolBiolPhys,2005,62(1):223-229.
[25]Chung YL,Lee YH,Yen SH,Chi KH.A novel approach for nasopharyngeal carcinoma treatment uses phenylbutyrate as a protein kinase C modulator:implications for radiosensitization and EBV-targeted therapy[J].Clin Cancer Res,2000,6(4):1452-1458.
Progress in relationship between histone deacetylase inhibitors-induced radiosensitization and the mechanism of DNA damage repair
HAN Yong-tao1,LUO Yue2,FENG Zhi-hui2
(1.Department of Pharmacy,Qilu Hospital,2.Department of Occupational Health and Occupational Medicine,School of Public Health,Shandong University,Jinan 250012,China)
Histone deacetylase inhibitors(HDACIs)are compounds that can inhibit histone deacetylase(HDAC)while inducing histone hyperacetylation,which are divided into four types:shortchain fatty acid,hydroximic acid,cyclic peptide and benzamide according to chemical structure features.It has been demonstrated that HDACIs can inhibit the growth of a number of tumor cells,and the study on anti-cancer effects of some HDACIs is in the stage of clinical trials.It has been found that HDACIs can increase the radiosensitivity to tumor cells,indicating that HDACIs may be a potential sensitizer to radiation.The mechanism of HDACIs-induced radiosensitization is still not so clear,which may be related to apoptosis,autophygy or the damage to DNA repair function.And it has been attracting more attention that disrupting DNA repair activity is associated with HDACIs-mediated radiosentization. Thus,research progress in the relationship between HDACIs-mediated radiosentization and the mechanism of DNA damage repair is reviewed in this paper.
histone deacetylase inhibitors;radiation tolerance;DNA damage
The project supported by National Natural Science Foundation of China(81172527);National Natural Science Foundation of China(81472800);and Science and Technology Program of Shandong Province(2013GGE27052)
FENG Zhi-hui,Tel:(0531)88382137,E-mail:fengzhihui@sdu.edu.cn
R979.1,R962
A
1000-3002-(2015)04-0633-05
10.3867/j.issn.1000-3002.2015.04.016
2015-02-04接受日期:2015-07-22)
(本文編輯:齊春會)
國家自然科學基金(81172527);國家自然科學基金(81472800);山東省科技發展計劃(2013GGE27052)
韓永濤,主管藥師,主要從事臨床藥學研究。
鳳志慧,Tel:(0531)88382137,E-mail:fengzhihui@sdu.edu.cn

