生物來源的固體顆粒制備Pickering乳液的研究進展
孫翠霞,劉夫國,楊 偉,袁 芳,高彥祥
(中國農業大學食品科學與營養工程學院,北京 100083)
生物來源的固體顆粒制備Pickering乳液的研究進展
孫翠霞,劉夫國,楊 偉,袁 芳,高彥祥*
(中國農業大學食品科學與營養工程學院,北京 100083)
天然來源、可再生和可生物降解的固體顆粒用于制備Pickering乳液已成為研究熱點。本文綜述了固體顆粒的種類、制備方法與性質表征,重點介紹了生物來源的有機顆粒如多糖和蛋白質對Pickering乳液的穩定作用,并總結了影響Pickering乳液穩定性的因素,同時闡述了Pickering乳液在生命科學領域的潛在應用。
固體顆粒,Pickering乳液,穩定性
乳液(emulsion)是由一種或幾種液體以小液滴的形式分散于另一種與其互不相溶的液體中形成的多相分散體系,通常分為水包油型(O/W)和油包水型(W/O)[1]。由于油-水界面積較大,乳液是一種熱力學不穩定體系,必須向體系中加入乳化劑,通過減少兩相之間的界面張力,才能獲得穩定的乳液[2]。然而,過量的非食品級乳化劑必須從樣品中去除,否則會對人體產生傷害,影響和破壞乳液后續的應用,如乳化劑會誘導組織發炎甚至造成細胞損傷,這使得由乳化劑制備的傳統乳液在醫藥制劑方面的應用受到限制[3]。
20世紀初,Ramsden等人最早發現將不溶性固體細粉與水和一些油性溶劑進行混合分散時,固體細粉包裹在分散相液滴的表面,形成一個固體殼層;當分散相液滴相互碰撞時,固體殼層對液滴的變形和聚集起到阻礙作用,可以形成較為穩定的乳液[4]。隨后,Pickering對該乳液體系進行了較為深入和系統的研究[5]。因此,由固體顆粒代替乳化劑而制備的乳液被命名為Pickering乳液,如圖1所示[6]。另外,由固體顆粒通過界面作用阻止乳液液滴聚結的機制稱為Pickering穩定[7]。Binks研究指出,固體顆粒在油-水界面產生不可逆的吸附,而表面活性劑在一定的時間范圍內其吸附和解吸速度相對較快[8]。因此,與傳統表面活性劑穩定的乳液相比,Pickering乳液具有更高的穩定性,可廣泛應用于醫藥、農業、食品和化妝品等領域。
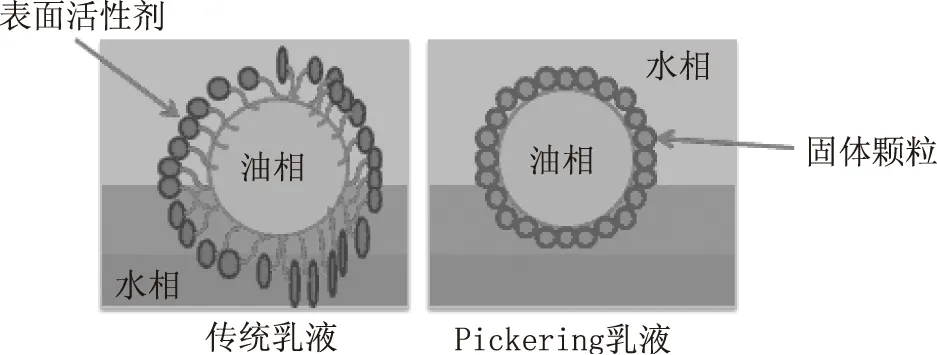
圖1 O/W型傳統乳液和Pickering乳液的結構圖示[3]Fig.1 Sketches of the Pickering emulsionand a classical emulsion[3]
研究表明,Pickering乳液的穩定性在很大程度上取決于固體顆粒的性質,因此,本文綜述了固體顆粒的種類、制備方法與性質表征,重點介紹了生物來源的有機顆粒如多糖和蛋白質對Pickering乳液的穩定機理,并總結了影響Pickering乳液穩定性的因素,同時闡述了Pickering乳液的應用前景。
1 用于制備Pickering乳液的固體顆粒
目前對于固體顆粒穩定Pickering乳液的研究集中于無機或合成粒子,如二氧化硅[9]、二氧化鈦[10]、鋰皂石粘土[11]、磁鐵礦[12]、氧化鋅[13]、氧化石墨烯[14]、各向異性的Janus顆粒[15]等。雖然由這些無機或合成粒子制備的Pickering乳液穩定性較好,但生物相容性較差,這極大限制了Pickering乳液在醫藥、農業、食品和化妝品等領域的應用。因此,尋求環境友好型、天然來源、可再生和可生物降解的固體顆粒用于穩定Pickering乳液已成為目前研究的熱點。
在現有的研究中,生物來源的膠體顆粒已用于穩定Pickering乳液,如多糖類,包括淀粉納米晶[16-18]、經化學修飾的淀粉納米顆粒[19]、纖維素納米晶[20-24]、甲殼素納米晶[25-26];蛋白質類,包括大豆分離蛋白[27-28]、豌豆分離蛋白[29]、乳鐵蛋白[30]、乳清蛋白[31]、玉米醇溶蛋白[32-33];另外,還有具有生物活性的小分子物質如黃酮[34-35]和植物甾醇[36]。
1.1 多糖
多糖是多分散性大分子,親水性強。一些多糖能夠吸附在油-水界面,通過界面相互作用,作為乳液的穩定劑。Li等[37]選用大米淀粉、小麥淀粉和蠟質玉米淀粉制備出穩定的乳液,其中大米淀粉(顆粒直徑為5.2 μm)制備的乳液穩定性最好。Rayner等[38]采用藜麥淀粉(顆粒直徑為2.5 μm)制備穩定的乳液,由于藜麥淀粉不含谷朊蛋白,無致敏性,顆粒直徑相對較小(直徑為0.5~3 μm)且分布均勻,使藜麥淀粉成為穩定Pickering乳液的研究熱點。
多糖膠體表面活性源于兩種途徑,一是某些非極性的化學基團吸附在親水多糖的骨架上,二是蛋白質與碳水化合物(如阿拉伯膠、甜菜果膠)發生部分共價結合[39-40]。即使多糖不具有表面活性,只要能與預先吸附的蛋白質通過靜電絡合形成次級空間保護層,也能夠促進乳液的界面穩定[41]。另外,多糖組分可通過誘導與蛋白質共價結合形成永久的結合物。最常用的方法是干熱處理,即美拉德反應。所得的具有表面活性的蛋白質-多糖結合物可以用于制備Pickering乳液[42-43]。
1.2 蛋白質
大多數蛋白質分子具有吸附在油-水界面、伸展并且聚集形成二維網絡的能力,可作為乳液有效的穩定劑[44]。用于吸附的主要熱力學驅動力使蛋白質的非極性側鏈遠離水溶液的不利環境,使界面區域的水分子濃度降低。次級驅動力與吸附的蛋白質分子的伸展有關。這會進一步導致蛋白質與蛋白質、蛋白質與水之間相互作用的平衡發生變化[45]。一旦吸附,蛋白質通常不能輕易地從界面解吸。因此,蛋白質的吸附通常認為是“不可逆”的。吸附在界面的蛋白質對分散顆粒和液滴的穩定作用與蛋白質的分子結構、水溶液的離子強度有關,可以結合空間作用和靜電作用進行解釋[46]。如無序的蛋白質如酪蛋白,是一種優良的空間穩定劑[47]。一旦蛋白質吸附在單個分散的油滴上,在油-水界面形成單吸附層,會產生較強的斥力屏障,可阻止相鄰液滴緊密靠近。球形蛋白質(乳蛋白)吸附層的界面結構有很大不同,可以看作是一個二維排列的緊湊顆粒層。蛋白質聚集體的吸附或蛋白質與多糖相互作用后的混合吸附會產生不均勻的吸附層或多重吸附層,具有更復雜的界面結構。蛋白質吸附層的結構區別可通過蛋白質的表面剪切流變性差異進行表征。酪蛋白的吸附層呈液體狀,容易移動,球狀蛋白的單吸附層剛性更強,具有二維凝膠或玻璃態的性質[44-45]。
1.3 蛋白質與多糖復合顆粒的協同穩定作用
通過對膠體顆粒的表面進行疏水改性,可改善顆粒的潤濕性,增強乳液的穩定性。疏水改性可通過加入小分子的表面活性劑,如十二烷基磺酸鈉(SDS)、吐溫系列(Tween 20、40、60、80)的乳化劑等[48-49]。為避免加入小分子表面活性劑而改善顆粒潤濕性的方法是,加入兩種帶相反電荷的納米顆粒,通過異種電荷的吸引聚合改善顆粒的潤濕性,顆粒混合物呈絮凝狀分散在水介質中,靜電荷足夠低,充分疏水吸附在油滴表面使其穩定,從而穩定乳液[50-51]。
2 固體顆粒的制備方法與性質表征
2.1 反溶劑沉淀法
最常用的制備固體顆粒的方法為反溶劑沉淀法,又稱為液液分散法或相分離法。Patel等[52]采用反溶劑沉淀法制備玉米醇溶蛋白—姜黃素復合膠體顆粒,透射電鏡結果表明顆粒呈球形,平均粒徑為100~150 nm;姜黃素在顆粒中的包埋率為86.8%,負載能力4.1%;通過差示掃描量熱法和X-射線衍射對固態膠體顆粒的研究表明,被包埋的姜黃素表現出非晶性質;紫外全波長掃描結果表明,膠體顆粒對姜黃素的包埋作用增強了姜黃素的耐光性;另外,Patel等[52]還發現,該顆粒在廣泛的pH范圍內(1.2,4.5,6.7和7.4)和在模擬腸道條件下具有良好的膠體穩定性;Patel等[52]通過體外粘膜吸附研究表明,姜黃素在粘膜中150 min的保留率仍在60%以上,Caco-2細胞粘蛋白的研究進一步證實了玉米醇溶蛋白-姜黃素復合納米顆粒的粘膜吸附特性。de Folter等[32]采用反溶劑沉淀法制備玉米醇溶蛋白膠體顆粒(ZCP),并首次采用ZCP制備出穩定的O/W型Pickering乳液,乳液穩定性與顆粒濃度、pH、離子強度有關。研究表明,未經改性的ZCP同時具有疏水性和親水性,在高于或低于玉米醇溶蛋白等電點(pH6.5)時,在10 mol/L的離子強度下,ZCP在O/W乳液中的三相接觸角在90°左右,可強力吸附于油-水界面,可以制備穩定的、不含表面活性劑的乳液,該乳液經高速剪切分散器13500 r/min,2 min的混合分散后,乳液的液滴粒徑范圍為10~200 μm。Zou等[53]采用液液分散法制備玉米醇溶蛋白-蔓越莓原花青素(Z-CPs)復合納米顆粒,結果表明,隨著CPs在Z-CPs中的比例由1∶8增加至1∶2,Z-CPs納米顆粒的直徑由392 nm增加至447 nm,包埋率由10%增加至86%。掃描電鏡結果表明,Z-CPs納米顆粒呈球形;傅里葉變換紅外光譜研究表明,Z與CPs之間的交互作用是氫鍵和疏水相互作用;通過人類前骨髓性白血病HL-60細胞的細胞培養研究表明,與CPs相比,包封在納米顆粒中的CPs降低了細胞毒性。
2.2 超臨界流體技術
Hu等[54]采用超臨界流體技術(SEDS)通過增強溶液的分散性能用于制備玉米醇溶蛋白-葉黃素(Z-L)納米顆粒。SEDS的壓力、溫度、葉黃素與玉米醇溶蛋白的比率、溶液流速等對負載量、包封率、平均粒徑、顆粒形態產生顯著影響。較低的溫度和流速結合高的壓力,能制備粒徑更小,更規則的球形顆粒。當工藝參數為壓力10 MPa,L與Z的質量比為1∶18,45 ℃下,控制溶液流速1.0 mL/min,能夠獲得粒徑尺寸范圍較小、具有緩釋能力的Z-L納米顆粒。
2.3 熱處理結合靜電絡合作用
最近的研究表明,球狀蛋白和帶電多糖的復合納米顆粒可通過熱處理結合靜電絡合作用制備。有兩種制備方法:一是在高于其熱變性溫度的條件下加熱球狀蛋白溶液形成蛋白顆粒,然后加入離子多糖,調整溶液條件,以促進多糖與蛋白質顆粒的靜電絡合[55];二是蛋白質-多糖先在室溫下通過靜電作用形成復合物,然后在高于其熱變性溫度的條件下加熱此復合物,以促進蛋白質聚集和微粒形成。這兩種方法都能形成非常小的生物聚合物顆粒,具有良好的穩定性,不易沉淀,不易受pH和離子強度的影響[56-57]。
Peinado等[58]采用熱處理的乳鐵蛋白(LF)與陰離子多糖(海藻酸鹽、卡拉膠、果膠)通過靜電絡合作用制備生物聚合物復合膠體顆粒,并研究了顆粒穩定性和形態特征。在高于LF的變性溫度下(91 ℃,20 min)加熱LF溶液(0.2% LF,pH7),可促進蛋白質的伸展,抑制蛋白質聚集,形成蛋白質顆粒,粒徑范圍為200~400 nm,等電點約為8.5。將該蛋白質顆粒與陰離子多糖在pH8時混合,然后降低pH,通過靜電作用促進多糖沉積在蛋白顆粒表面形成復合膠體顆粒。使用濁度儀、動態光散射和電泳研究不同pH(2~11)和離子強度(0~200 mmol/L NaCl)對顆粒穩定性的影響。在pH5~pH8的范圍內顆粒相對穩定,但在較低pH時顆粒發生明顯的聚集,這是因為蛋白質與多糖發生了靜電中和和橋連絮凝。LF-果膠復合膠體顆粒,在所研究的鹽濃度范圍內都比較穩定,但LF-卡拉膠和LF-海藻酸鹽絡合物在較高鹽濃度時發生聚集。
3 影響Pickering乳液穩定性的因素
3.1 固體顆粒的潤濕性
Pickering乳液的類型和傳統乳液類似,包括O/W、W/O、O/W/O、W/O/W等多種乳液[59]。Finkle[60]指出,Pickering乳液的穩定性很大程度上取決于固體顆粒的部分潤濕性,即要求顆粒具有親水和親油兩親特性,如果顆粒完全溶解于水或油,它們就會分散在兩相中的一相中,不能吸附在油-水界面,在這種情況下,不能制備穩定的乳狀液。Finkle還首次描述了顆粒的潤濕性及其穩定乳液能力之間的相關性,即根據油—顆粒—水界面處的接觸角度θ判斷乳液的類型和穩定性(圖2)。固體顆粒在油-顆粒-水界面的接觸角θ<90°時為O/W型乳液,而θ>90°時為W/O型乳液,θ=90°時乳液穩定性最好。
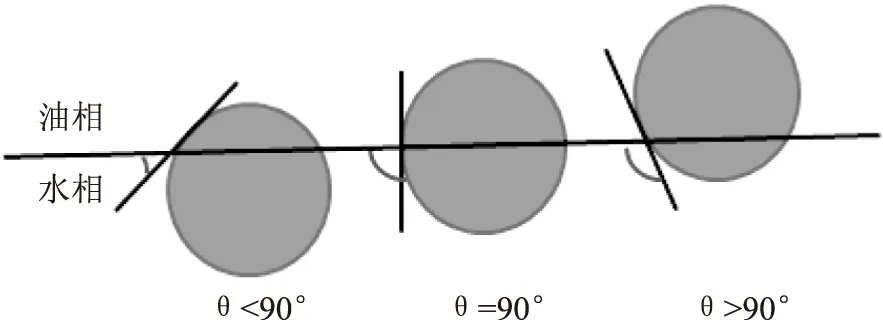
圖2 油—顆粒—水界面處的接觸角圖示[60]Fig.2 Position of Pickering-type stabilizers ata planar o/w interface for contact angles[60]
3.2 固體顆粒在油—水界面的吸附形式
固體顆粒與界面強烈的吸附作用形成了具有剛性的界面,而界面的剛性也決定了液滴抗絮凝的能力。吸附在界面的顆粒之間橫向的交互作用也是調節界面性質與維持乳液穩定的非常重要的因素。當兩個被顆粒吸附的液滴相互靠近時,顆粒在界面可能會產生不同的分布,從而影響乳液的穩定性。兩個在界面緊密排列的單顆粒層將相鄰分散相分割(圖3A),這是球形顆粒均一、單層吸附在界面用于穩定Pickering乳液的理想模型,但是即便通過高壓均質或高強度超聲處理也很難實現,因為顆粒通常是多分散性的[61-62]。已有研究表明,液滴即使不被顆粒完全包裹也能制備穩定的Pickering乳液,這就說明顆粒在界面的分布還存在其他的形式,如單層顆粒緊密排列,在相鄰液滴間形成橋連的致密吸附層,單個顆粒同時與兩個液滴吸附,但每個顆粒的主要部分仍處于連續的水相中(圖3B)[63]。這種單層排列的顆粒層能夠穩定Pickering乳液,是因為顆粒層產生空間阻礙作用,阻止大的顆粒脫離液滴或進入液滴內部。大多數固體粒子具有比較均勻的表面,這意味著顆粒吸附的液滴表面具有類似顆粒表面的性質。接觸角有利于強烈吸附在油-水界面,這也意味著顆粒在乳液中以弱聚集的狀態存在。因此,顆粒在界面的分布存在第三種形式即顆粒聚集體吸附在液滴表面用于穩定Pickering乳液(圖3C)[64-65]。在這種分布形式下,液滴表面不是簡單的單層或雙層吸附,也不是緊密堆積吸附。相反,顆粒形成的剛性吸附層是無序的,形成網絡結構吸附在油-水界面上,能夠通過分子間引力使整個聚集結構保持在一起從而阻止液滴聚集。
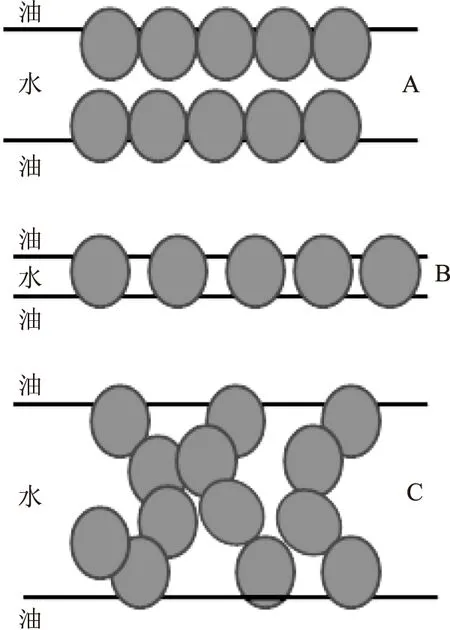
圖3 固體顆粒在油—水界面的分布形式示意圖Fig.3 a schematic distribution diagram of thesolid particles in the oil-water interface
3.3 固體顆粒的形狀
顆粒的形狀對顆粒在液滴表面的覆蓋率及與形狀有關的界面交互作用產生影響。Madivala等[66]研究了顆粒形狀對Pickering乳液聚集穩定性的影響。對于O/W或W/O乳液,作者發現乳液的穩定性很大程度上決定于顆粒的長寬比。當具有相似潤濕性的球形顆粒或較短的細長顆粒不能有效穩定乳液時,足夠長的顆粒是非常有效的乳化劑。顆粒的長寬比對乳液穩定性的影響可通過測定油-水界面的剪切流變性質進行表征。
3.4 固體顆粒的濃度
當固體顆粒濃度較低時,靜電相互作用在很大程度上受到抑制,由于顆粒較少,相鄰液滴間共享吸附的顆粒或大分子,起初形成的液滴迅速結合,通常發生某種程度的絮凝,直到液滴表面有足夠的顆粒或分子吸附形成空間保護層[67]。當顆粒濃度較高時,乳液穩定性主要由界面張力決定。隨著顆粒濃度的提高,顆粒在油-水界面吸附能力增強,引起界面張力降低,從而使液滴粒徑逐漸減小。繼續增加顆粒濃度,顆粒不再吸附于界面,而是進入連續相中,液滴粒徑基本保持不變,但水相黏度逐漸增加,乳液呈凝膠狀,阻止乳液分層、絮凝或聚集,乳液穩定性明顯增強[68]。
3.5 pH
固體顆粒可能在不同pH的產品中使用,在通過人體胃腸道時pH也不同,因此,探討pH對乳液的影響是非常重要的。pH的變化能夠改變顆粒的潤濕性和靜電性質,從而影響顆粒的界面吸附。Luo等[34]研究了pH對黃酮類化合物(山奈酚,蘆丁和柚皮苷)制備的O/W型Pickering乳液的影響。研究表明,在較高的pH時蘆丁穩定的乳液液滴的平均尺寸最小(5 μm)。蘆丁和山奈酚在油-水界面的表面活性在pH8時比pH2時略有增加。在pH較高時乳液的穩定性增加,這是因為黃酮類化合物顆粒的ζ-電勢顯著增加,改善了顆粒分散性能,增加了液滴的表面電荷。Liang和Tang[36]研究指出,豌豆分離蛋白(PPI)在pH3.0時以納米顆粒形式存在,粒徑為134~165 nm可用于制備穩定的O/W型Pickering乳液。Wen等[69]研究了不同pH(4.2,4.8,5.5,6.2,7.0和7.8)對纖維素納米晶(CNCs)制備的檸檬烯Pickering乳液的影響,結果表明隨著pH的增加,液滴表面的ζ-電位由-42.9 mV增加到-54.5 mV,液滴間靜電斥力增加,增強了乳液的穩定性。
3.6 離子強度
NaCl溶液加入主要影響顆粒的表面電位,NaCl溶液濃度較低時,會降低顆粒表面的電位,有助于顆粒在油-水界面的吸附。當NaCl濃度過高時,顆粒表面發生靜電屏蔽,顆粒聚集,粒徑增加,影響乳液的穩定性。de Folter等[32]研究了不同濃度NaCl溶液對玉米醇溶蛋白膠體顆粒(ZNP)制備的Pickering乳液的影響,結果表明,ZNP在1 mmol/L的NaCl溶液中親水性較強,三相接觸角為98°;1 mmol/L的NaCl溶液使Z疏水性增加,三相接觸角為87°,有利于ZNP在油-水界面的吸附;然而,0.1 mol/L的NaCl溶液使液滴聚集,發生分層,嚴重降低了乳液的穩定性。
4 Pickering乳液的應用
目前還沒有Pickering乳液制備的市售產品或材料。原因之一是Pickering乳液最近幾年才引起大家的關注。與傳統表面活性劑穩定的乳液相比,Pickering乳液由于不含表面活性劑,能有效避免表面活性劑可能引發的刺激性、毒性、溶血行為等不利影響,在生命科學領域有很多潛在的應用[70-71]。例如,研究表明固體顆粒在細胞表面有較強的粘附作用,因此Pickering乳液可作為藥物和具有生物活性物質的包埋和傳遞系統,并且可達到緩釋和靶向的效果[72-74];另外,由于固體顆粒吸附在液滴表面產生具有剛性的吸附層,經干燥的Pickering乳液可以用于制備固體劑型的生物材料[75-77]。
5 展望
近年來Pickering乳液的研究成果促進了乳液基礎理論的發展,并且拓展了乳液的實際應用范圍。隨著人們對Pickering乳液研究興趣的增加,尋求新型、安全、可降解的固體納米顆粒作為乳液的有效穩定劑應用于食品行業是食品領域面臨的挑戰。同時,固體顆粒的制備技術仍需突破,Pickering乳液的穩定機理有待進一步研究。
[1]McClements D J. Nanoemulsions versus microemulsions:terminology,differences,and similarities[J]. Soft Matter,2012,8(6):1719-1729.
[2]Zeeb B,Herz E,McClements D J,et al. Impact of alcohols on the formation and stability of protein-stabilized nanoemulsions[J].Journal of Colloid and Interface Science,2014,433(10):196-203.
[3]Schrade A,Landfester K,Ziener U. Pickering-type stabilized nanoparticles by heterophase polymerization[J]. Chemical Society Reviews,2013,42(16):6823-6839.
[4]Ramsden W. Separation of solids in the surface-layers of solutions and ‘suspensions’(observations on surface-membranes,bubbles,emulsions,and mechanical coagulation).-preliminary account[J]. Proceedings of the royal Society of London,1903,43(5):156-164.
[5]Pickering S U M. CXCVI.-Emulsions[J]. Journal of Chemistry Society Trans,1907,91(2),2001-2021.
[6]Chevalier Y,Bolzinger M A. Emulsions stabilized with solid nanoparticles:Pickering emulsions[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects,2013,439(11):23-34.
[7]Binks B P,Horozov T S. Colloidal particles at liquid interfaces:an introduction[J]. Colloidal Particles at Liquid Interfaces,Chapt,2006,83(6):1-74.
[8]Binks B P. Particles as surfactants-similarities and differences[J]. Current Opinion in Colloid & Interface Science,2002,7(1):21-41.
[9]Yin Y,Zhou S,You B,et al. Facile fabrication and self-assembly of polystyrene-silica asymmetric colloid spheres[J]. Journal of Polymer Science Part A:Polymer Chemistry,2011,49(15):3272-3279.
[10]Teixeira R F A,McKenzie H S,Boyd A A,et al. Pickering emulsion polymerization using Laponite clay as stabilizer to prepare armored “soft” polymer latexes[J]. Macromolecules,2011,44(18):7415-7422.
[11]Chen J H,Cheng C Y,Chiu W Y,et al. Synthesis of ZnO/polystyrene composites particles by Pickering emulsion polymerization[J]. European Polymer Journal,2008,44(10):3271-3279.
[12]Song X,Yin G,Zhao Y,et al. Effect of an anionic monomer on the Pickering emulsion polymerization stabilized by titania hydrosol[J]. Journal of Polymer Science Part A:Polymer Chemistry,2009,47(21):5728-5736.
[13]Zhao Y,Yin G,Zheng Z,et al. Preparation of polymer hollow microspheres covered by polymer solid particles via two polymerization steps[J]. Journal of Polymer Science Part A:Polymer Chemistry,2011,49(24):5257-5269.
[14]Yin G,Zheng Z,Wang H,et al. Preparation of graphene oxide coated polystyrene microspheres by Pickering emulsion polymerization[J]. Journal of Colloid and Interface Science,2013,394(7):192-198.
[15]Wu C H,Chiu W Y,Don T M. Conductive composite particles synthesized via Pickering emulsion polymerization using conductive latex of poly(3,4-ethylenedioxythiophene)(PEDOT)as stabilizer[J]. Polymer,2012,53(5):1086-1092.
[16]Li C,Sun P,Yang C. Emulsion stabilized by starch nanocrystals[J]. Starch-St?rke,2012,64(6):497-502.
[17]Miao M,Li R,Jiang B,et al. Structure and physicochemical properties of octenyl succinic esters of sugary maize soluble starch and waxy maize starch[J]. Food Chemistry,2014,151(9):154-160.
[18]Li C,Li Y,Sun P,et al. Starch nanocrystals as particle stabilisers of oil-in-water emulsions[J]. Journal of the Science of Food and Agriculture,2013,132(6):186-192.
[19]Tan Y,Xu K,Liu C,et al. Fabrication of starch-based nanospheres to stabilize pickering emulsion[J]. Carbohydrate Polymers,2012,88(4):1358-1363.
[20]Capron I,Cathala B. Surfactant-free high internal phase emulsions stabilized by cellulose nanocrystals[J]. Biomacromolecules,2013,14(2):291-296.
[21]Kalashnikova I,Bizot H,Bertoncini P,et al. Cellulosic nanorods of various aspect ratios for oil in water Pickering emulsions[J]. Soft Matter,2013,9(3):952-959.
[22]Kalashnikova I,Bizot H,Cathala B,et al. New Pickering emulsions stabilized by bacterial cellulose nanocrystals[J]. Langmuir,2011,27(12):7471-7479.
[23]Tasset S,Cathala B,Bizot H,et al. Versatile cellular foams derived from CNC-stabilized Pickering emulsions[J]. RSC Advances,2014,4(2):893-898.
[24]Kalashnikova I,Bizot H,Cathala B,et al. Modulation of cellulose nanocrystals amphiphilic properties to stabilize oil/water interface[J]. Biomacromolecules,2011,13(1):267-275.
[25]Tzoumaki M V,Moschakis T,Kiosseoglou V,et al. Oil-in-water emulsions stabilized by chitin nanocrystal particles[J]. Food Hydrocolloids,2011,25(6):1521-1529.
[26]Tzoumaki M V,Moschakis T,Scholten E,et al.Invitrolipid digestion of chitin nanocrystal stabilized o/w emulsions[J]. Food & function,2013,4(1):121-129.
[27]Paunov V N,Cayre O J,Noble P F,et al. Emulsions stabilised by food colloid particles:Role of particle adsorption and wettability at the liquid interface[J]. Journal of Colloid and Interface Science,2007,312(2):381-389.
[28]Liu F,Tang C H. Soy protein nanoparticle aggregates as Pickering stabilizers for oil-in-water emulsions[J]. Journal of Agricultural and Food Chemistry,2013,61(37):8888-8898.
[29]Liang H N,Tang C. Pea protein exhibits a novel Pickering stabilization for oil-in-water emulsions at pH3.0[J]. LWT-Food Science and Technology,2014,58(2):463-469.
[30]Shimoni G,Shani Levi C,Levi Tal S,et al. Emulsions stabilization by lactoferrin nano-particles underinvitrodigestion conditions[J]. Food Hydrocolloids,2013,33(2):264-272.
[31]Destribats M,Rouvet M,Gehin-Delval C,et al. Emulsions stabilised by whey protein microgel particles:towards food-grade Pickering emulsions[J]. Soft matter,2014,10(2):6941-6949.
[32]de Folter J W J,van Ruijven M W M,Velikov K P. Oil-in-water Pickering emulsions stabilized by colloidal particles from the water-insoluble protein zein[J]. Soft Matter,2012,8(25):6807-6815.
[33]Gao Z M,Yang X Q,Wu N N,et al. Protein-Based Pickering Emulsion and Oil Gel Prepared by Complexes of Zein Colloidal Particles and Stearate[J]. Journal of Agricultural and Food Chemistry,2014,62(12):2672-2678.
[34]Luo Z,Murray B S,Ross A L,et al. Effects of pH on the ability of flavonoids to act as Pickering emulsion stabilizers[J]. Colloids and Surfaces B:Biointerfaces,2012,92(4):84-90.
[35]Luo Z,Murray B S,Yusoff A,et al. Particle-stabilizing effects of flavonoids at the oil-water interface[J]. Journal of Agricultural and Food Chemistry,2011,59(6):2636-2645.
[36]Liu F,Tang C H. Phytosterol Colloidal Particles as Pickering Stabilizers for Emulsions[J]. Journal of Agricultural and Food Chemistry,2014,62(9):5133-5141.
[37]Li C,Li Y,Sun P,et al. Pickering emulsions stabilized by native starch granules[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects,2013,431(10):142-149.
[38]Rayner M,Timgren A,Sj?? M,et al. Quinoa starch granules:a candidate for stabilising food-grade Pickering emulsions[J]. Journal of the Science of Food and Agriculture,2012,92(9):1841-1847.
[39]Dickinson E. Hydrocolloids at interfaces and the influence on the properties of dispersed systems[J]. Food hydrocolloids,2003,17(1):25-39.
[40]Dickinson E. Hydrocolloids as emulsifiers and emulsion stabilizers[J]. Food Hydrocolloids,2009,23(6):1473-1482.
[41]Dickinson E,Euston S R. Stability of food emulsions containing both protein and polysaccharide[M]. Royal Society of Chemistry:Cambridge,UK,1991.
[42]Jourdain L,Leser M E,Schmitt C,et al. Stability of emulsions containing sodium caseinate and dextran sulfate:relationship to complexation in solution[J]. Food Hydrocolloids,2008,22(4):647-659.
[43]Akhtar M,Dickinson E. Whey protein-maltodextrin conjugates as emulsifying agents:an alternative to gum arabic[J]. Food Hydrocolloids,2007,21(4):607-616.
[44]McClements D J. Protein-stabilized emulsions[J]. Current opinion in colloid & interface science,2004,9(5):305-313.
[45]Dickinson E. Adsorbed protein layers at fluid interfaces:interactions,structure and surface rheology[J]. Colloids and surfaces B:Biointerfaces,1999,15(2):161-176.
[46]Semenova M G,Dickinson E. Biopolymers in food colloids:Thermodynamics and molecular interactions[M]. Brill,2010,141(7):124-133.
[47]Dickinson E. Caseins in emulsions:interfacial properties and interactions[J]. International Dairy Journal,1999,9(3):305-312.
[48]Binks B P,Rodrigues J A. Enhanced stabilization of emulsions due to surfactant-induced nanoparticle flocculation[J].Langmuir,2007,23(14):7436-7439.
[49]Whitby C P,Fornasiero D,Ralston J. Effect of adding anionic surfactant on the stability of Pickering emulsions[J]. Journal of Colloid and Interface Science,2009,329(1):173-181.
[50]Pichot R,Spyropoulos F,Norton I T. Mixed-emulsifier stabilised emulsions:investigation of the effect of monoolein and hydrophilic silica particle mixtures on the stability against coalescence[J]. Journal of Colloid and Interface Science,2009,329(2):284-291.
[51]Binks B P,Liu W,Rodrigues J A. Novel stabilization of emulsions via the heteroaggregation of nanoparticles[J]. Langmuir,2008,24(9):4443-4446.
[52]Patel A,Hu Y,Tiwari J K,et al. Synthesis and characterisation of zein-curcumin colloidal particles[J]. Soft Matter,2010,6(24):6192-6199.
[53]Zou T,Li Z,Percival S S,et al. Fabrication,characterization,and cytotoxicity evaluation of cranberry procyanidins-zein nanoparticles[J]. Food hydrocolloids,2012,27(2):293-300.
[54]Hu D,Lin C,Liu L,et al. Preparation,characterization,andinvitrorelease investigation of lutein/zein nanoparticles via solution enhanced dispersion by supercritical fluids[J]. Journal of Food Engineering,2012,109(3):545-552.
[55]Jones O G,McClements D J. Recent progress in biopolymer nanoparticle and microparticle formation by heat-treating electrostatic protein-polysaccharide complexes[J]. Advances in Colloid and Interface Science,2011,167(1):49-62.
[56]Hong Y H,McClements D J. Formation of hydrogel particles by thermal treatment of β-lactoglobulin-chitosan complexes[J]. Journal of Agricultural and Food Chemistry,2007,55(14):5653-5660.
[57]Jones O G,Decker E A,McClements D J. Formation of biopolymer particles by thermal treatment of β-lactoglobulin-pectin complexes[J]. Food Hydrocolloids,2009,23(5):1312-1321.
[58]Peinado I,Lesmes U,Andrés A,et al. Fabrication and morphological characterization of biopolymer particles formed by electrostatic complexation of heat treated lactoferrin and anionic polysaccharides[J]. Langmuir,2010,26(12):9827-9834.
[59]Aveyard R,Binks B P,Clint J H. Emulsions stabilised solely by colloidal particles[J]. Advances in Colloid and Interface Science,2003,100(10):503-546.
[60]Finkle P,Draper H D,Hildebrand J H. The theory of emulsification[J]. Journal of the American Chemical Society,1923,45(12):2780-2788.
[61]Binks B P,Clint J H,Mackenzie G,et al. Naturally occurring spore particles at planar fluid interfaces and in emulsions[J]. Langmuir,2005,21(18):8161-8167.
[62]Horozov T S,Binks B P. Particle-Stabilized Emulsions:A Bilayer or a Bridging Monolayer?[J]. Angewandte Chemie,2006,118(5):787-790.
[63]Pawar A B,Caggioni M,Ergun R,et al. Arrested coalescence in Pickering emulsions[J]. Soft Matter,2011,7(17):7710-7716.
[64]Gautier F,Destribats M,Perrier-Cornet R,et al. Pickering emulsions with stimulable particles:from highly-to weakly-covered interfaces[J]. Physical Chemistry Chemical Physics,2007,9(48):6455-6462.
[65]Arditty S,Schmitt V,Lequeux F,et al. Interfacial properties in solid-stabilized emulsions[J]. The European Physical Journal B-Condensed Matter and Complex Systems,2005,44(3):381-393.
[66]Madivala B,Vandebril S,Fransaer J,et al. Exploiting particle shape in solid stabilized emulsions[J]. Soft Matter,2009,5(8):1717-1727.
[67]Tcholakova S,Denkov N D,Lips A. Comparison of solid particles,globular proteins and surfactants as emulsifiers[J]. Physical Chemistry Chemical Physics,2008,10(12):1608-1627.
[68]Binks B P. Particles as surfactants—similarities and differences[J]. Current Opinion in Colloid & Interface Science,2002,7(1):21-41.
[69]Wen C,Yuan Q,Liang H,et al. Preparation and stabilization ofd-limonene Pickering emulsions by cellulose nanocrystals[J]. Carbohydrate polymers,2014,112(4):695-700.
[70]Tan A,Simovic S,Davey A K,et al. Silica-lipid hybrid(SLH)microcapsules:a novel oral delivery system for poorly soluble drugs[J]. Journal of controlled release,2009,134(1):62-70.
[71]Prestidge C A,Simovic S. Nanoparticle encapsulation of emulsion droplets[J]. International journal of pharmaceutics,2006,324(1):92-100.
[72]Simovic S,Prestidge C A. Nanoparticle layers controlling drug release from emulsions[J]. European journal of pharmaceutics and biopharmaceutics,2007,67(1):39-47.
[73]Frelichowska J,Bolzinger M A,Valour J P,et al. Pickering w/o emulsions:drug release and topical delivery[J]. International journal of pharmaceutics,2009,368(1):7-15.
[74]Simovic S,Hui H,Song Y,et al. An oral delivery system for indomethicin engineered from cationic lipid emulsions and silica nanoparticles[J]. Journal of Controlled Release,2010,143(3):367-373.
[75]Fujii S,Okada M,Sawa H,et al. Hydroxyapatite nanoparticles as particulate emulsifier:fabrication of hydroxyapatite-coated biodegradable microspheres[J]. Langmuir,2009,25(17):9759-9766.
[76]Maeda H,Okada M,Fujii S,et al. Pickering-type water-in-oil-in-water multiple emulsions toward multihollow nanocomposite microspheres[J]. Langmuir,2010,26(17):13727-13731.
[77]Aranberri I,Binks B P,Clint J H,et al. Synthesis of macroporous silica from solid-stabilised emulsion templates[J]. Journal of Porous Materials,2009,16(4):429-437.
Research progress in Pickering emulsions stabilized with biomass-based solid nanoparticles
SUN Cui-xia,LIU Fu-guo,YANG Wei,YUAN Fang,GAO Yan-xiang*
(College of Food Science and Nutritional Engineering,China Agricultural University,Beijing 100083,China)
Pickering emulsions prepared by natural,renewable and biodegradable solid particles have become a hot topic. Present studies have indicated that the stability of Pickering emulsions depended largely on the nature of the solid particles. Therefore,the types,fabrication and characterization of solid particles were reviewed in this paper,focusing on the stabilization of biological organic particles such as polysaccharides and proteins. The factors affecting the Pickering emulsion stability were summarized and potential applications of Pickering emulsions in life science were also illustrated.
solid particles;Pickering emulsions;characterization stability
2014-12-15
孫翠霞(1987-),女,博士,研究方向:功能食品研發,E-mail:scx0728@126.com。
*通訊作者:高彥祥(1961-),男,博士,教授,研究方向:超臨界加工技術,E-mail:gyxcau@126.com。
國家自然基金(31371835)。
TS202.3
A
1002-0306(2015)15-0370-07
10.13386/j.issn1002-0306.2015.15.070

