活性炭對廢水中表面活性劑的吸附研究
張新


摘要:以活性炭為吸附劑,研究其對表面活性劑溶液的吸附作用。利用Langmuir、Freundlich和Dubinin-Radushkevich等溫吸附模型對數據進行擬合,發現Langmuir模型擬合較好,并且吸附過程是物理過程。利用準一級、準二級動力學和顆粒內擴散模型檢驗動力學吸附數據,計算和比較這些動力學模型的吸附速率常數,發現用準二級動力學模型能最佳地描述吸附動力學。利用Thomas、Yoon-Nelson和Adams-Bohart模型對固定床吸附數據進行擬合,發現Thomas和Yoon-Nelson模型擬合較好.
關鍵詞:吸附模型; 表面活性劑; 活性炭
中圖分類號:X53 文獻標識碼:A 文章編號:0439-8114(2015)15-3642-04
DOI:10.14088/j.cnki.issn0439-8114.2015.15.014
Abstract: Removal of surfactant from aqueous solutions by activated carbon was investigated.As for the batch adsorptions, the experimental data were analyzed by Langmuir, Freundlich and Dubinin-Radushkevich isotherm model. The experiment results indicated that the adsorption data were fitted well with Langmuir isotherm model. The Dubinin-Radushkevich isotherm model indicates adsorption process is a physical adsorption. The kinetics of adsorption process data was examined using the pseudo-first-order, pseudo-second-order kinetics and the intra-particle diffusion models.The rate constants of adsorption for all these kinetics models were calculated and compared.The adsorption kinetics was best described by the pseudo-second-order model.As for the fixed-bed adsorptions, the experimental data were analyzed by Thomas、Yoon-Nelson and Adams-Bohart model. The experiment results indicated that the adsorption data were fitted well with Yoon-Nelson and Adams-Bohart model.
Key words: adsorption models; surfactant; activated carbon
土壤洗滌是一種異位土壤修復技術,可應用于土壤重金屬和有機污染修復,該技術始于歐洲20世紀80年代,美國從20世紀80年代末期開始應用于土壤修復,在中國目前基本上還處于實驗室階段[1]。該技術通常需要加入表面活性劑等添加劑來增強去除效果,洗滌后可以去除90%~99%的揮發性有機物和40%~90%的半揮發性的有機物[2,3]。通常認為添加非離子型表面活性劑的清洗效果最好,其中使用較多的是Triton X-100[4-6]。在土壤洗滌時,為達到一定的修復效果,需要投加較高濃度的表面活性劑,這樣產生的土壤洗滌液中表面活性劑濃度也較高,必須加以處理后才能排放。
本研究使用活性炭對含表面活性劑的廢水進行吸附處理,分別進行靜態吸附、動力學吸附和固定床吸附試驗,并使用多種模型對吸附數據進行擬合,旨在為含表面活性劑廢水處理提供理論指導和技術支持。
1 材料與方法
Triton X-100購于中國百靈威科技有限公司,活性炭購于中國西隴化工股份有限公司。活性炭比表面積為718.2 m2/g、孔容為0.845 cm3/g、孔隙分布0.200~2.000 nm、平均孔徑是0.845 nm、微孔體積是0.397 cm3/g、中孔體積是0.206 cm3/g、大孔體積是0.242 cm3/g。
靜態吸附試驗:配制濃度為5 g/L的TX100溶液,逐級稀釋至4.00、3.00、2.00、1.00、0.50和0.15 g/L。在150 mL錐形瓶中加入100 mL的TX100系列濃度溶液,然后加入1 g/L活性炭,使用封口膜封口,在轉速為120 r/min的恒溫振蕩箱(25±0.5℃)中振蕩48 h。
動力學試驗:使用濃度為5 g/L的TX100溶液,吸附條件同靜態吸附試驗,分別在10、20、30、40、60、120、180、240、480、600、900、1 080和1 440 min時將樣品取出。
固定床試驗:使用有機玻璃柱為吸附柱,其高20 cm,柱內徑2.5 cm,內填充活性炭,TX100濃度為5 g/L,流速為20 mL/min,分別取活性炭柱高為7.0、10.8和14.7 cm,溶液從上往下流動,每隔15 min取樣。吸附后使用離心機以4 500 r/min離心10 min,用玻璃注射器取上清液經PTFE過濾頭注射至2 mL進樣瓶中。使用DionexU3000的HPLC檢測,色譜柱為Agilent PAH柱(250×4.6 mm),流動相比例為乙腈∶水=85∶15,柱溫30 ℃,流速為1 mL/min,檢測UV波長為230 nm。
2 結果與分析
2.1 吸附等溫線
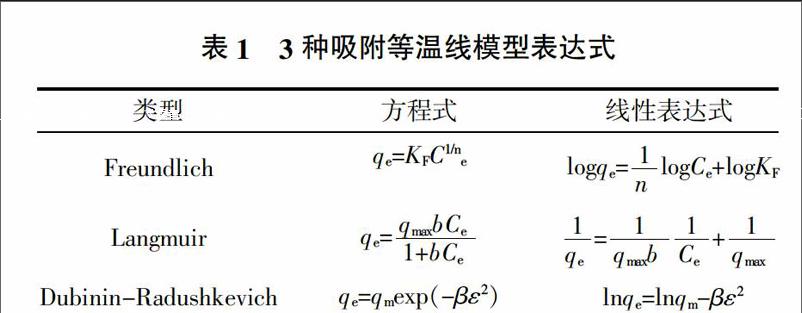
吸附等溫線是指在一定溫度下溶質分子在兩相界面上發生的吸附過程達到平衡時在兩相中濃度之間的關系曲線,是工業設計的基本依據。吸附等溫線的類型很多,適用于不同的條件。Langmuir模型是根據理論推導出的第一個吸附方程式,其出發點是吸附和解吸速率是相同的,分子只能在吸附劑的自由表面上才會被吸附并形成單分子層,被吸附分子之間沒有相互作用力[7]。Freundlich模型是一個經驗方程,其特征是吸附位非均勻分布,吸附能不同,多用于描述非均質表面的單分子層吸附行為[8]。該吸附方程式簡單,計算方便,應用廣泛。但式中的常數沒有明確的物理意義,不能說明吸附作用的機理。Dubinin-Radushkevich 模型假定吸附劑表面是不均勻的,吸附是吸附質填充吸附劑孔的過程[9],該模型可以判斷吸附是物理過程(E0<8 kJ/mol)、離子交換過程(8~16 kJ/mol)還是化學過程(E0 >16 kJ/mol)。當然也不能使用該模型判定一個吸附過程,即不能認為某一吸附只有化學吸附而沒有物理吸附,該模型通常判別一個吸附過程是以哪種性質的吸附為主。這3種吸附等溫線的表達式列于表1中。
活性炭對TX100的計算結果如表2所示,吸附結果如圖1所示。在一些研究中,非離子型的表面活性劑在其濃度超過CMC(臨界膠束濃度)時,吸附特征是先形成單分子層,然后是表面積聚形成多層吸附結構[9-11]。而在本研究中,Langmuir模型的擬合效果比Freundlich模型更好,這與其他類似研究結論相一致[12-14]。可以設想TX100只是形成單分層而沒有進一步的吸附,也就是說,TX100覆蓋在活性炭的表面,而活性炭的內部孔隙沒有起到主要作用。吸附過程的性質使用Dubinin-Radushkevich模型來判斷,由表2知,E值<8 kJ/mol,這說明吸附過程是一種物理過程,這與前人研究結論一致。
2.2 吸附動力學
吸附動力學是研究各種因素對化學反應速率影響的規律,研究化學反應過程經歷的具體步驟即所謂反應機理。準一級動力學模型的反應速度與一個反應物濃度成正比,應用時需要選取一個吸附平衡點[15]。一般情況下,準一級吸附動力學方程在全部吸附時間范圍內的相關性并不是很好,通常只適用于吸附的初始階段。準二級動力學模型的反應速度與兩個反應物濃度成正比,基于假定吸附速率受化學吸附機理的控制,這種化學吸附涉及到吸附劑與吸附質之間的電子共用或電子轉移[16]。內擴散模型假設液膜擴散阻力可以忽略或者是液膜擴散阻力只有在吸附的初始階段的很短時間內起作用[17],擴散方向是隨機的、吸附質濃度不隨顆粒位置改變且內擴散系數為常數,不隨吸附時間和吸附位置的變化而變化。如果吸附動力學曲線都不經過原點,說明內擴散不是控制吸附過程的惟一步驟。Elovich模型考慮到真實吸附過程中隨著吸附過程的進行,吸附和解吸活化能隨吸附劑表面覆蓋而線性變化的情況[18]。如果應用時不忽略解吸速率的影響,存在表面覆蓋率隨時間的變量,則方程式沒有解析解,只有數值解。這4種吸附動力學模型的表達式列于表3。
圖2是活性炭對TX100溶液吸附量隨時間的變化,表4是使用模型后的擬合結果。準二階動力學方程的R2值要高,而且吸附計算值接近試驗值826.63 mg/g,故此方程的擬合效果好,說明表面活性劑的吸附滿足準二階動力學方程。從內擴散模型的數據來看,其C值是一個正值,說明吸附過程受到了表面擴散所控制。
2.3 固定床吸附模型
動態吸附柱的工作過程可用穿透曲線來表示,其中縱坐標為出水中吸附質濃度或出水與進水濃度比、橫坐標為吸附時間。為模擬和預測動態柱內的吸附行為和規律,基于各種假設提出多種模型。Thomas模型假設溶液呈活塞流形態,通常用來描述吸附柱的動態吸附曲線[19],并能計算出吸附柱的飽和吸附容量與吸附速率常數。Yoon-Nelson模型是一個半經驗模型,該模型擬合時不需要考慮吸附流速和吸附劑用量[20],所需已知參數較少,形式簡單,得到的值可用于比較吸附速率。Adams-Bohart模型是描述吸附時間和柱高的關系,可用于計算吸附劑的吸附能力和吸附傳質速率[21]。常見的固定床吸附模型表達式列于表5。
當流速為20 mL/min,TX100濃度為5 g/L,活性炭柱高為14.7 cm時,TX100的穿透曲線如圖3所示,模型計算結果列于表6。隨著柱高的增加,TX100的穿透時間延長,對應于7.0、10.8和14.7 cm,TX100穿透90%的時間分別是90、105和180 min。柱高增加,可利用活性炭吸附面積增大,則活性炭柱飽和時間縮短,使用時間加長,吸附容量也仍能增大。表現于Tomas模型,隨著活性炭用量的增加,KTh和qe隨之增加,這與實際吸附過程中得到的吸附的變化趨勢相一致。表現于Adams-Bohart模型,活性炭用量大,則傳質系數加大,說明吸附過程主要受到外部擴散所影響,由于在數據擬合過程中得到的相關系數相對較低,因此該模型對此過程的應用有一定的限制。表現于Yoon-Nelson模型,隨著活性炭用量的增加,達到一半吸附量的時間自然會增加,KYN值也相應增加,從相關系數來看,該模型擬合效果較好,且達到一半吸附量的時間計算值與實測值較為接近,其較好地模擬了穿透行為。
3 小結與討論
活性炭對表面活性劑的靜態吸附符合Langmuir模型,這表示TX100在活性炭表面形成單分子層。從Dubinin-Radushkevich模型計算得到的E值<8 kJ/mol,說明吸附過程是物理過程。動力學吸附數據符合準二階動力學方程。Thomas模型和Yoon-Nelson模型具有較好的相關系數,說明該模型可運用于固定床中表面活性劑的吸附。
參考文獻:
[1] STEGMANN R, BRUNNER G, CALMANO W, et al. Treatment of contaminated soil: fundamentals, analysis, applications[M]. Berlin: Springer, 2001.
[2] MANN M J, ANDERSON W C, PETERSON G, et al. Innovative site remediation technology: soil washing - soil flushing[M]. American Academy of Environmental Engineers, 1993.
[3] DESHPANDE S, SHIAU B J, WADE D, et al. Surfactant selection for enhancing ex situ soil washing[J]. Water Research, 1999, 33(2): 351-360.
[4] LAHA S, TANSEL B, USSAWARUJIKULCHAI A. Surfactant–soil interactions during surfactant-amended remediation of contaminated soils by hydrophobic organic compounds: A review[J]. Journal of Environmental Management, 2009, 90(1): 95-100.
[5] AHN C K, KIM Y M, WOO S H, et al. Soil washing using various nonionic surfactants and their recovery by selective adsorption with activated carbon[J]. Journal of Hazardous Materials, 2008, 154(1-3): 153-160.
[6] MULLIGAN C N, YONG R N, GIBBS B F. Surfactant-enhanced remediation of contaminated soil: a review[J]. Engineering Geology, 2001, 60(1-4): 371-380.
[7] LANGMUIR I. The constitution and fundamental properties of solids and liquids Part I Solids[J]. Journal of the American Chemical Society, 1916, 38(38): 2221-2295.
[8] FREUNDLICH H. Ueber die Adsorption in Loesungen[J]. Physchem, 1996(57): 385-470.
[9] CESTARI A R, VIEIRA E, VIEIRA G S, et al. Aggregation and adsorption of reactive dyes in the presence of an anionic surfactant on mesoporous aminopropyl silica[J]. Journal of Colloid and Interface Science, 2007, 309(2): 402-411.
[10] ERDINC N, GOKTURK S, TUNCAY M. A study on the adsorption characteristics of an amphiphilic phenothiazine drug on activated charcoal in the presence of surfactants[J]. Colloids and Surfaces B-Biointerfaces, 2010, 75(1): 194-203.
[11] ZHU X, ZHAO T. Surface solubilization[J]. J Chem Soc, 1988, 84(11): 3951-3960.
[12] PUNYAPALAKUL P, TAKIZAWA S. Selective adsorption of nonionic surfactant on hexagonal mesoporous silicates (HMSs) in the presence of ionic dyes[J]. Water Research, 2006, 40(17): 3177-3184.
[13] LEVITZ P E. Adsorption of non ionic surfactants at the solid/water interface[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2002, 205(1-2): 31-38.
[14] GONZALEZ-GARCIA C,GONZALEZ-MARTIN M L,GOMEZ-SERRANO V, et al. Analysis of the adsorption isotherms of a non-ionic surfactant from aqueous solution onto activated carbons[J]. Carbon, 2001, 39(6): 849-855.
[15] KAYRANLI B. Adsorption of textile dyes onto iron based waterworks sludge from aqueous solution; isotherm, kinetic and thermodynamic study[J]. Chemical Engineering Journal, 2011, 173(3):782-791.
[16] LIU J, CHEN J, JIANG L, et al. Adsorption of mixed polycyclic aromatic hydrocarbons in surfactant solutions by activated carbon[J]. Journal of Industrial and Engineering Chemistry, 2014, 20(2): 616-623.
[17] BACCAR R, BLNQUEZ P, BOUZID J, et al. Equilibrium, thermodynamic and kinetic studies on adsorption of commercial dye by activated carbon derived from olive-waste cakes[J]. Chemical Engineering Journal, 2010, 165(2): 457-464.
[18] KHALED A, NEMR A E, EL-SIKAILY A, et al. Removal of Direct N Blue-106 from artificial textile dye effluent using activated carbon from orange peel: Adsorption isotherm and kinetic studies[J]. Journal of Hazardous Materials, 2009, 165(1-3): 100-110.
[19] HAN R, WANG Y, ZHAO X, et al. Adsorption of methylene blue by phoenix tree leaf powder in a fixed-bed column: experiments and prediction of breakthrough curves[J]. Desalination, 2009, 245(1-3): 284-297.
[20] LIU J, YAN Y, ZHANG H. Adsorption dynamics of toluene in composite bed with microfibrous entrapped activated carbon[J]. Chemical Engineering Journal, 2011, 173(2): 456-462.
[21] CHEN S, YUE Q, GAO B, et al. Adsorption of hexavalent chromium from aqueous solution by modified corn stalk: A fixed-bed column study[J]. Bioresource Technology, 2012, 113(10): 114-120.

