術前支氣管動脈灌注化療治療Ⅲa(N2)期非小細胞肺癌
李萬剛,崔靜,王建軍,王繼云,張建偉,劉本剛,陳紹華
術前支氣管動脈灌注化療治療Ⅲa(N2)期非小細胞肺癌
李萬剛,崔靜,王建軍,王繼云,張建偉,劉本剛,陳紹華
目的探討術前支氣管動脈灌注(BAI)化療在Ⅲa(N2)期非小細胞肺癌(NSCLC)治療中的臨床應用價值。方法臨床確診的Ⅲa(N2)期非小細胞肺癌186例,隨機分為觀察組和對照組,每組93例。觀察組患者在接受2次BAI后手術,對照組確診后直接手術,觀察BAI療效,比較兩組患者的手術情況和術后生存率。結果觀察組的臨床和組織學有效率分別為80.6%和83.9%,TNM分期下降50.53%,不良反應輕微;觀察組根治性手術切除率為93.4%,顯著高于對照組的72.0%,差異有統計學意義(P<0.05);術中出血量和術后并發癥兩組間無差別;觀察組與對照組1、3、5年生存率分別為97.8%、64.8%、36.3%和89.3%、50.5%、18.3%,兩組間差異有顯著統計學意義(P<0.01)。結論術前BAI可獲得較好的臨床和組織學療效,并能提高Ⅲa(N2)期NSCLC的根治性手術切除率和術后生存率,值得臨床推廣應用。
支氣管動脈灌注;新鋪助化療;非小細胞肺癌;Ⅲa(N2)期;手術
【Abstract】ObjectiveTo evaluate the clinical application of preoperative bronchial artery infusion(BAI)chemotherapy in treating stageⅢa(N2)non-small cell lung cancer.Methods A total of 186 cases with clinically-confirmed non-small cell lung cancer of stageⅢa(N2)were enrolled in this study.The patients were randomly and equally divided into observation group(n=93)and control group(n=93).Surgical resection was performed after twice BAI for patients of the observation group,while patients of the control group received operation directly after the diagnosis was made.Therapeutic efficacy of all patients was evaluated.Surgical findings and postoperative survival rate were determined,and the results were compared between the two groups.ResultsThe clinical and histopathological effective rate of the observation group was 80.6%and 83.9%respectively,and the TNM staging of the tumor was decreased by 50.5%,the adverse reaction was slight.The radical resection rate of the observation group was 93.4%,which was significantly higher than that of the control group(72.0%),and the difference was statistically significant(P<0.05).No statistically significant differences in the intraoperative blood loss and the occurrence of postoperative complications existed between the two groups.The one-,3-and 5-year survival rates were 97.8%,64.8% and 36.3%respectively in the observation group,and 89.3%,50.5%and 18.3%respectively in the control group,and the difference between the two groups was statistically significant(P<0.01).Conclusion Preoperative BAI has both clinical and histopathological effect.It can improve the radical resection rate as well as the long-term survival rate of stageⅢa(N2)non-small cell lung cancer.Therefore,this technique is worthy to be popularized in clinical practice.(J Intervent Radiol,2015,24:160-165)
【Key words】bronchial artery infusion;neoadjuvant;non-small cell lung cancer;stageⅢa(N2);surgery
支氣管動脈灌注(bronchial artery infusion,BAI)化療是治療中晚期肺癌的重要方法,其顯著近期療效、可以降低肺癌分期和不良反應少等優點被臨床廣泛應用[1]。Ⅲa(N2)非小細胞肺癌(non small cell lung cancer,NSCLC)屬于局部晚期,約占NSCLC的45%~50%,其治療方法一直是臨床研究的熱點。我們對一組NSCLC的Ⅲa(N2)期患者術前行2個周期的BAI進行了前瞻性研究,取得滿意療效,現予報道。
1 材料與方法
1.1材料
1.1.1入選標準①經纖維支氣管鏡咬檢、刷檢、針吸活檢,CT定位下肺穿刺活檢,痰脫落細胞學檢查等方法獲得病理確診的NSCLC;②先經系統影像學初步篩查,然后對可疑縱隔離淋巴結行纖維支氣管鏡針吸活檢,超聲胃鏡下針吸活檢(EUS-FNA),縱隔鏡活檢,胸腔鏡活檢獲得淋巴結病理的N2期肺癌,依據1997年國際抗癌聯盟(UICC)修訂后的TNM分期方案,臨床分期確定為Ⅲa(N2)期,即T1-3N2M0;③Karnofsky評分≥80分,無手術禁忌證;④未曾接受過放、化療;⑤年齡≤70歲;⑥簽署知情同意書,愿意接受術前支氣管動脈灌注化療。

表1 兩組患者的資料比較
1.1.2患者資料2005年5月—2008年4月經臨床確診的Ⅲa(N2)期NSCLC患者共297例,愿意入組的患者186例,采用隨機抽簽法分為術前支氣管動脈灌注化療組(觀察組)和單獨手術組(對照組),每組93例。兩組例數、性別、年齡、組織學類型和部位比較,差異均無統計學意義(P>0.05),見表1。
1.2方法
1.2.1觀察組采用Seldinger穿刺技術,經一側股動脈穿刺置入4~6 F Cobra、Mik、Simmons或RH等不同形狀的導管,尋找支氣管動脈,當導管嵌入靶支氣管動脈開口,以非離子型對比劑8~10 ml手推造影,確認有無腫瘤染色,仔細辨認有無脊髓動脈分支,再次造影確認無誤后,固定導管,通過導管或微導管灌化療藥物[2]。化療方案為多西他賽聯合順鉑(DP)方案,多西他賽75 mg/m2,順鉑75 mg/m2,每3周灌注1次,共灌注2次。常規給地塞米松、抗組織胺H1受體阻滯劑和止吐劑,常規水化。灌注化療療程結束后第3周進行全面復查。WBC和(或)PLT降低Ⅲ度以上,予重組人粒細胞集落刺激因子(G-CSF)200 μg,皮下注射,每日1次,WBC上升到10×109/L以上時停止。
1.2.2對照組直接手術。手術方法為病肺切除加系統縱隔淋巴結清掃。
兩組術后皆給予4個周期的吉西他濱聯合長春瑞濱方案化療,吉西他濱1 000 mg/m2,長春瑞濱30 mg/m2,均為第1、8天給藥。不完全切除者加50~60 Gy局部放療。
1.2.3療效評估支氣管動脈灌注化療的近期療效按國際最常用的RECIST1.0標準進行評價,完全緩解(CR),指所有靶病灶消失,持續4周;部分緩解(PR),指所有靶病灶最長經之和縮小≥30%,持續4周;病變穩定(SD),指靶病灶最長經之和縮小≤30%,增大≤20%;病變進展(PD),指靶病灶最長經之和增加≥20%,或有新病灶出現。CR+PR為總有效率。
1.3統計學處理
將2012 年“7·21”特大暴雨提取三個不同降雨歷時,用不同的降水系列對其重現期進行分析,相同的降水量在不同降水系列中重現期是有差異的,其中降雨歷時為1h、6h,結論相差不大;而當降雨歷時為24h時,按系列延長至2012年的重現期明顯高于原計算成果,兩者基本相差一個量級(表1)。
采用SPSS17.0統計軟件進行處理,以P<0.05為差異有統計學意義,P<0.01為差異有顯著統計學意義。本研究采用的統計方法有:t檢驗、F檢驗、χ2檢驗、秩和檢驗、對數秩和檢驗和Kaplan-Meier生存曲線。
2 結果
2.1BAI的臨床療效
93例觀察組患者經2個周期BAI化療后,胸部CT檢查顯示CR 7例(圖1、2),PR 68例,SD 14例,PD 4例。CR+PR 75例,總有效率80.6%(75/ 93)其中21例肺葉不張患者復張8例,5例全肺不張復張1例。BAI前縱隔淋巴結腫大87例,BAI后縮小43例(49.4%),其中19例縱隔淋巴結最短徑縮小至1 cm以下(21.8%),與BAI前相比有顯著性差異(P<0.05)。BAI前與胸壁、膈肌、心包和縱隔胸膜關系密切的31例,BAI后改善21例(67.7%)。
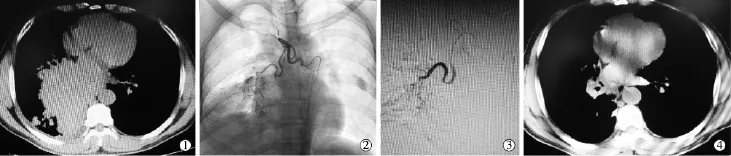
圖1 右肺下葉大細胞癌BAI過程圖像

圖2 左上肺鱗癌BAI后消失
2.2BAI化療的不良反應
全組患者未發生食管支氣管瘺和脊髓麻痹等嚴重并發癥。43例(46.2%)患者表現為Ⅰ~Ⅱ度的惡心、嘔吐、腹瀉、白細胞降低、脫發及丙氨酸轉氨酶升高。其中1例患者出現低熱,體溫37.2~38.3℃之間,2 d后體溫恢復正常,未發生肺部感染。所有不良反應均經對癥處理、支持療法和G-CSF治療很快恢復正常,不影響手術的進行。
2.3手術結果
93例觀察組患者中,4例PD患者有2例為中心型肺癌,具體分期為T3N2M0退出改為放療。91例進行了手術,其中1例因壁層胸膜多發粟粒樣結節,術中冷凍病理證實為轉移灶而放棄手術,其余90例均進行了不同方式的手術切除加系統淋巴結清掃,手術切除率98.9%(90/91),5例患者隆凸下轉移淋巴結切除后,發現其已侵犯對側支氣管,也無法行隆突切除再造,局部放一金屬標記物以備術后放療放棄根治,根治性手術切除率為93.4%(85/ 91)。對照組93例,開胸探查5例,手術切除率為94.6%(88/93),其中67例完成了根治性切除,根治性手術切除率為72.0%(67/93)。觀察組和對照組的根治性手術切除率有顯著統計學意義(P<0.05),兩組患者的手術方式見表2。
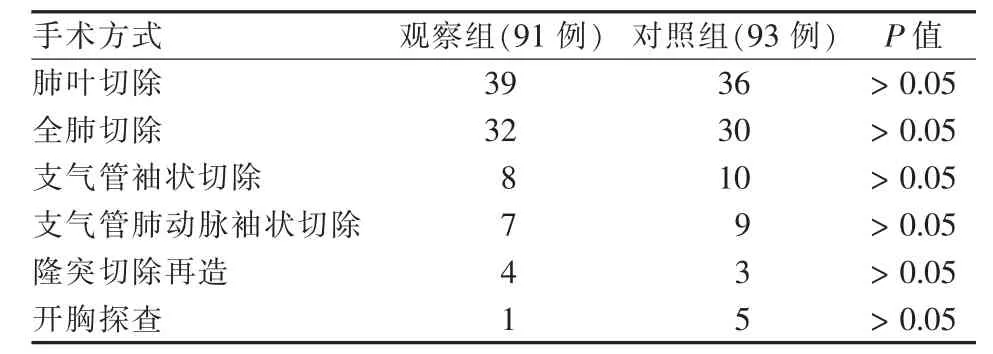
表2 觀察組和對照組手術方式及切除率
觀察組手術失血量為110~450 ml,平均(289.86± 23.51)ml;對照組失血量130~410 ml,平均(305.25 ±20.78)ml。兩組比較差異無統計學意義(P>0.05)。觀察組和對照組術后并發癥發生率分別為20.87%(19/91)和18.27%(17/93),均無手術死亡,兩組比較差異無統計學意義(P>0.05),詳見表3。
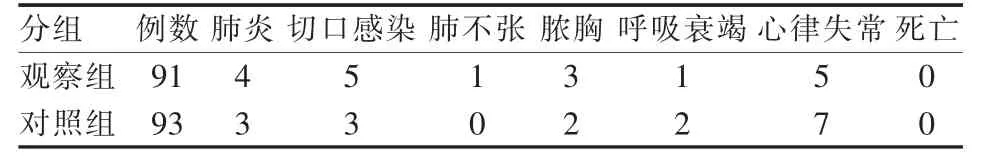
表3 兩組患者的手術并發癥和死亡情況比較(例)
2.5BAI化療后病理改變
觀察組術后病理標本檢查,7例CR、8例PR和 1例SD共16例患者光鏡下原發灶內未發現癌細胞,僅見到增生的纖維組織;54例PR加8例SD共62例患者病灶內見癌細胞不同程度的壞死并有纖維組織增生,殘存的癌細胞明顯變性,間質有少量淋巴細胞和漿細胞浸潤,其中1例PR腺鱗癌患者,病灶內僅發現少量變性的腺癌細胞和纖維組織,無鱗癌細胞。原發病灶組織學有效率83.9%(78/93),影像學評價與組織學評價符合率為96.2%(80.6%/ 83.9%),兩種評價方法的差異無統計學意義(P>0.05)。術后縱隔淋巴結檢查,47例患者縱隔淋巴結未發現癌細胞,縱隔淋巴結轉陰率51.6%(47/91),淋巴結影像學評價與組織學評價符合率為95.7%(49.4%/51.6%),兩種方法差異無統計學意義(P>0.05)。術后TNM分期:Ⅰb 2例,Ⅱa 18例,Ⅱb 27例,Ⅲa(N2)期43例,Ⅲb(T4N1M0)1例,TNM分期下降50.53%(47/93)。觀察組術后TNM分期與BAI前和對照組比較差異有統計學意義(P<0.01)。
2.6術后隨訪和生存分析
兩組患者術后隨訪12~60個月,隨訪率為97.8%,失訪率為2.2%,失訪病例按死亡計算。觀察組1、3、5年生存率分別為97.8%、64.8%和36.3%;對照組1、3、5年生存率為89.3%、50.5%和18.3%。經Kaplan-Meier生存曲線和對數秩和檢驗,兩組間比較差異有統計學意義(P<0.01,圖3)。
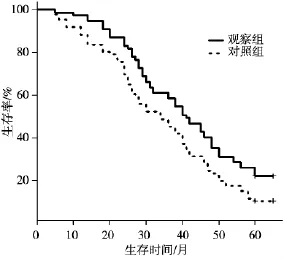
圖3 觀察組與對照組的生存曲線
3 討論
20世紀80年代以前,N2期肺癌稱為肺癌縱隔疾病,并被列為外科手術禁忌,只能施行放化療,其中位生存時間只有6~8個月,1年生存率只有20%~25%。隨著醫學科學技術的發展,尤其是外科手術為主的多學科綜合治療理論和技術在Ⅲa(N2)期NSCLC中的應用,也促使N2期肺癌的治療水平得到了長足進步,進而使25%~34%Ⅲa(N2)的NSCLC獲得較長期生存,甚至能重新走上工作崗位[3]。
術前BAI實為新輔助化療(neoadjuvant chemotherapy,NCT)的一種特殊方法。但后來Depierre等[4]報道一組多中心包括373例可手術治療的I期(除外T1N0)-Ⅲa期NSCLC前瞻性隨機研究結果,受益者僅限于N0和N1期患者,NCT并沒有延長其他分期患者的生存期。20余年來國內外進行了大量臨床研究[5-8],由于所選擇的NSCLC分期存在較大差異,所得結果迥異,NSCLC的全身NCT也因此爭論不休[9]。
術前BAI局部藥物濃度增加1倍,對癌細胞殺傷力增加10倍[10]。另外進入血液循環的化療藥可再次被腫瘤組織攝取,發揮二次抗癌效應,對原發灶、轉移灶以及肺門和縱隔淋巴結均有殺滅作用。因此BAI顯著優于全身化療,更能夠使手術如期進行。
觀察組BAI總有效率80.6%,高于全身NCT 62.5%~66%的總有效率[11-12],Ⅰ~Ⅱ度不良反應占46.23%,在程度和發生率上均低于Liao等[13]報告的59%不良反應率。本組原發病灶組織學有效率83.9%,縱隔淋巴結轉陰率51.7%,術前影像學評價與術后組織學評價無統計學差異,與文獻報道一致[14],但William等[15]認為組織學有效率更能預測患者遠期生存率。全身NCT能夠使腫瘤的分期下降,已被業界公認,本組BAI后TNM分期下降50.5%%,高于Kappers等[16]報告的全身NCT32.3%的降期率。
本世紀初So[17]為3例Ⅲb患者BAI后行了根治性袖狀切除或隆凸再造,開辟了難切除的中晚期肺癌術前BAI后根治性切除的先河。本組根治性手術切除率為93.41%,顯著高于對照組,也高于Davidov等[18]報道的全身NCT 77.6%的完全性切除率。Ceylan等[19]一組臨床對照研究結果顯示全身NCT后可造成組織充血水腫和肺血管脆性增加,本組也發現縱隔、肺門部和肺動脈外膜較對照組有輕度水腫,但不影響組織分離和血管的結扎,術中出血量和術后并發癥兩組間無差別。
閆東等[20]報道58例Ⅲ期(其中Ⅱb 3例,Ⅲa 26,Ⅲb 29例)NSCLC,BAI后31例行手術切除,27例行放化療和支持治療,結論是手術患者中位生存期顯著長于非手術患者,Ⅲa期顯著長于Ⅲb期,但總的5年生存率為31.9%,經統計學處理與本研究36.3%的5年生存率無差別(P>0.05),不難看出,閆東的研究結果遠優于本研究。姚珂等[21]為234例Ⅲ期(其中30例Ⅲb)NSCLC術前行全身NCT,結果1、3、5年生存率分別為76.07%、52.99%、34.18%,經統計學處理,除1年生存率顯著低于本組的97.80%外(P<0.01),3年與5年生存率與本組無差別(P>0.05)。但Koshy等[22]報道的全身NCT的5年生存率為27.1%,顯著低于閆東等[20]和本組的術前BAI研究結果。理論上推測,BAI與全身NCT相比,BAI不僅給腫瘤及其轉移淋巴結一個高強度的重點打擊,而且進入血液循環的抗癌藥物對其他部位的微轉移灶有全身化療的作用,所以BAI是局部化療和全身化療的完美結合,這可能是療效好于全身NCT的重要原因,但有待于前瞻性的對照研究證實。
本研究表明,術前BAI用于治療Ⅲa(N2)期NSCLC具有良好耐受性,使腫瘤和縱膈淋巴結縮小,TNM分期下降,顯著提高根治性手術切除率,且不增加手術并發癥及病死率,明顯提高Ⅲa(N2)期患者的近期和遠期生存率,是肺癌綜合治療的一種有效方法,值得在臨床推廣應用。
[1]趙真真,王忠敏,茅愛武.非小細胞肺癌的介入治療現狀[J].介入放射學雜志,2014,23:272-276.
[2]李萬剛,崔進國.支氣管動脈灌注治療肺癌的現狀與展望[J].實用醫學雜志,2013,29:3460-3462.
[3]Kolek V,Grygarkova I,Hajduch M,et al.Long term follow-up of neoadjuvant-adjuvant combination treatment ofⅢA stage nonsmall-cell-lung cancer:results of neoadjuvant carboplatin/ vinorelbine and carboplatin/paclitaxel regimens combined with selectiveadjuvantchemotherapyaccordingtoin-vitro chemoresistance test[J].Biomed Pap Med Fac Univ Palacky Olomouc Czech Repub,2008,152:259-266.
[4]Depierre A,Milleron B,Moro-Sibilot D,et al.Preoperative chemotherapy followed by surgery compared with primary surgery in resectable stageⅠ(except T1N0),Ⅱ,andⅢa non-small-cell lung cancer[J].J Clin Oncol,2002,20:247-253.
[5]MellasN,ElmesbahiO,MasbahO,etal.Neoadjuvant chemotherapy in non-small cell lung cancer:current state and future[J].Bull Cancer,2010,97:211-223.
[6]Song WA,Zhou NK,Wang W,et al.Survival benefit of neoadjuvant chemotherapy in non-small cell lung cancer:an updated meta-analysis of 13 randomized control trials[J].J Thorac Oncol,2010,5:510-516.
[7]Bozcuk H,Abali H,Coskun S,et al.The correlates of benefit from neoadjuvant chemotherapy before surgery in non-small-cell lung cancer:a metaregression analysis[J].World J Surg Oncol,2012,10:161-169.
[8]Hellmann MD,Chaft JE,William WN,et al.Pathological response after neoadjuvant chemotherapy in resectable non-small-cell lung cancers:proposal for the use of major pathological response as a surrogate endpoint[J].Lancet Oncol,2014,15:e42-e50.
[9]Vallières E.More questions about neoadjuvant chemotherapy in lung cancer[J].Oncology(Williston Park),2009,23:892-896.
[10]Kim ES,Lee JJ,He G,et al.Tissue Platinum concentration and tumor response in non-small-cell lung cancer[J].J Clin Oncol,2012,30:3337-3344.
[11]Schallier D,Neyns B,Fontaine C,et al.A novel triplet regimen with paclitaxel,carboplatin and gemcitabine(PACCAGE)as induction chemotherapy for locally advanced unresectable non small cell lung cancer(NSCLC)[J].Lung Cancer,2007,56:247-254.
[12]Betticher DC,Hsu Schmitz SF,T?tsch M,et al.Mediastinal lymph node clearance after docetaxel-cisplatin neoadjuvant chemotherapy is prognostic of survival in patients with stageⅢA pN2 non-small-cell lung cancer:a multicenter phaseⅡtrial[J]. J Clin Oncol,2003,21:1752-1759.
[13]Liao WY,Chen JH,Wu M,et al.Neoadjuvant chemotherapy with docetaxel-cisplatin in patients with stageⅢN2 non-small-cell lung cancer[J].Clin Lung Cancer,2013,14:418-424.
[14]Jakobsen JN,Santoni-Rugiu E,Sorensen JB.Longitudinal assessment of TUBB3 expression in non-small cell lung cancer patients[J].Cancer Chemother Pharmacol,2014,73:43-51.
[15]William WN,Pataer A,Kalhor N,et al.Computed tomography RECIST assessment of histopathologic response and prediction of survival in patients with resectable non-small-cell lung cancer after neoadjuvant chemotherapy[J].J Thorac Oncol,2013,8:222-228.
[16]Kappers I,Van Sandick JW,Burgers SA,et al.Surgery after induction chemotherapy in stageⅢA-N2 non-small cell lung cancer:why pneumonectomy should be avoided[J].Lung Cancer,2010,68:222-227.
[17]So T,Osaki T,Nakata S,et al.Carinal resection after induction bronchial arterial infusion for locally advanced non-small cell lung cancer[J].Jpn J Thorac Cardiovasc Surg,2004,52:143-147.
[18]Davidov MI,Polotzky BE,Marenich AF,et al.Gemcitabine combined with cisplatin as neoadjuvant chemotherapy in stage IB-ⅢA non-small cell lung cancer[J].Anticancer Drugs,2011,22:569-575.
[19]Ceylan KC,Kaya SO,Samancilar O,et al.The effects of neoadjuvantchemotherapyonpulmonarystructures:a quantitative analysis[J].Thorac Cardiovasc Surg,2012,60:111-115.
[20]閆東,周純武,劉德忠,等.中心型非小細胞肺癌支氣管動脈灌注療效分析[J].中華腫瘤雜志,2011,33:302-304.
[21]姚珂,向明章,閔家新,等.Ⅲ期非小細胞肺癌術前新輔助化療的隨機對照臨床試驗[J].中國腫瘤臨床,2004,31:611-613.
[22]Koshy M,Fedewa SA,Malik R,et al.Improved survival associated with neoadjuvant chemoradiation in patients with clinical stageⅢa(N2)non-small-cell lung cancer[J].J Thorac Oncol,2013,8:915-922.
Preoperative bronchial artery infusion chemotherapy in the treatment of stageⅢa(N2)non-small celllung cancer
LI Wan-gang,CUI Jing,WANG Jian-jun,WANG Ji-yun,ZHANG Jian-wei,LIU Ben-gang,CHEN Shao-hua.Department of Thoracic Surgery,Affiliated Petroleum Central Hospital of Tianjin Medical University,Central Hospital of China National Petroleum and Gas Corporation,Langfang,Hebei Province 065000,China
WANG Jian-jun,E-mail:bgjjw@aliyun.com
R735
B
1008-794X(2015)-02-0160-06
2014-07-20)
(本文編輯:俞瑞綱)
10.3969/j.issn.1008-794X.2015.02.018
065000河北廊坊天津醫科大學附屬石油中心醫院、中國石油天然氣集團公司中心醫院胸外科(李萬剛、崔靜、王繼云、張建偉、劉本剛、陳紹華);華中科技大學附屬協和醫院胸外科(王建軍)
王建軍E-mail:bgjjw@aliyun.com

