肺移植麻醉330例臨床分析
胡春曉,陳靜瑜,王志萍,王桂龍,吳金波(.南京醫科大學附屬無錫市人民醫院麻醉科,江蘇 無錫 403;.南京醫科大學附屬無錫市人民醫院肺移植科,江蘇 無錫 403)
肺移植是終末期肺病的有效治療手段,受者移植術后可長期存活,生活質量得到改善。自2002年9月至2014年10月,無錫市人民醫院共完成了肺移植麻醉330例,現結合臨床資料,對肺移植麻醉的肺隔離技術、圍麻醉期處理、體外膜肺氧合的應用探討如下。
1 臨床資料
1.1 一般資料:自2002年9月至2014年10月,本院共完成肺移植330例(男性234例,女性96例),年齡15~74歲,平均(51.4±9.6)歲。ASA分級Ⅲ或Ⅳ級。患者原發疾病情況見表1。所有受者術前均需臥床吸氧治療,其中包括6例氣管切開患者和12例氣管插管呼吸支持患者;肺功能為中、重度阻塞性通氣功能障礙的患者有89例,143例為中、重度限制性通氣功能障礙,53例為混合性通氣功能障礙,45例患者因無法脫離吸氧機而未進行通氣功能檢查。血氣分析結果顯示,受者動脈血氧分壓(PaO2)為(62.3±18.5)mmHg(1 mmHg=0.133 kPa),動脈血二氧化碳分壓(PaCO2)為(69.5±23.6)mmHg。術前心臟彩色超聲檢查顯示,7例受者肺動脈平均壓小于30 mmHg,107例為30~50 mmHg,176例為51~70 mmHg,47例大于70 mmHg。79例患者左心室射血分數(LVEF)小于55%,202例為56%~65%,49例大于66%。
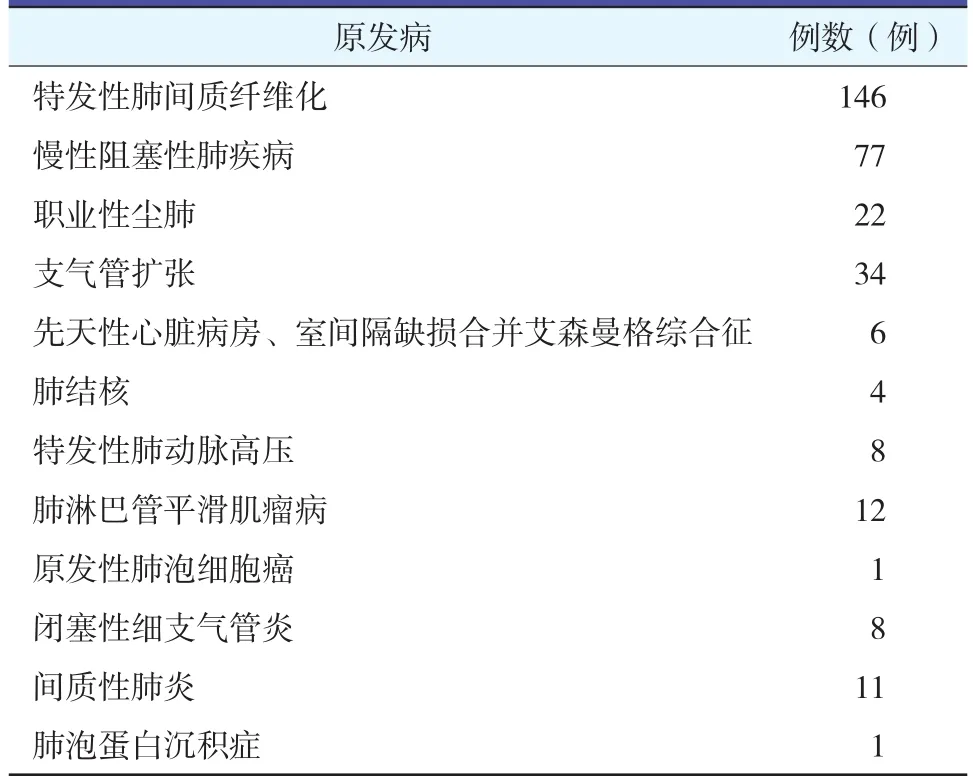
表1 原發疾病類型
1.2 麻醉方法及管理:入室后常規監測心電圖(ECG)、心率(HR)和血壓(BP)。麻醉誘導:靜脈注射咪達唑侖0.05~0.1 mg/kg、芬太尼4 μg/kg、依托咪酯0.2~0.4 mg/kg及維庫溴銨0.1 mg/kg后,行氣管內插管,連接呼吸機,行機械通氣。氣管導管根據手術需要分別選擇雙腔支氣管導管、單腔雙囊氣管導管(Univent導管)或支氣管阻塞器。麻醉維持:靜脈輸注異丙酚0.03~0.05 mg/(kg·min)、維庫溴銨1~2 μg/(kg·min),間斷靜脈注射芬太尼。術中連續監測ECG、呼吸末二氧化碳分壓(PetCO2)、脈搏血氧飽和度(SpO2)、肺動脈收縮壓(SPAP)、平均肺動脈壓(MPAP)、肺動脈動脈壓(PAWP)、心排指數(CI)、心排出量(CO)、氧飽和度(SO2)、PaO2、PaCO2、潮氣量(VT)、呼吸頻率(RR)、呼吸末正壓通氣(PEEP)、氣道峰壓(Ppeak)、氣道阻力(Raw)、動態胸肺順應性(Cdyn)及氧合指數等指標。通氣方式均采用壓力控制,呼吸機參數設置如下:Pinsp(吸氣壓力)為18~30 cmH2O(1 cmH2O=0.098 kPa),f(呼吸頻率)為12~16 次/ min ,Tinsp(吸氣時間)為1.5~2.5 s。根據血氣指標及生命體征調節通氣參數,必要時行手控通氣。對于術中不能耐受單肺通氣或心功能異常的患者給予體外膜肺氧合(ECMO)輔助。
1.3 手術方式及循環支持:330例肺移植患者中,單肺移植132例,雙肺移植198例。其中,177例受者在非體外循環下完成肺移植手術;5例(雙肺1例,單肺4例)在體外循環(CPB)支持下完成肺移植;148例患者在ECMO輔助下完成肺移植。
1.4 統計學分析:采用SPSS15.0進行統計分析。
2 結 果
2.1 術中氣道管理及麻醉處理:132例單肺移植患者中,121例應用非術側雙腔支氣管導管;3例術前氣管切開患者和6例術前氣管插管給予呼吸支持患者均應用支氣管阻塞器;2例患者因身材矮小而應用Univent導管。198例雙肺移植患者中,187例應用左側雙腔支氣管導管,其中5例因手術操作刺破套囊原因而更換導管,7例在吻合左側支氣管時退管;6例應用Univent導管;5例(2例術前氣管切開患者和3例術前氣管插管患者)應用支氣管阻塞器。
所有患者中,5例支氣管擴張患者和3例特發性肺纖維化(IPF)患者在麻醉誘導后出現氣道阻力增加,SO2下降,聽診兩肺濕啰音,氣管鏡檢查發現兩側支氣管均被痰液阻塞,給予吸痰后4例患者好轉;1例因持續低氧血癥而死亡;57例患者麻醉誘導后因低氧血癥〔(62.4±6.5)mmHg〕不能耐受單肺通氣而給予ECMO支持;2例患者在直接阻斷肺動脈后出現心跳驟停,其中1例經緊急CPB支持后繼續手術并存活;1例因未能及時建立CPB而搶救無效死亡;3例患者因試阻斷肺動脈后出現心律失常而給予ECMO支持;1例應用雙腔支氣管導管患者在吻合左主支氣管時因導管影響手術操作而調整至右主支氣管,而后因導管移位出現氣道阻力突然增大、氧飽和度下降,經處理后恢復正常。其余患者麻醉過程順利,均順利完成肺移植手術。
2.2 ECMO應用情況:148例術中應用ECMO輔助的患者中包括69例肺動脈高壓患者;心功能不全17例;低氧血癥57例;高碳酸血癥5例。所有患者均順利完成肺移植手術。133例患者術畢即刻撤除ECMO,15例患者因血流動力不穩定、氧合差,術后繼續使用ECMO。
2.3 肺移植療效及死亡原因:術后早期死亡25例,病死率為7.5%(18/330),死亡原因包括肺部感染13例,原發性移植物失功10例,急性排斥反應1例,肺梗死1例。對其他患者進行術后長期隨訪,術后1、2、3、5年累積生存率分別是73.3%、61.6%、53.5%和40.7%,存活患者心肺功能及生存質量均良好。
3 討 論
需要進行肺移植的均為終末期肺疾病和嚴重呼吸衰竭的患者[1]。本研究中的病例術前均需吸氧、臥床,部分患者甚至需給予呼吸機支持或ECMO輔助轉流后才能維持生存。因此,這些患者對麻醉、手術的耐受能力極差,尤其在麻醉誘導、單肺通氣和單側肺動脈阻斷時容易發生呼吸、循環功能衰竭。如何對圍麻醉期患者的呼吸和循環進行有效的管理,是麻醉醫生不可回避的難題,也是確保肺移植手術成功的前提。
3.1 肺隔離技術的合理應用:與普通胸科手術相同,完善的肺隔離技術是順利完成肺移植手術的前提。除非患者需要運用CPB,否則單肺通氣需要持續到移植肺通氣為止。單肺通氣的技術包括插入雙腔支氣管導管、Univent導管及支氣管阻塞器。
Bernard等[2]認為,肺移植手術中可使用左側雙腔支氣管導管,因為右側雙腔管有可能阻塞右上肺葉的開口。而在進行左側支氣管吻合時,偶爾需要將插管退回來一些,但在大多數情況下,左側雙腔氣管內插管沒有任何問題[3]。應根據手術醫師的手術方式和習慣而采取不同的單肺通氣技術。對于單肺移植的患者來說,氣管插管采用相對應的雙腔管即可;而對于雙肺移植尤其是非CPB下序貫式的雙肺移植,插管方式的選擇尤為重要,往往會因為通氣不全或氣道阻塞而導致麻醉意外的發生。本研究187例應用左側雙腔支氣管導管行雙肺移植的患者中,5例因手術操作原因刺破套囊而更換導管;7例在吻合左側支氣管時退管,其中1例因導管影響手術操作而調整至右主支氣管,之后因導管移位而出現氣道阻力突然增大、氧飽和度急劇下降。
無錫市人民醫院肺移植中心在雙肺移植時,一般根據患者身高、氣管長度及手術方式進行評估,對身材矮小、上葉支氣管開口距離隆突長度較短及分泌物較少的患者采用Univent導管或支氣管阻塞器。本研究的病例中部分患者采用了Univent導管(6/198)或支氣管阻塞器(5/198)進行單肺通氣,效果良好。對于一些特殊患者如身材矮小等,麻醉前應對其肺隔離方法進行充分評估,Univent導管或支氣管阻塞器應是首選。Compos[4]報道了鼻插管和氣管切開患者應用支氣管阻塞器進行單肺通氣。對于術前氣管插管或氣管切開的患者來說,應用支氣管阻塞器有其特殊的優點:首先,可以避免麻醉誘導后更換導管,只要從氣管導管或氣管切開處放入阻塞器就可以達到滿意的肺隔離效果;同時,此類患者術后存在呼吸機依賴的可能性,因此,手術結束后不用換管[5],必要時放入阻塞器可以進行分側肺通氣。本研究中共有8例患者(單肺移植2例,雙肺移植6例)使用Univent導管;14例患者(單肺移植9例,雙肺移植5例)使用支氣管阻塞器,均順利完成手術。
3.2 圍麻醉期呼吸和循環管理:圍麻醉期的呼吸和循環管理是肺移植麻醉管理的難點。肺移植患者因體質差、長期臥床,常合并嚴重的肺部感染,因此,對患者進行麻醉誘導時,應注意緩慢、聯合用藥,在用藥時要密切觀察患者氧合和血流動力學變化。插管后應及時進行導管定位和氣道清理,及時吸盡氣道內分泌物。本研究中最初對5例支氣管擴張患者和3例IPF患者麻醉誘導后,因其分泌物阻塞氣道而導致嚴重低氧血癥,在給予吸痰后4例好轉,但1例因持續低氧血癥而死亡。在以后的肺移植手術中,我們對有大量分泌物的患者均常規在坐位下先插單腔氣管導管,然后在氣管鏡吸引下逐漸平臥甚至頭低位吸凈分泌物后再更換雙腔支氣管導管,獲得了良好的治療效果。
在受者麻醉誘導完畢后,應盡早行單肺通氣,其目的是使機體逐漸適應單肺通氣帶來的改變,同時,在肺移植術前有足夠的時間來判斷單肺通氣對呼吸和循環帶來的影響[6]。對于不能耐受單肺通氣的患者需及時應用ECMO輔助轉流以完成手術。本研究中,57例患者在麻醉誘導后單肺通氣時因存在嚴重低氧血癥而給予ECMO支持完成手術。
病肺切除和移植肺期間,手術側肺動脈是需要夾閉的。在阻斷一側肺動脈后,肺動脈壓會急劇升高而導致右心衰和血流動力學嚴重紊亂,甚至會導致心跳驟停[7]。因此,在切除病肺之前需試阻斷肺動脈,以觀察患者心功能和血流動力學變化,必要時給予循環支持。本研究中有2例患者在未試阻斷肺動脈的情況下直接阻斷肺動脈后出現心跳驟停,其中1例患者經緊急建立CPB支持后繼續手術并存活,1例因未能及時建立CPB而搶救無效死亡;另3例患者因試阻斷肺動脈后出現心律失常而給予ECMO支持,效果滿意。
移植肺開放時,麻醉醫師在滿足患者氧合的基礎上應盡量減小移植肺的缺血/再灌注損傷。移植肺開放后會因血容量暫時性相對減少而出現血壓下降,因此,移植肺開放之前提前應用或增加血管活性藥物的劑量可以避免血流動力學的劇烈波動[8]。手術醫師應在人為控制下逐步、緩慢地開放肺動脈,灌注移植肺,盡量減少對移植肺的損傷。
3.3 ECMO在肺移植中的應用:在肺移植單肺通氣過程中,所有患者都可能出現低氧血癥、二氧化碳蓄積、肺動脈高壓和心功能異常[9]。部分患者經處理后仍可在非CPB下完成肺移植手術[5]。但對于低氧血癥和高碳酸血癥加重不能耐受單肺通氣的患者來說,給予ECMO輔助可有效改善氧合并排除CO2。同時,ECMO還可提供操作上的便利和更好的血流動力學穩定性。病肺切除和供肺移植期是肺移植手術期間機體血流動力學變化最劇烈的時期,除單肺通氣外,還需夾閉肺動脈,這會進一步增加右心室的壓力,同時肺動脈壓力和肺通氣阻力也會急劇上升[10-11]。為避免在阻斷單側肺動脈后肺動脈壓急劇升高導致右心衰和血流動力學嚴重紊亂,運用ECMO輔助轉流可有效降低肺動脈壓力,改善氧合,維持血流動力學穩定。在序貫式雙肺移植過程中,由于先植入的一側肺再植入第二個肺的過程中承擔了整個CO。此時可能發生嚴重的組織間隙水腫和肺泡水腫,表現為肺動脈壓升高和氣體交換障礙。建立ECMO不僅有利于呼吸道管理,更可明顯減輕第一側移植肺的損傷,并維持血流動力學的穩定[12-13]。本研究中69例肺動脈高壓術中應用ECMO輔助患者,術前肺動脈收縮壓為(9.2±2.4)kPa,手術風險大。在術中使用ECMO轉流后,有效地為肺動脈分流了心輸出量,降低了肺動脈的灌注壓力(6.3±1.5)kPa,尤其在阻斷一側肺動脈后有效地避免了因肺動脈壓急劇升高而導致的右心衰竭和血流動力學嚴重紊亂,效果理想。本研究中另有57例和17例患者分別因術中不能耐受單肺通氣和心功能異常而給予ECMO輔助轉流,均取得滿意的治療效果。
移植肺開放時,由于肺動脈壓力進一步下降,移植肺會因血流灌注的急劇增加而導致移植肺的急性損傷,因此,通過調節ECMO的流量可以在保證氧合的基礎上盡量減少移植肺的缺血/再灌注損傷。本研究中56例術中ECMO輔助轉流患者在移植肺開放前均以20 cmH2O的氣道壓力持續膨脹移植肺,再以50%氧、5 cmH2O的PEEP,氣道峰壓維持在20~25 cmH2O,在增大ECMO流量的基礎上,逐步開放肺動脈,灌注移植肺[12]。移植肺開放后,由于ECMO的保護作用,因而采用了小潮氣量、低氣道壓、適度的高CO2血癥的通氣方法,盡量使用較低濃度的氧和吸氣壓力以滿足患者氧供,避免機械通氣引起的氣道損傷,效果理想。

