抗結核固定劑量復合劑微生物限度檢查方法的建立和驗證
陳 娟
抗結核固定劑量復合劑微生物限度檢查方法的建立和驗證
陳 娟
【摘要】目的 探討抗結核固定劑量復合劑的微生物限度檢查方法的建立。方法 按照《中國藥典》2010年版附錄X ⅢC進行驗證實驗。結果 抗結核固定劑量復合劑對金黃色葡萄球菌、枯草芽胞桿菌、大腸埃希菌有一定的抑制作用。結論 抗結核固定劑量復合劑對細菌的計數方法應為離心沉淀法-薄膜過濾法,常規法進行霉菌(酵母菌)計數檢驗,薄膜過濾法進行控制菌檢驗。
【關鍵詞】驗證試驗;抗結核固定劑量復合劑;離心沉淀集菌-薄膜過濾法;常規法
【中圖分類號】R978.3;R927.1
【文獻標志碼】A
【文章編號】1673-5846(2015)10-0023-04
【Abstract】Objective To set up a method for microbial limit of Rifampin and Isoniazid Tablets.Methods Validation of microbial limit tests according to Chinese Pharmacopoeia edition 2010.Results FDCs has very strong inhibiting effect on Staphylococcus aureus,Bacillus subtilis and Candida albicans.Conclusion Low speed centrifuge-filtration methods were used with take count of bacterium;General methods were used with take count of mold and yeasts of FDCs.Pathogenic bacteria can be tested when filtration methods were used.
貴州省畢節市食品藥品檢驗所,貴州畢節 551700
Establishment and Validation of Microbial Limit Method for Anti-tuberculosis Fixed Dose Combinations
Chen Juan
【Key Words】Validation;FDCs;Filtration method;General method
世界衛生組織為遏制全球結核病的威脅,主張使用抗結核藥物的固定劑量復合劑(FDCs)代替抗結核單藥制劑來治療結核病患者。使用FDCs可以提高單一化療效果,減少耐藥菌的產生,根據患者服藥劑量,無需詳細計算藥物劑量,以簡便處方和服用。因為FDCs中的利福平有一定程度的抑菌作用,所以在對有抗菌活性的藥物進行微生物限度檢查時,必須先消除其抗菌活性,通過試驗驗證抗菌活性去除是否徹底,保證檢驗結果的有效性。為了消除FDCs的抗菌活性,真實地反映該藥物所污染微生物的程度,參考《中國藥典》[1]和研究資料[2-4]對FDCs進行微生物限度檢驗方法驗證。本試驗采用2010年版中國藥典規定的3株細菌(大腸埃希菌、金黃色葡萄球菌、枯草芽胞桿菌)、2株真菌(黑曲霉菌、白色念珠菌),采用常規法和低速離心-薄膜過濾法分別對3批利福平異煙肼片、乙胺利福異煙片、乙胺吡嗪利福異煙片進行細菌、霉菌及酵母菌計數和控制菌進行方法驗證,建立適合于FDCs的微生物限度檢查方法。
1 儀器與材料
1.1 試驗儀器 GHP-9000型隔水式恒溫培養箱(上海益恒實驗儀器有限公司);HC-TP-12型架盤天平(天津市天平儀器有限公司);LMQ.C型立式壓力蒸汽滅菌鍋(山東新華醫療器械股份有限公司);TG16-WS型臺式離心沉淀器(長沙湘儀離心機儀器有限公司);SHA-C型電熱恒溫振蕩器(金壇市盛藍儀器制造有限公司);DLM型鼓風干燥箱(常州創威實驗儀器廠);薄膜過濾器(畢節市食品藥品檢驗所)。
1.2 試驗材料 異福片(沈陽紅旗制藥有限公司,批號:1009011、1009021、1009031);利福平異煙肼片(沈陽紅旗制藥有限公司,批號:1009011、1009021、1009031);乙胺吡嗪利福異煙片(沈陽紅旗制藥有限公司,批號:1009011、1009021、1009031);大腸埃希菌(Escherichiacoli)[CMCC (B)44102];金黃色葡萄球菌(Staphylococcus aureus)[CMCC(B)26003];枯草芽胞桿菌(Bacillus subtilis)[CMCC(B)63501];白色念珠菌(Candida albicans)[CMCC(F)98001];黑曲霉(Aspergillus niger)[CMCC(F)98003];菌種來源(中國藥品生物制品檢定所提供,各菌株均為第3代)。
1.3 培養基 營養瓊脂(島高科園海博生物技術有限公司,批號:20131121);改良馬丁培養基(島高科園海博生物技術有限公司,批號:20120907);膽鹽乳糖培養基(北京陸橋技術有限責任公司,批號:111006);玫瑰紅鈉瓊脂(北京陸橋技術有限責任公司,批號:110109);麥康凱瓊脂培養基(北京陸橋技術有限責任公司,批號:121024);MUG培養基
(北京陸橋技術有限責任公司,批號:110212),按照《中國藥典》2010年版規定配制及滅菌。
2 試驗方法
2.1 供試品溶液的制備 取供試品10 g,加入200 ml 的pH7.0無菌氯化鈉-蛋白胨緩沖液,置40 ℃水浴中溶化,振搖,制成1:10的供試品溶液。
2.2 菌液制備 ①取經35 ℃培養24 h的大腸埃希菌、金黃色葡萄球菌、枯草芽胞桿菌的肉湯培養物,用0.9%無菌氯化鈉溶液制成每1 ml含細菌數為10~100 cfu的菌懸液,做活菌技術用。②取培養48 h的白色念珠菌至改良馬丁瓊脂斜面培養基中,用0.9%無菌氯化鈉溶液制成1 ml含細菌數為10~100 cfu的菌懸液,做活菌技術用。③接種預先活化的黑曲霉菌種至改良馬丁瓊脂斜面培養基中,培養7 d,用0.9%無菌氯化鈉溶液制成1 ml含細菌數為10~100 cfu的菌懸液,做活菌技術用。
2.3 驗證步驟
2.3.1 細菌、霉菌及酵母菌計數方法
2.3.1.1 常規法 ①供試品對照組:取靜置15 min 的1:10的供試液1 ml,測定供試品的本底菌數。②試驗組:供試液放置15 min后,取1 ml注入一平皿中,然后再取含細菌數為10~100 cfu的試驗菌液1 ml,立即傾注20 ml營養瓊脂培養基,每株試驗菌平行制備2個平皿,按平皿法測定菌落數。③稀釋劑對照組:分別取10~100 cfu的試驗菌和稀釋劑各1 ml,按試驗組菌數測定方法測定菌數。④菌液組:測定所加的試驗菌數。
2.3.1.2 離心沉淀集菌+薄膜過濾法 取靜置15 min 后1:20的供試液的上清液10 ml,經500轉3 min離心后,吸取5 ml(菌種的回收率能達到70%以上),然后再加入100 ml的pH7.0無菌氯化鈉-蛋白胨緩沖液混勻,通過濾膜,用500 ml的上述緩沖液分次沖洗,每次80 ml,最后在沖洗液中加入試驗菌,過濾,將濾膜貼于營養瓊脂培養基上培養,測定菌數。①供試品對照組:測定供試品本底菌數。②試驗組:取離心后的上清液適量,按上述方法測定試驗組菌數。③稀釋劑對照組:取供試品對照組供試液等量的稀釋劑和10~100 cfu試驗菌,按試驗組的菌數測定方法測定菌數。④菌液組:主要測定試驗中所加入的菌數是否合適。
2.3.2 驗證控制菌的檢查方法 菌液的制備:將活化好的大腸埃希菌、金黃色葡萄球菌菌種接種至營養瓊脂培養基中,24 h后將上述培養物用0.9%無菌氯化鈉溶液制成1 ml含10~100 cfu的菌懸液。
2.3.2.1 常規法 ①陰性菌對照組:取靜置15 min后供試液(1:20)10 ml,加入100 ml LBL增菌培養基中,然后再加入金黃色葡萄球菌試驗菌,搖勻,按照控制菌檢查法檢查。②試驗組:取靜置15 min后供試液(1:20)10 ml及大腸埃希菌的試驗菌入100 ml LBL增菌培養基中,混勻,依照控制菌法檢查。
2.3.2.2 薄膜過濾法 ①陰性菌對照組:供試液靜置15 min后,取上清液10 ml于50 ml pH7.0的無菌氯化鈉-蛋白胨緩沖液中搖勻,過濾,用上述溶液500 ml分次沖洗濾膜,每次50 ml,最后在沖洗液中加入上述金黃色葡萄球菌,取出濾膜接入100 ml LBL增菌培養基中,按照大腸埃希菌法檢查。②試驗組:供試液靜置15 min后,取上清液10 ml于100 ml pH7.0的無菌氯化鈉-蛋白胨緩沖液中搖勻,過濾,用該溶液500 ml分次沖洗濾膜,每次50 ml,最后在沖洗液中加入上述大腸埃希菌,取出濾膜接入100 ml LBL增菌培養基中,按照大腸埃希菌法檢查。
2.4 結果及回收率測定判斷標準


3 結果
3.1 利福平異煙肼片試驗結果 見表1~3。
3.2 乙胺利福異煙片試驗結果 見表4~6。
3.3 乙胺吡嗪利福異煙片試驗結果 見表7~9。

表1 利福平異煙肼片枯草芽胞桿菌、金黃色葡萄球菌、大腸埃希菌驗證結果
4 結論
通過試驗結果可以看出,利福平異煙肼片、乙胺利福異煙片、乙胺吡嗪利福異煙片微生物限度檢查法,細菌計數可采用離心沉淀集菌+薄膜過濾法,且供試品的供試液終濃度為1:1000;霉菌(酵母菌)
計數可采用常規法;控制菌檢查可采用薄膜過濾法進行檢驗。
由于抗結核固定劑量復合劑具有很強的抑菌作用,在檢驗時應排除其抑制作用,使其不干擾染菌限度檢查,結果才有效。
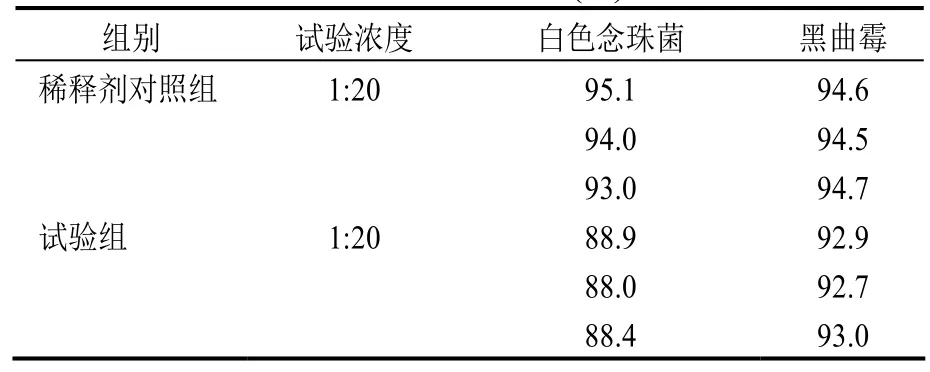
表2 常規法驗證利福平異煙肼片白色念珠菌、黑曲霉的回收率(%)

表3 控制菌試驗結果

表4 乙胺利福異煙片枯草芽胞桿菌、金黃色葡萄球菌、大腸埃希菌驗證結果

表5 常規法驗證乙胺利福異煙片白色念珠菌、黑曲霉的回收率(%)
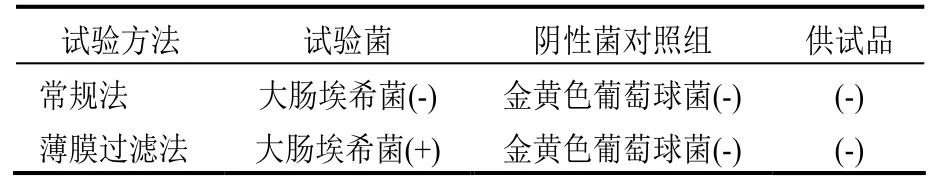
表6 控制菌常規法試驗結果

表7 乙胺吡嗪利福異煙片枯草芽胞桿菌、金黃色葡萄球菌、大腸埃希菌驗證結果

表8 常規法驗證乙胺吡嗪利福異煙片白色念珠菌、黑曲霉的回收率(%)

表9 控制菌常規法試驗結果
參考文獻
[1] 中華人民共和國國家藥典委員會.中國藥典·二部(附錄)2010
版[S].北京:中國醫藥科技出版社,2012:107-116.
[2] 中國藥品生物制品檢定所.中國藥品檢驗標準操作規范[S].北京:中國醫藥科技出版社,2010:351-389.
[3] 劉鵬,馬仕洪,戴翠,等.加替沙星微生物限度檢查方法的建立[J].藥物分析雜志,2007,27(6):881-881.
[4] 馬緒榮.藥品微生物學檢驗手冊[M].北京:科學出版社,2000: 289-290.

