厄貝沙坦聯合氨氯地平與氨氯地平單用對老年高血壓患者血壓變異性及血管內皮細胞功能影響的對比研究
楊瑩瑩,陳秋娟,袁 文,何永銘
·療效比較研究·
厄貝沙坦聯合氨氯地平與氨氯地平單用對老年高血壓患者血壓變異性及血管內皮細胞功能影響的對比研究
楊瑩瑩,陳秋娟,袁 文,何永銘
目的 比較厄貝沙坦聯合氨氯地平與氨氯地平單用對老年高血壓患者血壓變異性及血管內皮細胞功能的影響。方法 選取2014年3月—2016年3月第三軍醫大學第二附屬醫院收治的老年高血壓患者150例,隨機分為對照組和觀察組,每組75例。對照組患者給予氨氯地平治療,觀察組患者在對照組治療基礎上加用厄貝沙坦;兩組患者均連續治療12周。比較兩組患者治療前后血壓、血壓變異性及血清內皮素、一氧化氮水平,并觀察治療期間兩組患者不良反應發生情況。結果 治療前兩組患者24 h平均收縮壓(24 h SBP)、24 h平均舒張壓(24 h DBP)、白晝平均收縮壓(dSBP)、白晝平均舒張壓(dDBP)、夜間平均收縮壓(nSBP)、夜間平均舒張壓(nDBP)比較,差異均無統計學意義(P>0.05);治療后觀察組患者24 h SBP、24 h DBP、dSBP、nSBP、nDBP低于對照組(P<0.05),而治療后兩組患者dDBP比較,差異無統計學意義(P>0.05)。治療前兩組患者24 h收縮壓變異性(24 h SBPV)、24 h舒張壓變異性(24 h DBPV)、白晝收縮壓變異性(dSBPV)、白晝舒張壓變異性(dDBPV)、夜間收縮壓變異性(nSBPV)、夜間舒張壓變異性(nDBPV)比較,差異無統計學意義(P>0.05);治療后觀察組患者24 h SBPV、24 h DBPV、dSBPV、dDBPV、nSBPV、nDBPV低于對照組(P<0.05)。治療前兩組患者血清內皮素和一氧化氮水平比較,差異無統計學意義(P>0.05);治療后觀察組患者血清內皮素水平低于對照組,血清一氧化氮水平高于對照組(P<0.05)。治療期間,對照組患者出現腹脹1例,觀察組患者出現腹瀉2例。結論 與單用氨氯地平相比,厄貝沙坦聯合氨氯地平能更有效地降低老年高血壓患者血壓、血壓變異性并改善血管內皮細胞功能,且安全性較高。
高血壓;老年人;厄貝沙坦;氨氯地平;血壓變異性;內皮細胞
楊瑩瑩,陳秋娟,袁文,等.厄貝沙坦聯合氨氯地平與氨氯地平單用對老年高血壓患者血壓變異性及血管內皮細胞功能影響的對比研究[J].實用心腦肺血管病雜志,2016,24(12):62-65.[www.syxnf.net]
YANG Y Y,CHEN Q J,YUAN W,et al.Comparative study for impact on blood pressure variability and vascular endothelial cell function of elderly hypertension patients between irbesartan combined with amlodipine and amlodipine alone[J].Practical Journal of Cardiac Cerebral Pneumal and Vascular Disease,2016,24(12):62-65.
原發性高血壓是老年人常見心血管疾病之一,隨著年齡增長其發病率呈升高趨勢[1-3]。近年研究表明,長期高血壓可導致腎功能不全、血管內皮細胞功能損傷、中小血管及微血管病變等,并已成為導致老年高血壓患者死亡的主要原因。隨著血管內皮細胞功能損傷的發生發展,老年高血壓患者血管彈性減弱、僵硬度增加,進而導致患者血壓變異性增大[4-5]。相關研究表明,血壓變異性與高血壓患者靶器官損傷和心腦血管疾病的發生具有密切聯系[6-8]。血管內皮細胞不僅是一道維持液體滲透平衡的屏障,還在維持血管壁正常彈性和張力、保持血管壁通透性及免疫反應中發揮著重要作用。因此,研究血管內皮細胞功能障礙機制已成為心血管領域的熱點,而一氧化氮和內皮素是具有代表性的血管活性物質[9-10]。本研究旨在比較厄貝沙坦聯合氨氯地平與氨氯地平單用對老年高血壓患者血壓變異性及血管內皮細胞功能的影響,以為臨床醫師選擇合理的降壓藥物提供參考依據。
1 資料與方法
1.1 一般資料 選取2014年3月—2016年3月第三軍醫大學第二附屬醫院收治的老年高血壓患者150例,隨機分為對照組和觀察組,每組75例。兩組患者性別、年齡、高血壓病程、基線收縮壓(SBP)和基線舒張壓(DBP)比較,差異無統計學意義(P>0.05,見表1),具有可比性。本研究經醫院醫學倫理委員會審核批準,所有患者自愿參加本研究并簽署知情同意書。

表1 兩組患者一般資料比較
注:SBP=收縮壓,DBP=舒張壓;a為χ2值
1.2 納入與排除標準 納入標準:(1)符合“中國高血壓防治指南”中高血壓的診斷標準:SBP≥160 mm Hg(1 mm Hg=0.133 kPa)和/或DBP≥90 mm Hg;(2)年齡>60歲。排除標準:(1)繼發性高血壓;(2)研究期間發生急性腦血管事件和心血管事件者;(3)合并嚴重肝腎功能不全者。
1.3 治療方法 對照組患者給予氨氯地平(生產廠家:輝瑞制藥有限公司;國藥準字H10950224;規格:5 mg×7)治療,5 mg/次,1次/d;觀察組患者在對照組治療基礎上加用厄貝沙坦(生產廠家:修正藥業集團股份有限公司;國藥準字H20053912)治療,150 mg/次,1次/d。兩組患者均連續治療12周。
1.4 觀察指標 比較兩組患者治療前后血壓、血壓變異性及血清內皮素、一氧化氮水平,觀察治療期間兩組患者不良反應發生情況。
1.4.1 血壓和血壓變異性檢測方法 兩組患者均采用24 h動態血壓監測儀進行監測,計算機自動記錄其血壓和血壓變異性。血壓包括24 h平均收縮壓(24 hours mean systolic blood pressure,24 h SBP)、24 h平均舒張壓(24 hours mean diastolic blood pressure,24 h DBP)、白晝平均收縮壓(daytime mean systolic blood pressure,dSBP)、白晝平均舒張壓(daytime mean systolic blood pressure,dDBP)、夜間平均收縮壓(night time mean systolic blood pressure,nSBP)、夜間平均舒張壓(night time mean diastolic blood pressure,nDBP);血壓變異性包括24 h收縮壓變異性(24 hours systolic blood pressure variability,24 h SBPV)、24 h舒張壓變異性(24 hours diastolic blood pressure variability,24 h DBPV)、白晝收縮壓變異性(daytime systolic blood pressure variability,dSBPV)、夜間收縮壓變異性(night time systolic blood pressure variability,nSBPV)、白晝舒張壓變異性(daytime diastolic blood pressure variability,dDBPV)、夜間舒張壓變異性(night time diastolic blood pressure variability,nDBPV)。
1.4.2 一氧化氮和內皮素檢測方法 兩組患者均空腹8 h后于晨起抽取靜脈血4 ml,采用雙抗體夾心酶聯免疫吸附試驗檢測血清內皮素水平,采用硝酸還原酶法檢測血清一氧化氮水平。
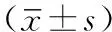
2 結果
2.1 血壓 治療前兩組患者24 h SBP、24 h DBP、dSBP、dDBP、nSBP、nDBP比較,差異均無統計學意義(P>0.05);治療后觀察組患者24 h SBP、24 h DBP、dSBP、nSBP、nDBP低于對照組,差異有統計學意義(P<0.05),而治療后兩組患者dDBP比較,差異無統計學意義(P>0.05,見表2)。
2.2 血壓變異性 治療前兩組患者24 h SBPV、24 h DBPV、dSBPV、dDBPV、nSBPV、nDBPV比較,差異無統計學意義(P>0.05);治療后觀察組患者24 h SBPV、24 h DBPV、dSBPV、dDBPV、nSBPV、nDBPV低于對照組,差異有統計學意義(P<0.05,見表3)。
2.3 血清內皮素和一氧化氮水平 治療前兩組患者血清內皮素和一氧化氮水平比較,差異無統計學意義(P>0.05);治療后觀察組患者血清內皮素水平低于對照組,血清一氧化氮水平高于對照組,差異有統計學意義(P<0.05,見表4)。
表4 兩組患者治療前后血清內皮素和一氧化氮水平比較
Table 4 Comparison of serum levels of endothelin and NO between the two groups before and after treatment

組別例數內皮素(ng/L)治療前 治療后一氧化氮(μmol/L)治療前 治療后對照組7545.84±9.3635.82±8.1331.32±8.7644.47±7.51觀察組7544.56±7.1232.84±8.3630.13±9.0854.21±10.23t值0.942.210.820.41P值0.350.030.650.00

表2 兩組患者治療前后血壓比較
注:24 h SBP=24 h平均收縮壓,24 h DBP=24 h平均舒張壓,dSBP=白晝平均收縮壓,dDBP=白晝平均舒張壓,nSBP=夜間平均收縮壓,nDBP=夜間平均舒張壓

表3 兩組患者治療前后血壓變異性比較
注:24 h SBPV=24 h收縮壓變異性,24 h DBPV=24 h舒張壓變異性,dSBPV=白晝收縮壓變異性,dDBPV=白晝舒張壓變異性,nSBPV=夜間收縮壓變異性,nDBPV=夜間舒張壓變異性
2.4 不良反應 治療期間,對照組患者出現腹脹1例,未停藥,后自行緩解;觀察組患者出現腹瀉2例,未進行相關治療,后自行緩解。
3 討論
據統計,我國老年高血壓患者數量已超過8 000萬,而由于老年人血管壁彈性減退、各項生理功能衰退,故老年高血壓患者具有SBP高、脈壓及血壓變異性大等特點[11]。大動脈彈性減退導致機體對心排血量的微小變動反應遲鈍,進而導致血壓變異性增大[12-13]。收縮壓可反映動脈管壁硬化程度,脈壓可反映大動脈硬化程度[14],故控制收縮期高血壓是治療老年高血壓的重點。
血管內皮細胞覆蓋于全身血管內表面,其不僅是血液與細胞外液之間進行物質交換和維持液體滲透壓平衡的屏障,還具有代謝活性、內分泌功能和多種生物學效應。內皮細胞在血流機械作用及神經刺激下可分泌內皮素和一氧化氮,而內皮素和一氧化氮對血管舒張與收縮功能具有調節作用。內皮素具有強大的縮血管功能,可促進血管內皮增生;一氧化氮主要影響血管張力。正常情況下,循環系統中一氧化氮和內皮素通過相互拮抗而維持平衡,該平衡使血管內皮細胞保持著正常的舒張與收縮功能。一氧化氮、內皮素異常可引起血壓異常;反之,血壓異常可加重血管內皮細胞分泌功能異常,嚴重者可導致血管內皮細胞功能損傷。
氨氯地平能持久發揮阻滯血管平滑肌細胞鈣離子通道的作用,能增強老年高血壓患者的降壓療效,進而發揮心血管保護作用。厄貝沙坦作為血管緊張素Ⅱ轉換受體拮抗劑,能抑制血管緊張素Ⅱ轉換,且不受血管緊張素轉換酶(ACE)基因多態性的影響。本研究報道顯示,治療后觀察組患者24 h SBP、24 h DBP、dSBP、nSBP、nDBP、24 h SBPV、24 h DBPV、dSBPV、dDBPV、nSBPV、nDBPV及血清內皮素水平低于對照組,血清一氧化氮水平高于對照組,結合既往研究報道考慮血壓變異性的改善可能與雙聯降壓治療對內皮細胞分泌一氧化氮及內皮素具有一定的調節有關。
綜上所述,與單用氨氯地平相比,厄貝沙坦聯合氨氯地平能更有效地降低老年高血壓患者血壓、血壓變異性并改善血管內皮細胞功能,且安全性較高。本研究結果可在一定程度上為臨床醫師選擇降壓方案提供參考。
[1]吳澤兵,張穎,余其貴,等.纈沙坦聯合氨氯地平或氫氯噻嗪對老年高血壓患者血壓變異性的影響[J].中華心血管病雜志,2012,40(1):8-13.
[2]潘春奇,王琳,劉文民.氨氯地平聯合培哚普利對老年原發性高血壓患者血壓變異性的影響[J].中華全科醫學,2016,14(8):1335-1337.
[3]STEWART D L,HARSHFIELD G A,ZHU H,et al.Stress and salt sensitivity in primary hypertension[J].Curr Hypertens Rep,2015,17(2):2.
[4]MANNING L,HIRAKAWA Y,ARIMA H,et al.Blood pressure variability and outcome after acute intracerebral haemorrhage:a post-hoc analysis of INTERACT2,a randomised controlled trial[J].Lancet Neurol,2014,13(4):364-373.
[5]OMBONI S,POSOKHOV I N,ROGOZA A N.3D.05:RELATIONSHIP BETWEEN 24-HOUR BLOOD PRESSURE VARIABILITY AND 24-HOUR AORTIC PRESSURE AND STIFFNESS IN HYPERTENSIVE PATIENTS[J].J Hypertens,2015,33 Suppl 1:e41-42.
[6]李鎮洲,張少鑫,萬建新.血壓變異性與高血壓靶器官損害的關系[J].中華高血壓雜志,2014,12(11):13-14.
[7]CUI H,WANG F,FAN L,et al.Association factors of target organ damage:analysis of 17 682 elderly hypertensive patients in China[J].Chin Med J(Engl),2011,124(22):3676-3681.
[8]PITANGA T N,DE ARAGO FRAN?A L,ROCHA V C,et al.Neutrophil-derived microparticles induce myeloperoxidase-mediated damage of vascular endothelial cells[J].BMC Cell Biol,2014,15:21.
[9]HIASA K,ISHIBASHI M,OHTANI K,et al.Gene transfer of stromal cell-derived factor-1alpha enhances ischemic vasculogenesis and angiogenesis via vascular endothelial growth factor/endothelial nitric oxide synthase-related pathway:next-generation chemokine therapy for therapeutic neovasculariza[J].Circulation,2014,109(20):2454-2461.
[10]LIU J,ZHANG X Y.Vascular Endothelial Cell Injury and Repair Mechanisms[J].Chemical Engineering Progress,2014,100(4):27-34.
[11]CHOWDHURY E K,OWEN A,KRUM H,et al.Systolic blood pressure variability is an important predictor of cardiovascular outcomes in elderly hypertensive patients[J].J Hypertens,2014,32(3):525-533.
[12]叢曉榮,秦景梅,史孝玲.厄貝沙坦氫氯噻嗪片對原發性高血壓患者血壓及血壓變異性的影響[J].中國醫藥,2013,8(7):911-912.
[13]謝軍,孫彩霞,孫媛媛.老年高血壓患者血壓變異性與早期腎功能損害的相關性研究[J].臨床和實驗醫學雜志,2012,11(3):180-181.
[14]CORREIA S,SALLOWAY S,MALLOY P,et al.Systolic blood pressure variability and subcortical hyperintensities in patients with mild-to-moderate Alzheimer′s disease[J].Neurobiology of Aging,2014,25(4):S278-279.
(本文編輯:謝武英)
Comparative Study for Impact on Blood Pressure Variability and Vascular Endothelial Cell Function of Elderly Hypertension Patients between Irbesartan Combined with Amlodipine and Amlodipine Alone
YANGYing-ying,CHENQiu-juan,YUANWen,HEYong-ming.
DepartmentofPharmacy,theSecondAffiliatedHospitaloftheThirdMilitaryMedicalUniversity,Chongqing400037,China
Objective To compare the impact on blood pressure variability and vascular endothelial cell function of elderly hypertension patients between irbesartan combined with amlodipine and amlodipine alone.Methods A total of 150 elderly hypertension patients were selected in the Second Affiliated Hospital of the Third Military Medical University from March 2014 to March 2016,and they were randomly divided into control group and observation group,each of 75 cases.Patients of control group were given amlodipine alone,while patients of observation group were given irbesartan combined with amlodipine;both groups continuously treated for 12 weeks.Blood pressure and its variability,serum levels of endothelin and NO before and after treatment were compared between the two groups,meanwhile incidence of adverse reactions during the treatment was observed.Results No statistically significant differences of 24-hour SBP,24-hour DBP,daytime SBP,daytime DBP,nighttime SBP or nighttime DBP was found between the two groups before treatment,nor was daytime DBP between the two groups after treatment(P>0.05),while 24-hour SBP,24-hour DBP,daytime SBP,nighttime SBP and nighttime DBP of observation group were statistically significantly lower than those of control group after treatment(P<0.05).No statistically significant differences of 24-hour SBP variability,24-hour DBP variability,daytime SBP variability,daytime DBP variability,nighttime SBP variability or nighttime DBP variability was found between the two groups before treatment(P>0.05),while 24-hour SBP variability,24-hour DBP variability,daytime SBP variability,daytime DBP variability,nighttime SBP variability and nighttime DBP variability of observation group were statistically significantly lower than those of control group after treatment(P<0.05).No statistically significant differences of serum level of endothelin or NO was found between the two groups before treatment(P>0.05);after treatment,serum endothelin level of observation group was statistically significantly lower than that of control group,while serum NO level of observation group was statistically significantly higher than that of control group(P<0.05).During the treatment,1 case of control group occurred abdominal distention,2 cases of observation group occurred diarrhea.Conclusion Compared with amlodipine alone,irbesartan combined with amlodipine can more effectively reduce the blood pressure and its variability,improve the vascular endothelial cell function,has higher safety.
Hypertension;Aged;Irbesartan;Amlodipine;Blood pressure variability;Endothelium
400037重慶市,第三軍醫大學第二附屬醫院藥劑科(楊瑩瑩,陳秋娟,袁文),心血管內科(何永銘)
R 544.1
B
10.3969/j.issn.1008-5971.2016.12.016
2016-09-26;
2016-12-13)

