基于仿真技術的血管支架工藝設置的研究
張永濤賈延明
摘要:醫用冠脈血管支架加工工藝復雜,工藝條件的設置對支架的性能有較大的影響。為清晰的了解壓握、擴張尺寸設置對支架性能的影響,利用計算機仿真技術研究不同工藝設置對支架性能的影響。通過研究發現:壓握工況設置下的支架安全性能隨壓握尺寸減小而變差;擴張工況設置下的支架安全性能隨擴張尺寸減小而變好;并且不同的壓握、擴張條件對支架的應力也產生一定的影響。結果表明:可以利用仿真技術預見不同的工藝設置對支架的性能影響,完善工藝設置。
關鍵詞:醫用血管支架;壓握;擴張,計算機仿真
中圖分類號:TP391.9文獻標識碼:A
1引言
《中國心血管病報告2013》統計出2012年我國患有心血管病的病人中,每10萬人就有255例病人死亡,平均每5例死亡中就有2例死于心血管病,死亡率居各種疾病之首。隨著人們生活質量的提高,以及對心血管疾病的研究越來越深入,如何高效的治療這類疾病受到廣泛的重視。球囊擴張式醫用血管支架是在細的金屬管材進行切割處理,通過輸入裝置輸送到血管病變處,利用球囊對支架進行擴張從而支撐起狹窄病變血管的微創手術器械[1],這類支架目前已經廣泛應用到臨床治療之中。
計算機仿真近些年發展迅速,在國內呈現蓬勃的發展趨勢,在醫療器械領域的應用也逐漸展開。計算機仿真其優點在于能夠直觀的模擬出支架壓握、球囊擴張、植入人體等過程,可有效預測出不同階段支架的變形、應力分布及疲勞安全性能[2-4]。基于計算機仿真技術的支架分析結果,對產品的設計有重要的指導意義,可以減少研發時間、成本,同時提高產品的安全性能。本文研究了基于計算機仿真技術的工藝條件的設置對支架性能的影響,希望通過這項研究來預見工藝條件對性能的影響規律,對支架生產和植入提供指導意見。國內外利用仿真技術對工藝方法研究的文獻鮮有出現。
球囊擴張支架的完整變形過程包括支架植入前的壓握、植入后的球囊擴張和球囊撤出后支架的彈性恢復等幾個階段,是一個同時具有幾何非線性和邊界條件非線性的過程[5]。每一步的工藝條件的設置對支架的性能都有一定的影響,本文將通過計算機仿真直觀的研究工藝條件對支架性能的影響規律。
2材料和方法
2.1計算機仿真模型
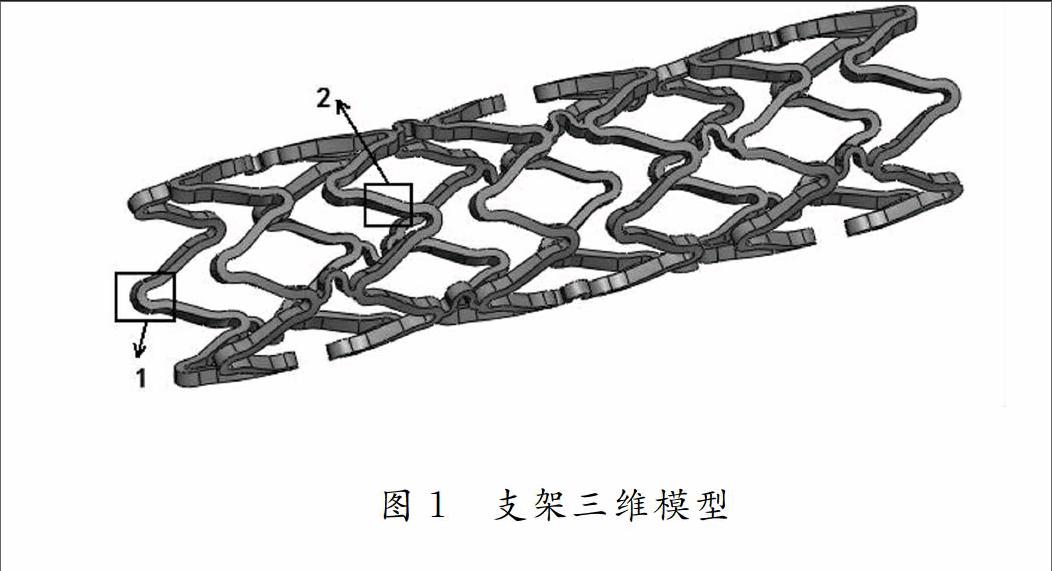
鈷鉻(Co-Cr)合金材料具有優良的抗腐蝕性能和機械性能,并且生物相容性較好,很好的滿足人體植入性材料的使用要求。使用鈷鉻合金材料制備的心血管支架利用材料本身的塑性性能支撐起病變血管,保證病變血管的通暢。支架結構設計種類多樣,最終的目的都是保證植入的安全性和有效性,本文設計了一種常用的支架結構來完成對工藝條件的研究,利用Solidworks建立的三維模型見圖1,支架外徑為1.8mm,壁厚100微米,長度8.2mm,并利用Abaqus完成仿真分析。支架結構中,位置1指的是加強環位置,連接兩個加強環的位置2指的是連接桿。
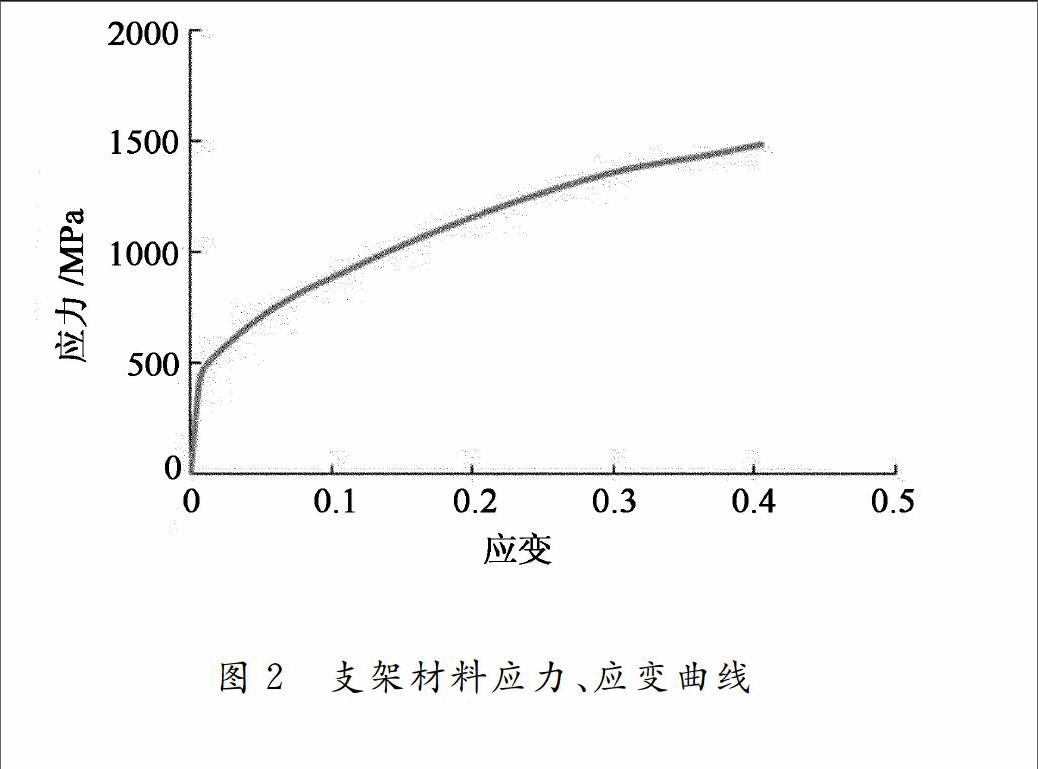
支架材料的應力、應變關系是通過對采用和實際工藝完全相同方法處理后的標準試件進行拉伸卸載實驗后得到的,材料曲線見圖2。材料的密度為7.8×10-9Kg/m3,楊氏模量為231Gpa,屈服強度為410Mpa,抗拉強度為1507Mpa,泊松比為0.3。
2.2邊界條件
支架在壓握、擴張過程中,涉及到支架結構大變形、材料非線性和幾何非線性,有效邊界條件設置可以保證求解過程收斂,以及結果的準確度。為模擬支架真實的變形過程,邊界條件的設置與支架生產加工,植入的實際情況嚴格保持一致。有限元模型的邊界條件是:支架在壓握、擴張等過程中,認為支架中間部位是固定的,對支架的中間部位的節點施加軸向及周向的位移約束,限制支架在軸向和周向的位移;球囊、壓握工具利用剛性管替代,對其軸向、周向施加位移約束,固定軸向的位移,在周向施加位移條件,以完成支架的壓握和擴張。支架有限元分析過程中的接觸較多,主要有:支架壓握過程中,支架與壓握工具的接觸;擴張過程中,支架與球囊的接觸;并且在壓握過程中支架本身有自接觸[6]。
支架疲勞分析時,建立起支架與血管之間的接觸關系。分析中的血管材料定義為超彈性材料模型[7],血管內徑變化比值需滿足血管順應性的要求[8]。支架表面作為從面,血管表面作為主面,并對血管內表面施加相當于生理血壓的外載荷,并按照正弦曲線的變化規律進行設計,低壓為80mmHg,高壓為180mmHg[9],通過對血管施加脈動載荷模擬支架外表面受到的脈動載荷,進行支架疲勞分析。所有的接觸方式定義為面對面接觸,接觸屬性定義中,采用非線性罰剛度的罰函數法。
2.3工藝條件設置方法
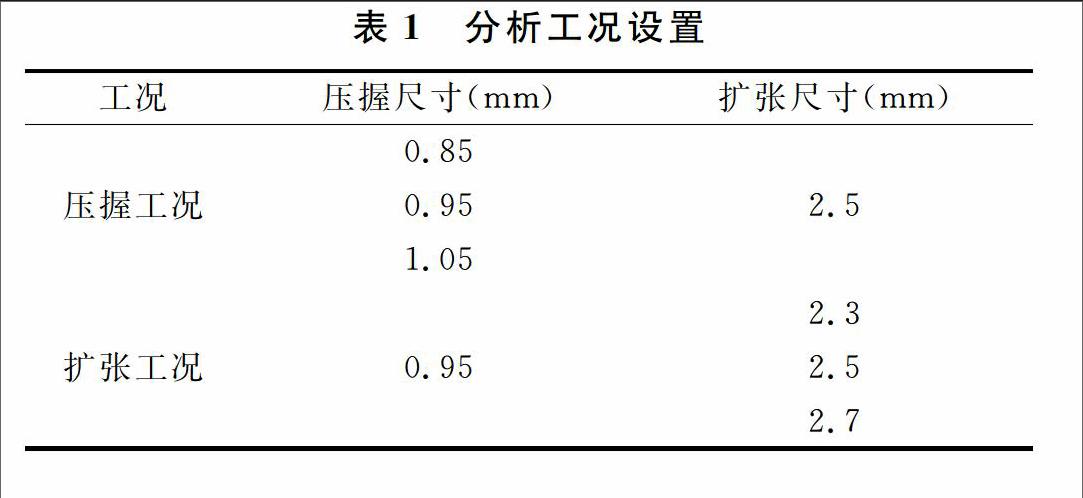
為清晰的了解工藝條件設置對支架性能的影響,本文研究了不同壓握尺寸,相同擴張尺寸;相同壓握尺寸,不同擴張尺寸對支架性能的影響。支架原始外徑1.8mm,壁厚0.1mm,支架結構模型和有限元網格處理方式是統一的。分析工況共2種:壓握工況、擴張工況,分別有3種設置,具體設置見表1。
3分析結果
3.1支架應力分析結果
支架在加工、植入過程中會產生較大的變形,以方便植入和支持病變血管,在這個過程中支架隨著自身形狀的改變產生塑性變形,支架某些部位的應力隨之增大,甚至會破壞支架的結構,因而良好的結構設計是產品的必要條件。拉應力會使支架斷裂,支架在壓握、擴張過程中對的應力一定不能超過材料的抗拉極限。
支架壓握過程的拉應力一般不會太大。壓握時,支架的最大應力是871.7MPa,出現在支架的加強環處。支架壓握后的應力大多集中在支架的加強環的周圍,連接桿處的應力都比較小,因而支架加強環的設計至關重要。支架壓握尺寸的大小直接的影響是支架的輸送性能,壓握尺寸越小支架輸送時通過病變部位狹小空間的通過性能會較高,但過小的壓握尺寸又會引起支架壓握時應力增大,并有可能將球囊擠破。不同壓握尺寸、相同擴張尺寸的支架應力變化趨勢見圖3,壓握應力隨著支架壓握外徑的減小而增大,在壓握過程中變形量越大,支架產生的應力越大,因而不能夠只追求支架的通過性能而使支架壓握應力過大。
壓握回彈后,支架應力減小到626.5MPa,外徑從壓握尺寸的0.95mm,回彈到0.975mm,徑向回彈率為2.63%。
擴張時,支架的最大應力是1479MPa,同樣出現在加強環處。支架擴張后的應力同樣隨著壓握外徑的減小而增大,壓握尺寸不只是影響支架的壓握應力,對擴張應力同樣有影響。支架擴張后可以有效的支撐起病變血管,使血管順暢。支架擴張引起的應力集中較為明顯,這一階段也最容易出現支架斷裂的風險。在設計支架時,應考慮到支架擴張對支架的影響,臨床植入時,遇到病變情況很不一致,有些情況需要將擴張尺寸增加一些,以滿足臨床需求,但過擴尺寸對支架性能的影響要小,否則會產生風險。相同擴張尺寸,不同壓握尺寸的支架,最大應力隨擴張尺寸的變化趨勢見圖4。
對于相同壓握尺寸,不同擴張尺寸的支架,最大應力隨擴張尺寸的增大而增大。在保證壓握尺寸相同的情況下,支架在不同血管的擴張會造成應力的不同,這也是很多產品在設計時,考慮不同規格對應不同擴張尺寸的重要原因。
3.2疲勞分析結果
支架植入人體后,支撐起病變血管,同時受到血管舒張壓和收縮壓的影響,由于人體的生理周期作用,血管壁會對支架施加周期性的脈動循環載荷。美國藥品食品監督局[10],推薦用Goodman準則來評價支架的疲勞壽命。本研究的疲勞計算方式按照本準則進行計算。壓握0.95mm,擴張至2.5mm的工況,支架應力為650.6MPa,遠低于擴張階段的應力,主要是因為支架植入人體后,在人體的生理血壓的作用下,支架的彈性性能完全釋放,依靠材料的塑性性能支撐血管,支架應力下降,其他工況的分析結果是一致的。支架內徑從擴張尺寸的2.5mm,回彈到2.42mm,徑向回彈率為3.2%。在血管脈動載荷的作用下,支架的疲勞安全系數是2.61,滿足支架的使用要求。
從圖5的Goodman圖可以看到,由于支架結構的抗外載荷能力強,應力坐標點的整體分布均勻。疲勞曲線是一條連接材料抗拉強度和疲勞極限的直線,因此應力坐標點和疲勞極限直線的距離會隨著平均應力的增大而越來越近,在Goodman圖中離疲勞極限直線越近的點越容易失效。從圖6中可以看出,不同壓握尺寸,相同擴張尺寸的支架安全系數隨著壓握尺寸的增大而增大,表明支架的壓握尺寸對支架安全性能有一定的影響。在支架加工過程中,可以在保證支架安全性能的前提下,壓握尺寸盡量小些,以獲得較好的彎曲通過性能。相同壓握尺寸,不同擴張尺寸的支架的安全系數隨著擴張尺寸的增大而變小,清晰的表明擴張尺寸不同對支架安全性能是線性的,在支架植入時應該按照支架設計的擴張尺寸進行擴張,過度擴張可能會導致支架擴張失效。
4結論
本文利用計算機仿真技術分析了不同工藝設置對支架性能的影響,主要包括壓握、擴張、疲勞分析等。通過這些分析可以看到支架在整個工藝過程中的應力分布情況,以及最終的疲勞情況。通過這些分析表明:不同壓握尺寸,相同擴張尺寸的支架應力,壓握、擴張時隨壓握尺寸的減小而增大,安全系數隨壓握尺寸的減小而減低。相同壓握尺寸,不同擴張尺寸的支架的應力隨擴張尺寸的增大而增大,安全系數隨擴張尺寸的增大而減小。當支架植入人體后,在血管周期載荷的作用下,支架的應力會下降到一個較小的值。
工藝條件設置不同,對支架的植入影響是不同的。合理的工藝設計可以降低支架植入的風險。計算機仿真可以有效的、快速的對支架產品的性能進行查看,對工藝設置是否合理進行探索。通過對比分析最終結果,可以幫助設計人員較快的對其支架設計效果進行分析與評價,從而縮短設計周期,減少研發費用。
參考文獻
[1]HSIAO H M, Chiu Y H, LEE K H, Lin C H. Computational modeling of effects of intravascular stent design on key mechanical and hemodynamic behavior[J]. ComputerAided Design,2012,44:757-765.
[2]HOUMAN Z, DANIEL J K, LALLY C. Simulation of a balloon expandable stent in a realistic coronary artery Determination of the optimum modelling strategy[J]. Journal of Biomechanics.2010,43:2126-2132.
[3]CHUA S N, DONALD, B J. HASHMI M S J. Finite element simulation of stent and balloon interaction[J]. Journal of Materials Processing Technology.2003.143-144:591-597.
[4]DUMOULIN C, COCHELIN B. Mechanical behaviour modelling of balloonexpandable stents[J]. Journal of Biomechanics.2000,33:1461-1470.
[5]王明,馬全超,張文光,等. 壓握過程對球囊擴張支架性能的影響[J].上海交通大學學報.2012,46(4):646-650.
[6]RAMESH V M, ROBERT B, GRISHABER R B, RITCHIE R O. Fatigue and life prediction for cobaltchromium stents:A fracture mechanics analysis[J].Biomaterials. 2006,27:1988-2000.
[7]ESHGHI N, HOJJATIA M H, IMANI M, GOUDARZI A M. Finite Element Analysis of Mechanical Behaviors of Coronary Stent[J].Procedia Engineering,2011,10:3056-3061.
[8]BS EN ISO 25539-1:2009,Cardiovascular implants. Endovascular devices. Endovascular prostheses[S].
[9]HSIAO H M, NIKANOROY A, PRABHU S, RAZAYI M K. Respirationinduced Kidney Motion on Cobaltchromium Stent Fatigue Resistance[J]. Journal of Biomedical Materials Research: Part BApplied Biomaterials, 2009,91(2):508-516.
[10]Food and Drug Administration. NonClinical Engineering Tests and Recommended Labeling For Intravacular Stents and Associated Delivery Systems. 2010.

