LSD1在消化道腫瘤中的研究進展
?
·綜述·
LSD1在消化道腫瘤中的研究進展
葛蓓蕾1徐霞2
(1.鄭州大學 實驗動物中心河南 鄭州450001; 2.鄭州大學 藥學院河南 鄭州450001)
【關鍵詞】LSD1;去甲基化;食管癌;胃癌;腸癌
傳統觀點認為,腫瘤是由基因突變引起的。但近年來的研究證實,表觀遺傳機制在腫瘤的病理變化中起著非常重要的作用。表觀遺傳機制表現異常會影響基因的轉錄。基因具有組織特異性,并廣泛參與細胞的生長、分化、凋亡、轉化以及腫瘤進程,對腫瘤的預防、臨床診斷和治療均具有重要意義[1]。食管癌、胃癌和腸癌是目前比較常見的消化道惡性腫瘤,其發病率和死亡率均居世界前列,嚴重影響了我國居民的健康。消化道腫瘤目前最主要的治療手段是手術、放療和化療,但預后較差。因此,積極尋找特定的生物標志物,建立科學有效的預防措施和診斷方法成為目前抗腫瘤領域的研究熱點。
一直以來,大家認為組蛋白賴氨酸甲基化只是一個穩定的組蛋白標記,不具有可逆性。直到2004年,第1個組蛋白賴氨酸去甲基化酶(lysine specific demethylase 1,LSD1)被發現[2],這個觀點才被改變。此后,日漸增多的研究證據表明LSD1表達失調在人類腫瘤形成過程中具有十分重要的作用,同時LSD1與腫瘤細胞的增殖關系密切。前期大量研究發現,LSD1過表達能促進前列腺癌、乳腺癌等腫瘤細胞的增殖、侵襲和轉移,而LSD1表達對消化道腫瘤的作用報道較為少見。本文就LSD1的結構與功能以及LSD1在食管癌、胃癌和腸癌中的最新研究進展作一綜述。
1LSD1的結構和功能
1.1LSD1的結構LSD1又稱為KDM1A、AOF2或BHC110,屬于FAD依賴型胺氧化酶家族成員,主要由3部分組成:N末端的SWIRM結構域,中間的Tower結構域和C末端的胺氧化酶結構域(amine oxidase like domain,AOL)。見圖1。其中,SWIRM結構域高度保守,是由85個氨基酸殘基組成的小α螺旋結構域。Tower結構域位于AOL兩葉之間,呈莖狀,由兩個很長的平行螺旋構成,這對于維持AOL結構域的空間構型非常重要[3]。研究人員證實,Tower結構域的缺失突變能使LSD1喪失活性[4]。AOL是LSD1的活性區域,被Tower結構域分成FAD結合結構域和催化活性中心兩個部分,而在三級結構中,這兩部分結構域仍然緊密結合在一起,形成完整的具有催化活性的結構域[5]。
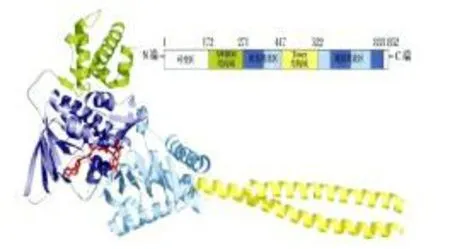
圖1 LSD1的結構圖
1.2LSD1的功能LSD1是一種核內黃素依賴的單胺氧化酶,其功能主要是對組蛋白和非組蛋白的去甲基化作用。腫瘤細胞中LSD1定位于細胞核內,調控基因轉錄的激活和抑制,被譽為細胞深處的基因“開關”,在胚胎發育和腫瘤發生過程中起著重要的作用[6]。LSD1能夠特異性脫去H3K4和H3K9位點上的單甲基和二甲基基團,調節基因的轉錄活性。研究發現,包含JmjC結構域的組蛋白去甲基化酶(JmjC domain-containing histone demethylase,JHDM)家族可以催化組蛋白三甲基(Me3)的去甲基化修飾[7]。在LSD1與底物反應時,FAD從甲基化的組蛋白賴氨酸得到質子,生成FADH2,甲基化的賴氨酸失去質子生成亞胺中間物,FADH2再由分子氧化生成FAD和H2O2[8]。LSD1催化氧化反應時需要FAD參與,且中間產物形成時需要1個質子,因此LSD1只能催化單甲基化和二甲基化的賴氨酸底物,使其去甲基化。
2LSD1與消化道腫瘤
2.1LSD1與食管癌食管癌是我國常見的惡性腫瘤,多為鱗狀細胞癌[9],其發病機制尚不清楚,DNA甲基化是目前研究最多的表觀遺傳學修飾方式。于妍妍等[10]采用免疫組化法研究發現,LSD1 在食管鱗癌組織中的表達顯著高于正常組織和食管癌癌前病變組織,且鱗癌組織中LSD1的表達陽性率與另兩種組織中LSD1的表達陽性率差異顯著。研究還發現,食管鱗癌組織中LSD1的表達程度與淋巴結轉移呈正相關,提示LSD1可能參與了食管鱗癌的淋巴結轉移。LSD1的表達與食管鱗癌的分化程度和浸潤深度無顯著相關,與食管鱗癌的增殖能力有關,進而影響患者的預后。LSD1高表達的食管鱗癌患者預后不良。林邵峰等[11]通過免疫組化法研究發現,與對應的正常食管黏膜相比,LSD1在食管鱗癌組織中高表達,且LSD1的高表達與食管鱗癌的不良預后相關,與淋巴結轉移、分期和分化等臨床因素無顯著相關。這與前面于妍妍等[10]的研究結果不一致,還需要做進一步的深入研究。沈瓊等[12]通過免疫組化法研究發現,LSD1在腫瘤細胞內定位在細胞核部位;LSD1在食管癌組織中高表達,在癌旁組織中低表達。LSD1高表達的比率與腫瘤大小、淋巴結是否轉移、腫瘤分期及預后明顯相關。LSD1高表達患者生存率明顯低于低表達患者。以上研究結果表明,LSD1 的高表達與食管鱗癌的惡性行為具有一定的相關性,提示LSD1可能參與了食管癌的增殖和轉移,并且可能與患者的預后有關。
2.2LSD1與胃癌胃癌是目前常見的胃腸道惡性腫瘤之一,盡管目前對化療藥物尤其是靶向藥物的研發進展很大,使得胃癌的化療效果得到提高,但是胃癌患者的預后還是不容樂觀。所以,進一步探索胃癌發生發展及轉移過程的分子生物學機制相當重要。盧太亮[13]利用免疫組化技術檢測80例胃癌組織及相應的癌旁組織中LSD1的表達,分析其與胃癌臨床病理特征及預后的關系。結果發現,LSD1在80例胃癌組織及癌旁組織中的陽性表達差異有統計學意義,LSD1在不同年齡、性別、腫瘤大小的胃癌組織中表達差異均無統計學意義,在不同組織病理學分級、TNM分期和淋巴結轉移的胃癌組織中表達差異有統計學意義。LSD1在低分化胃癌組織、較晚TNM分期及有淋巴結轉移的胃癌組織中表達明顯增高。LSD1在發生遠處轉移的胃癌中陽性表達率高達90%,但與無遠處轉移的胃癌組織比較,差異無統計學意義。陶厚權等[14]分別采用PCR和免疫組化技術檢測125例胃癌組織及正常胃黏膜中LSD1 mRNA的表達,以及其與胃癌臨床病理及預后的關系。結果發現與正常胃黏膜組織相比,胃癌組織中LSD1 mRNA顯著增高;LSD1蛋白在胃癌中高表達,在非腫瘤胃黏膜組織中僅為弱陽性表達;LSD1蛋白表達的高低與組織的分化程度、有無漿膜浸潤及淋巴結有無轉移有明顯的相關性。鄭一超[15]則首次報道了可抑制腫瘤細胞增殖和轉移的LSD1抑制劑,并揭示了胃癌細胞MGC-803及正常胃黏膜上皮細胞GES-1中TGF-β1對LSD1的調控機制。
2.3LSD1與結腸癌與食管癌和胃癌相同,結腸癌也是死亡率較高的惡性腫瘤之一。且超過30%的結腸癌患者術后會發生轉移。因此,研究結腸癌轉移的機制就顯得尤為重要。多個研究發現在結腸癌組織中LSD1高表達。Jie等[16-17]采用免疫組化法分析LSD1、E-鈣黏蛋白和N-鈣黏蛋白在108例結腸癌樣本中的表達,同時采用RT-PCR和Western blot方法檢測LSD1在5種結腸癌細胞株中的表達,并分析其對結腸癌細胞侵襲轉移的影響。病理切片結果顯示,LSD1在結腸癌細胞中的表達明顯高于正常細胞,LSD1與E-鈣黏蛋白在結腸癌中的表達呈負相關,與N-鈣黏蛋白的表達則不具有顯著相關性。體外細胞試驗表明,LSD1的表達與結腸癌細胞的侵襲性呈正相關。張元元等[18]通過免疫組化法檢測52例結腸癌組織中LSD1的表達水平,發現LSD1的表達率在結腸癌組織中明顯高于癌旁組織。且LSD1的表達與分化程度、淋巴結轉移及分期具有相關性,差異有統計學意義。另外,還發現下調LSD1的表達能夠顯著抑制結腸癌細胞的遷移,進一步表明LSD1表達與結腸癌細胞的轉移緊密相關。Huang等[19]聯合使用LSD1 抑制劑與DNA甲基轉移酶(DNA methyltransferase,DNMT)抑制劑對結腸癌細胞HCT116進行試驗,發現單獨使用LSD1劑抑制后抑癌基因SFRP會重新表達,二者聯合使用則能夠明顯誘導沉默的抑癌基因SFRP2重新表達,體外動物實驗也顯示聯合使用二者的抑制劑能夠明顯抑制腫瘤的生長。
3結語
作為第1個被確認的組蛋白去甲基化酶,LSD1在多種腫瘤中的發生和發展中起著重要的作用,LSD1在不同腫瘤中以不同的角色出現,在各種復雜的腫瘤相關分子通路上發揮組蛋白脫甲基化作用來調節腫瘤細胞的增殖、侵襲和轉移能力。大量研究證實,通過下調LSD1的表達可以顯著抑制腫瘤細胞的發展和轉移。LSD1作為抗腫瘤藥物作用的靶點已成為廣大科研工作者的研究熱點,而LSD1作為藥物靶點的適用性已經在相關藥物在多種腫瘤治療中的應用中得到了證實。這對于新藥研發具有重要的指導意義。希望通過對LSD1廣泛深入的研究為其在惡性腫瘤早期診斷、臨床治療及預后評估等方面提供更多的理論依據。
參考文獻
[1]鄭偉慧,凌志強,毛偉敏.食管癌表觀遺傳調控機制研究進展[J].國際消化病雜志,2013,33(1):12-16.
[2]Shi Y,Lan F,Matson C,et al.Histone demethylation mediated by the nuclear amine oxidase homolog LSD1[J].Cell,2004,119(7):941-953.
[3]Anand R,Marmorstein R.Structure and mechanism of lysine-specific demethylase enzymes[J].J Biol Chem,2007,282(49):35425-35429.
[4]Chen Y,Yang Y,Wang F,et al.Crystal structure of human histone lysine-specific demethylase 1 (LSD1)[J].Proc Natl Acad Sci USA,2006,103(38):13956-13961.
[5]阮建斌,臧建業.組蛋白去甲基化酶LSD1的結構和功能研究進展[J].中國科學技術大學學報,2008,38(8):930-940.
[6]許可珍,馬旭東.組蛋白賴氨酸特異性脫甲基酶(LSD1)在腫瘤治療中的應用進展[J].哈爾濱醫藥,2014,34(6):405-407.
[7]Metzger E,Wissmann M,Yin N,et al.LSD1 demethyylates repressive histone marks to promote androgen-receptor-dependent transeription[J].Nature,2005,437(7057):436-439.
[8]Suzuki T,Miyata N.Lysine demethylases inhibitors[J].J Med Chem,2011,54(24):8236-8250.
[9]Jemal A,Bray F,Center M M,et al.Global cancer statistics[J].CA Cancer J Clin,2011,61(2):69-90.
[10]于妍妍,雷增杰,郭嚴,等.賴氨酸特異性去甲基化酶1在食管鱗癌中的表達及其臨床意義[J].第三軍醫大學學報,2013,35(9):910-913.
[11]林邵峰,陳燕坪,朱偉峰,等.食管鱗癌組織LSD1表達與預后相關性分析[J].中華腫瘤防治雜志,2014,21(4):280-283.
[12]沈瓊,陳陸俊,徐斌,等.組蛋白賴氨酸去甲基化酶1在食管癌中的表達及其意義[J].中華實驗外科雜志,2015,32(5):1168-1170.
[13]盧太亮. LSD1在胃癌組織中的表達及意義[D].長沙:中南大學,2014.
[14]陶厚權,葉再元,王元宇,等. LSD1在胃癌中的表達及其意義[C].浙江省外科學學術年會論文匯編,2009.
[15]鄭一超.LSD1對胃癌發生發展的調控機制及小分子抑制劑干預研究[D].鄭州:鄭州大學,2014.
[16]Jie D,Zhongmin Z,Guoqing L,et al.Positive expression of LSD1 and negative expression of E-cadherin correlate with metastasis and poor prognosis of colon cancer[J].Dig dis sci,2013,58(6):1581-1589.
[17]丁杰,張忠民,徐開盛,等.LSD1, E-鈣黏蛋白及N-鈣黏蛋白的表達對結腸癌細胞侵襲轉移的影響[J].廣東醫學,2014,35(18):2831-2834.
[18]張元元,付曉,汪曉鶯.結腸癌組織LSD1表達對結腸癌LoVo細胞轉移潛能影響研究[J].中華腫瘤防治雜志,2014,21(18):1435-1439.
[19]Huang Y,Stewart T M,Wu Y,et al.Novel oligoamine analogues inhibit lysine-specific demethylase 1 and induce reexpression of epigenetically silenced genes[J]. Clin Cancer Res,2009,15(23):7217-7228.
(收稿日期:2015-10-13)
【中圖分類號】R 735
doi:10.3969/j.issn.1004-437X.2016.03.035
基金項目:河南省教育廳科學技術研究重點項目(13A350598);河南省自然科學基金研究項目(152300410160)。

