復方腸泰制劑對潰瘍性結腸炎小鼠腸黏膜屏障的保護作用
何麗娟,張軍東,安毛毛,姜遠英
?
·>臨床醫學·
復方腸泰制劑對潰瘍性結腸炎小鼠腸黏膜屏障的保護作用
何麗娟,張軍東,安毛毛,姜遠英
[摘要]目的觀察復方腸泰制劑在小鼠潰瘍性結腸炎中對腸黏膜屏障的保護作用,并探討其作用機制。方法建立葡聚糖硫酸鈉誘導小鼠實驗性潰瘍性結腸炎模型,實驗分為空白組、模型組、不同劑量治療組(4.3 g/kg與17.1 g/kg)、美沙拉嗪對照組和硫唑嘌呤對照組。造模7 d內,觀察記錄各組小鼠體質量和疾病活動指數變化;采用透射電鏡觀察各組小鼠結腸的超微結構;HE染色觀察各組小鼠炎癥; ELISA法測定各組小鼠結腸組織TNF-α、IL-6、IFN-γ、IL-10;蛋白質印跡方法檢測各組小鼠結腸組織中ZO-1、Occludin和Claudin-1蛋白的表達。結果模型組小鼠體質量、DAI和結腸長度與空白對照組比較,差異均有統計學意義(P<0.05);結腸組織中TNF-α、IL-6和IFN-γ水平顯著降低,差異有統計學意義(P<0.05);組織病理顯示炎性細胞明顯浸潤,ZO-1、Occludin和Claudin-1蛋白的表達顯著下降,差異有統計學意義(P<0.05);高劑量復方腸泰組與空白對照組比較,差異均無統計學意義(P>0.05)。結論高劑量復方腸泰制劑對小鼠腸黏膜屏障功能具有一定的保護作用,其機制可能與腸上皮緊密連接蛋白表達升高以及腸道免疫功能調節有關。
[關鍵詞]潰瘍性結腸炎;緊密連接蛋白;腸屏障功能
潰瘍性結腸炎(ulcerative colitis,UC)是一種自身免疫性疾病,病因不明,發病機制至今也沒有確定,一般認為是環境因素、基因和免疫因素三者相互作用的結果[1]。在臨床上,這種疾病發病率逐年增高,治療難度較大,且反復發作,較難有效控制。國內外近期研究普遍認為其發作與腸道屏障功能密切相關[2],本研究采用更接近人類UC病理及免疫特點的葡聚糖硫酸鈉(dextran sulfate sodium,DSS)誘導C57小鼠建立實驗性UC模型,探討UC發病的可能機制。現報道如下。
1材料與方法
1.1材料
1.1.1實驗動物清潔級6~8級雌性C57BL/6小鼠共60只,購自上海斯萊克實驗動物有限責任公司。采用數字表法隨機分為空白對照組(Control)、模型組(Model)、低劑量腸泰組(4.3 g/kg,LCT)、高劑量腸泰組(17.1 g/kg,HCT)、美沙拉嗪對照組(Mesalazine)和硫唑嘌呤對照組(Azathioprine)共6組。實驗動物飼養于上海同濟大學醫學院清潔級動物房。
1.1.2藥物及復方腸泰制備黃柏(CortexPhellodendri)50 g,地榆(radixsanguisorbae)、地錦草(EuphorbiahumifusaWilld.)和辣蓼(PolygonumflaccidumMeissn.)各37.5 g(購自上海同仁堂藥店)。藥物制備方法:取黃柏粗粉,加7倍量的70%乙醇,提取2次,每次2 h,濾過,合并濾液,回收乙醇,備用。藥渣與其余3味,加15倍的水煎煮2次,每次1.5 h,合并濾液,濃縮至相對密度為1.00~1.05,與黃柏濃縮液合并,繼續濃縮,最終得到的濃縮液分裝后凍存于-80 ℃冰箱備用。
1.1.3實驗試劑DSS(MP公司)、莎爾福美沙拉嗪腸溶片(Dr. Falk Pharma GmbH公司)、硫唑嘌呤片(上海信誼藥廠有限公司)、羧甲基纖維素鈉(國藥集團化學試劑有限公司)、甲醛(國藥集團化學試劑有限公司)、水合氯醛(美侖生物)、RIPA裂解液(碧云天生物技術研究所)、ELISA試劑盒(eBioscience公司)、Western blot 抗體抗(Cell Signaling Technology公司)、二抗(北京鼎國生物技術公司)。
1.1.4主要儀器旋轉蒸發儀(上海亞榮生化儀器廠)、電子天平(梅特勒-托利多公司)、酶標儀(Thermo scientific公司)、Haier立式超低溫保存箱(青島海爾特種電器有限公司)、冷凍高速離心機與轉膜儀(Bio-rad公司)、化學發光成像系統(GE公司)、透射電鏡(日立H-800公司)。
1.2方法
1.2.1模型的建立和評價60只C57BL/6小鼠分完組后進入清潔級動物房,正常飼養3 d后造模,除空白對照組自由飲用滅菌水外,其余各組均自由飲用配置完畢的1.5% DSS水溶液共7 d。每天在固定時間段對小鼠進行灌胃等藥物干預(各組給藥劑量為:美沙拉嗪500 mg/kg,硫唑嘌呤2 mg/kg,低劑量復方腸泰4.3 g/kg,高劑量復方腸泰17.1 g/kg,模型組和空白組以生理鹽水代替),藥物均以0.5%羧甲基纖維素鈉(sodium carboxymethylcellulose,CMC)溶液助溶,同時每天按時稱質量記錄,仔細觀察各組小鼠活動形態。每天換一次墊料,觀察糞便形態并測隱血評分。7 d后取材,每組取1只留作透射電鏡用,剩余所有小鼠麻醉后取出結腸段,迅速量取長度并選取各組代表性的結腸段作直觀對照圖。每組各3只小鼠的整段結腸凍存于-80 ℃冰箱留作檢測細胞因子;剩余3只留作檢測蛋白使用,剪取一段結腸組織后均用PBS緩沖液沖洗后凍存于-80 ℃冰箱。
1.2.2小鼠結腸組織HE染色檢測各組炎癥細胞水平差異在距離小鼠肛門1 cm處剪取一段長約2 cm的結腸組織,縱向剖開,并用預冷的PBS緩沖液沖洗腸道內容物、組織液及血液,將洗凈后的結腸組織浸入4%多聚甲醛中固定,常規石蠟包埋,切片后進行蘇木精-伊紅(HE)染色,脫水透明后樹膠封固,光鏡下觀察。
1.2.3透射電鏡(TEM)觀察各組結腸組織緊密連接每組各1只小鼠進行麻醉,從麻醉后的小鼠體內取出一小段結腸末端組織,用4 ℃預冷的PBS沖洗內容物和組織液,迅速使用預冷的手術刀片取下一小片所需的組織,立即放入4 ℃存放的2.5%戊二醛固定液中固定2 h后漂洗,并用1%鋨酸后固定,乙醇梯度脫水并樹脂包埋,過夜固化,切片后枸櫞酸鉛染色,水洗干燥后電鏡觀察。
1.2.4Western blot檢測ZO-1,Occludin,Claudin-1蛋白的表達從-80 ℃取出不同組別間各3只小鼠的一段結腸組織置于研缽中,液氮處理后使用研磨棒將其徹底碾成粉末,將這些粉末混勻后收集到EP管中,加入適量RIPA裂解液,混勻后置于4 ℃高速震蕩20 min后,轉入高速冷凍離心機中4 ℃離心10 min后取上清,95 ℃蛋白變性10 min后分裝,存入-80 ℃冰箱備用。將制備好的蛋白液體進行SDS-PAGE電泳,半干轉將蛋白從凝膠上轉至PVDF膜上,5%脫脂牛奶封閉,一抗孵育過夜,PBST沖洗后二抗孵育,最后在化學發光系統下進行顯影。
1.2.5ELISA檢測小鼠結腸組織中細胞因子水平截取小鼠整段結腸,置于勻漿器中研磨成漿液,4 ℃離心后取上清,分裝后放入-80 ℃備用。使用相應的ELISA試劑盒按照規定檢測TNF-α、IL-6、IFN-γ、IL-10這4個細胞因子水平。
1.3統計學處理采用GraphPad Prism 5.0進行數據處理并統計學分析,2組數據間的比較用t檢驗,P<0.05表示差異有統計學意義。
2結果
2.1復方腸泰制劑抑制小鼠實驗性潰瘍性結腸炎生成小鼠經DSS造模后出現體質量明顯下降、少動、便血等癥狀,造模完成后,模型組小鼠結腸明顯縮短并且整體充血紅腫。和空白對照組相比,HCT組小鼠的結腸長度和體質量差異均無統計學意義(P>0.05)。該結果提示高劑量復方腸泰制劑對小鼠結腸炎的發生具有明顯抑制作用,見圖1。

注:A為各組小鼠在整個實驗周期內的體質量相對變化量的比較;B為各組小鼠在整個實驗周期中的疾病活動指數評分比較;C為各組小鼠的結腸長度比較;D為各組小鼠代表性結腸外觀比較;Control為空白對照組,Model為模型組,LCT為低劑量組,HCT為高劑量組,Mesalazine為美沙拉嗪對照組,Azathioprine為硫唑嘌呤對照組圖1 復方腸泰制劑對各組小鼠體質量、疾病活動指數及長度外觀的影響
2.2光鏡下小鼠結腸組織病理變化表現DSS誘導模型組小鼠結腸組織黏膜受損,潰瘍累及黏膜全層,黏膜下層水腫,炎細胞浸潤,而HCT組由于藥物干預,結果為較少形成潰瘍,甚至沒有出現炎癥,見圖2。
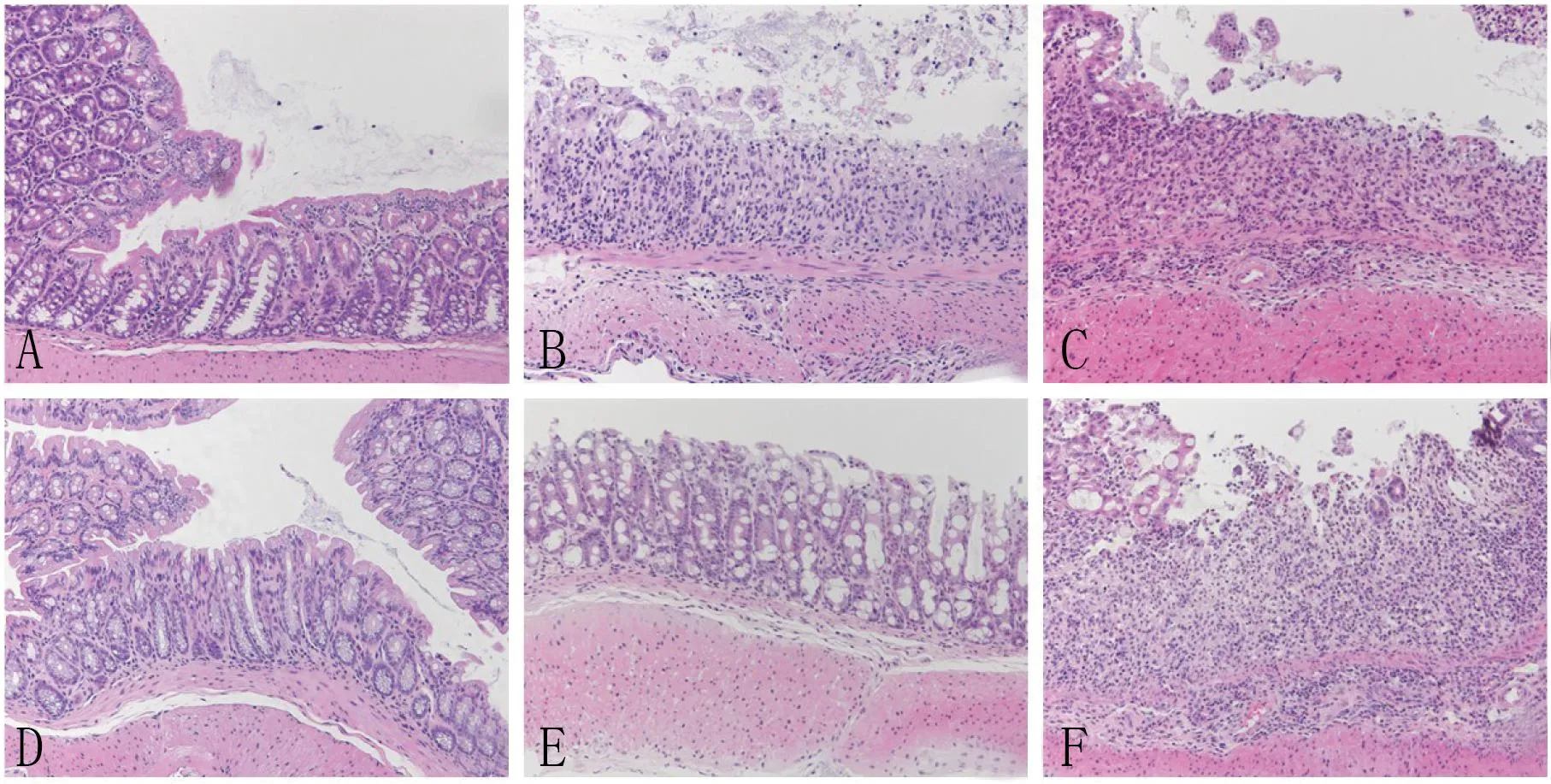
注:A為空白對照組; B為模型組;C為低劑量腸泰組;D為高劑量腸泰組; E為美沙拉嗪對照組;F為硫唑嘌呤對照組圖2 各組小鼠結腸遠端的組織病理結果(HE染色×200)
2.3各組小鼠結腸組織超微結構的觀測結果與空白對照組相比,模型組小鼠結腸段超微結構可見部分微絨毛萎縮脫落,排列稀疏,緊密連接處稍有開放,細胞間隙擴大。高劑量組結腸微絨毛排列整齊,緊密連接處結構清晰無損壞,與空白對照組沒有可見差異。該結果提示高劑量復方腸泰對小鼠腸黏膜屏障功能具有保護作用,見圖3。
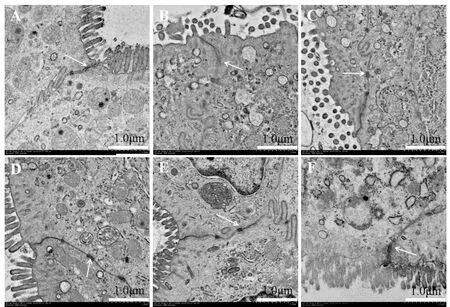
注:A為空白對照組; B為模型組;C為低劑量腸泰組;D為高劑量腸泰組; E為美沙拉嗪對照組;F為硫唑嘌呤對照組圖3 各組小鼠結腸組織超微結構觀察結果(TEM×5 000)
2.4緊密連接蛋白ZO-1,Occludin,Claudin-1的表達水平通過Western blot檢測,可以得出結果,即DSS造成模型組小鼠腸道組織緊密連接蛋白受到較大破壞,緊密連接蛋白水平明顯降低;相比空白對照組小鼠腸道組織緊密連接蛋白的高表達,HCT組小鼠無明顯可見差異,見圖4。
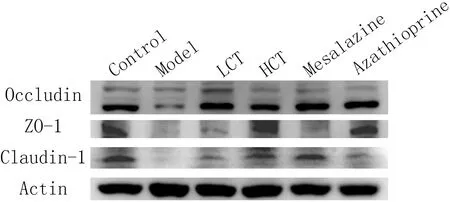
注:Control為空白對照組,Model為模型組,LCT為低劑量組,HCT為高劑量組,Mesalazine為美沙拉嗪對照組,Azathioprine為硫唑嘌呤對照組圖4 各組小鼠結腸組織中ZO-1,Occludin,Claudin-1水平
2.5小鼠結腸組織中TNF-α、IL-6、IFN-γ、IL-10的表達水平DSS誘發UC小鼠后,模型組結腸勻漿液中促炎細胞因子TNF-α、IL-6、IFN-γ水平明顯升高,與空白對照組相比差異有統計學意義(P<0.05)。HCT組經過藥物干預后,這些細胞因子水平與模型組相比差異無統計學意義(P>0.05)。而對于抑炎細胞因子IL-10的水平,模型組和HCT組相比表現出升高趨勢,但差異無統計學意義(P>0.05),見圖5。
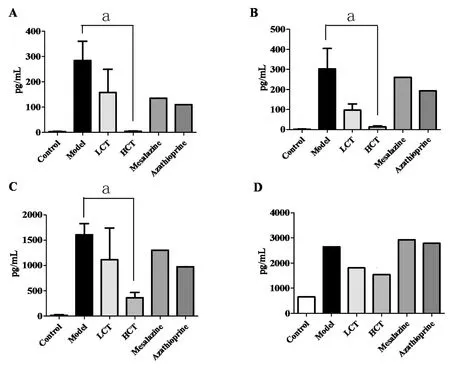
注:Control為空白對照組,Model為模型組,LCT為低劑量組,HCT為高劑量組,Mesalazine為美沙拉嗪對照組,Azathioprine為硫唑嘌呤對照組;A為TNF-α;B為IL-6;C為IFN-γ;D為IL-10。與空白對照組比較aP<0.05圖5 各組小鼠結腸組織勻漿液中細胞因子檢測水平
3討論
正常情況下,腸道除具有消化吸收功能外,在預防腸源性感染方面也起著非常重要的作用,這主要是基于完整的腸道黏膜屏障功能。其可以選擇性的轉運離子、營養成分及其他有用物質,且有效阻止腸腔內細菌、毒素及炎性介質等的旁細胞滲透轉運,維持機體的生理平衡[3-5]。研究認為UC易感基因和環境因素誘導腸黏膜屏障損壞,一旦腸黏膜屏障受損,黏膜下層暴露在大量抗原中,機體激活天然免疫反應如升高促炎細胞因子 TNF-α、IFN-γ等,這些炎性因子可明顯損傷腸道屏障功能[6-7],使腸黏膜通透性增加,腸道內寄居的大量微生物及其代謝產物可引發或進一步惡化腸道炎癥。無論從實驗研究還是從臨床病例來看,在各種腸道疾病中都能觀察到腸屏障功能受損,腸道通透性增加[8-9]。因此可以判斷腸道感染及炎癥與UC發病過程密切相關。
UC已被世界衛生組織評為世界難治性疾病之一,并發癥多,常易復發。目前臨床治療藥物主要為氨基水楊酸類、糖皮質激素類和免疫抑制劑類,但是這些藥物往往治標不治本[10]。中藥安全性高,不良反應少,并以其多靶點多組分的特點在多病因的復雜慢性疾病中具有西藥無法比擬的優勢[11]。復方腸泰制劑的治療作用前期已有研究證實[12],也已經進入臨床研究階段。該復方制劑由黃柏、地榆、地錦草、辣蓼共4味傳統中藥組成,黃柏性寒味苦,能清腸腑之熱,燥腸中之濕,為君藥;地榆味苦、酸,性微寒,清熱涼血,瀉火斂瘡;地錦草性平味辛,清熱解毒止瀉,兩者為臣藥;辣蓼味辛性溫,溫中化濕,既可加強燥濕止瀉之力,又可制約黃柏過于苦寒之弊,為佐使藥。四藥合用,具有清熱燥濕、涼血解毒之效。現代醫學研究表明,黃柏中的多種生物堿成分能夠通過下調促炎細胞因子及其他炎癥介質表達、抑制T細胞過度增殖活化等發揮抗炎、免疫調節作用[13-14];地榆、地錦草、辣蓼也分別具有抗病原微生物、抗炎、免疫調節作用[15-17]。
本實驗采用中藥復方腸泰制劑對UC小鼠發病進程進行有效控制,通過7 d一個完整的造模周期,觀察發現HCT組的動物在體質量及疾病活動指數等指標上均強于模型組,證實復方腸泰制劑對UC小鼠的保護作用;通過常規HE染色觀察到動物體內結腸組織的炎癥狀況,HCT組沒有出現符合炎癥的病理組織學改變,說明腸泰對炎癥形成具有一定的抑制作用。同時從超微結構和蛋白免疫印跡發現HCT組緊密連接蛋白的水平沒有出現大幅度改變,進一步說明復方腸泰制劑對UC小鼠腸黏膜屏障的修復能力。最后通過ELISA檢測到細胞因子TNF-α、IFN-γ和IL-6的變化水平,從側面反映復方腸泰制劑對UC發病的減輕和維護作用。
綜上,本研究結果顯示復方腸泰制劑對UC可有效預防,其機制可能通過修復受損的腸道屏障功能來抑制炎癥,緩解炎癥進程,啟示可以從維護腸道黏膜屏障方面來深入研究UC發病機理。了解腸黏膜屏障在UC發病過程中的病理生理作用有助于發現新的治療方法,也可為臨床治療UC提供參考。
[參考文獻]
[1]Basso PJ, Fonseca MT, Bonfá G, et al. Association among genetic predisposition, gut microbiota, and host immune response in the etiopathogenesis of inflammatory bowel disease[J]. Braz J Med Biol Res, 2014, 47(9): 727-737.DOI:10.1590/1414-432.x2014932.
[2]Camilleri M, Madsen K, Spiller R, et al. Intestinal barrier function in health and gastrointestinal disease[J]. Neurogastroenterol Motil, 2012, 24(6): 503-12.DOI:10.1111/j.1365-2982.2012.01921.x.
[3]Sanchez de Medina F, Ortega-Gonzalez M, Gonzalez-Perez R, et al. Host-microbe interactions: the difficult yet peaceful coexistence of the microbiota and the intestinal mucosa[J]. Br J Nutr, 2013, 109(suppl 2): S12-S20.DOI:10.1017/s0007114512004035.
[4]Sánchez de Medina F, Romero-Calvo I, Mascaraque C, et al. Intestinal inflammation and mucosal barrier function[J]. Inflamm Bowel Dis, 2014, 20(12): 2394-2404.DOI:10.1097/MIB.0000000000000204.
[5]Knights D, Lassen KG, Xavier RJ. Advances in inflammatory bowel disease pathogenesis: linking host genetics and the microbiome [J]. Gut, 2013, 62(10): 1505-1510.DOI:10.1136/gutjnl-2012-303954.
[6]Alex P, Zachos NC, Nguyen T, et al. Distinct cytokine patterns identified from multiplex profiles of murine DSS and TNBS-induced colitis[J]. Inflamm Bowel Dis, 2009, 15(3): 341-352.DOI:10.1002/i6d.20753.
[7]Lee SH. Intestinal permeability regulation by tight junction: implication on inflammatory bowel diseases[J]. Intest Res, 2015, 13(1): 11-18.DOI:10.5217/ir.2015.13.1.11.
[8]Zhao H, Zhang H, Wu H, et al. Protective role of 1,25(OH)2 vitamin D3 in the mucosal injury and epithelial barrier disruption in DSS-induced acute colitis in mice[J]. BMC Gastroenterol, 2012, 12: 57.DOI:10.1186/1471-230x-12-57.
[9]Dorofeyev AE, Vasilenko IV, Rassokhina OA, et al. Mucosal barrier in ulcerative colitis and Crohn's disease[J]. Gastroenterol Res Pract, 2013, 2013: 431231.DOI:10.1155/2013/431231.
[10] de Boer NK, van Bodegraven AA, Jharap B, et al. Drug Insight: pharmacology and toxicity of thiopurine therapy in patients with IBD[J]. Nat Clin Pract Gastroenterol Hepatol, 2007, 4(12): 686-694.DOI:10.1038/ncpgasthep1000.
[11] Salaga M1, Zatorski H, Sobczak M, et al. Chinese herbal medicines in the treatment of IBD and colorectal cancer: a review[J]. Curr Treat Options Oncol, 2014, 15(3): 405-420.DOI:10.1007/s11864-014-0288-2.
[12] Liu BG1, Jia XM, Cao YY, et al. Changtai granule, a traditional Chinese drug, protects hapten-induced colitis by attenuating inflammatory and immune dysfunctions[J]. J Ethnopharmacol, 2008, 115(1): 1-8.DOI:10.1016/j.jep.2007.08.045.
[13] Kawano M, Takagi R, Kaneko A, et al. Berberine is a dopamine D1- and D2-like receptor antagonist and ameliorates experimentally induced colitis by suppressing innate and adaptive immune responses[J]. J Neuroimmunol, 2015, 289: 43-55.DOI:10.1016/j.jneuroim.
[14] Yan F, Wang L, Shi Y, et al. Berberine promotes recovery of colitis and inhibits inflammatory responses in colonic macrophages and epithelial cells in DSS-treated mice[J]. Am J Physiol Gastrointest Liver Physiol, 2012, 302(5): G504-514.DOI:10.1152/ajpgi.00312.2011.
[15] Jo S, Ryu J, Kim H, et al. Anti-inflammatory effects of Sanguisorbae Radix on contact dermatitis induced by dinitrofluorobenzene in mice[J]. Chin J Integr Med, 2015, 11(1):37-39.DOI:10.1007/s11655-015-2148-8.
[16] Luyen BT, Tai BH, Thao NP, et al. Anti-inflammatory components of Euphorbia humifusa Willd[J]. Bioorg Med Chem Lett, 2014, 24(8): 1895-1900.DOI:10.1016/j.6mll.2014.03.014.
[17] Mazid MA, Datta BK, Nahar L, et al. Analgesic and diuretic properties of alpha-santalone from Polygonum flaccidum[J]. Phytother Res. 2010, 24(7): 1084-1087.DOI:10.1002/ptr.3053.
(本文編輯:張陣陣)
Protective effect of compound Changtai on the intestinal mucosal barrier in the treatment of ulcerative colitis in rats
He Lijuan, Zhang Jundong, An Maomao, Jiang Yuanying
(New Drug Research and Development Center, School of Pharmacy, Second Military Medical University,Shanghai 200433, China)
[Abstract]ObjectiveTo verify the protective effect of compound Changtai on the intestinal mucosal barrier in the treatment of ulcerative colitis (UC), and also to explore the possible mechanism involved.Methods The animal model of ulcerative colitis induced by dextran sodium sulfate (DSS) was established as a first step. The experimental animals were divided into 6 groups, i.e. the blank control group, the model group, the compound Changtai treatment groups with two different dosages (4.3 g/kg, 17.1g/kg), the mesalazine and azathioprine control groups. Seven days after the development of the model, changes in body weight and disease activity index (DAI) were observed and recorded. Colon ultrastructures in the animals of various groups were closely observed by transmission electron microscopy; inflammation in the animals of various groups was observed by HE staining; the levels of TNF-α, IL-6, IFN-γ and IL-10 in the colon of various animal groups were detected by ELISA; and the expression levels of ZO-1, Occludin and Claudin-1 in the colon of various groups were detected by Western blot.ResultsSignificant differences could be seen in the body weight, DAI, colon length in the animals of the model group, as compared with those of the control group(P<0.05). The levels of TNF-α,IL-6 and IFN-γ in the colon were significantly decreased(P<0.05), and the expression levels of Occludin, Claudin-1 and ZO-1 were also significantly decrease(P<0.05). Histopathological detection indicated that inflammatory infiltration was evident. Transmission electron microscopy detection showed a damaged opening dot in the tight junction protein in the colon of the model group. No significant differences could be noted, when comparisons were made between the high dosage Changtai group and the blank control group(P<0.05).ConclusionThe high dosage compound Changtai seemed to have certain protective effect on the intestinal mucosal barrier, the possible mechanism involved might be related with the increased expression level of the tight junction protein and the regulation of intestinal immune function.
[Key words]Ulcerative colitis; Tight junction protein; Intestinal barrier function
(收稿日期:2016-02-02)
[中圖分類號]R735.2
[文獻標識碼]A[DOI]10.3969/j.issn.1009-0754.2016.02.007
[通信作者]姜遠英,電子信箱:13761571578@163.com
[基金項目]國家自然科學基金項目(81274164)
·論著·
[作者單位]200433上海,第二軍醫大學藥學院新藥研究中心(何麗娟、姜遠英);同濟大學附屬第十人民醫院(張軍東);同濟大學醫學院(安毛毛)

