不同檢測系統C反應蛋白測定結果可比性研究
盧錦沛
(珠海市平沙醫院檢驗科,廣東珠海 519055)
?
·臨床研究·
不同檢測系統C反應蛋白測定結果可比性研究
盧錦沛
(珠海市平沙醫院檢驗科,廣東珠海 519055)
摘要:目的探討3種不同檢測系統對C反應蛋白測定結果的可比性。方法對60例患者分別采用艾可美(ichroma)免疫熒光分析儀,邁瑞BS-400全自動生化儀和德靈BN Prospec 特定蛋白儀進行C-反應蛋白檢測,對測定結果比對分析。結果兩個實驗系統與比較系統間呈顯著的正相關(r1=0.994 0,r2=0.992 2),測定均值無明顯偏差,兩種實驗儀器的CRP測定值的系統誤差均在可接受范圍內。結論3種不同檢測系統檢測的CRP結果具有較好的相關性和可比性,快速測定儀測定C反應蛋白值得臨床推廣應用。
關鍵詞:快速檢測;C反應蛋白;對比研究
C-反應蛋白(CRP)是由肝臟合成的血清β球蛋白,作為一種重要的急性時相反應蛋白,當機體出現炎癥時,其值會迅速升高,因此CRP可作為細菌或病毒感染的一個首選指標,良好的應用于感染及炎癥的診斷鑒別和抗菌藥物療效的觀察等[1]。故CRP的檢測方法也越來越引起重視,快速、準確、定量的檢測CRP值可有效提高診斷效率、減少疾病的發生等,更好地滿足臨床的需求。在此基礎上快速CRP分析儀應運而生,并且逐漸被廣泛應用于臨床實驗室。不同檢測系統間可能存在一定的差異,為了探討快速CPR分析結果的可靠性,本文將C-反應蛋白在艾可美(ichroma)免疫熒光分析儀、邁瑞BS-400全自動生化儀上的檢測結果與在德靈BN Prospec 特定蛋白儀上的測定結果進行相關性分析、偏差估計和系統誤差估計等,對結果進行比對分析。現將報道如下。
1資料與方法
1.1一般資料以2015年3月20~30日本院收治的需行CRP檢測的60例患者為研究對象,每天測試12例患者,連續5 d,采集靜脈血后需及時測定。
1.2儀器與試劑ichroma免疫熒光分析儀,試劑為儀器的配套試劑,檢測時均使用同一批號試劑;邁瑞BS-400全自動生化儀,試劑為儀器的配套試劑,檢測時均使用同一批號;德靈BN Prospec 特定蛋白儀,試劑為其原裝配套試劑,檢測時均使用同一批號。
1.3方法按照美國臨床和實驗室標準化協會(CLSI)EP9-A2文件操作要求,每例標本分別在3臺儀器上平行測定兩次,檢測順序為:第1次檢測按標本隨機編號1、2、3、4、5、6、7、8、9、10、11、12的順序,第2次檢測按編號12、11、10、9、8、7、6、5、4、3、2、1順序進行檢測,測定需在兩小時內完成。因BN Prospec全自動特定蛋白分析儀精密度評價試驗較好[2],故以其作為目標檢測系統比較方法(X),ichroma免疫熒光分析儀與邁瑞BS-400全自動生化儀為試驗方法(Y1、Y2),進行方法間CRP的比較試驗。具體操作嚴格按照各說明書進行。
1.4統計學處理剔除明顯存在人為操作誤差的檢測結果,按照EP9-A2文件對3種結果進行方法內和方法間離群值檢驗,保留符合要求的結果;采用Microsoft Office EXCEL 2007進行線性相關性回歸分析、偏差估計,并對系統誤差(SE)進行估計。
2結果
2.1直線回歸方程以BN Prospec全自動特定蛋白分析儀作為目標檢測系統,ichroma免疫熒光分析儀、邁瑞BS-400全自動生化儀與其進行相關與回歸分析,得到回歸方程分別為Y1=1.001 3X+0.824 3,r=0.994 0;Y2=0.956 6X-0.941 7;r=0.992 2。各檢測系統間的r均不小于0.975,說明回歸的斜率和截距可靠。均值散點圖見圖1~2。

圖1 BN Prospec與ichroma免疫熒光分析儀

圖2 BN Prospec與邁瑞BS-400全自動生化儀
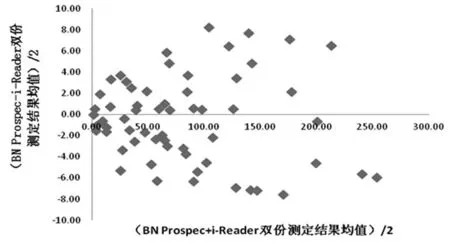
圖3 BN Prospec與ichroma免疫熒光分析儀
2.2雙份測定均值偏差以比較方法測定結果均值結果為X軸,實驗方法測定結果均值為Y軸,繪制CRP均值散點圖,以比較方法測定結果均值與實驗方法測定結果均值的和的一半為X軸,以比較方法測定結果均值與實驗方法測定結果均值的差的絕對值的一半為Y軸,繪制CRP均值偏倚散散點圖[3]。從圖中可以看出,ichroma免疫熒光分析儀、邁瑞BS-400全自動生化儀與BN Prospec全自動特定蛋白分析儀測定結果比較,數據較均勻分布于X軸兩側,無明顯偏差。均值偏差散點圖見圖3~4。
2.3系統誤差SE估計以BN Prospec作為目標檢測系統,將CRP的不同醫學決定水平XC代入各自相應的回歸方程,以此來判斷各檢測系統的臨床可接受性能,由于美國臨床實驗室修正法案(CLIA′88)沒有明確規定CRP 的允許誤差[4],本文根據臨床的實踐經驗暫定為SE%≤10%為臨床可接受標準,以醫學決定水平Xc處的SE來判斷系統間誤差是否可接受。分析結果見表1[用Xc代表不同的醫學決定水平(mg/L)],從表格中可以看出,ichroma免疫熒光分析儀、邁瑞BS-400全自動生化儀的CRP測定值系統誤差均在臨床可接受范圍內。
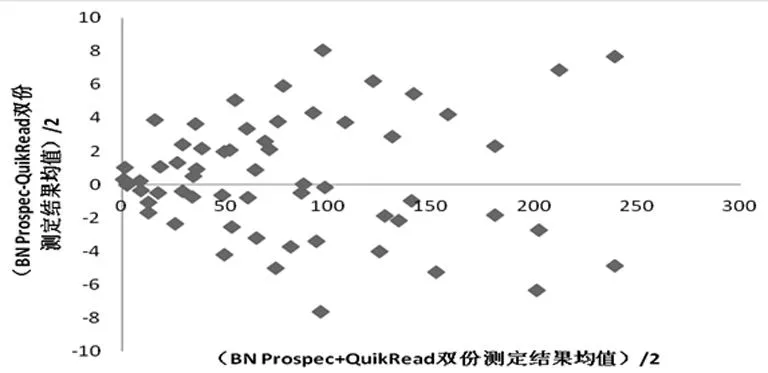
圖4 BN Prospec與邁瑞BS-400全自動生化儀

儀器相關系數(r)回歸方程Xc(mg/L)SE(%)可接受標準(%)可接受評判ichroma免疫熒光分析儀0.9940Y1=1.0013X+0.8243108.3710接受501.7810接受1000.9510接受邁瑞BS-400全自動生化儀0.9922Y2=0.9566X-0.9417104.7110接受501.4510接受1001.0410接受
3討論
CRP是1930年由Tillett和Francis從肺炎患者血清中發現的,后被Macleod和Avery證實為一種急性感染時出現的蛋白質[5]。CRP由5個完全相同的非糖基化的亞單位非共價聯接,每個亞單位有206個氨基酸殘基組成。CRP主要由肝細胞在L-6、L-1β、TNF-α刺激下合成的。CRP的正常合成率是1~10 mg/d,半衰期為19 h,不耐熱[6]。其檢測方法大致可分為三類:免疫沉淀試驗、免疫濁度法和乳膠凝集試驗[7]。
隨著檢驗醫學的快速發展,為了提高檢測效,快速CRP檢測儀相繼產生,與常規儀器相比,具有操作簡單、檢測迅速、小巧靈敏等優點,尤其適合門、急診檢驗等。在同一實驗室,可用不同檢測系統對相同項目進行定期檢測和比對,根據比對結果做出相應的調整,以確保不同檢測系統間檢測結果的一致性。本文對實驗室快速CRP檢測系統間測定同一項目的結果的可比性進行了研究,參照CLSI EP9-A2文件對ichroma免疫熒光分析儀、邁瑞BS-400全自動生化儀與BN Prospec全自動特定蛋白分析儀3種不同的檢測系統CRP測定進行了相關回歸分析、偏差估計和系統誤差評估。數據結果顯示:ichroma免疫熒光分析儀、邁瑞BS-400全自動生化儀與BN Prospec全自動特定蛋白分析儀的相關性均較好,且ichroma免疫熒光分析儀CRP測定結果的相關性稍高于邁瑞BS-400全自動生化儀;ichroma免疫熒光分析儀與邁瑞BS-400全自動生化儀的CRP測定值系統誤差均在臨床可接受范圍內,且隨著CRP濃度升高,ichroma免疫熒光分析儀、邁瑞BS-400全自動生化儀的 相對偏差逐漸減小;從測定均值偏差可以看出,ichroma免疫熒光分析儀、邁瑞BS-400全自動生化儀與BN Prospec全自動特定蛋白分析儀比較,數據較均勻地分布于X軸的兩側,且當CRP<150 mg/L時,偏差相對較小,當CRP>150 mg/L時,偏差相對較大。結果表明,3種快速CRP分析儀的測量值均具有良好的可比性。
研究發現,CRP與多種疾病密切相關,急性炎癥時CRP的合成率比正常值高出幾百甚至幾千倍[8];CRP是發展為2型糖尿病的重要預測因素[9],CRP水平每增加1個標準差,發展成2型糖尿病的危險性1.55倍;高血壓患者CRP水平明顯高于健康人;急性腦血管疾病發病早期血清CRP水平明顯升高;CRP還與風濕病的診斷、心血管事件的發生等有一定的關系[10]。因此,ichroma免疫熒光分析儀、邁瑞BS-400全自動生化儀等快速CRP檢測系統的出現可準確地了解患者的病情,有助于臨床醫生為患者作出快速準確診斷,并進行有效合理的治療,更好地服務患者。
參考文獻
[1]張秀明,莊俊華,徐寧,等.不同檢測系統血清酶測定結果的偏倚評估與可比性研究[J].中華檢驗醫學雜志,2006,29(4):346-349.
[2]The National Committee for Clinical Laboratory Standards.EP9-A2 Method comparison and bias estimation using patient samples[S].Wayne,PA,USA:NCCLS,2002.
[3]Cai J,Yu C,Liu Y,et al.Generation of homogeneous PDX1(+) pancreatic progenitors from human ES cell-derived endoderm cells[J].J Mol Cell Biol,2010,2(1):50-60.
[4]林莉,黃憲章,莊俊華,等.不同檢測系統測定總膽汁酸的比對試驗[J].國際檢驗醫學雜志,2006,27(6):484-486.
[5]稅國順,何代莉,楊曉紅.C-反應蛋白的測定及臨床應用[J].現代醫藥衛生,2005,21(11):1365-1367.
[6]金盾,胡大琴,金新政.國內外臨床信息系統對比研究[J].中國衛生質量管理,2011,18(3):7-10.
[7]Ngom B,Guo Y,Wang X,et al.Development and application of lateral flow test strip technology for detection of infectious agents and chemical contaminants:a review[J].Anal Bioanal Chem,2010,397(3):1113-1135.
[8]張鶯鶯,陶青松,浦春,等.不同檢測系統15項常規生化檢測結果的比對和偏倚評估[J].檢驗醫學與臨床,2011,8(3):257-259.
[9]竺澎波,許婉華,陳劍峰,等.自建生化檢測系統檢測結果溯源性分析[J].現代醫院,2008,8(12):46-47.
[10]李萍,劉小娟,徐克和,等.利用Westgard標準決定圖判定測定方法性能[J].臨床檢驗雜志,2006,24(1):69-70.
(收稿日期:2016-01-08)
DOI:10.3969/j.issn.1673-4130.2016.08.040
文獻標識碼:A
文章編號:1673-4130(2016)08-1110-02

