六價鉻在磚紅壤中淋溶特征的模擬研究
鐘來元,鐘燕彬,楊杰文(廣東海洋大學農學院資源與環境系,廣東湛江524088)
?
六價鉻在磚紅壤中淋溶特征的模擬研究
鐘來元,鐘燕彬,楊杰文*
(廣東海洋大學農學院資源與環境系,廣東湛江524088)
摘要:通過室內土柱淋溶實驗,研究了六價鉻在磚紅壤中淋溶特征以及有機肥和陪伴離子[Cu(Ⅱ)、磷酸根]對該過程的影響,并探討了模擬酸雨條件下,土壤中六價鉻溶出特征。結果表明:高氧化鐵含量磚紅壤對C(rⅥ)有很強吸附能力,當C(rⅥ)輸入量小于240 mg·kg-1水平,其在淋溶液中濃度低于二苯碳酰二肼比色法檢測限。土壤添加有機肥后,初始階段淋溶液C(rⅥ)濃度較對照處理高,但經歷一段時間后,則較對照處理小,這表明有機肥一定程度上可減少C(rⅥ)淋溶量。Cu(Ⅱ)能提高土壤表面ζ-電位和促進C(rⅥ)吸附,并降低磚紅壤C(rⅥ)淋溶量;磷酸根可減小土壤表面ζ-電位和土壤對C(rⅥ)吸附量,從而促進C(rⅥ)淋溶。模擬酸雨條件下,土壤中C(rⅥ)淋溶量呈現出先逐漸增加后減少特征。當Cu(Ⅱ)存在時,盡管土壤中C(rⅥ)保持量最大,但其在淋溶液中濃度卻較對照低,說明Cu(Ⅱ)與C(rⅥ)之間的相互作用有助于降低后者淋溶量。
關鍵詞:六價鉻;磚紅壤;淋溶-遷移
鐘來元,鐘燕彬,楊杰文.六價鉻在磚紅壤中淋溶特征的模擬研究[J].農業環境科學學報, 2016, 35(5):901-906.
ZHONG Lai-yuan, ZHONG Yan-bin, YANG Jie-wenl. Characteristics of Cr(Ⅵ)leaching in oxisol under simulated column experiment[J]. Journal of Agro-Environment Science, 2016, 35(5):901-906.
受電鍍、皮革加工、印染、木材處理以及采礦等行業廢水、廢渣不當處置的影響,鉻(Cr)已成為土壤常見污染物之一[1]。據報道,我國某地冶煉廠周邊農田土壤中總Cr含量高達3500 mg·kg-1[2]。此外,某些蛇紋石或玄武巖發育的土壤,如廣泛分布于我國海南島、雷州半島的磚紅壤,由于成土母質Cr含量比較高,即使沒有明顯外源性輸入,這類土壤總Cr平均含量也近300 mg·kg-1[3]。在自然環境中,Cr主要以+3和+6價等化學價態存在。相對而言,+3價態的生物毒性和在土壤的遷移程度較小,而+6價態不但對植物、人體都有很強毒害作用,還容易通過淋溶過程從土壤遷移至地下水[4]。因此,研究土壤中Cr(Ⅵ)淋溶特征,對于了解和評價高鉻土壤地區地下水的環境與健康風險具有重要意義。
土壤及工業廢渣中Cr(Ⅵ)的淋溶-遷移程度與基質理化性狀(如:質地、孔隙度、礦物組成)、水文特征、溶液pH、陪伴離子類型、有機質含量等因素密切相關,受Cr(Ⅵ)在基質固-液界面吸附-解吸、氧化-還原、沉淀-溶解等反應以及地球水文過程的綜合控制[5]。研究證實,土壤表面對有機物還原Cr(Ⅵ)反應有催化作用,從而導致在某些富含有機質土壤中,即使與惰性淋溶示蹤離子Br-相比,Cr(Ⅵ)淋溶行為也會呈現出明顯滯后現象[6-7]。在強堿性水解條件下,某些礦物晶格中Fe(Ⅱ)可被釋放到溶液,將Cr(Ⅵ)還原成Cr(Ⅲ),并使后者生成沉淀,最終減少Cr的淋溶-遷移量[8]。EDTA、檸檬酸等有機酸以及H2SO4、HNO3無機酸可溶解土壤固相、解吸表面吸附態Cr(Ⅵ),從而提高了Cr(Ⅵ)在溶液相的分配數量,促進其淋溶[9-11]。
磚紅壤是我國雷州半島、海南島等地區主要土壤類型,其高度風化、富含鐵氧化物,一方面對Cr(Ⅵ)的吸附量較大,另一方面又可催化有機物,將Cr(Ⅵ)還原為遷移性較低的Cr(Ⅲ)[12]。在這兩種因素綜合作用下,Cr(Ⅵ)能否表現出不同的淋溶-遷移狀況還需深入研究。同時,土壤重金屬復合污染現象普遍存在,大量養分離子通過施肥被引入土壤,這些陪伴離子對Cr(Ⅵ)吸附過程有重要影響,但尚不清楚在此影響下Cr(Ⅵ)的淋溶過程將有何變化。此外,我國華南地區是典型酸雨區,在酸沉降影響下土壤Cr(Ⅵ)淋溶程度大小也有待探討。因此,基于以上分析,本文將利用自制土柱裝置,研究有機肥、Cu(Ⅱ)和磷酸根對磚紅壤中Cr(Ⅵ)淋溶過程的影響,并在此基礎上考察模擬酸雨條件下磚紅壤中Cr(Ⅵ)溶出特征。選擇研究Cu(Ⅱ)和磷酸根等陪伴離子的作用是因為前者對Cr(Ⅵ)吸附反應的影響已有文獻報道[13],故此有利于本文結果解釋,而后者是典型專性吸附陰離子,且因磷肥施用普遍存在于磚紅壤。
1 材料與方法
1.1實驗材料
供試土壤采自廣東省徐聞縣0~40 cm層磚紅壤,經風干、研磨,過20目或100目篩后備用。按參考文獻[13]規定方法,用pH復合玻璃電極測得土壤pH值為4.83,有機質含量15.8 g·kg-1(重鉻酸鉀-外加熱法),游離態氧化鐵和無定形氧化鐵分別用連二亞硫酸鈉-檸檬酸鈉-碳酸氫鈉溶液(DCB法)和pH3.0草酸銨溶液浸提,含量分別為126.1 g·kg-1和10.4 g· kg-1。用虹吸管法提取到土壤膠體,X-射線衍射法鑒定出其所含主要礦物是高嶺石、赤鐵礦和三水鋁石。
1.2實驗方法
1.2.1土柱淋溶實驗
所用自制土柱裝置如圖1所示(柱高40 cm,內徑4.2 cm)。
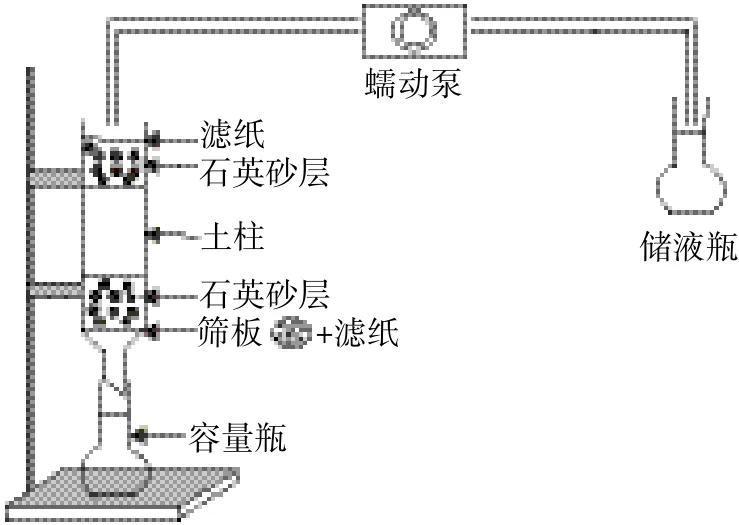
圖1 室內土柱淋溶裝置示意圖Figure 1 Diagram of soil leaching experiment
為使淋溶液均勻擴散進入土柱,需在其上方放置約2 cm厚石英砂層和濾紙。稱取200 g土壤,過20目篩裝入土柱,并用橡皮錘輕輕敲擊土柱以使上下緊實度均勻。研究有機肥對Cr(Ⅵ)淋溶過程的影響時,則需將相同質量的土壤與10.00 g有機肥混合均勻后再裝柱。淋溶實驗開始前,用蠕動泵(重慶杰恒蠕動泵有限公司BT-100EA型)按3.5 r·min-1流速向土柱滴加水以飽和土壤,待水淋出速率與加入速率相等時,即認為土壤水分達到飽和。
隨后,按上述流速(以下同)將以0.01 mol·L-1NaClO4為支持電解質的0.1 mmol·L-1Cr(Ⅵ)溶液(pH值調節為4.0)輸入土柱。用100 mL容量瓶接受淋溶液,體積到達刻度線后,即完成1次取樣(每日取樣兩次)。淋溶液過0.2 μm濾膜后,測定其中Cr(Ⅵ)濃度。當淋溶液中Cr(Ⅵ)濃度保持基本不變時,實驗結束,整個實驗共持續24 d。按相同步驟研究陪伴離子對淋溶過程的影響,所不同的是輸入溶液除含有相同濃度的Cr(Ⅵ)外,還含有1.0 mmol·L-1Cu(Ⅱ)或磷酸根。
為進一步考察土壤中Cr(Ⅵ)溶出情況,本文還用模擬酸雨溶液對其進行淋溶。按摩爾比2:1將濃硫酸和濃硝酸混合得到酸雨母液,再用超純水稀釋至pH=4.00±0.05。隨后將模擬酸雨輸入到上述土柱中,按相同方法取樣和處理淋溶液。考慮到當地降雨量和酸雨頻次,整個實驗酸雨淋溶總量約為4000 mL。
1.2.2磚紅壤催化有機肥還原Cr(Ⅵ)反應動力學
創傷性顱內損傷的致傷因素主要有交通傷、高處墜落傷、平地跌倒傷、運動傷、物體砸落傷、機械致傷、利器穿刺傷、毆打施加傷等。其中,交通傷是最主要的致傷因素(占33.8%),其次為意外損傷(占21.5%)、毆打施加傷(占17.3%)等。高處墜落傷導致的平均住院時間、住院費用以及藥品費用均居第1位,分別為20.7天、57 023.7元、19 703.0元,提示高處墜落所導致的創傷性顱內損傷可能往往更為嚴重;而交通傷導致的創傷性顱內損傷占比居第1位,詳見表1。
稱取若干份0.500 0 g土壤樣品、0.150 0 g有機肥(按5%有機碳添加水平)于50 mL塑料離心管,并將離心管與內容物稱重計為m1。隨后,加入用0.01 mol·L-1NaClO4作支持電解質的0.1 mmol·L-1Cr(Ⅵ)溶液25 mL,同時再向管內加入微量0.1 mol·L-1HCl 或NaOH以調節懸液初始pH值為3.50±0.05。在不同反應時刻(0.5、1、2、3、4、5、6、7 d)取出其中1只離心管,4000 r·min-1離心5 min,將上清液傾倒完全后,測定其中Cr(Ⅵ)和總Cr濃度。將離心管與固體殘渣稱重(m2)后,加入0.01 mol·L-1KH2PO4溶液25 mL,以計算解吸土壤表面吸附態Cr(Ⅵ)數量[14]。
1.2.3磚紅壤對Cr(Ⅵ)吸附等溫線及Cu(Ⅱ)或磷酸根與Cr(Ⅵ)的競爭吸附
稱取若干份0.500 0 g土壤樣品于50 mL塑料離心管,依次加入用0.01 mol·L-1NaClO4作支持電解質的0.1、0.2、0.4、0.8 mmol·L-1和2.0 mmol·L-1的Cr(Ⅵ)溶液25 mL(初始pH均調節為4.0)。振蕩24 h后,4000 r·min-1離心5 min,過濾,測定濾液Cr(Ⅵ)濃度。根據反應前后,溶液Cr(Ⅵ)濃度差計算其吸附量。
本文還進一步研究了不同pH條件下Cu(Ⅱ)或磷酸根對Cr(Ⅵ)吸附和土壤表面ζ-電位的影響,以探明它們對Cr(Ⅵ)淋溶過程的影響機理。具體步驟分別是:(1)稱取若干份0.500 0 g土壤樣品于50 mL塑料離心管,依次加入用0.01 mol·L-1NaClO4作支持電解質且含有0.1 mmol·L-1Cr(Ⅵ)和1.0 mmol·L-1陪伴離子的溶液25 mL,隨后再加入微量0.1 mol·L-1HCl或NaOH以將懸液pH值控制在3.0至6.0范圍。振蕩24 h,離心、過濾,測定濾液pH和Cr(Ⅵ)濃度;(2)稱取一定質量過300目篩土壤樣品于錐形瓶中,再按0.2 g·L-1顆粒濃度加入一定體積以0.01 mol·L-1NaClO4為支持電解質的1.0 mmol·L-1Cu(Ⅱ)或磷酸根溶液。懸液經超聲波分散后,等分于若干個50 mL塑料離心管,并將懸液pH調至所需范圍(3.0~8.0),平衡2 d后,取數毫升懸液測定其ζ-電位(ZetaPals,Brookhaven儀器公司,美國)。以上實驗均以不加陪伴離子為對照。
1.3分析方法
溶液Cr(Ⅵ)濃度測定用二苯碳酰二肼比色法[13],總Cr濃度測定用火焰原子吸收分光光度法,兩者濃度差即為Cr(Ⅲ)濃度。
2 結果與討論
2.1有機肥對磚紅壤中Cr(Ⅵ)淋溶過程的影響
從圖2可知,在所研究的0.1~2.0 mmol·L-1初始濃度范圍內,土壤對Cr(Ⅵ)的吸附量隨初始濃度增加而增加,且未達到飽和,吸附量最大可達555.9 mg· kg-1。這表明富含氧化鐵的磚紅壤對Cr(Ⅵ)有較強吸附能力。前人研究已證實,針鐵礦、赤鐵礦等土壤中常見氧化鐵在自然環境pH條件下對Cr(Ⅵ)等陰離子形態污染物有很強烈的吸附作用,吸附方式以形成表面單齒或雙齒絡合物為主[15]。因此,如圖3所示,未添加有機肥時,第40次取樣溶液中Cr(Ⅵ)濃度仍低于DCB比色法檢測限。計算可知,此時Cr(Ⅵ)輸入量達到240 mg·kg-1水平,但此后淋溶液中Cr(Ⅵ)濃度隨輸入量的增加而逐漸增加。

圖2 磚紅壤對Cr(Ⅵ)吸附等溫線Figure 2 Adsorption isotherm of Cr(Ⅵ)by oxisol
從圖3還可以看出,加入有機肥后,Cr(Ⅵ)淋溶行為特征有所變化。與對照相比,初始階段淋溶液中即可檢測到較高濃度Cr(Ⅵ),并在一段時間內持續增加。此外,值得關注的是,淋溶液中Cr(Ⅵ)濃度達到最大值后,隨著實驗進行又逐漸降低,且在所研究時間范圍內趨于恒定。產生這種現象的部分原因是在土壤-有機肥復合體系中部分Cr(Ⅵ)被還原為遷移性較低的Cr(Ⅲ)。如圖4所示,在初始pH=3.5條件下,7 d內溶液中Cr(Ⅵ)濃度逐漸減小至零,而Cr(Ⅲ)逐漸升高。已有研究證實,土壤腐殖質某些官能團(如:羥基)具有一定還原性,還原反應速率從數天至數月不等[16]。
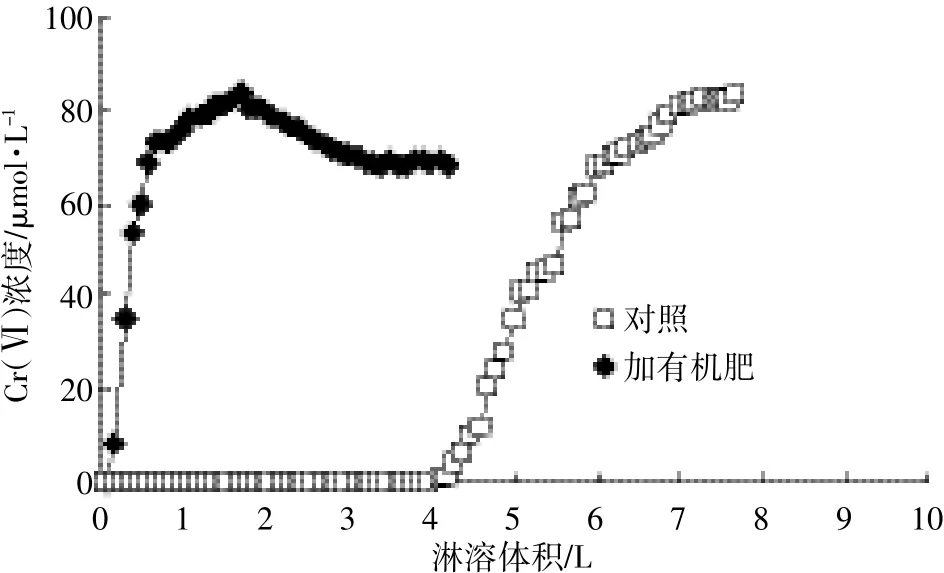
圖3 有機肥對磚紅壤中Cr(Ⅵ)淋溶過程的影響Figure 3 Influence of organic fertilizer on leaching of Cr(Ⅵ)in oxisol

圖4 磚紅壤-有機肥復合體系中Cr(Ⅵ)還原動力學Figure 4 Kinetics of Cr(Ⅵ)reduction in oxisol-organic fertilizer complex systems
2.2陪伴離子對磚紅壤中Cr(Ⅵ)淋溶過程的影響
如圖5所示,Cu(Ⅱ)和磷酸根兩種陪伴離子對Cr(Ⅵ)淋溶過程有重要影響。與對照相比,Cu(Ⅱ)可減少Cr(Ⅵ)的淋溶量而磷酸根則有促進作用,如在pH=5.30±0.05條件下,對照處理Cr(Ⅵ)吸附百分比為36.35%,加Cu(Ⅱ)和磷酸根處理則分別為51.17% 和22.24%(圖6)。一般認為,離子在土壤溶液相中分配數量越多,越容易被淋溶。因此,以上現象應從陪伴離子如何影響土壤吸附Cr(Ⅵ)角度進行解釋。如圖6所示,Cu(Ⅱ)可促進磚紅壤吸附Cr(Ⅵ),而磷酸根表現為抑制作用。徐仁扣等[17]發現Cu(Ⅱ)對廣西紅壤、江西紅壤和湖南紅壤吸附Cr(Ⅵ)有促進作用,且氧化鐵含量越高,促進作用越明顯。該研究還進一步指出其中可能機理是:(1)Cu(Ⅱ)增加了土壤表面正電荷數量,從而有利于Cr(Ⅵ)的靜電和專性吸附;(2)Cu(Ⅱ)與Cr(Ⅵ)生成表面沉淀。盡管本文未對所得結果的機理加以深入探討,但根據磚紅壤的組成特征來看,以上兩種機理在本文所研究的體系中也應成立。正如圖7所示,加入Cu(Ⅱ)后,土壤表面ζ-電位值較對照高,這是土壤表面對Cu(Ⅱ)產生專性吸附和正電荷數量增加的有力證據。由于磚紅壤中氧化鐵含量明顯高于紅壤,Cu(Ⅱ)的促進作用將更加顯著,從而使得Cr(Ⅵ)淋溶量降低。

圖5 陪伴離子對磚紅壤中Cr(Ⅵ)淋溶過程的影響Figure 5 Influence of coexisting ions on leaching of Cr(Ⅵ)in oxisol
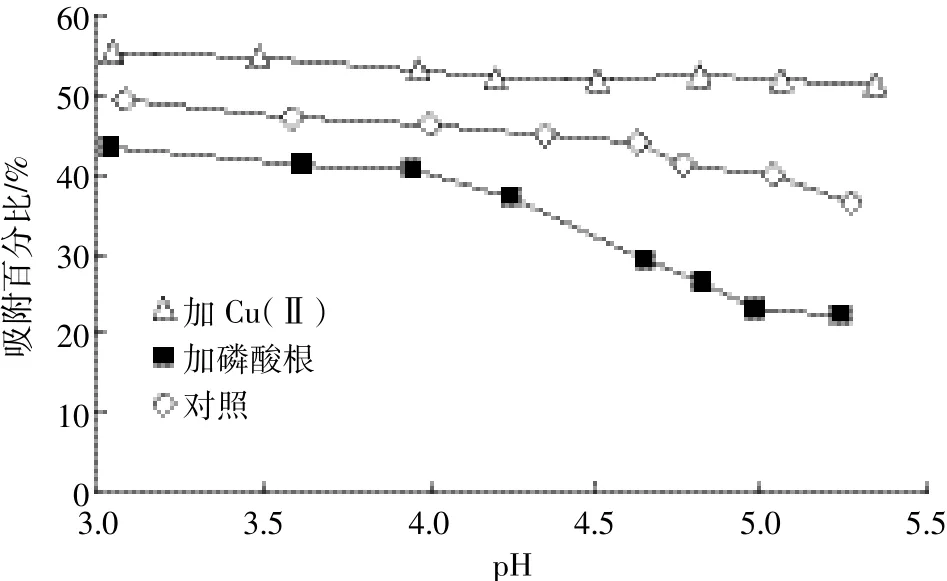
圖6 陪伴離子對磚紅壤吸附Cr(Ⅵ)的影響Figure 6 Influence of coexisting ions on Cr(Ⅵ)adsorption by oxisol
與Cu(Ⅱ)相反,磷酸根屬于典型專性吸附陰離子,其減少土壤吸附Cr(Ⅵ)有以下3方面影響機制:(1)降低土壤表面ζ-電位(圖7),增強了土壤表面對Cr(Ⅵ)的靜電排斥作用;(2)與Cr(Ⅵ)競爭某些吸附位點,并對吸附態Cr(Ⅵ)有解吸作用[14];(3)自身吸附到土壤表面過程中釋放出的羥基(OH-)對Cr(Ⅵ)吸附也有抑制作用[18]。因此,磷酸根的存在將使得更多Cr(Ⅵ)保存在土壤溶液相,這將促進后者淋溶和遷移。
2.3酸雨對磚紅壤中Cr(Ⅵ)溶出的影響
從圖8可知,酸雨影響下土壤中Cr(Ⅵ)溶出過程可分為兩個階段,開始數次淋溶液中,其濃度迅速升高,達到最大值后則逐漸降低。張麗華等[19]也觀察到酸雨作用下,污染土壤中鉻的釋放過程可分為快速釋放和慢速釋放兩個階段,前者主要包括土壤表面易交換態和水溶態鉻離子,而后者主要包括以專性吸附方式或其他難交換態方式保留在土壤表面的鉻離子。同時,不同處理間Cr(Ⅵ)溶出特征有所不同。加磷酸根處理,Cr(Ⅵ)溶出過程比其他兩個處理較早達到平衡。這大致是因為磷酸根與Cr(Ⅵ)之間的競爭吸附,導致后者靜電吸附的比例增加,從而易被溶出。更為重要的是,雖然加Cu(Ⅱ)處理中土壤所保持的Cr(Ⅵ)數量較對照多,但其溶出量卻相對減少,具體原因如下:
通常認為酸雨加速土壤重金屬溶出主要有兩種方式[20-21]:第一,溶液中H+與表面金屬陽離子的離子交換反應;第二,礦物晶格溶解反應,即H+吸附到礦物表面并引起羥基質子化,使礦物晶格中金屬離子與氧離子之間的結合強度降低和化學鍵斷裂,最終導致礦物晶格破壞和表面吸附態離子隨之釋放到溶液中。根據以上分析可知,當Cr(Ⅵ)與Cu(Ⅱ)共存時,由于相當數量的Cu(Ⅱ)吸附到土壤表面,從而使得輸入到土壤中的部分H+因與Cu(Ⅱ)之間的交換反應而被消耗,減少了對表面吸附態Cr(Ⅵ)的溶出。
此外,如圖7所示,Cu(Ⅱ)可使土壤表面ζ-電位增加,這同樣不利于H+的吸附和礦物溶解反應。更進一步的是,根據徐仁扣等[17]研究結果,當Cr(Ⅵ)與Cu(Ⅱ)共存時,兩者還可能在表面生成沉淀,這也增強了前者在土壤中的穩定性。相反,在對照處理中,Cr(Ⅵ)吸附到土壤將引起表面ζ-電位降低和負電荷數量增加[22],而這有利于H+吸附和礦物溶解。Eick等[23]也報道表面吸附態離子的存在可促進H+溶解礦物反應。

圖7 Cu(Ⅱ)和磷酸根對土壤表面ζ-電位的影響Figure 7 Effect of Cu(Ⅱ)and phosphate on zeta potential of oxisol surface
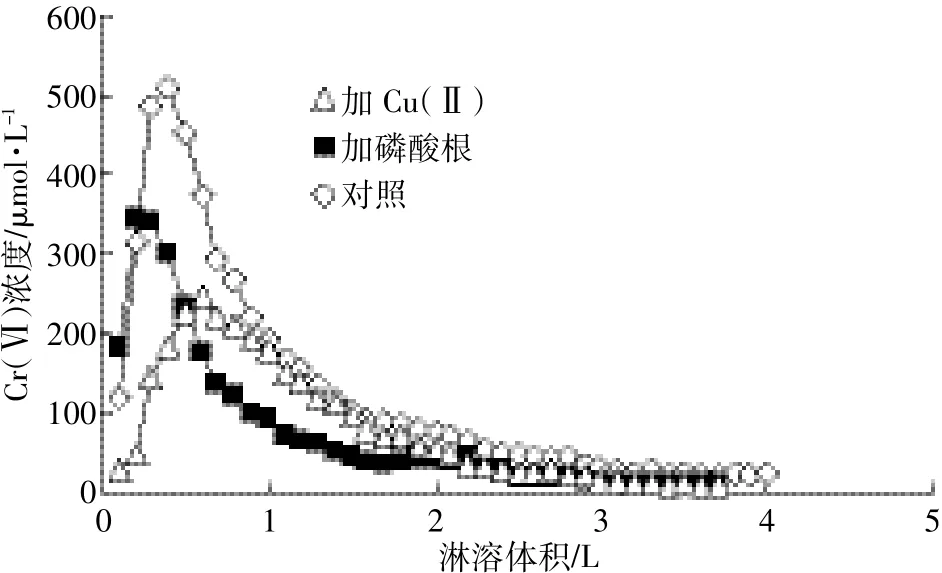
圖8 模擬酸雨條件下土壤中Cr(Ⅵ)溶出特征Figure 8 Release of Cr(Ⅵ)in oxisol under simulated acidic rain
3 結論
高氧化鐵含量磚紅壤對Cr(Ⅵ)的吸附作用較強,有助于降低后者的淋溶強度,表現為輸入量小于240 mg·kg-1時,淋溶液中Cr(Ⅵ)濃度小于DCB比色法檢測限。土壤添加有機肥后,前期淋溶液Cr(Ⅵ)濃度較高,但后期則有所降低,部分原因歸結為在土壤表面催化作用下,有機肥將Cr(Ⅵ)還原為遷移程度較小的Cr(Ⅲ),這說明施用有機肥可一定程度降低Cr(Ⅵ)淋溶量。Cu(Ⅱ)可降低Cr(Ⅵ)淋溶量,磷酸根則有促進作用。酸雨將提高土壤中Cr(Ⅵ)淋溶量,但Cu(Ⅱ)的存在能一定程度減小這種不利影響。
參考文獻:
[1]Choppala G, Bolan N, Park J H. Chromium contamination and its risk management in complex environmental settings[J]. Advance in Agronomy, 2013, 120:129-172.
[2]Wang Z X, Chen J Q, Chai L Y, et al. Environmental impact and sitespecific human health risks of chromium in the vicinity of a ferro-alloy manufactory, China[J]. Journal of Hazardous Materials, 2011, 190(1-3):980-985.
[3]關卉,王金生,李丕學,等.湛江市農業土壤與作物鉻含量及其健康風險[J].環境科學與技術, 2008, 31(1):120-124. GUAN Hui, WANG Jin-sheng, LI Pi-xue, et al. Concentration of chromiuminagriculturalsoiland cropsand their healthyrisk[J].Environmental Science and Technology, 2008, 31(1):120-124.
[4]Choppala G, Bolan N, Lamb D, et al. Comparative sorption and mobility of Cr(Ⅲ)and Cr(Ⅵ)speciesin a range of soils:Implicationsto bioavailability[J]. Water Air and Soil Pollution, 2013, 224(11):1699-1711.
[5]Zachara J M, Ainsworth C C, Browm Jr G E, et al. Chromium speciation andmobilityinahighlevelnuclearwastevadosezoneplume[J].Geochimicaet Cosmochimica Acta, 2004, 68(1):13-30.
[6]Tokunaga T K, Wan J M, Firestone M K, et al. Chromium diffusion and reduction in soil aggregates[J]. Environmental Science and Technology, 2001, 35(15):3169-3174.
[7]Banks M K,Schwab AP,Henderson C.Leaching and reduction of chromium in soil as affected by soil organic content and plants[J]. Chemospher, 2006, 62(2):255-264.
[8]Qafoku N P, Ainsworth C C, Heald S M. Cr(Ⅵ)fate in mineralogically altered sediments by hyperalkaline waste fluids[J]. Soil Science, 2007, 172(8):598-613.
[9]Tinjuma J M, Bensonb C H, Edil T B. Mobilization of Cr(Ⅵ)from chromite ore processing residue through acid treatment[J]. Science of the Total Environment, 2008, 391(1):13-25.
[10]Zhao X M, Dong D M, Hua X Y, et al. Investigation of the transport and fate of Pb, Cd, Cr(Ⅵ)and As(V)in soil zone derived from moderately contaminated farmland in Northeast, China[J]. Journal of Hazardous Materials, 2009, 170(2/3):570-577.
[11]Soro L J, Bordas F, Bollinger J C. Column leaching of chromium and nickel from a contaminated soil using EDTA and citric acid[J]. Environmental Pollution, 2012, 164:175-181.
[12]Yang J W, Zhong L Y, Liu L M. Coupling of tartaric acid-promoted soil dissolution and Cr(Ⅵ)reduction in an Oxisol[J]. Journal of Geochemical Exploration, 2013, 125(1):138-143.
[13]Sparks D L. Methods of soil analysis[M]. Madsion:Soil Science Society of America, 1996.
[14]Feng X H, Zhai L M, Tan W F, et al. The controlling effect of pH on oxidation of Cr(Ⅲ)by manganese oxide minerals[J]. Journal of Colloid and Interface Science, 2006, 298(1):258-266.
[15]Fendorf S. Surfaces reactions of chromium in the soils and waters[J]. Geoderma, 1995, 67(1):55-71.
[16]Wittbrodt P R, Palmer C D. Reduction of Cr(Ⅵ)by soil humic acids [J]. European Journal of Soil Science, 1996, 47(1):151-162.
[17]徐仁扣,肖雙成,趙安珍. Cu(Ⅱ)對紅壤吸附Cr(Ⅵ)的影響[J].農業環境科學學報, 2008, 27(3):944-947. XU Ren-kou, XIAO Shuang-cheng, ZHAO An-zhen. Effect of Cu(Ⅱ)on adsorption of Cr(Ⅵ)by red soils[J]. Journal of Agro-Environment Science, 2008, 27(3):944-947.
[18]Yu T R. Chemistry of variable charge soils[M]. New York:Oxford University Press, Inc, 1996.
[19]張麗華,朱志良,鄭承松,等.模擬酸雨對三明地區受重金屬污染土壤的淋濾過程研究[J].農業環境科學學報, 2008, 27(1):151-155. ZHANG Li-hua, ZHU Zhi-liang, ZHENG Cheng-song, et al. Leaching of heavy metals from sanming polluted soil with simulated acid rain[J]. Journal of Agro-Environment Science, 2008, 27(1):151-155.
[20]Sposito G. The chemistry of soils[M]. Second edition. New York:Oxford University Press, Inc, 2008.
[21]Stumm W. Chemistry of the solid-water interface[M]. New York:John Wiley & Sons Inc, 1992.
[22]Xu R K, Xiao S C, Zhao A Z, et al. Effect of Cr(Ⅵ)anions on adsorption and desorption behavior of Cu(Ⅱ)in the colloidal systems of two authentic variable charge soils[J]. Journal of Colloid and Interface Science, 2005, 284(1):22-29.
[23]Eick M J, Peak J D, Brady W D. The effect of oxyanions on the oxalatepromoted dissolution of goethite[J]. Soil Science Society America of Journal, 1999, 63(5):1133-1141.
中圖分類號:X53
文獻標志碼:A
文章編號:1672-2043(2016)05-0901-06
doi:10.11654/jaes.2016.05.012
收稿日期:2015-12-08
基金項目:國家自然科學基金面上項目(41371316);廣東海洋大學大學生創新創業訓練計劃項目(CXXL2015059)
作者簡介:鐘來元(1966—),男,湖南武岡人,博士,教授,從事土壤重金屬污染控制研究。E-mail:zhly66@163.com
*通信作者:楊杰文E-mail:jw_yang@126.com
Characteristics of Cr(Ⅵ)leaching in oxisol under simulated column experiment
ZHONG Lai-yuan, ZHONG Yan-bin, YANG Jie-wen*
(Department of Resources and Environmental Sciences, College of Agriculture, Guangdong Ocean University, Zhanjiang 524088, China)
Abstract:Understanding Cr(Ⅵ)leaching is important for assessments of groundwater and health risk of soil Cr. A simulated soil column experiment was conducted to examine the effects of organic fertilizer and coexisting ions on the release of soil Cr(Ⅵ)under simulated acid rain condition, using an oxisol. At Cr(Ⅵ)inputs less than 240 mg·kg-1, concentrations of Cr(Ⅵ)in leachate were below the detection limit of diphenylcarbazide colorimetric spectrophotometic method used in this study, which was attributed to the large adsorption capacity of Fe-rich soil for Cr(Ⅵ). In amendment of organic fertilizer, leaching of Cr(Ⅵ)was enhanced at the early stage, but reduced at the later stage, in comparison with the control, partially ascribed to the reduction of Cr(Ⅵ)to less mobile Cr(Ⅲ)on the soil surface by organic fertilizer. At the coexistence of Cu(Ⅱ), the mobility of Cr(Ⅵ)in the soil was inhibited because soil surface ζ-potential became more positive under the presence of Cu(Ⅱ)and Cr(Ⅵ)adsorption was then promoted. On the contrary, more Cr(Ⅵ)was leached out of the soil in the presence of phosphate because of competition for surface adsorption sites. Acidic rain increased the release of Cr(Ⅵ)in the soil during the initial period but decreased as the experiment prolonged. Overall, this study would be helpful for us to understand the mobility of Cr(Ⅵ)in oxisol and to assess the environmental risk of Cr(Ⅵ)-polluted soil.
Keywords:hexavalent chromium; latosol; leaching

