蘇教版選修四“化學反應原理”教學
鄭碧芬
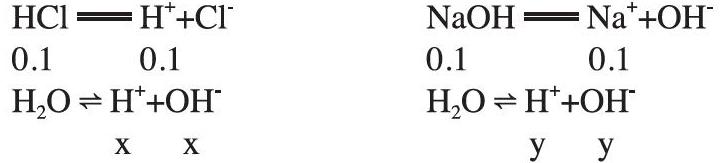
一、注重夯實基礎
由于各學生之間的智力差異和學習基礎不同,學生對化學知識的掌握能力不同,應針對學生實際情況因材施教。 在教學中,教師可通過習題形式讓學生回顧、理解所學知識,而不是教師一味講授。教學設計如下:
1.溫故而知新
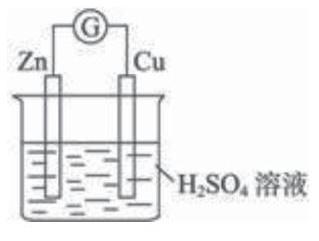
該裝置為 池,Zn是 極,Cu是 極,電子從 經 流向 ,電流從 流向 ,離子從 流向 ,電極反應式分別是 總反應式 。
該習題可以讓學生上課馬上作答,教師根據學生回答情況及時調整,學生能夠很好地回憶、理解原電池的工作原理。
2.設置問題情境,引出鹽橋
在實驗中,為什么Zn、Cu附近都有氣泡產生?學生進行各種猜想,教師一一進行評價,提出解決辦法,引入鹽橋。鹽橋的作用是平衡兩極的電荷。
二、注重實驗教學
化學是一門實驗學科,要讓學生真正了解每個實驗涉及的化學反應原理、裝置原理和操作原理,多給機會讓學生動手做實驗。以“強電解質和弱電解質的區分”這一教學目標為例,教學設計如下。
1.學生分組實驗
(1)測定濃度均為0.1mol/L的鹽酸、醋酸溶液的PH;(2)兩支試管中分別放入形狀相同的鎂條,取濃度均為0.1mol/L的鹽酸、醋酸溶液各10ml于氣球中,并將氣球扣在試管口,同時迅速加入到試管中,觀察現象。
2.現象
(1)鹽酸的PH小于醋酸的PH;(2)鹽酸中氣球漲得比較快,但最終兩氣球大小一樣。
3.解析
(1)鹽酸是強酸,醋酸是弱酸,當物質的量濃度相同時,由于鹽酸完全電離,醋酸部分電離導致鹽酸中氫離子濃度大。酸性越強,PH越小。(2)反應開始時,鹽酸中氫離子濃度大于醋酸中氫離子濃度,離子濃度大,反應速率就越快。但由于鎂條足量,促進醋酸往電離的方向進行,最終完全電離出氫離子,所以兩者產生的氫氣一樣多。
4.拓展思考
(1)比較物質的量濃度相同的氫氧化鈉溶液和氨水的PH大小;(2)比較PH相同的氫氧化鈉溶液和氨水的物質的量濃度大小;(3)物質的量濃度、體積均相等的鹽酸與醋酸,分別和足量的Zn反應,比較反應開始時的速率和產生氫氣的物質的量;(4)PH、體積均相等的鹽酸與醋酸,分別和足量的Zn反應,比較反應開始時的速率和產生氫氣的物質的量。
三、注重分析、對比能力培養
很多學生上課時,感覺所學內容不難,但是真正碰到習題時,卻不知道如何下手,眼高手低的現象十分普遍,甚至出現所學知識混淆不清的現象。在教學中,如果能采用分析對比的方法,可以大大提高學習效率。
1.題目
常溫下,分別計算濃度均為0.1mol/L的鹽酸、氫氧化鈉溶液的PH。
2.解題思路
知道PH與氫離子濃度之間的關系,分析鹽酸、氫氧化鈉溶液中存在的電離過程,認識水電離出的氫離子與氫氧根離子濃度一定相等。
3.具體解析
假設鹽酸、氫氧化鈉溶液中水電離出的氫離子濃度分別是x、y。
從電離方程式看出,酸和堿中水的電離受到抑制。
計算酸PH的時候,把水電離出的氫離子忽略掉,因此PH=-lg0.1=1;計算堿PH的時候,把水電離出的氫氧根離子忽略掉,因此溶液中氫氧根離子濃度為0.1mol/L,根據Kw計算出氫離子濃度(來自水的電離),再算PH。C(H+)=10-14/0.1=10-13,mol/L,PH=-lg10-13=13。
四、注重構建知識網絡
化學知識點比較零散,尤其是在元素和有機化學當中,很多的特性是無規律可循的卻存在規律性,學生容易混淆。因此,構建知識網絡體系顯得十分重要。教師要提高學生的學習效率,增強知識鏈中的薄弱環節,實現基礎知識到位,邏輯思維到位,分析問題和解決問題的能力到位,就要注重方法的探索。
五、注重教學方法
“化學反應原理”這部分內容知識跨越大、難度大,教師在教學中要認真分析學生的學情,摸清他們的知識儲備,針對不同模塊的知識采取不同的教學方法,才能獲得良好的教學效果。在教學活動中,教師要關注和反思教學行為,注意教學方法的靈活多樣性,調動學生學習積極性手段的有效性,教師在課堂所有活動的取向性,學生在課堂教學活動的參與性等諸多方面。
參考文獻:
趙華,高峰.“化學反應原理”模塊的學習情況調查和認知策略研究[J].化學教育,2011(3).

