塞來昔布對老年三陰性乳腺癌患者血清IL-6及IL-8的影響
袁雁,徐丹英
(浙江省嘉興市第二醫院 乳腺外科,浙江 嘉興 314000)
塞來昔布對老年三陰性乳腺癌患者血清IL-6及IL-8的影響
袁雁Δ,徐丹英
(浙江省嘉興市第二醫院 乳腺外科,浙江 嘉興 314000)
目的 探究塞來昔布對老年三陰性乳腺癌患者血清白介素-6(IL-6)及白介素-8(IL-8)水平影響。方法 收集2013年3月~2015年4月浙江省嘉興市第二醫院腫瘤科收治的老年三陰性乳腺癌患者64例,隨機分為對照組和試驗組,各32例。2組患者均給予TAC方案,對照組在化療結束后給予枸櫞酸他莫昔芬片10 mg口服,2次/天,試驗組在化療結束后給予塞來昔布膠囊200 mg口服,2次/天。2組患者1個療程均為3周,共治療6個療程。治療結束后對比分析2組臨床療效、血清IL-6、IL-8、雌激素水平以及不良反應。結果 治療后,試驗組臨床總有效率顯著高于對照組(93.75%vs. 75.00%,χ2=4.267,P<0.05),治療后2組血清IL-6、IL-8、雌酮(oestrone,E1)、雌二醇(estradiol,E2) 水平下降(P<0.05),促卵泡生成素(follicle-stimulating hormone,FSH)、促黃體生成素(luteinizing hormone,LH)水平上升(P<0.05),與對照組相比,試驗組血清IL-6、IL-8、E1、E2水平較低(P<0.05),FSH、LH水平較高(P<0.05)。與對照組相比,試驗組總不良反應發生率較低(21.88%vs. 56.25%,χ2=7.94,P<0.05)。結論 塞來昔布對老年三陰性乳腺癌的臨床療效顯著,有效降低血清IL-6、IL-8水平,調節機體雌激素水平,藥物安全性高。
塞來昔布;老年三陰性乳腺癌;白介素-6;白介素-8
三陰性乳腺癌(triple negative breast cancer,TNBC)是雌激素受體(estrogen receptor,ER)、孕激素受體 (progesterone receptor,PR)和人表皮生長因子受體2(human epidermal growth factor receptor 2,HER-2)均陰性的乳腺癌[1],其病理以及分子生物學特征具有獨特性,占乳腺癌發病率的15%。由于本疾病缺乏內分泌及抗HER-2治療的靶點,預后差、易發生侵襲轉移,并且尚無針對性的治療方案,嚴重影響患者日常生活,甚至危及患者生命,死亡率較高。因此,三陰性乳腺癌的早期診斷以及治療尤為關鍵。抗癌活性的他莫昔芬是治療三陰性乳腺癌的臨床常用藥物,但其發揮藥效的用時易產生如骨髓抑制等一系列不良反應。現代研究顯示,低毒藥物聯用化療藥物后對腫瘤化療產生的體質量減輕、進食量減少毒副反應有不同程度的改善作用[2],增強化療藥物對腫瘤細胞的敏感性。塞來昔布是一種新型COX-2選擇性抑制劑[3],臨床用于急性期或慢性期骨關節炎和類風濕關節炎的癥狀和體征,近年研究顯示,塞來昔布對上皮組織癌有一定的抑制作用[4],基本無細胞毒性,與化療藥物聯用不會造成二次傷害。本研究以老年三陰性乳腺癌患者64例為研究對象,探究塞來昔布對老年三陰性乳腺癌患者血清IL-6及IL-8水平影響,為臨床提供理論依據。
1 資料與方法
1.1 一般資料 收集2013年3月~2015年4月浙江省嘉興市第二醫院腫瘤科收治的老年三陰性乳腺癌患者64例,年齡55~85歲,平均年齡(72.46±7.39)歲,中位體表面積1.61 m2(1.34~1. 89 m2) ,中位Karnofsky功能狀態評分(KPS)92( 80 ~100) ,病理類型均為浸潤性導管癌,腫瘤>2 cm 21例,腫瘤≤2 cm 43例,按國際抗癌協會TNM臨床分期,Ⅰ期32例,Ⅱ期20例,Ⅲ期10例,Ⅳ期2例,均為絕經后。采用隨機數字分配法,隨機分配為試驗組與對照組,其中試驗組32例,年齡57~85歲,平均年齡(73.64±7.54)歲;對照組32例,年齡55~83歲,平均年齡(71.04±7.10)歲。2組患者平均年齡、KPS評分、病理類型、病理分型以及腫瘤大小等一般資料均相仿,差異無統計學意義。
納入標準:①診斷符合按照美國國立綜合癌癥網絡(National Comprehensive Cancer Network,NCCN)乳腺癌臨床實踐指南[5]中三陰性乳腺癌的診斷標準,患者乳腺出現大小不一的腫塊,邊界不清楚;病變時乳房局部皮膚凹陷;乳腺刺痛、脹痛以及隱痛;乳腺輪廓改變、乳頭乳暈改變;乳頭溢液伴有腫塊,溢液可為無色、乳白色、淡黃色或血性等;②經乳腺癌鉬靶X射線、乳腺B超以及乳腺腫塊切除病理檢查確診為三陰性乳腺癌;③患者年齡>55歲,均為自愿參與本實驗,并簽署知情同意書。本研究經本院醫學倫理委員會批準。
排除標準:①對本研究中使用藥物有過敏體質者,接受免疫抑制劑治療的患者,消化道潰瘍/出血,乙肝、艾滋病等嚴重傳染性疾病患者,阿司匹林或其他NSAIDs后誘發哮喘、蕁麻疹或過敏反應的患者;②冠狀動脈搭橋手術(CABG)圍手術期疼痛以及嚴重心、肝、腎等多臟器功能障礙或衰竭,重度心力衰竭患者;③合并其他惡性腫瘤、癲癇等神經系統疾病。
1.2 方法
1.2.1 治療方法:2組患者給予TAC方案,其中紫杉醇注射液(海口市制藥廠有限公司,國藥準字H20043045)175 mg/m2+ 注射用鹽酸吡柔比星(深圳萬樂藥業有限公司,國藥準字H10930106)50 mg/m2+注射用異環磷酰胺(江蘇恒瑞醫藥股份有限公司,國藥準字H10950291)500 mg/m2靜脈滴注,1次/天,每周期第1天使用,對照組在化療結束后給予枸櫞酸他莫昔芬片(海南海靈化學制藥有限公司,國藥準字H46020268)10 mg口服,2次/天,試驗組在化療結束后給予塞來昔布膠囊(輝瑞制藥有限公司,國藥準字J20120063)200 mg口服,2次/天。2組患者1個療程均為3周,共治療6個療程。患者每3周進行肝腎功能以及血常規檢測,每3月行1次胸片檢查。
1.2.2 觀察指標:
① 療效評定標準:根據世界衛生組織推薦《實體瘤療效評價標準》[6],療效評定標準如下,治療結束后病灶完全消失,乳腺疼痛、乳頭溢液、皮膚凹陷、脹痛以及隱痛等臨床癥狀和體征完全消失為顯效;最大徑之和縮小≥30%,臨床癥狀和體征明顯改善為有效;頭顱CT或MRI發現新病灶,臨床癥狀和體征無改善或加重,最大徑之和縮小不足30%或增大為無效。總有效率=[(顯效例數+有效例數)/本組患者例數]×100%。
② 2組患者白介素-6(IL-6)、白介素-8(IL-8)、雌激素水平檢測:于患者治療前后采取空腹外周靜脈血3 mL,置于無菌無抗凝管內,靜置30 min,3000 r/min離心15 min,取上清液,收集其血清標本于-70 ℃冰柜內冷凍保存。實驗時,取出并解凍,采用ELISA法檢測血清IL-6、IL-8、雌酮(oestrone,E1)、雌二醇(estradiol,E2)、促卵泡生成素(follicle-stimulating hormone,FSH)與促黃體生成素(luteinizing hormone,LH)水平。

2 結果
2.1 臨床療效比較 治療后,試驗組臨床總有效率顯著高于對照組(93.75%vs. 75.00%,χ2=4.267,P<0.05)。見表1。

表1 2組患者臨床療效比較[n(%)]
*P<0.05,與對照組比較,compared with control group
2.2 血清IL-6、IL-8以及雌激素水平比較 治療前2組患者血清IL-6、IL-8、E1、E2、FSH、LH水平比較差異無統計學意義;治療后2組血清IL-6、IL-8、E1、E2水平下降(P<0.05),FSH、LH水平上升(P<0.05),與對照組相比,試驗組血清IL-6、IL-8、E1、E2水平較低(P<0.05),FSH、LH水平較高(P<0.05)。見表2。
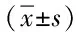
表2 2組患者血清IL-6、IL-8以及雌激素水平比較
*P<0.05,與同組治療前比較,compared with the same group pre-treatment;#P<0.05,與對照組治療后比較,compared with control group post-treatment
2.3 安全性評價 試驗組出現2例輕微消化道反應,2例肌肉關節痛,2例脫發,1例潮熱,總不良反應發生率為21.88%(7/32),對照組出現3例肌肉關節痛,4例輕微消化道反應,2例脫發,3例陰道出血,2例尿潴留,4例白細胞減少,總不良反應發生率為56.25% (18/32)。試驗組總不良反應發生率顯著低于對照組(χ2=7.94,P<0.05)。
3 討論
乳腺癌是我國女性最常見的惡性腫瘤之一[7],位居女性惡性腫瘤死亡率的首位,其發病率在各種惡性腫瘤中上升幅度最快,40歲左右是乳腺癌發病高峰年齡。三陰性乳腺癌是乳腺癌的一個特殊亞型,患者的癌細胞突變并喪失正常細胞功能,組織結構紊亂,癌細胞脫落隨著血行轉移以及淋巴結等通路轉移至全身,臨床治愈越發困難,易復發轉移,嚴重影響患者正常工作生活,威脅生命健康。老年患者存在免疫力功能下降等,但相比年輕患者病情進展緩慢,惡性程度較低,更易治療。因此,老年三陰性乳腺癌的早期治療備受當今學者關注。
塞來昔布是新一代非甾體抗炎鎮痛藥,在癌痛治療中應用廣泛[8],能夠通過選擇性抑制環氧化酶-2(COX-2),從而抑制炎癥、鎮痛,由于其有效成分中不含有抑制胃腸道保護作用的環氧化酶-1(COX-1),因此其不良反應較小。本研究顯示,與對照組相比,試驗組臨床總有效率較高(P<0.05),與對照組相比,試驗組總不良反應發生率較低(P<0.05),證實塞來昔布對老年三陰性乳腺癌的臨床療效顯著,能夠減輕脫發、陰道出血、尿潴留以及白細胞減少等不良反應,藥物安全性高。
IL-6是一種具有復雜生物功能的細胞因子,在肝細胞中表達存在,具有較高的生物性能,由單核細胞、B細胞及骨髓瘤細胞等細胞分泌,并具有協同造血細胞、成纖維細胞以及肝細胞等細胞增殖分化的作用,正常機體內IL-6水平低,但在病變情況下IL-6水平增高,導致IL-6堆積,損傷免疫功能。研究顯示,IL-6的高度表達可能導致ER陽性乳腺癌患者預后較差[9]。IL-8是一種反映腫瘤生長以及轉移的細胞因子,在機體內由纖維細胞、內皮細胞、肝細胞、上皮細胞以及單核巨噬細胞等分泌生成,參與哺乳動物整個生殖過程,具有強效促血管生成作用。曾有研究顯示[10],IL-8能夠促進乳腺癌組織的轉移,乳腺癌患者IL-8含量是否呈高表達狀態,有助于判斷乳腺癌有無淋巴結轉移及預后。雌激素是女性相關的重要內分泌指標,對機體內分泌紊亂,尤其是雌激素分泌過多,孕激素以及黃體酮分泌量降低,對乳腺癌變具有診斷作用。本研究顯示,與對照組相比,試驗組血清IL-6、IL-8、E1、E2水平較低(P<0.05),FSH、LH水平較高(P<0.05),證實塞來昔布能夠抑制IL-6、IL-8的分泌以及表達,調節激素水平,降低腫瘤細胞侵襲轉移的可能性。
本研究通過對本院腫瘤科收治的老年三陰性乳腺癌患者64例的臨床療效、血清IL-6、IL-8、雌激素水平以及不良反應進行研究,證實了塞來昔布對老年三陰性乳腺癌的臨床療效顯著,有效降低血清IL-6、IL-8水平,調節機體雌激素水平,藥物安全性高。在下一步研究中,本課題組將進行藥理學方面研究,對本研究做進一步研究。
[1] 韓華正.三陰性乳腺癌分子靶向治療的研究進展[J].臨床腫瘤學雜志,2012,17(5):470-474.
[2]鞠海,柳芳,李洪梅,等.健脾散結丸對胃腸功能影響的實驗研究[J].中國藥學雜志,2014,49(7):564-566.
[3]周海存,劉宏斌.塞來昔布防治胃癌的機制及應用前景[J].中華消化外科雜志,2013,12(4):317-320.
[4]余文韜,蔣剛.塞來昔布抗乳腺癌的臨床應用[J].中國藥業,2013,22(23):1-3.
[5]徐兵河.2009年《NCCN乳腺癌臨床實踐指南》(中國版)重點內容解讀[J].中華乳腺病雜志(電子版),2009,3(4):4-8.
[6]馬建輝.重視實體瘤療效評價標準的變革--RECIST概要[J].中華泌尿外科雜志,2006,27(2):77-79.
[7]李富.磁共振成像在乳腺癌診斷及新輔助化療中的應用[J].廣西醫科大學學報,2015,32(4):673-675.
[8]李泓錫,姚鵬.非甾體抗炎鎮痛藥物用于癌痛治療的最新進展[J].中國新藥雜志,2015,24(18):2081-2084.
[9]孫平,張洋,張靜.乳腺癌患者血清內IL-6和CCL-18的表達及臨床意義[J].現代腫瘤醫學,2015,23(8):1072-1074.
[10]林文源,劉華,陳琳,等.乳腺癌患者血清IGF-I、CA153和IL-8水平檢測的臨床意義[J].標記免疫分析與臨床,2013,20(4):218-220.
(編校:王儼儼)
Effect of celecoxib on serum IL-6 and IL-8 in senile triple negative breast cancer
YUAN YanΔ, XU Dan-ying
(Department of Breast Surgery, Jiaxing Second Hospital, Jiaxing 314000, China)
ObjectiveTo explore the effect of celecoxib on serum levels of IL-6 and IL-8 in patients with senile triple negative breast cancer.Methods64 cases with senile triple negative breast cancer collected from March 2013 to April 2015 in our hospital, and randomly divided into control group and experimental group, 32 cases in each group. The two groups
TAC scheme, the control group received tamoxifen citrate tablets 10 mg orally, twice daily and the experimental group received celecoxib capsules 200 mg orally, twice daily, at the end of the chemotherapy, for a consecutive treatment of 6 courses, three weeks as one course. The clinical curative effect, serum interleukin-6 and interleukin-8, estrogens levels and adverse reactions were compared between two groups post-treatment.ResultsAfter treatment, the total effective rate in experimental group was higher than that in control group (93.75%vs. 75.00%,χ2=4.267,P<0.05). The serum levels of IL-6,IL-8, oestrone(E1)and estradiol(E2) decreased (P<0.05) and the serum levels of follicle-stimulating hormone (FSH) and luteinizing hormone(LH) increased in two groups post-treatment (P<0.05). The total adverse reactions in experimental group was lower than that in control group(21.88%vs. 56.25%,χ2=7.94,P<0.05).ConclusionCelecoxib has the significant efficacy in the treatment of patients with senile triple negative breast cancer, could reduce serum IL-6 and IL-8 levels and regulate estrogens levels with fewer adverse reactions.
celecoxib; senile triple negative breast cancer; interleukin-6; interleukin-8
浙江省自然科學基金 (LY12H29004)
袁雁,通信作者,女,本科,主治醫師,研究方向:乳腺癌化療,E-mail:cookyydr@163.com。
R737.9
A
10.3969/j.issn.1005-1678.2016.03.11

