黃芩素對阿爾茨海默病大鼠早期腦組織蛋白表達譜的影響
王文瀟 衛東鋒 張占軍 程衛東
摘要:目的 觀察黃芩素對阿爾茨海默病(AD)大鼠發病早期認知功能和皮層、海馬組織蛋白表達譜的影響,探討其作用機制。方法 實驗大鼠隨機分為對照組、模型組、黃芩素組,每組12只。黃芩素組大鼠予黃芩素藥液灌胃,模型組和對照組大鼠予等量生理鹽水灌胃。灌胃體積均為2 mL,連續10 d。利用Morris水迷宮評估治療效果,并運用雙向凝膠電泳技術對腦組織蛋白進行分離,考馬斯藍染顯色,應用PDQuest8.0軟件對雙向電泳圖譜進行差異分析,通過MALDI-TOF-MS/MS和數據庫查詢鑒定差異明顯的蛋白質點,并利用String在線分析軟件對差異表達蛋白進行生物信息學分析。結果 黃芩素可顯著緩解β-淀粉樣蛋白(Aβ)1-40導致的認知功能減退。黃芩素作用下,位于大鼠大腦皮層和海馬組織的8種蛋白表達水平變化明顯。質譜鑒定結果顯示,差異蛋白涉及4種生物學功能,與神經傳導關系最為密切,其中3種蛋白與其他蛋白存在相互作用關系。結論 黃芩素對AD大鼠早期認知功能損傷的改善作用與其能夠調節神經傳導相關蛋白的表達相關。
關鍵詞:阿爾茨海默病;β-淀粉樣蛋白;黃芩素;神經傳導;蛋白組學;學習記憶;大鼠
DOI:10.3969/j.issn.1005-5304.2016.08.016
中圖分類號:R285.5 文獻標識碼:A 文章編號:1005-5304(2016)08-0059-05
阿爾茨海默病(Alzheimers disease,AD)是一種危害老年人健康、影響老年人生活質量的神經退行性疾病。自20世紀90年代起我國步入老齡化社會,AD發病率逐年增高[1]。其主要臨床表現為記憶下降與認知功能障礙,病理學表現有腦細胞外β-淀粉樣蛋白(β-amyloid protein,Aβ)沉積形成的神經炎性斑(neuritic plaques,NP)與腦細胞內高度磷酸化的tau蛋白形成神經元纖維纏結(neurofibrillary tangles,NFTs)[2]。目前,由于AD病因不明,現有西藥只能緩解癥狀而不能針對病因進行治療,新藥的研發又處于瓶頸期難以突破。藥用植物學逐漸成為近年來的研究熱點。因此,從傳統中草藥中尋找對AD有療效的活性單體是一項具有廣闊前景與實際意義的工作。黃芩(Radix Scutellariae)為唇形科植物黃芩Scutellaria baicalensis Georgi的干燥根。《神農本草經》載黃芩有“諸熱黃膽,腸泄痢,逐水,下血閉,惡瘡疽蝕火瘍”功效。現代藥理研究表明,黃芩不僅有傳統的抗菌、抗炎等功效,還可作用于神經系統。黃芩水提物對腦出血大鼠血腦屏障損傷有一定的治療和保護作用[3]。黃芩中具有生物活性的黃酮類物質黃芩素可通過抗細胞凋亡、抗氧化等機制起到神經保護作用[4]。本實驗旨在利用蛋白組學技術對比黃芩素治療前后AD模型大鼠腦組織皮層及海馬組織蛋白表達譜的差異,利用雙向凝膠電泳(2-DE)、MALDI-TOF-MS/MS、數據庫查詢和生物信息學分析技術研究由Aβ1-40和黃芩素治療所導致的大鼠大腦皮層和海馬的差異蛋白,從亞細胞蛋白水平尋找證據,為黃芩素作為治療AD的臨床藥物提供更充分的實驗依據。
1 實驗材料
1.1 藥物
黃芩素,瑞士Fluka Bio Chemika公司,溶于生理鹽水,用NaOH溶液將pH值調至10。
1.2 動物
雄性SPF級SD大鼠36只,4月齡,體質量250~300 g,北京華阜康生物科技股份有限公司,許可證號SCXK(京)2009-0015。飼養于北京中醫藥大學東方醫院實驗中心SPF級動物實驗室,溫度(22±2)℃,相對濕度(55±5)%,人工光照時間為明暗各12 h。
1.3 主要試劑與儀器
Aβ1-40,美國Sigma-Aldrich公司,實驗前將其用無菌生理鹽水稀釋至10 mg/mL,4 ℃孵育48 h至Aβ1-40多聚體,4 ℃冰箱保存備用。0.25%TrypsinEDTA(美國Gibco公司),六氟異丙醇[阿拉丁試劑(中國)有限公司];二甲基亞砜(DMSO,北京索萊寶科技有限公司)。IPG緩沖液、蛋白酶抑制劑,美國Sigma公司;Morris水迷宮DMS-3,中國醫學科學院藥物所;CLASS100型超凈工作臺,珠海造鑫企業有限公司;MilliQ超純水系統,Millipore公司;IX71型倒置熒光相差顯微鏡、BX-60型倒置熒光相差顯微鏡數碼相機,日本Olympus公司;JY92-2D超聲波細胞破碎機,寧波新芝公司;ELX80酶標儀,美國Bio-Tek公司;1/1000A2005型精密電子天平,德國Saitorius公司;5415D型低溫高速多功能離心機,德國Eppendorf公司。
2 實驗方法
2.1 分組
實驗大鼠隨機分為對照組、模型組、黃芩素組,每組12只。
2.2 造模
參照文獻[5]方法,大鼠腹腔注射1%戊巴比妥鈉40 mg/kg麻醉,麻醉后利用腦立體定向儀固定大鼠頭部,分離骨膜暴露頭骨,按照大鼠腦立體定位圖譜,選擇雙側海馬CA1區為注射靶區,用牙科鉆打開顱骨,用5 μL微量進樣器顯微注射,5 min內緩慢勻速注入4 μL Aβ1-40多聚體并留針5 min,縫合傷口。
2.3 給藥
造模后4 d開始灌胃給藥,參照文獻[6-7]及前期實驗基礎,黃芩素組每日予黃芩素80 mg/kg灌胃,模型組和對照組每日予等量生理鹽水灌胃。灌胃體積均為2 mL,連續10 d。
2.4 Morris水迷宮實驗
造模給藥結束后,應用Morris水迷宮對大鼠的空間學習和記憶能力進行評價。水迷宮直徑150 cm,高50 cm,恒溫23 ℃。水池被平均分為4個象限,在其中一個象限中央放置距離水面2 cm、直徑15 cm的圓形平臺。正式測試前進行連續5 d的可視平臺實驗,平臺位于目標象限并使其頂部高于水面2 cm,記錄大鼠找到平臺的逃避潛伏期和總路線。再進行定位巡航實驗,目標象限為第三象限,平臺位于水面下2 cm,實驗連續進行5 d,大鼠從除目標象限外的任一點入水,測定大鼠找到平臺的逃避潛伏期和搜索距離。
2.5 雙向凝膠電泳
2.5.1 蛋白質樣品制備與純化 水迷宮測試結束后,將各組大鼠斷頭處死,冰上去除顱骨后,迅速取出腦組織,分離出皮層及海馬組織,精確稱重。將各組大鼠皮層和海馬組織放入組織勻漿器中,加1.5 mL雙向電泳組織裂解液[含7 mol/L尿素、2 mol/L硫脲、4%CHAPS、40 mmol/L Tris、65 mmol/L DTT和0.5%(V/V)Bio-Lyte,pH 3~10],勻漿處理,冰上靜置裂解20 min,液氮反復凍融3次,加RNase 50 ?g/mL、DNase 200 ?g/mL,4 ℃放置10 min,冰水混合物中進行超聲破碎(100 W,工作3 s,間歇2 s,15個循環),8000 r/min離心10 min×2次,去除未溶解雜質,再以12 000 r/min離心10 min,吸取上清液即為總蛋白溶液。采用Bradford法測定提取的蛋白質濃度,分裝后-70 ℃冰箱貯存備用或直接用于雙向電泳。
2.5.2 雙向電泳 2-DE參照Bio-Rad雙向電泳指南進行,沿聚焦盤邊緣緩慢加入300 μL含1 mg蛋白質樣品的水化上樣緩沖液(7 mol/L尿素,2 mol/L硫脲,4%CHAPS,65 mmol/L DTT,0.5%兩性電解質,0.001%溴酚藍),將膠條膠面朝下放入聚焦槽內,并覆蓋2 mL礦物油,設置程序后進行第一向等電聚焦。待膠條平衡30 min后進行第二向SDS-PAGE電泳。電泳結束后取出凝膠進行考馬斯亮藍G-250染色。
2.5.3 凝膠圖像分析 應用透射掃描儀對凝膠掃描獲取凝膠圖像,以對照組為參考膠,采用PDQuest8.0圖像分析軟件對凝膠圖譜依次進行點檢測、背景消減、標準化、匹配、建立平均凝膠,結合人工校正進行凝膠圖像分析。選取圖譜中蛋白點體積相對變化量大于2倍且P<0.05的蛋白點作為差異蛋白點。
2.6 差異蛋白質譜分析
將凝膠上差異明顯的10個蛋白點通過切膠、脫色、酶解、萃取等操作制備蛋白樣品。將樣品放入API4800串聯飛行時間質譜儀MALDI-TOF-MS/MS中分析,采用正離子模式和自動獲取模式進行數據采集,選擇強度最大的10個峰進行二級質譜鑒定,得到PMF指紋圖譜。應用GPS3.6和Mascot2.1軟件進行質譜數據分析和蛋白鑒定。
2.7 差異表達蛋白相互作用圖譜分析
將差異明顯8個蛋白上傳至String9.05蛋白-蛋白相互作用關系在線分析軟件(http://www.string-db.org),通過調節可信度和附加節點參數,獲得差異表達蛋白的相互作用圖譜,篩選中心節點蛋白。
3 統計學方法
采用SPSS17.0統計軟件進行分析。計量資料以—x±s表示,方差齊性者采用方差分析,組間比較采用LSD檢驗。P<0.05表示差異有統計學意義。
4 結果
4.1 大鼠Morris水迷宮測試結果
水迷宮定位巡航實驗結果顯示,與對照組比較,模型組大鼠第4日逃避潛伏期明顯延長,差異有統計學意義(P<0.05);與模型組比較,黃芩素組第4日逃避潛伏期明顯縮短,差異有統計學意義(P<0.05)。可視平臺實驗結果顯示,各組大鼠逃避潛伏期無明顯變化(P>0.05)。結果見表1。
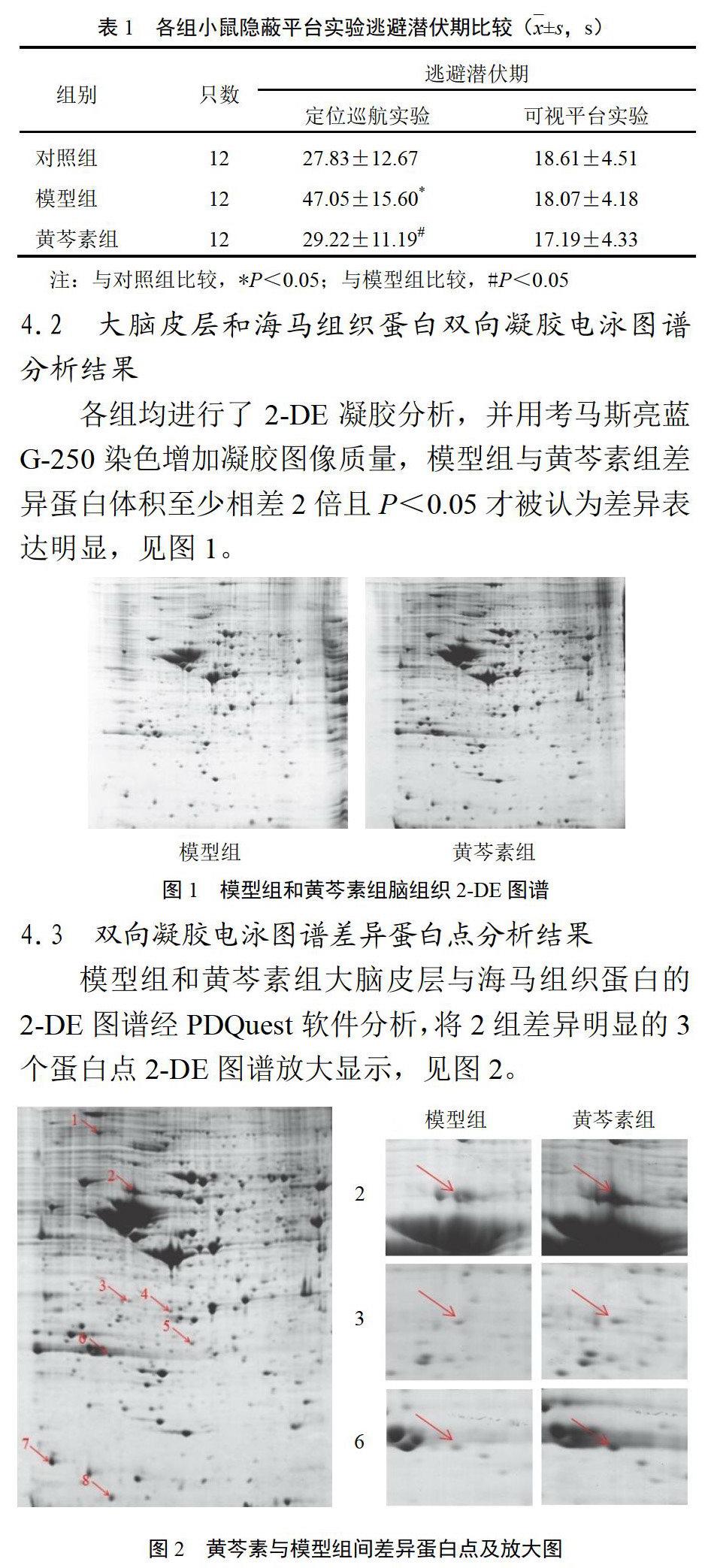
4.2 大腦皮層和海馬組織蛋白雙向凝膠電泳圖譜分析結果
各組均進行了2-DE凝膠分析,并用考馬斯亮藍G-250染色增加凝膠圖像質量,模型組與黃芩素組差異蛋白體積至少相差2倍且P<0.05才被認為差異表達明顯,見圖1。
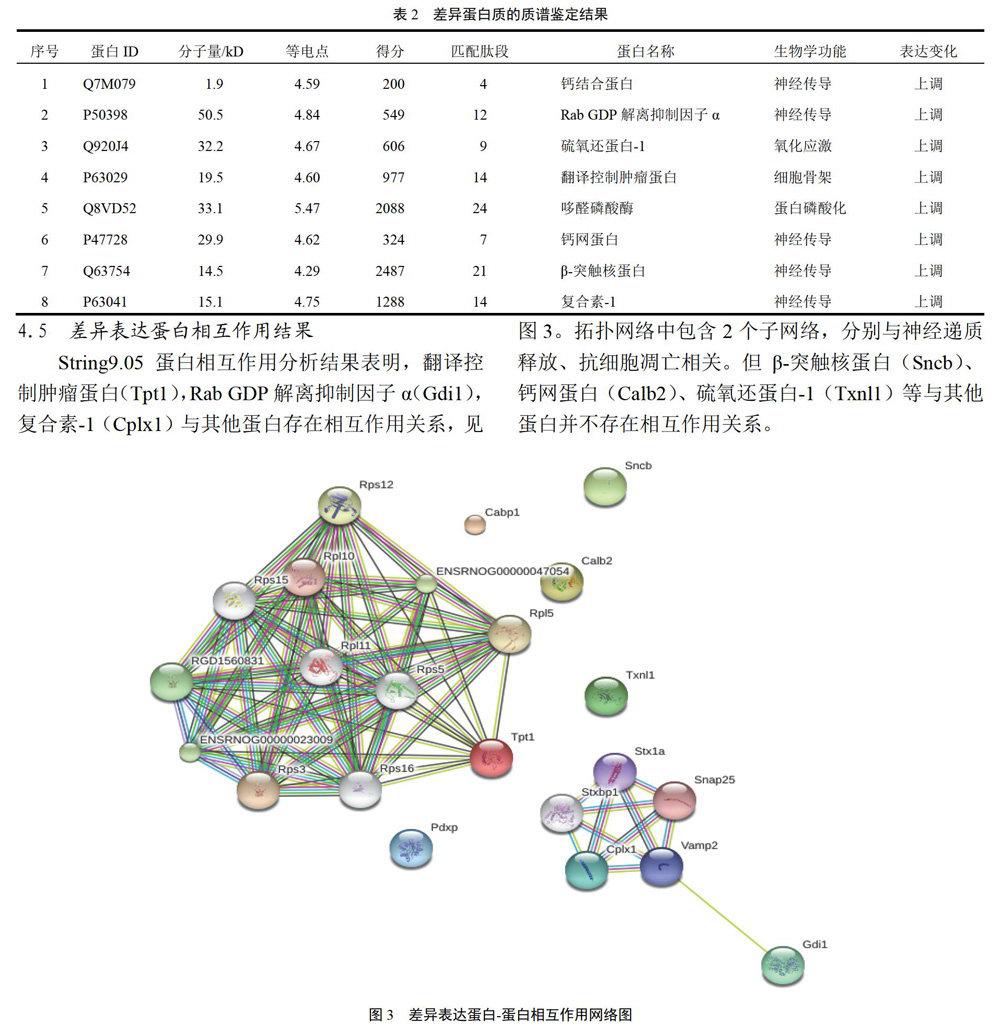
4.3 雙向凝膠電泳圖譜差異蛋白點分析結果
模型組和黃芩素組大腦皮層與海馬組織蛋白的2-DE圖譜經PDQuest軟件分析,將2組差異明顯的3個蛋白點2-DE圖譜放大顯示,見圖2。
4.4 差異蛋白點質譜鑒定結果
選取其中差異較為明顯的可能為關鍵功能蛋白的10個蛋白點進行質譜分析,通過檢索NCBI數據庫,共有8個蛋白得到成功鑒定,見表2。差異蛋白涉及4種生物學功能,其中與神經傳導關系最為密切,還與其他功能如抗細胞凋亡、抗氧化應激等相關。
4.5 差異表達蛋白相互作用結果
String9.05蛋白相互作用分析結果表明,翻譯控制腫瘤蛋白(Tpt1),Rab GDP解離抑制因子α(Gdi1),復合素-1(Cplx1)與其他蛋白存在相互作用關系,見圖3。拓撲網絡中包含2個子網絡,分別與神經遞質釋放、抗細胞凋亡相關。但β-突觸核蛋白(Sncb)、鈣網蛋白(Calb2)、硫氧還蛋白-1(Txnl1)等與其他蛋白并不存在相互作用關系。
5 討論
AD是老年期最常見的癡呆類型,是一種以進行性認知功能障礙和行為損害為特征的中樞神經系統退行性疾病。目前FDA批準AD治療藥物主要有膽堿酯酶抑制劑安理申和NMDA受體非競爭性拮抗劑美金剛,但其不能阻止疾病進展,也無法恢復已受損的認知功能。黃芩作為傳統中醫藥在臨床常被用于治療中風、感染性疾病、高血壓等疾病[8]。黃芩素是其中最主要的類黃酮提取物之一,已有研究表明,黃芩素可通過抑制氧化應激來減少細胞凋亡,同時減少對超氧化物歧化酶、丙二醛的激活來減輕Aβ25-35導致的神經病理學改變和認知功能損傷[9-10]。
AD發病機制的主流觀點是具有神經毒性的Aβ1-40沉積于腦內引起腦損傷。因此,本實驗利用Aβ1-40制備具有AD病理學特征的大鼠模型。利用Morris水迷宮實驗評估造模是否成功、黃芩素的治療效果,發現Aβ對大鼠的空間學習與記憶功能的損傷較大,黃芩素可顯著改善這種損傷。本實驗利用蛋白組學研究方法成功鑒定出黃芩素治療AD大鼠模型大腦皮質和海馬組織8種蛋白表達上調,是黃芩素預防和治療AD的直接靶標。
本研究驗證的蛋白可能與以下機制相關:Gdi1主要通過調節Rab小G蛋白的神經遞質釋放起到神經保護作用[11]。Sncb上調可通過抑制α-Synuclein聚集改善神經元變性,緩解神經退行性病變[12]。黃芩素上調Calb2可能作為載體蛋白的內質網分子伴侶使淀粉樣蛋白保持溶解狀態,從根源上減少Aβ沉積[13-14]。Trx-1作為體內重要的抗氧化蛋白,可通過清除過量氧自由基,修復過氧化的巰基蛋白,調節轉錄因子活性,抑制細胞凋亡以及調控胞內氧化還原平衡,發揮對神經元的保護作用[15]。Cplx1是突觸前結構中重要的神經遞質釋放調節蛋白,Tannenberg等[16]發現AD患者腦中Cplx1顯著下降,Cplx1的治療機制可能與改變突觸可塑性有關[17]。Tpt1在癌細胞和其他分裂活躍細胞中表達水平較高[18],而在腦等停止分裂的組織中低表達[19]。以往研究在對AD死者尸檢時發現,一些區域的腦細胞中翻譯控制腫瘤蛋白(TCTP)水平下降,細胞凋亡增加,故黃芩素可能是通過上調TCTP發揮抗細胞凋亡作用保護神經元。
綜上所述,本實驗利用蛋白組學研究方法檢測黃芩素治療AD大鼠模型大腦皮質和海馬組織蛋白,發現黃芩素可上調神經保護相關的靶蛋白,作用機制可能與神經傳導、氧化應激、細胞骨架等有關。但黃芩素對AD治療作用及其分子機制仍需要進一步研究,以深入探討其神經保護機制,為黃芩素作為AD治療藥提供實驗依據。
參考文獻:
[1] 于大林,肖軍.阿爾茨海默病的流行病學調查現況[J].實用醫院臨床雜志,2011,8(3):152-155.
[2] BLENNOW K, DE LEON M J, ZETTERBERG H, et al. Alzheimer's disease[J]. Lancet,2006,368(9533):387-403.
[3] SHIN J W, KANG H C, SHIM J, et al. Scutellaria baicalensis attenuates blood-brain barrier disruption after intracerebral hemorrhage in rats[J]. Am J Chin Med,2012,40(1):85-96.
[4] 周錫欽,梁鴻,路新華,等.中藥黃芩主要黃酮類成分及其生物活性研究[J].北京大學學報(醫學版),2009,41(5):578-584.
[5] SHAERZADEH F, M0TAMEDI F, MINAI-THRANI D, et al. Monitoring of neuronal loss in the hippocampus of Ab-injected rat:autophagy, mitophagy, and mitochondrial biogenesis stand against apoptosis [J]. Neuromol Med,2014,16(1):175-190.
[6] KIM Y O, LEEM K, PARK J, et al. Cytoprotective effect of Scutellariabaicalensis in CA1 hippocampal neurons of rats after global cerebral ischemia[J]. J Ethnopharmacol,2001,77(2/3):183-188.
[7] GAO Y, LU J, ZHANG Y, et al. Baicalein attenuates bleomycin- induced pulmonary fibrosis in rats through inhibition of miR-21[J]. Pulm Pharmacol Ther,2013,26(6):649-654.
[8] 宋琳莉,孟慶剛.黃芩的藥理作用研究進展[J].中華中醫藥學刊, 2008,26(8):1676-1678.
[9] LIU C, WU J, GU J, et al. Baicalein improves cognitive deficits induced by chronic cerebral hypoperfusion in rats[J]. Pharmacol, Biochemistry Behav,2007,86(3):423-430.
[10] WANG S Y, WANG H H, CHI C W, et al. Effects of baicalein on beta-amyloid peptide-(25-35)-induced amnesia in mice[J]. Eur J Pharmacol,2004,506(1):55-61.
[11] ISHIZAKI H. Role of rab GDP dissociation inhibitor alpha in regulating plasticity of hippocampal neurotransmission[J]. Proc Natl Acad Sci USA,2000,97(21):11587-11592.
[12] YAMIN G, MUNISHKINA L A, Karymov M A, et al. Forcing nonamyloidogenic beta-synuclein to fibrillate[J]. Biochemistry, 2005,44(25):9096-9107.
[13] ERICKSON R R, DUNNING L M, OLSON D A, et al. In cerebrospinal fluid ER chaperones ERp57 and calreticulin bind β-amyloid[J]. Biochem Biophys Res Commun,2005,322(1):50-57.
[14] JOHNSON R J, XIAO G, SHANMUGARATNAM J, et al. Calreticulin functions as a molecular chaperone for the β-amyloid precursor protein[J]. Neurobiol Aging,2001,22(3):387-395.
[15] 趙麗娟,孫茂民.硫氧還蛋白與阿爾茨海默病的研究進展[J].中國醫療前沿,2010,5(1):18-21,23.
[16] TANNENBERG R K, SCOTT H L, TANNENBERG A E, et al. Selective loss of synaptic proteins in Alzheimer's disease:evidence for an increased severity with APOE varepsilon4[J]. Neurochem Int, 2006,49(7):631-639.
[17] 黃玲.SAMP8小鼠海馬突觸活性帶蛋白complexin及syntaxin1含量與年齡相關性空間學習記憶損害的關系[D].合肥:安徽醫科大學,2012.
[18] 呂素芳,郭廣君,蔡永萍.翻譯控制腫瘤蛋白(TCTP)研究進展[J].科學技術與工程,2006,6(4):424-428.
[19] ANDREE H, THIELE H, FAHLING M, et al. Expression of the human TPT1 gene coding for translationally controlled tumor protein (TCTP) is regulated by CREB transcription factors[J]. Gene,2006, 380(2):95-103.

