應用microCT技術對中藥干預去卵巢小鼠骨組織微結構的分析
張文明 鄧紅敏 張媛媛 黃云梅 黃美雅 林燕萍*
1.福建中醫藥大學中西醫結合研究院,福州 350108 2.河南省林州市中醫院,安陽 456550 3.江西省新余市中醫院,新余 338000
絕經后骨質疏松癥(postmenopausal osteoporosis,PMOP)是原發性骨質疏松癥最常見的一種類型,因骨密度下降、骨組織顯微結構退化、骨脆性增加[1],PMOP骨折率約為正常人的4倍[2]。研究該病的發病機制以及治療藥物,越來越受到人們的重視。以往PMOP的形態學評價方法只有組織形態學、形態計量學等,隨著影像學的進步,能更為準確、高效反映骨組織結構的顯微CT(microCT),越來越多地應運于PMOP的研究中。本文將這一新的體視學檢測方法運用于中藥藥物治療評價中,為PMOP的藥效學評價提供了新途徑。
1 材料與方法
1.1 動物
4周齡C57雌性小鼠,清潔級,20 g±2 g,30只,中科院上海實驗動物中心提供,動物合格證號:SCXK(滬)2007-0005。
1.2 藥物
健骨顆粒,由煅狗骨、淫羊藿、山茱萸、黨參、山藥等藥物組成,原藥材統一由福建省藥材公司提供,福建中醫藥研究院中試車間加工制備,每克顆粒含原生藥2.9 g。健骨顆粒小鼠灌胃劑量為2 g/(kg·d)(每只小鼠每天灌胃藥以生理鹽水0.5 ml溶解,1次/d)。
1.3 儀器
microCT(ZKKS-MCT-Sharp-I,廣州中科愷盛醫療科技有限公司);萬能材料試驗機(IG-A1000N型,日本島津公司)。
1.4 方法
1.4.1動物造模及藥物干預:在福建中醫藥大學實驗動物中心SPF級動物房適應性飼養一周后其隨機分成分為三組(假手術一組10只、去卵巢兩組各10只),采用卵巢切除法建立PMOP小鼠模型:卵巢切除小鼠經腹腔注射戊巴比妥麻醉(給藥濃度為40 mg/kg),腹位固定,備皮,3%碘伏消毒,背部中下部肋緣下1 cm與脊柱旁開1 cm交界處行0.5 cm縱行切口,結扎輸卵管和血管,將卵巢完整切除,逐層關閉切口。假手術組只切除卵巢周圍脂肪,不切除卵巢。術后3 d青霉素(20×104IU/kg)常規腹腔注射預防感染。兩組去卵巢小鼠手術1周后,按照人(臨床健骨顆粒成人常規給藥劑量為3 g/次,3次/d。每克顆粒含原生藥2.9 g)與動物間體表面積折算的等效劑量換算公式計算出小鼠的給藥劑量,分別灌服健骨顆粒2 g/kg/d(以生理鹽水0.5 ml溶解)和生理鹽水0.5 ml/d;假手術組用生理鹽水0.5 ml/d灌胃,連續2個月。
1.4.2檢測方法及觀察指標
1.4.2.1骨組織微結構體視學:三組小鼠經戊巴比妥鈉腹腔注射麻醉后,取出每只小鼠左脛骨,固定在microCT載物臺上對脛骨近端進行掃描。以 360°掃描角度、10 μm 的掃描分辨率沿小鼠脛骨長軸方向掃描脛骨近端, 獲取連續的平面μCT 圖像。掃描完成后在主機上選出生長板下1 mm和脛骨近端1.5 mm的區域為感興趣區域(range of interests ROI),進行骨小梁三維圖像重建,利用機載軟件分析,主要檢測參數如下:骨密度參數—骨礦物質含量BMC(Bone Mineral Content)、骨密度或骨礦物質密度BMD(Bone Mineral Density,BMD)、組織礦物含量TMC(Tissue Mineral Content)、組織礦物質密度TMD(Tissue Mineral Density)、骨表面積BS(Bone Surface)、骨體積BV(Bone Volume);骨結構參數—骨表面積和骨體積的比值BS/BV、骨表面積和組織體積的比值BS/TV、選取ROI體積TV(Total Volume)、相對骨體積或骨體積分數BV/TV、骨小梁數量Tb.N(Trabecular Number)、骨小梁分離度Tb.Sp(trabecular Separation/apacing)、骨小梁厚度Tb.Th(Trabecular Thickness)、結構模型指數SMI(Structure Model index)、各向異性程度DA(Degree of Anisotropy)。
1.4.2.2骨生物力學:三組小鼠經戊巴比妥鈉腹腔注射麻醉后,取出每只小鼠右脛骨,在萬能材料試驗機上完成三點抗壓最大載荷檢測(單位:kN)。小鼠脛骨跨距為30 mm,萬能材料機應力加載速率為0.5 mm/min,至脛骨折斷瞬間電腦自動采集到三點抗壓最大載荷。每組采集10只小鼠右側脛骨最大抗彎載荷,取平均值。
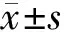
2 結果
2.1 microCT骨量及骨微結構參數
骨量參數(表1):與假手術組比較,去卵巢組BMC、BMD、Mean、BV、BS指標顯著下降(P<0.01),TMC下降(0.01
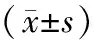

組別nMean(1)S.D(1)BV(mm3)BS(mm2)BMC(g)TMC(g)BMD(mg/cm3)TMD(mg/cm3)假手術組10236±23.0▲▲135±11.00.05±0.006▲ 2.53±0.26▲0.07±0.007▲▲0.25±0.004236±23.0 ▲▲493±29.0去卵巢組1068.9±10.8##126±9.64 0.02±0.004##1.37±0.15##0.02±0.003##0.01±0.002#68.9±10.8##432±11.8去卵巢中藥組10141±18.1△△120±11.10.03±0.0041.67±0.170.04±0.005△△ 0.01±0.002141±18.1△△436±14.3
注:與中藥組比較,▲0.05>P>0.01,▲▲P<0.01; 與假手術組比較,#0.05>P>0.01,##<0.01;與去卵巢組比較,△0.05>P>0.01,△△P<0.01
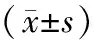

組別nBV/TV (%)BS/BV(1/mm)BS/TV(1/mm)Tb.N (1/mm)Tb.Sp(μm)Tb.Th(μm)SMI(1)DA(1)假手術組1016.2±2.12▲52.7±2.048.40±0.86▲4.20±0.43▲213±57.0▲38.3±1.461.74±0.120.83±0.04去卵巢組107.57±1.22##62.7±4.294.53±0.51##2.27±0.25##440±57.0##32.8±2.602.22±0.11#0.73±0.04去卵巢中藥組1010.1±1.2555.8±3.105.53±0.572.76±0.28346±41.236.4±1.982.02±0.100.77±0.02
注:與中藥組比較,▲0.05>P>0.01,▲▲P<0.01;與假手術組比較,#0.05>P>0.01,##<0.01
2.2 microCT二維/三維圖像
去卵巢組較假手術組骨小梁數量明顯減少,稀疏、斷裂,形態細小、不連續呈扭曲或斷裂狀等,靠近生長板的初級和次級網狀骨小梁幾乎消失(圖1、2),骨皮質薄,骨髓腔增大(圖3、4)。去卵巢中藥組與去卵巢組比較,骨小梁數量、寬度、長度、形態和分布部分恢復、密度和聯結性增加,但還不能恢復到假手術組水平(圖1、2),中藥干預后皮質骨面積增加,骨髓腔縮小,基本恢復到假手術組水平(圖3、4)。

圖1 各組小鼠脛骨上段microCT X-Y三維圖(上排)、三維剖面圖(下排)。(從左向右為:假手術組,去卵巢中藥干預組,去卵巢組,下同)Fig.1 Micro CT X-Y 3-dimensional image of mouse tibia (upper row), cross-section image (lower row).From left to right: sham group, OVX intervention group, OVX group, the same below)

圖2 小鼠脛骨上段microCT X-Y剖面二維圖Fig.2 Micro CT X-Y 2-dimensional image of mouse tibia

圖3 小鼠脛骨上段microCT Y-Z三維圖(上排)、剖面二維圖(下排)Fig.3 Micro CT X-Y 3-dimensional image of mouse tibia (upper row), cross-section image (lower row)

圖4 小鼠脛骨上段microCT X-Z三維圖(上排),剖面二維圖(下排)Fig.4 Micro CT X-Y 3-dimensional image of mouse tibia (upper row), cross-section image (lower row).
2.3 骨生物力學三點抗壓最大載荷
小鼠右脛骨三點抗壓最大載荷(單位:N)假手術組與去卵巢組、假手術組與去卵巢中藥組相比均有顯著差異(P<0.01),去卵巢中藥干預組與去卵巢組相比有差異(0.01 圖5 各組小鼠右脛骨三點抗壓試驗最大載荷(單位:kN):假手術組與去卵巢組、去卵巢中藥組相比P<0.01,去卵巢中藥干預組與去卵巢組相比Fig.5 Three-point maximum load test of mouse right tibia (unit: kN).Sham group VS OVX group, P<0.01; OVX intervention group VS OVX group, 0.01 嚙齒目動物(rodents)是PMOP模型最常用的動物,大鼠模型研究基本成熟[3],更多運用于骨結構代謝研究,但大鼠不易發生自發脆性骨折,這對PMOP骨生物力學的研究產生了影響。最近研究證實C57BL/6J小鼠峰值骨量低[4],是目前證實可隨増齡出現脆性骨折的動物[5]。用小鼠進行骨代謝遺傳因素的研究,已經成為目前骨質疏松研究領域的前沿課題[6]。本實驗中,除BS/BV外,去卵巢組和假手術組骨量和骨微結構各項指標均具有明顯差異(P<0.01),顯示出小鼠PMOP模型的成功建立。但是骨量和骨微結構的差異并不代表骨強度的差異,骨的組織形態結構的變化,能否導致骨的強度和承重功能的改變,需要骨生物力學檢測。通常測定藥物對骨生物力學性能的影響,能反映藥物對骨質疏松的骨質量、骨質疏松性骨折作用的評價。本實驗三組小鼠右脛骨三點抗壓最大載荷試驗各組間差異有統計學意義(P<0.05)(圖5)。由此我們認為,小鼠PMOP模型更與人類PMOP模型接近。 可靠的循證醫學證據已經表明無論哪種西藥,在治療PMOP中都不可避免存在副作用[7],與此同時,中醫藥卻顯現出抗絕經后骨質疏松的獨特優勢,特別是以補腎、健脾為代表的健骨顆粒對防治PMOP有明確效果[8],其主要成分是:煅狗骨、淫羊藿、山茱萸、黨參、山藥等。臨床上在增加骨強度,緩解骨疼痛,降低骨折率上有良好療效[9]。本實驗用健骨顆粒對PMOP小鼠模型進行干預,從骨組織形態學和生物力學方面闡明補腎健脾中藥健骨顆粒的抗骨質疏松作用。實驗結果表明,該中藥在提高骨量方面效果顯著,其中骨礦物質含量BMC和骨密度BMD兩項指標與模型組相比,具有極顯著差異(P<0.01)(表1),說明健骨顆粒可提升骨量,從而增加骨密度。在改善骨小梁結構上也具有顯著作用(圖1、2、3、4),表明健骨顆粒在改善骨質疏松方面還表現在對骨小梁的形態進行重建。 3.3.1microCT骨量及骨微結構參數在本實驗中的應用 在骨量指標中,骨礦物質含量(BMC)、骨密度或骨礦物質密度(BMD),是最能代表骨含量的參數,本實驗結果顯示假手術組和去卵巢組相比BMD、BMC以及骨表面積(BS)、骨體積(BV)等指標有極顯著差異(P<0.01)(表1),說明造模2個月即可使小鼠骨量嚴重丟失。在骨微結構中,Tb.N代表了給定長度內骨組織與非骨組織的交點數量,發生骨質疏松時,Tb.N的值減少;Tb.Sp為骨小梁之間的髓腔寬度,其增加提示骨吸收增加,可能發生骨質疏松。本實驗中假手術組和去卵巢組相比,Tb.N和Tb.Sp均差異明顯(P<0.01)(表2),說明去卵巢2月后對小鼠的骨小梁數量和密度均造成巨大影響。Tb.Th作為骨小梁平均厚度的參數,發生骨質疏松時,Tb.Th值減小;SMI用來定義骨小梁板狀和桿狀的程度,發生骨質疏松癥時,骨小梁從板狀向桿狀轉變,SMI數值增加,本實驗中去卵巢組較假手術組SMI有明顯提高(P<0.05),說明骨小梁的形態變化是去卵巢后骨量丟失同時發生的又一骨質疏松特征。在骨質疏松初期,承重骨小梁的DA增加,DA是ROI(感興趣區)平均截距長度橢圓中長徑和短徑的比值,隨骨質疏松加劇,DA會減小,本實驗中Tb.Th、BS/BV和DA從指標變化上來看有趨勢,但是統計學意義不明顯,可能與造模時間短有關,也可能說明這些指標的非特異性,更可能說明去卵巢造成的斷崖式雌激素劇減還不能很好模擬人類絕經期雌激素呈斜坡式下降的狀態。 3.3.2microCT在骨質疏松藥效學評價中的優勢 在PMOP診斷中骨密度檢測不能反映骨微結構變化,難以完整體現骨質疏松病理特征;中醫藥治療PMOP的藥效學評價需要全面和準確的評價方法。骨組織形態計量學可從靜態、動態學參數定性和定量分析骨量、骨微結構,但仍然存在標本獲取的創傷性、制作過程的繁瑣性等缺陷。比其更為準確、高效反映骨組織結構的顯微CT(Micro-CT)。所測得的參數誤差小,且操作簡便,定位準確,能獲得真正各項同性的容積圖像,提高空間分辨率和采集圖像的速度,最高檢測精度達到5μm以下,在本實驗中從掃描圖像直觀和清晰地觀察到中藥干預模型后,松質骨的骨小梁數量、寬度、長度部分恢復,密度和聯結性增加(圖1、2);而中藥干預后皮質骨面積增加,骨髓腔縮小,基本恢復到假手術組水平(圖3、4)。本實驗采集數據精度高,數據采集的同一性使得后期統計結果更加準確、科學。由于不需樣品制備,且對活體和離體標本均可掃描[10],本實驗因為局限于動物飼養和檢測設備的空間距離較大,因此采用離體標本,即便如此,仍較傳統的骨組織計量學標本處理省時省力,節約了大量成本,標本也可反復利用或作它途,極具經濟性。骨質疏松藥效學評價包括藥物對單位面積(二維結構)或單位體積(三維結構)骨量、骨組織結構、骨礦密度、骨有機物含量、骨生物力學性能的變化,這些指標能定量闡明藥物是否對PMOP病理特征的骨量、骨組織微結構、骨脆性、骨折危險性等有療效[11],因為治療骨質疏松的最終目的是預防骨折[12]。本實驗采取microCT加骨生物力學的藥效學評價方式即是基于以上考量。從實驗結果上看,去卵巢后,microCT所檢測到的去卵巢模型以及健骨顆粒干預模型后骨組織骨量和骨微結構的變化趨勢,與以往的藥效學報道一致[8],這說明了microCT在PMOP藥效學評價中的科學性。 綜上,去卵巢2月后成功建立小鼠PMOP模型;健骨顆粒抗骨質疏松作用明顯,主要通過增加骨量和改善骨小梁微結構來最終提高骨強度;microCT對骨質疏松參數分析簡潔、高效,圖像多維、全面,與傳統的檢測方法相比,具有一定的優勢。
3 討論
3.1 PMOP小鼠模型的建立與評價
3.2 中藥干預PMOP
3.3 microCT在PMOP模型研究中的應用

