2型糖尿病患者血清chemerin水平與骨密度相關性研究
施良 張浩 李林 徐萍 高健青 周建明 毛朝明*
1.江蘇大學附屬江濱醫院核醫學科,鎮江 212001 2.江蘇大學附屬江濱醫院急診內科, 鎮江 212001 3.江蘇大學附屬江濱醫院內分泌科, 鎮江 212001
糖尿病患者常合并骨質疏松或骨代謝異常,2型糖尿病和骨質疏松癥關系已被廣泛研究,但兩者之間的關系仍無定論[1]。目前多數研究認為糖尿病和骨質疏松有共同的病理生理過程—慢性免疫炎癥反應[2]。通過對糖尿病和骨質疏松機制的研究發現,糖尿病患者通過對機體眾多炎癥介質及細胞因子進行調節,可抑制成骨細胞分化,促進破骨細胞分化,進而減少骨形成并增加骨吸收[3]。chemerin 是一種新發現的脂肪細胞因子,迄今研究表明,chemerin主要表達在白色脂肪組織、肝、卵巢、骨組織等組織中[4]。其表達水平與炎癥、肥胖、代謝綜合征、糖尿病、冠心病和腫瘤發病有著重要的關系[5,6]。國外學者研究發現:chemerin及其受體表達于人關節軟骨細胞內,并可以誘導趨化因子CCL2和TLR4信號通路促進炎癥介質的釋放,其表達水平與IL-6、超敏C反應蛋白及TNF-α等密切相關[7]。提示chemerin可能與骨代謝有關,并在骨質疏松發生的病理過程中發揮重要作用。
本試驗研究旨在探討2型糖尿病患者血清chemerin水平與骨密度及相關因素的關系,以進一步揭示糖尿病患者發生骨質疏松的病理生理學機制。并為糖尿病和骨質疏松之間關系研究及 chemerin抗體治療骨質疏松提供一定理論依據。
1 對象與方法
1.1 研究對象
選取2012年1月至2014年12月我院內分泌科住院的2型糖尿病患者150人。根據WHO骨質疏松診斷標準(DEXA)[8]分為三組:2型糖尿病骨量正常組42例;2型糖尿病骨量減少組50例;2型糖尿病骨質疏松(OP)組58例。選取同期在我院體檢中心行體檢健康人群30名為對照組。排除標準:糖尿病急性并發癥者,使用噻唑烷二酮類、激素類、調脂類、鈣片等影響骨代謝藥物者, 其它影響骨代謝的內分泌疾病(如甲狀腺疾病、甲狀旁腺疾病、庫欣病等),合并其他系統性骨病、惡性腫瘤、風濕免疫性疾病、嚴重肝腎功能疾病、心血管疾病、血液系統疾病者,妊娠及哺乳者,有嗜煙、酒、藥物等不良生活習慣者,近期有急慢性感染者,近2周臥床靜息制動者。本研究經醫院倫理委員會批準,所有受試者均簽署知情同意書。
1.2 研究方法
所有研究對象禁食12 h,清晨空腹抽取肘靜脈血6 ml, 3 000 r/min離心20 min,分離血清至Eppendorf管,置于-80℃冰箱保存待檢。化學發光法檢測血清TNF-α水平;酶聯免疫吸附法(ELISA)檢測血清chemerin(美國Millipore 公司試劑盒)及IL-6水平(武漢博士德生物工程有限公司)。詳細記錄患者性別、年齡、身高、體重、糖尿病病程等相關資料,計算體重指數(body mass index,BMI),并測定空腹血糖(fasting blood glucose,FBG),采用柱狀層析法測定糖化血紅蛋白(glycosylated hemoglobin,HbA1c),由我院檢驗科完成。
采用美國GE公司生產的Lunar DPX-NT雙能X線骨密度儀檢測正位腰椎(腰1-4)骨密度,取平均值;雙側髖部(股骨頸、大轉子、粗隆間)骨密度,取平均值。每日測量之前均進行機器校正。儀器測量變異系數(腰椎和股骨頸)分別是0.8%和1.6%。
1.3 統計學方法
2 結果
2.1 各組一般資料比較
2型糖尿病骨量正常組、減少組及骨質疏松組間在年齡、性、身高、BMI、HbA1c水平、糖尿病病程方面比較均無統計學差異(P>0.05)。三組患者FBG及HbA1c水平均高于正常組,差異均有統計學意義(P<0.05)。糖尿病骨質疏松組BMI高于正常組,差異有統計學意義(P<0.05)。見表1。
2.2 各組血清chemerin、TNF-α及IL-6水平比較
與對照組比較,糖尿病骨量正常組、減少組及骨質疏松組血清chemerin水平升高,差異均有統計學意義;其中糖尿病骨質疏松組升高最明顯(P<0.01)。糖尿病骨質疏松組血清chemerin水平高于糖尿病骨量正常組、減少組,差異有統計學意義(P<0.05)。與對照組比較,糖尿病骨量減少組及骨質疏松組血清TNF-α水平升高,差異有統計學意義(P<0.05)。糖尿病骨量正常組與對照組TNF-α水平差異無統計學意義(P>0.05)。糖尿病骨質疏松組血清TNF-α水平高于糖尿病骨量正常組、減少組,差異有統計學意義(P<0.05)。與對照組比較,糖尿病骨質疏松組IL-6水平顯著性升高(P<0.05);糖尿病骨量正常組及減少組IL-6水平亦高于對照組,但差異無統計學意義(P>0.05)。見表1。
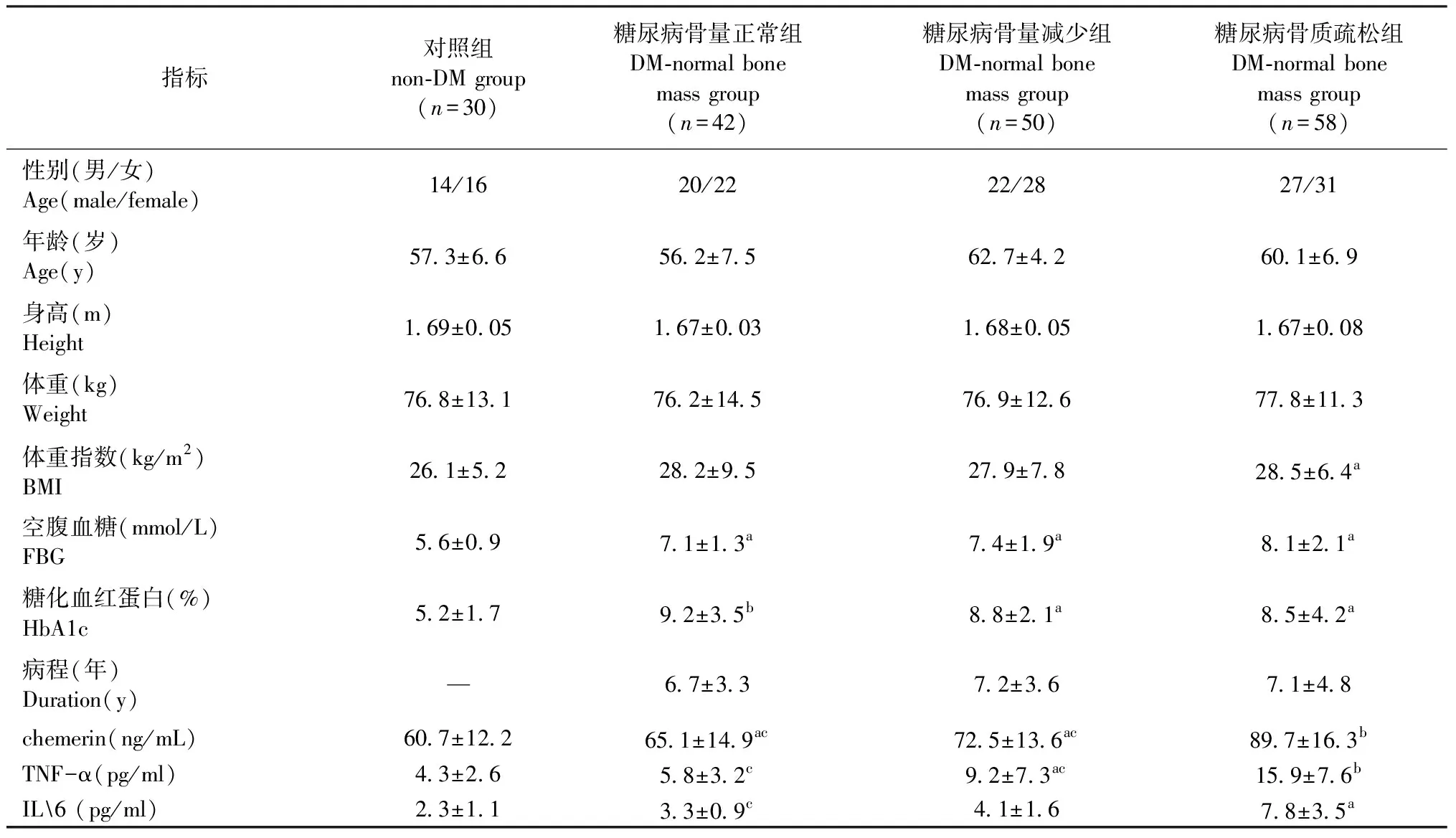
指標對照組non-DM group(n=30)糖尿病骨量正常組DM-normal bone mass group(n=42)糖尿病骨量減少組DM-normal bone mass group(n=50)糖尿病骨質疏松組DM-normal bone mass group(n=58)性別(男/女)Age(male/female)14/1620/2222/2827/31年齡(歲)Age(y)57.3±6.656.2±7.562.7±4.260.1±6.9身高(m)Height1.69±0.051.67±0.031.68±0.051.67±0.08體重(kg)Weight76.8±13.176.2±14.576.9±12.677.8±11.3體重指數(kg/m2)BMI26.1±5.228.2±9.527.9±7.828.5±6.4a空腹血糖(mmol/L)FBG5.6±0.97.1±1.3a7.4±1.9a8.1±2.1a糖化血紅蛋白(%)HbA1c5.2±1.79.2±3.5b8.8±2.1a8.5±4.2a病程(年) Duration(y)—6.7±3.37.2±3.67.1±4.8chemerin(ng/mL)60.7±12.265.1±14.9ac 72.5±13.6ac 89.7±16.3bTNF-α(pg/ml)4.3±2.6 5.8±3.2c9.2±7.3ac 15.9±7.6bIL6 (pg/ml)2.3±1.13.3±0.9c4.1±1.6 7.8±3.5a
a:與對照組比較P<0.05;b:與對照組比較P<0.01;c:與糖尿病骨質疏松組比較P<0.05
2.3 血清chemerin與各臨床指標的相關性分析
血清chemerin水平與TNF-α、BMI、HbA1c、病程呈正相關,與腰椎(L1-4)骨密度平均值呈負相關。見表2。
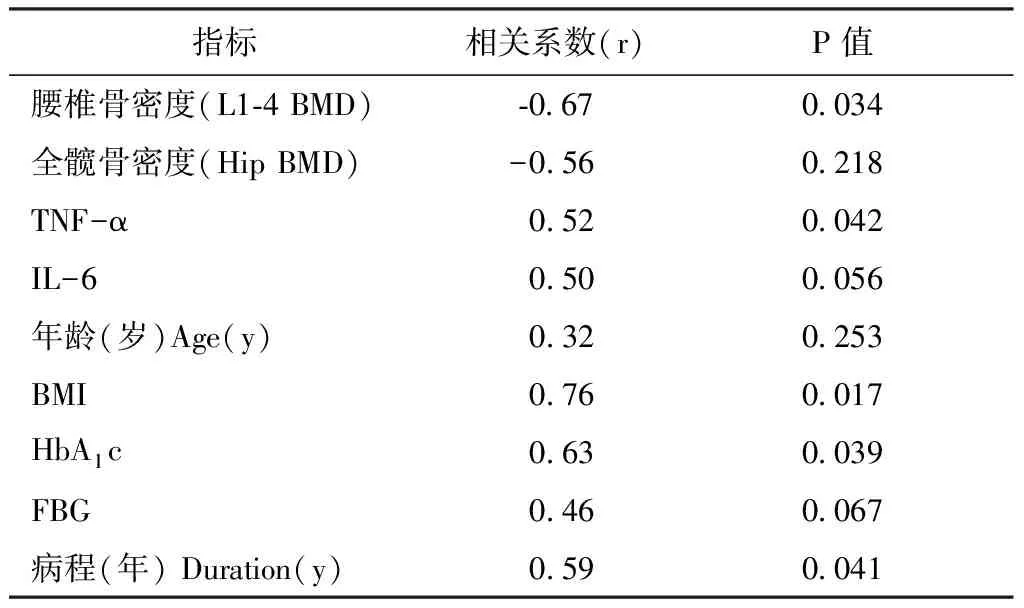
表2 血清chemerin水平與各臨床指標的相關性分析Table 2 Correlation analysis of serum Chemerin level and clinical parameters
3 討論
近年來,2型糖尿病(type 2 diabetes mellitus,T2DM)和骨質疏松癥之間的關系被廣泛研究,大多學者認為糖尿病增加患者骨質疏松和骨折的發生率[9],但兩者關系仍無定論。Abdulameer等薈萃分析顯示[10]:大多數文獻(26篇)報道T2DM患者BMD增加,部分文獻(13篇)報道T2DM患者BMD降低,少量文獻(8篇)報道T2DM患者BMD正常或與對照組比較無顯著性變化。糖尿病導致骨質疏松的發病機制不明,目前認為可能與高血糖、炎癥反應和氧化應激等因素相關[11]。DM患者長期血糖控制不佳,高血糖可以通過多種途徑引起骨代謝異常。一方面,高血糖導致滲透性利尿致使鈣、磷、鎂等礦物質排泄增加,同時高尿糖又阻礙腎對鈣、鎂、磷的重吸收,致使血清鈣、磷等礦物質濃度降低,骨質脫鈣,骨密度下降[12]。另一方面,長期高血糖狀態導致DM患者體內糖基化終產物(Advanced Glycation End Products, AGEs) 蓄積,AGEs 可影響骨蛋白及骨細胞分化,直接或間接導致骨形成減少,骨質量下降,骨脆性增加,引發骨質疏松[13]。此外,糖尿病導致微血管病變會降低骨血流量,導致骨脆性增加、骨量流失[12]。
TNF-α通過激活T細胞,一方面使之分泌大量核因子-κ B 受體活化因子配體(Receptor Activator for Nuclear Factor-κ B Ligand,RANKL),RANKL與破骨細胞表面RANK 識別結合并激活破骨細胞,導致骨吸收增加[14];另一方面,激活的T細胞分泌IL-1、IL-6、IL-11、IL-17等炎癥因子,通過Wnt/β-catenin 信號通路調節破骨細胞分化成熟。IL-1、IL-6等炎癥因子可通過激活P38MAPK、NF-κB等一系列細胞內信號通路激活破骨細胞,誘導骨髓干細胞向破骨細胞分化,骨吸收效應增強,導致骨質疏松[15]。李糧等研究發現[16]:絕經后2型糖尿病患者BMD 與絕經年限、TNF-α及IL-6 密切相關。本研究發現:糖尿病骨量正常組、減少組及骨質疏松組血清TNF-α及IL-6水平均高于對照組,其中糖尿病骨質疏松組升高最明顯。因此有理由推斷,炎癥反應可能是介導了糖尿病患者骨質疏松的發生。
脂肪因子一直是內分泌代謝性疾病的研究熱點,近年來已有多項研究報道脂肪因子adiponectin、leptin、resistin與骨密度存在相關性并直接或間接參與骨代謝活動。chemerin是一種新的脂肪因子,于2007年由Goralski等發現[4]。它是一種多靶器官、多功能的細胞因子,具有多種生物學特性[17,18]。其表達水平與炎癥、肥胖、糖尿病、代謝綜合征、骨質疏松等疾病有密切聯系[19]。Berg等[20]研究發現,chemerin與其相應受體結合后可進一步激活炎癥信號,導致炎癥因子和基質金屬蛋白酶的釋放。近年來,有研究證實,chemerin的表達和分泌促進骨髓間充質細胞向脂肪細胞分化[21]。沉默chemerin基因則阻礙脂肪細胞分化,增加成骨細胞骨相關活性基因的表達并促進礦化作用[22]。本研究發現:與對照組比較,糖尿病骨量正常組、減少組及骨質疏松組血清chemerin水平升高,差異均有統計學意義;其中糖尿病骨質疏松組升高最明顯(P<0.01)。并且糖尿病骨質疏松組血清chemerin水平亦明顯高于糖尿病骨量正常組、減少組(P<0.05)。相關性分析顯示:血清chemerin水平與TNF-α、BMI、HbA1c、病程呈正相關,與腰椎(L1-4)骨密度平均值呈負相關。因此,我們推測,作為一種脂肪因子,chemerin不僅參與調節間充質干細胞(bone marrow mesenchymal stem cells,BMSCs)向成骨細胞或者脂肪細胞分化,也與炎癥因子相互作用組成一個復雜的免疫、炎癥調控網絡共同調節糖尿病患者骨代謝活動。
綜上所述,T2DM合并骨質疏松患者血清chemerin及炎癥因子水平顯著升高,且與骨密度呈負相關。提示chemerin、TNF-α參與了T2DM及骨質疏松的發生與發展,chemerin 可能對T2DM合并骨質疏松患者體內的慢性亞臨床炎癥狀態起一定作用。Chemerin可能直接或間接影響著骨代謝,在該領域的深入研究工作有望為骨質疏松的治療開辟一條新途徑。

