分化型甲狀腺癌患者術后TSH抑制治療對骨密度影響的前瞻性研究
王玉 賀亮 蔣森 張浩 李玉姝* 單忠艷 滕衛(wèi)平
1.中國醫(yī)科大學附屬第一醫(yī)院內分泌與代謝病科 沈陽 2.中國醫(yī)科大學附屬第一醫(yī)院甲狀腺綜合外科 沈陽 3.中國醫(yī)科大學附屬第一醫(yī)院核醫(yī)學科 沈陽
甲狀腺癌是內分泌腫瘤中常見的腫瘤,其中分化型甲狀腺癌較多見。分化型甲狀腺癌術后TSH抑制治療就是指術后應用甲狀腺激素將TSH抑制低于正常低限或低限以下、甚至檢測不到的程度,一方面補充DTC(differentiated thyroid carcinoma)患者所缺乏的甲狀腺激素,另一方面抑制DTC細胞生長[1]。眾所周知,骨的生長發(fā)育和重建受到甲狀腺激素(thyroid hormone,TH)的影響。適量的甲狀腺激素水平對骨形成和骨吸收的過程都非常重要。諸多研究證明甲狀腺疾病是引起繼發(fā)性骨質疏松的重要疾病之一。例如甲狀腺機能亢進癥、甲狀腺功能減退癥等,以上疾病干擾了骨代謝的過程,導致骨量減少、骨質疏松、甚至骨折的風險大大增加[2]。TSH抑制治療導致患者機體內環(huán)境發(fā)生變化,保持亞臨床甲亢的狀態(tài),但是這種狀態(tài)對骨密度及骨代謝的影響存在著爭議。
本研究首次在中國北方漢族DTC患者中,探討了甲狀腺全切或次全切術后應用L-T4行TSH抑制治療對骨密度和骨代謝標志物的影響,為臨床合理、個體化地進行甲狀腺癌的術后管理提供科學依據(jù)。
1 對象和方法
1.1 對象
研究選取2013年11月至2014年8月于中國醫(yī)科大學第一附屬醫(yī)院甲狀腺綜合外科行甲狀腺切除手術的患者。1)入組標準:(1)分化型甲狀腺癌患者,行甲狀腺全切或次全切除手術術后;(2)入院期間完善甲狀腺功能、甲狀腺相關抗體、骨代謝標志物、骨密度等指標;(3)術后口服左旋甲狀腺素鈉片(L-T4)行促甲狀腺素(TSH)抑制治療,抑制目標TSH<0.5 mU/L;(4)隨訪半年以上。2)排除標準:(1)隨訪發(fā)現(xiàn)遠處轉移癌灶,或殘留再發(fā)的癌灶;(2)甲狀腺切除術造成甲狀旁腺損傷,血清鈣、磷及甲狀旁腺激素因手術而降低或升高的患者;(3)TSH抑制治療過程中,F(xiàn)T3及FT4明顯升高,或出現(xiàn)甲狀腺機能亢進被迫停藥者;(4)應用影響骨代謝的相關藥物,例如雌激素、雙膦酸鹽、糖皮質激素等;(5)放棄治療的患者;(6)拒絕復查骨密度的患者;(7)隨訪期間因病或意外死亡的患者。
1.2 方法
納入研究對象72例,期間發(fā)生甲狀腺功能亢進者1例,術前未行骨密度檢查者10例,放棄治療者1例,拒絕復查骨密度者30例,最終入組患者30例,男性6例(20%),女性24例(80%)。根據(jù)隨訪時間、性別及月經(jīng)情況、補鈣情況分別分為隨訪不足1年組(12人,40%)、隨訪1年組(18人,60%);男性組(6人,20%)、絕經(jīng)前女性組(16人,53%)、絕經(jīng)后女性組(8人、27%);補鈣組(8人,400-1200mg元素鈣,27%)、不補鈣組(22人,73%)。
所有試驗對象分別于術前及隨訪結束后測定骨密度(雙能X線骨密度儀DEXA,法國MEDI LINK公司)(注:因患者人數(shù)較少,年齡跨度大,故選擇應用與正常同年齡相比較所得的Z值及BMD進行研究),空腹采血測定β-膠原特殊序列(C-terminal telopeptide of type I collagen, β-CTX,β-Cross Laps)(德國羅氏生化測定儀及配套試劑)和總I型膠原氨基酸延長肽(Procollagen I N-terminal peptide,PINP)(德國羅氏診斷公司人試劑盒及配套試劑)。
1.3 統(tǒng)計學處理
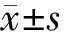
2 結果
2.1 入組患者基線狀態(tài)分析
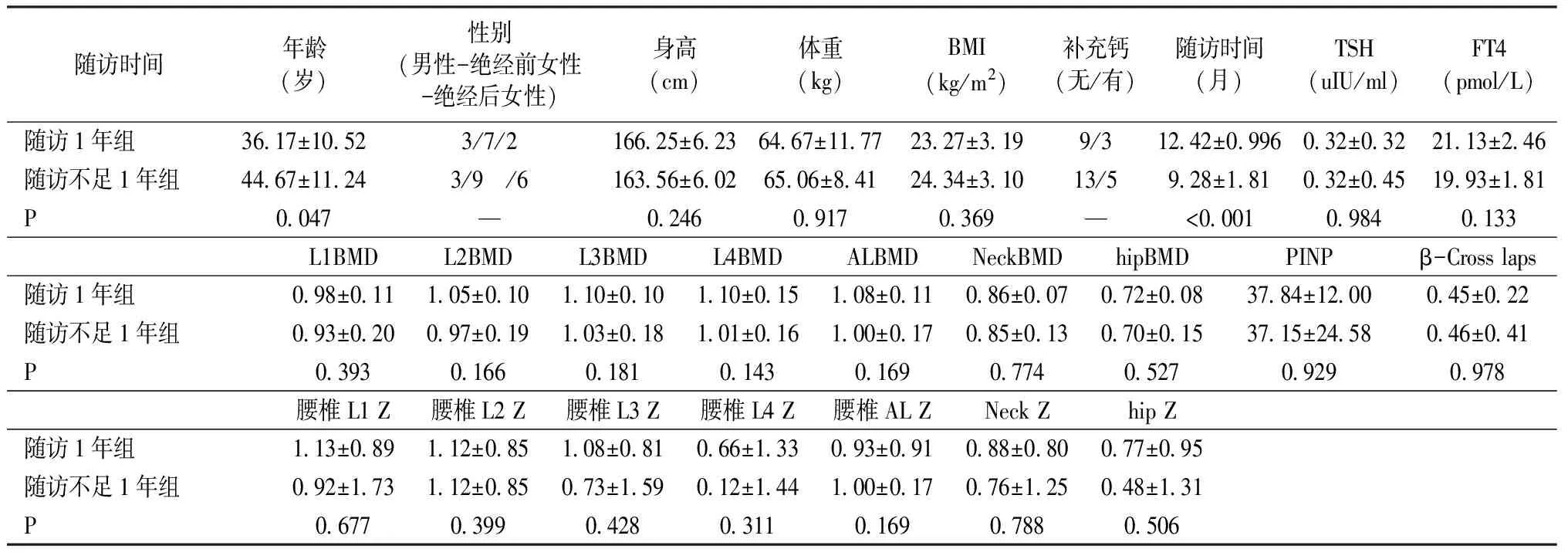
將入組患者根據(jù)隨訪時間分為隨訪1年組(12個月-15個月,12.42±0.996)和隨訪不足1年組(6個月-11個月,9.28±1.81),隨訪1年組共12例,年齡(36.17±10.52)歲;隨訪不足1年組18例,年齡(44.67±11.24)歲。對基線時兩組患者的年齡、身高、體重、BMI、TSH、FT4和術前各部位(包括腰椎、股骨頸及整體髖關節(jié))的骨密度(BMD)和Z值進行比較,結果顯示隨訪1年組與隨訪不足1年組以上指標無明顯差異(表1)。
2.2 入組患者TSH抑制治療前后的比較
比較所有入組患者術前及應用L-T4治療半年以上時骨密度及骨密度的Z值(包括腰椎、股骨頸及整體髖關節(jié))的變化。發(fā)現(xiàn)在總體患者各處骨密度及Z值在治療前后均無統(tǒng)計學差異。β-膠原特殊序列治療后較治療前明顯降低,總I型膠原氨基酸延長肽治療后較治療前明顯升高(P值分別為0.007、0.014)(表2)。
2.3 隨訪1年組及隨訪不足1年組骨密度變化的比較
經(jīng)治療后末次骨密度的結果與治療前骨密度的結果的差值表示各部位骨密度變化程度,比較隨訪1年組和隨訪不足1年組變化程度的差異,觀察TSH抑制治療時間長短與骨密度變化的關系。腰椎L3段BMD或全部腰椎BMD在隨訪半年組有所下降但隨訪1年組卻較治療前有所增加(治療1年組前后的比較P<0.05)。治療不足1年組和治療1年組前述腰椎治療前后BMD差值具有顯著差異(P值分別為0.013、0.004)。腰椎L3段和全部腰椎BMD的Z值變化在兩組有同樣的趨勢(P值分別為0.009、0.001)。整體髖關節(jié)BMD在隨訪不足1年組及隨訪1年組均降低,但隨著隨訪時間的延長下降的更明顯(治療1年后較術前顯著下降P<0.05),隨訪1年組較隨訪不足1年組下降的差值顯著增加(全髖P值為0.005)(治療前后絕對值的變化見表2,差值的變化見表3)。兩組間整體髖關節(jié)BMD的Z值變化具有同樣結果平均值以降低為主,而隨訪不足1年組以升高為主,且較隨訪1年組變化幅度大(P值分別為0.004和0.000)(表3)。綜上所述,隨訪時間越長腰椎L3段及全部腰椎骨密度反而有所升高,而隨訪時間越長整體髖關節(jié)骨密度降低越明顯。
骨吸收指標β-Cross Laps在隨訪不足1年組及隨訪1年組均有所降低,但僅隨訪1年組降低,與術前相比具有顯著差異(P=0.013)。代表骨形成的指標PINP在抑制治療不足1年和1年組均有升高,但與術前比均未達到統(tǒng)計學差異。β-Cross Laps和PINP的差值在隨訪1年組與隨訪不足1年組無顯著差異(P>0.05,表2)。
2.4 補充鈣劑對骨密度的影響
因為隨訪患者中有應用鈣劑補充的病例,故將30例患者分為鈣劑補充組(每天400~1 200 mg元素鈣,服用半年以上)及非鈣劑補充組,其中鈣劑補充組8例,鈣劑不補充組22例,比較兩組腰椎、股骨頸及整體髖關節(jié)的BMD及骨密度的Z值的前后差值。兩組無統(tǒng)計學差異。鈣劑補充組與非鈣劑補充組治療前后BMD及骨密度的Z值的變化程度無明顯差異。β-Cross Laps治療前后的差值, 鈣劑補充組較非鈣劑補充組明顯降低。(表4)
2.5 性別、絕經(jīng)對骨密度變化的影響
因為患者中存在著性別的差異及月經(jīng)情況的不同,故將隨訪1年組與隨訪不足1年組分為男性組、絕經(jīng)前女性組及絕經(jīng)后女性組,應用單因素方差分析對三組進行比較,經(jīng)比較無統(tǒng)計學差異者無需行兩兩組間比較。隨訪1年組的腰椎L3的Z值治療前后差值三組比較的P值為0.034(P<0.05);隨訪不足1年組的腰椎L3的BMD及腰椎L3的Z值治療前后的差值三組比較的P值分別為0.042及0.033(P<0.05)。對以上分別進行男性組、絕經(jīng)前女性組及絕經(jīng)后女性組的兩兩比較,經(jīng)比較隨訪1年組腰椎L3的Z值變化男性組與絕經(jīng)前女性組和絕經(jīng)后女性組均有統(tǒng)計學意義,男性與絕經(jīng)前女性比較P值為0.028,男性與絕經(jīng)后女性比較P值為0.017,女性腰椎L3的 Z值治療前后的變化程度比男性大,根據(jù)變化趨勢男性與女性比較明顯降低(表4)。隨訪不足1年組的腰椎L3的BMD治療前后差值男性組與絕經(jīng)前女性組差異有統(tǒng)計學意義(0.02±0.03 g/cm2、-0.04±0.04 g/cm2,P<0.05),絕經(jīng)前女性與男性比較明顯降低。隨訪不足1年組腰椎L3的Z值治療前后的差值男性組與絕經(jīng)前女性組差異有統(tǒng)計學意義(0.27±0.32、-0.30±0.35,P<0.05),絕經(jīng)前女性變化程度較男性大,絕經(jīng)前女性與男性相比明顯降低。(表4)
2.6 影響TSH抑制治療患者骨密度、骨密度Z值的多因素分析
根據(jù)以上結果,為了判斷是否因TSH抑制程度及抑制時間長短而影響骨密度的變化,分別對可能影響各個部位的骨密度和骨密度的Z值的因素進行多元逐步回歸分析。
首先以全部腰椎BMD治療前后的變化值為因變量,以年齡、體重、身高、BMI、FT4、TSH、隨訪時間、β-Cross Laps治療前后變化值和PINP治療前后變化值為自變量進行多元逐步回歸分析,結果顯示TSH及體重是影響全部腰椎BMD治療前后變化的相關因素,其中與TSH正相關、與體重負相關,所得回歸方程為Y=0.016+0.051T-0.001G(T代表TSH,G代表體重)。其次以隨訪1年組的整體髖關節(jié)BMD治療前后變化值為因變量,以年齡、體重、身高、BMI、FT4、TSH、隨訪時間、β-Cross Laps治療前后變化值和PINP治療前后變化值為自變量進行多元逐步回歸分析,結果顯示FT4、TSH、BMI與整體髖關節(jié)骨密度BMD的改變相關,其中整體髖關節(jié)骨密度BMD的改變與FT4及TSH為負相關,與BMI為正相關,所得回歸方程為:Y=0.004-0.014F-0.073T+0.004B(F代表FT4,T代表TSH,B代表BMI)。
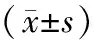
隨訪時間年齡(歲)性別(男性-絕經(jīng)前女性-絕經(jīng)后女性)身高(cm)體重(kg)BMI(kg/m2)補充鈣(無/有) 隨訪時間(月)TSH(uIU/ml)FT4(pmol/L)隨訪1年組 36.17±10.523/7/2166.25±6.23 64.67±11.7723.27±3.199/312.42±0.996 0.32±0.32 21.13±2.46隨訪不足1年組 44.67±11.243/9 /6163.56±6.0265.06±8.4124.34±3.10 13/5 9.28±1.81 0.32±0.45 19.93±1.81P0.047 —0.2460.9170.369— <0.0010.9840.133L1BMDL2BMD L3BMDL4BMDALBMDNeckBMDhipBMD PINPβ-Cross laps隨訪1年組0.98±0.111.05±0.101.10±0.101.10±0.151.08±0.11 0.86±0.07 0.72±0.0837.84±12.000.45±0.22隨訪不足1年組0.93±0.200.97±0.191.03±0.181.01±0.16 1.00±0.17 0.85±0.13 0.70±0.1537.15±24.580.46±0.41P0.393 0.166 0.1810.1430.1690.7740.5270.929 0.978腰椎L1 Z 腰椎L2 Z腰椎L3 Z腰椎L4 Z腰椎AL ZNeck Zhip Z隨訪1年組1.13±0.891.12±0.851.08±0.810.66±1.330.93±0.910.88±0.800.77±0.95隨訪不足1年組0.92±1.73 1.12±0.850.73±1.590.12±1.441.00±0.170.76±1.250.48±1.31P0.6770.3990.4280.3110.1690.788 0.506
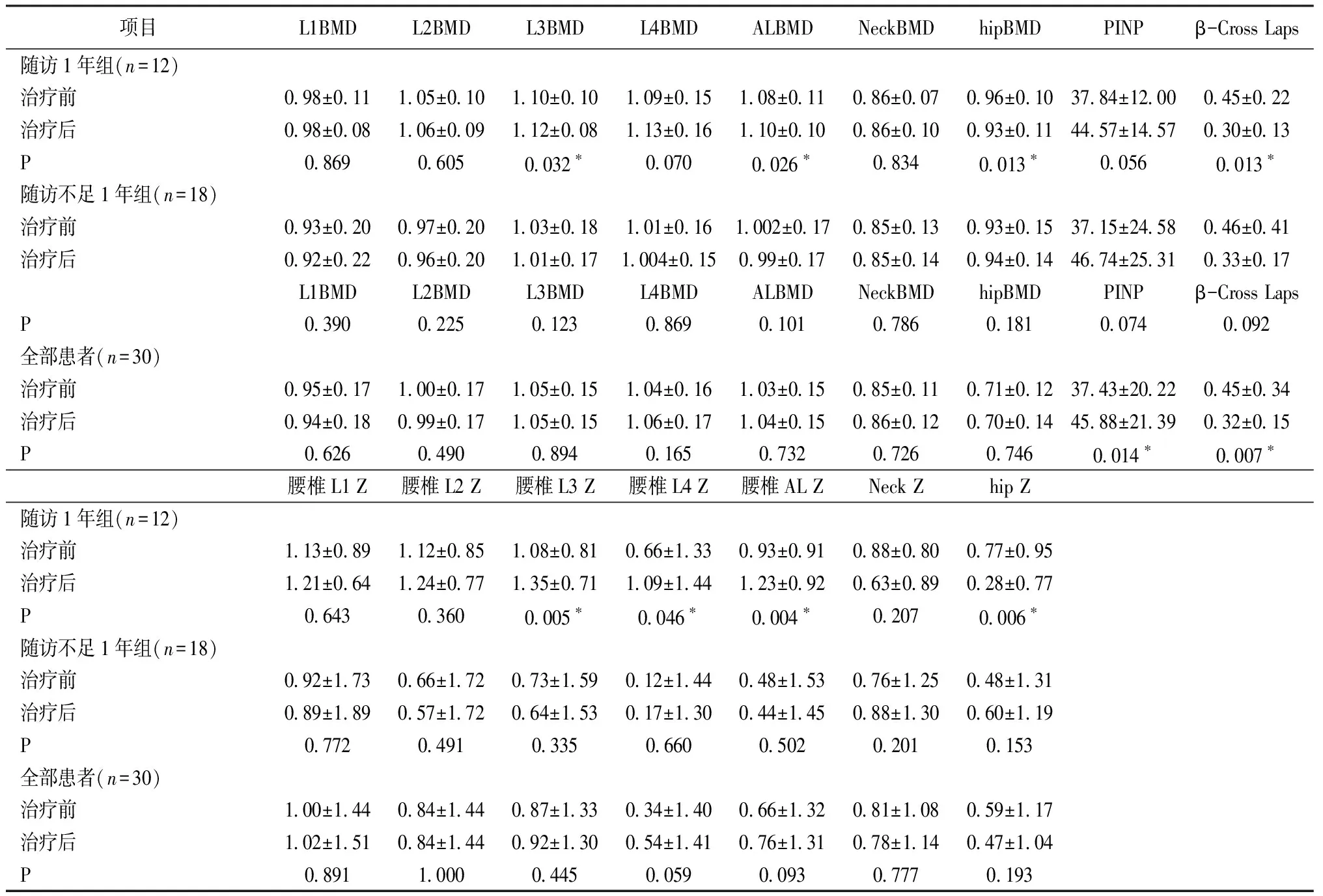
表2 不同隨訪時間及總體患者TSH抑制治療前后各部位骨密度(BMD)及Z值的比較Table 2 The comparison of BMD and Z score of various location before and after TSH suppressive therapy for overall patients at different follow-up time
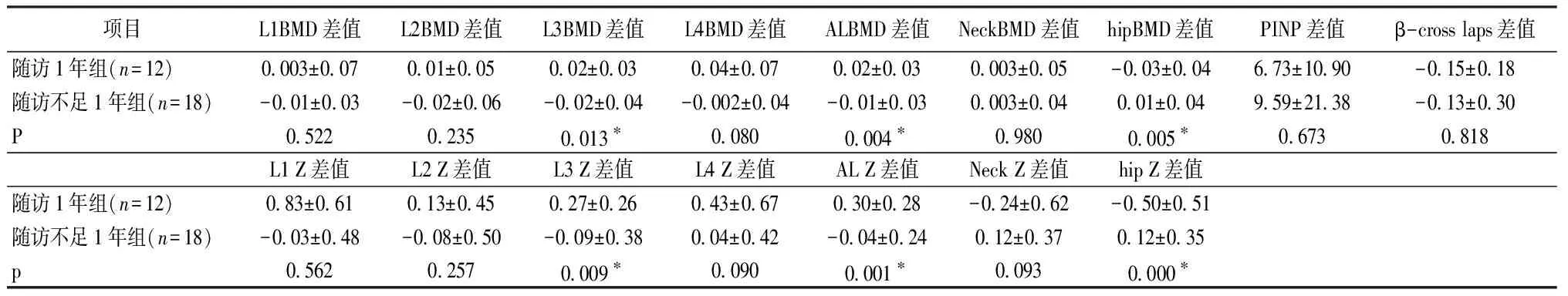
表3 不同隨訪時間的患者各部位治療前后BMD、Z值及PINP、β-CrossLaps差值的比較Table 3 The comparison of BMD, Z value, and PINP and β-CrossLaps difference before and after treatment in patients at different follow-up time
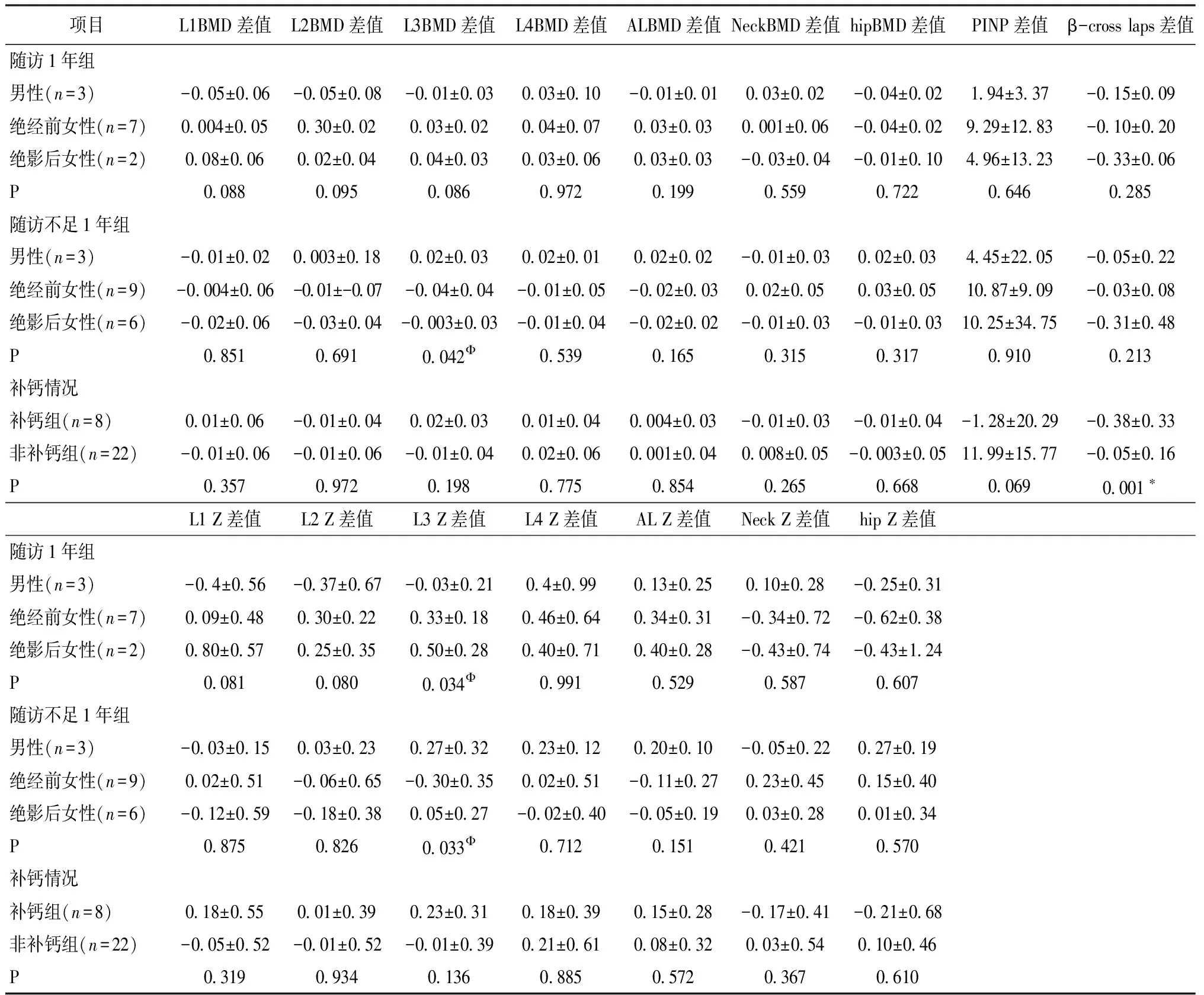
表4 在不同隨訪時間組中按照性別及月經(jīng)情況分組全部患者按補鈣情況分組各組之間治療前后BMD、Z值及PINP、β-Cross Laps差值的比較Table 4 The comparison of BMD, Z value, and PINP and β-Cross Laps difference in patients grouped according to sex, menstruation, and calcium supplementation before and after treatment at different follow-up time
備注:“*”表示P<0.05,組間比較或組內比較有統(tǒng)計學差異。“Φ”表示表示P<0.05,多組間比較有統(tǒng)計學意義,需進一步行兩兩比較。BMD的單位是(g/cm2),PINP的單位是(μg/L),β-Cross Laps單位是(ng/ml)
3 討論
有研究證明高TSH是惡性腫瘤發(fā)生危險因素,TSH抑制治療對抑制甲狀腺癌的復發(fā)或轉移非常重要。TSH主要通過作用于促甲狀腺激素受體(TSHR),形成配體-受體復合物,從而能激活TSHR,TSHR與G蛋白偶聯(lián)后,激活細胞內cAMP信號通路,刺激癌細胞的生長[3]。在成骨細胞和破骨細胞上也存在TSHR,TSH與TSHR結合,直接影響骨的重建,并且TSH可以獨立控制骨吸收和骨形成[4]。TSH可以通過RANK-L的JNK/C-jun和NF-κB信號通路抑制破骨細胞的形成和存活,從而影響破骨細胞的作用,當然TSH也可以通過抑制TNF-α應答抑制破骨細胞的形成,甚至可以通過下調Wnt(LRP-5)H和VEGF(Flk)信號抑制破骨細胞的分化。TSH也可以對成骨細胞產(chǎn)生作用,抑制1型膠原蛋白在Runx-2和轉錄因子中的表達,從而控制骨吸收及骨形成[4]。綜上所述,TSH水平變化可以影響骨密度及骨代謝。
本研究發(fā)現(xiàn)TSH抑制治療對髖關節(jié)的骨密度有顯著的負面影響,而對腰椎骨密度未見負面作用,相反有輕度升高的趨勢。國外學者的多篇報道中也發(fā)現(xiàn)導致TSH抑制的亞臨床甲亢患者髖部及非椎體骨折風險增加。Dr.Jennifer S.Lee等對美國3567例大于65歲的老年人進行研究,發(fā)現(xiàn)每1000例亞臨床甲亢男性患者有13.65例男性發(fā)生髖關節(jié)骨折、每1000例亞臨床甲亢女性患者有8.93例女性發(fā)生髖關節(jié)骨折,提示亞臨床甲亢增加了老年人髖關節(jié)骨折的風險[5]。Christina D.Wirth, MD等對8篇文獻進行薈萃分析和系統(tǒng)性的綜述,結果也顯示亞臨床甲亢可能增加了髖關節(jié)及非脊椎性骨折的風險[6-13]。有研究提示皮質骨的破骨細胞較松質骨的破骨細胞更活躍[14],也有文獻報道在高甲狀腺素狀態(tài)下股骨頸比腰椎更早出現(xiàn)骨量的丟失[15],這可能由于股骨及髖關節(jié)處以皮質骨為主較以松質骨為主的腰椎更容易受甲狀腺激素的影響。但在本研究中TSH抑制治療的患者隨著治療時間的延長腰椎的骨密度有升高的趨勢,根據(jù)上文所述皮質骨中的破骨細胞較松質骨更活躍,那么以松質骨為主的腰椎中的成骨細胞應較股骨和髖關節(jié)處活躍,有文獻報道在成骨細胞中加入TSH可以使成骨細胞減少[16],那么當TSH明顯降低時成骨細胞會更為活躍,因而我們推測TSH抑制治療對腰椎成骨細胞的影響要比股骨及髖關節(jié)更為明顯,由于我們的隨訪時間較短成骨細胞所介導的骨形成會更為突出,從而使骨密度有升高的趨勢。
本研究中發(fā)現(xiàn)應用L-T4時間較長的患者發(fā)生髖部骨密度下降的風險增加。Mee Kyoung Kim等對初始應用L-T4治療(早期術后時期)超過12個月的93名DTC患者進行隨訪。同時他們也對其他長期應用L-T4治療(晚期術后時期)的33名DTC患者進行隨訪,分別對以上隨訪患者進行基礎的和1年后的骨密度測定,結果示術后早期組比術后晚期組的骨量丟失的平均值更高即骨量丟失的更多,尤其在腰椎和股骨頸有意義(腰椎P=0.041;股骨頸P=0.010),從而得出結論左旋甲狀腺激素TSH抑制治療增加骨量丟失,主要是發(fā)生在甲狀腺術后早期治療期間的絕經(jīng)后女性[17]。考慮術后晚期組行TSH抑制治療的DTC患者TSH水平不用抑制的過低,術后早期組TSH抑制在(0.5±0.8)IU/L[17],而術后晚期組TSH則抑制在(1.3±2.1)IU/L[17],所以術后早期組骨量丟 失要比術后晚期組更加明顯,也就是治療時間長組較治療時間短組未見骨密度明顯降低的原因。
PINP被眾多研究者接受的代表骨形成的標志物,它是骨基質的重要組成成分,它是I型膠原蛋白形成的產(chǎn)物,通過在成骨細胞中I型原骨膠原的氨基末端和羧基末端的拼接而形成[18]。相反的,β-Cross Laps被認為是骨吸收的標志物,通過破骨細胞產(chǎn)生的氨基末端和羧基末端的片段反映I型膠原蛋白的降解[19]。最近,PINP和β-CTX已經(jīng)被國際骨質疏松基金會(IOF)及國際臨床化學和醫(yī)學實驗聯(lián)合會(IFCC)公認為骨質疏松癥骨形成和骨吸收的衡量標準[20]。
本研究顯示經(jīng)治療后的患者較治療前β-膠原特殊序列降低(P<0.01),而且隨著治療延長而逐漸明顯;治療后的PINP較治療前升高(P<0.05),但是治療時間的延長未見明顯的影響(P>0.05)。Toivonen J等對應用TSH抑制治療的患者分化型甲狀腺患者與正常對照組進行比較,TSH抑制治療組較正常對照組PINP明顯升高(P<0.001,+46%)[21];Gao YC等對50例應用L-T4治療DTC男性患者停止用藥4周與40例甲狀腺功能亢進患者進行比較,β-CTX較對照組明顯降低(P<0.001,-35.5%)[22]。本研究發(fā)現(xiàn)TSH抑制治療對腰椎與髖關節(jié)有不同的影響趨勢,而且血清學顯示骨吸收標志物明顯降低,同時骨形成標志物則明顯升高,然而我們未測定其他部位(如橈骨遠端等)的骨密度,故推測TSH抑制治療對全身骨的影響仍傾向于使骨吸收減少并使骨形成增多。
本研究顯示補鈣的患者的β-Cross Laps較不補鈣患者的β-Cross Laps明顯降低。Cheng X等研究認為破骨細胞的形成是受鈣濃度的增高而抑制的[23]。根據(jù)本研究的結果可能由于鈣的補充抑制破骨細胞的形成,導致骨吸收降低。
本研究應用多元逐步回歸分析顯示全部腰椎及整體髖關節(jié)的BMD變化與TSH的抑制相關。其中全部腰椎BMD的變化與TSH呈正相關,那么TSH越低全部腰椎BMD的變化越小,也就是可以認為TSH抑制治療對腰椎的影響小;整體髖關節(jié)的BMD變化與TSH呈負相關,那么TSH越低整體髖關節(jié)BMD的變化越大,說明TSH抑制治療對髖關節(jié)影響較大。根據(jù)以上結果,TSH抑制治療對髖關節(jié)的骨密度影響以降低為主,故可以推測TSH抑制治療明顯降低DTC患者的髖關節(jié)的骨密度。
本研究有一定局限性。首先,本研究入組病例數(shù)較少,雖然顯示TSH抑制治療時間較長與髖關節(jié)的骨密度下降風險相關,但是由于病例數(shù)較少,分析誤差較大,特別是行性別差異分析及女性月經(jīng)情況對骨密度及骨代謝的影響時,例數(shù)過少,影響檢驗效能。其次,本研究隨訪時間較短,不能充分反映對骨密度及骨代謝的影響。我們仍需要增加病例并延長隨訪時間進一步觀察甲狀腺素治療對骨密度及骨代謝的影響。

