黃芪甲苷對腦缺血再灌注后血腦屏障的保護作用及IL-1β含量、MMP-9蛋白表達的影響
曲友直 楊震 李敏 高國棟
?
·論 著·
黃芪甲苷對腦缺血再灌注后血腦屏障的保護作用及IL-1β含量、MMP-9蛋白表達的影響
曲友直 楊震 李敏 高國棟
目的 探討黃芪甲苷對大鼠腦缺血再灌注后血腦屏障的保護作用及其機制。方法 將SD大鼠72只隨機等分為4組:假手術組、生理鹽水對照組、小劑量黃芪甲苷治療組(10 mg/kg)和大劑量黃芪甲苷治療組(20 mg/kg),采用分光光度計法、酶聯免疫吸附法及免疫組化法分別檢測各組大鼠腦組織伊文氏藍、IL-1β含量及MMP-9蛋白的表達水平。結果 與假手術組相比,生理鹽水對照組腦組織伊文氏藍含量明顯增多、IL-1β含量顯著增高、MMP-9蛋白的表達明顯增強(P<0.01);與生理鹽水對照組相比,小劑量黃芪甲苷治療組及大劑量黃芪甲苷治療組腦組織伊文氏藍含量均顯著減少、IL-1β含量明顯降低、MMP-9蛋白表達明顯減弱(P<0.05);小劑量黃芪甲苷治療組與大劑量黃芪甲苷治療組相比,伊文氏藍、IL-1β含量及MMP-9蛋白表達無顯著差異(P>0.05)。結論 黃芪甲苷對腦缺血再灌注后血腦屏障具有保護作用,這可能與其下調IL-1β含量、抑制MMP-9蛋白的表達有關。
黃芪甲苷 腦缺血再灌注 血腦屏障 IL-1β MMP-9
血腦屏障(Blood-brain barrier,BBB)的破壞可導致血管源性腦水腫,是腦缺血再灌注損傷后腦水腫的重要病理基礎[1-2]。基膜在維持BBB穩定性中起重要作用。基質金屬蛋白酶-9(matrix metalloproteinases-9,MMP-9)可通過降解毛細血管內皮細胞外基質破壞BBB基膜,與腦缺血再灌注后BBB的破壞密切相關[3]。黃芪甲苷是中藥黃芪的主要活性成分,常作為黃芪及含黃芪(君藥)的中成藥定性定量評價的指標[4-5]。已有研究表明黃芪甲苷具有減少腦缺血再灌注后腦組織白細胞浸潤、抗炎性反應、減輕腦水腫等作用,但目前作用機制尚不明確[4-6]。本研究通過觀察黃芪甲苷對大鼠腦缺血再灌注后腦組織伊文氏藍(Evans Blue,EB)含量、IL-1β含量及MMP-9蛋白表達的影響,進一步探討其對BBB的保護作用及其機制。
1 材料與方法
1.1 材料
黃芪甲苷購自中國藥品生物制品檢定所(批號為110781-200613)。伊文氏藍購自美國Sigma公司。IL-1β定量ELISA測定試劑盒購于美國BIOSOUCE公司。MMP-9蛋白免疫組化試劑盒購自美國Zymed公司。醫學圖像分析系統,型號Olympus BX-51。健康成年雄性SD大鼠,體重250~300 g,購自本校實驗動物中心。
1.2 動物分組與模型建立
將72只SD大鼠隨機等分為4組,每組各18只,假手術組:栓線僅插入頸總動脈6 mm,不阻塞大腦中動脈,其余步驟同生理鹽水對照組;生理鹽水對照組:參照Zea Longa[7]報道的方法,采用線栓法制備局灶性腦缺血1.5 h再灌注24 h模型,再灌注即刻經腹腔注射等體積生理鹽水;小劑量黃芪甲苷治療組:再灌注即刻經腹腔注射黃芪甲苷10 mg/kg;大劑量黃芪甲苷治療組:再灌注即刻經腹腔注射黃芪甲苷20 mg/kg。
1.3 指標測定
1.3.1 每組中隨機取6只大鼠于處死前1 h經股靜脈緩慢注入2.5%伊文氏藍生理鹽水液0.2 mL/100 g,斷頭取腦稱重后放入甲酰胺中浸泡,收集浸泡的甲酰胺溶液,用分光光度計測得其吸光度,計算腦組織中EB含量。
1.3.2 每組中再隨機取6只大鼠斷頭取腦,于冰盤上迅速剝離缺血側大腦皮質,按腦濕重∶生理鹽水=100 mg∶1 mL的比例加入生理鹽水勻漿,離心后取上清液,采用ELISA法測定IL-1β含量。
1.3.3 每組其余6只大鼠,在術后相應的時間點4%多聚甲醛溶液固定,斷頭取腦,鼠腦自額極至枕葉分為A、B、C、D、E 5等份,取C腦片在恒溫冰凍切片機上做厚度為15 μm的冠狀面切片,進行免疫組化染色。免疫組化染色用圖像分析系統采集照片,在400倍視野下每張切片在梗死灶周圍隨機選取10個視野,計數免疫組化陽性細胞。
1.4 統計學處理
2 結 果
與假手術組相比,生理鹽水對照組大鼠腦組織伊文氏藍含量明顯增多、IL-1β含量顯著增高、MMP-9蛋白表達明顯增強(P<0.01);與生理鹽水對照組相比,小劑量黃芪甲苷治療組和大劑量黃芪甲苷治療組伊文氏藍含量均顯著減少、IL-1β含量明顯降低、MMP-9蛋白表達顯著減弱(P<0.05);小劑量黃芪甲苷治療組與大劑量黃芪甲苷治療組比較,伊文氏藍、IL-1β含量及MMP-9蛋白免疫組化陽性細胞數無顯著差異(P>0.05)(表1)。
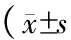
表1 各組大鼠腦組織伊文氏藍、IL-1β含量及MMP-9 蛋白表達的變化,n=6)
注:與假手術組比較,△P<0.01;與生理鹽水對照組比較,*P<0.05; 與小劑量黃芪甲苷治療組比較,▲P>0.05
3 討 論
腦水腫是腦缺血再灌注損傷的基本病理變化之一,也是導致病情加重、甚至引起患者死亡的常見病因。血腦屏障的破壞可導致血管源性腦水腫,是腦缺血再灌注損傷后腦水腫的重要病理基礎[1-2]。腦毛細血管內皮基膜在維持BBB穩定性中起重要作用[3]。MMP-9是一種糖蛋白,可由中性粒細胞、單核細胞、血管內皮細胞、星形膠質細胞、小膠質細胞等多種細胞分泌,屬于Zn2+依賴性蛋白酶,主要功能是降解和重疊內皮細胞外基質。分泌MMP-9的細胞也同時分泌組織金屬蛋白酶抑制劑(tissue inhibitor of metalloproteinase,TIMP),腦缺血再灌注后MMP-9高表達,使其與TIMP-1之間的平衡失調是引起基質破壞的重要因素[8]。近年研究已表明,IL-1β是一種具有多效性作用的促炎性細胞因子,是啟動炎癥反應的關鍵細胞因子之一,在介導炎癥反應中起重要作用。IL-1β在腦缺血再灌注損傷中具有增加缺血組織興奮性氨基酸的神經毒性,增加腦缺血神經細胞鈣超載,刺激內皮細胞表達白細胞黏附因子,誘導神經元凋亡基因的表達等重要作用。
IL-1β可通過促進白細胞和內皮細胞粘附激發炎癥反應,從而上調MMP-9蛋白表達,破壞腦毛細血管內皮基膜,血腦屏障損害導致血管源性腦水腫和出血,加重繼發性腦損傷。同時,MMP-9通過對富含基底膜的毛細血管床過度降解而使BBB開放,導致炎癥細胞和因子侵入,發揮正反饋作用,因此MMP-9是炎癥反應重要的“調節劑”[9-10]。
本實驗結果表明,大、小劑量黃芪甲苷均可降低腦缺血再灌注后腦組織伊文氏藍含量。正常情況下伊文氏藍進入體內后與血清白蛋白結合不能通過BBB。大鼠腦缺血再灌注后腦伊文氏藍含量顯著增加,表明血腦屏障在缺血再灌注損傷中結構遭到破壞,通透性顯著提高;使用黃芪甲苷治療后伊文氏藍含量明顯降低,提示黃芪甲苷能夠減輕缺血、缺氧造成的BBB通透性改變,一定程度上降低了腦細胞的水腫程度,遏制腦缺血病程的發展,從而發揮對腦缺血的保護作用。
本實驗結果表明,大、小劑量黃芪甲苷均可顯著下調缺血再灌注后腦組織MMP-9蛋白的高表達,從而改善腦缺血再灌注后MMP-9蛋白與TIMP-1之間平衡失調的狀態、減少內皮細胞外基質的降解、保護血腦屏障、減輕血管源性腦水腫。本實驗結果還發現大、小劑量黃芪甲苷均可抑制腦缺血再灌注后腦組織IL-1β含量,從而減輕炎性反應、抑制MMP-9蛋白的高表達、保護血腦屏障。另外,作為炎癥反應重要的“調節劑”,MMP-9蛋白高表達的抑制又可進一步發揮其正反饋作用,減少炎癥因子的侵入,從而降低腦缺血再灌注后腦組織IL-1β含量。這可能是黃芪甲苷發揮對腦缺血再灌注后血腦屏障保護作用的分子機制之一。
本研究還發現,大劑量黃芪甲苷與小劑量黃芪甲苷比較,缺血再灌注后腦組織伊文氏藍含量、IL-1β含量及MMP-9蛋白表達無顯著差異,說明黃芪甲苷對BBB的保護作用在一定范圍內與劑量大小無關,機制尚不清楚,這可能與腦缺血再灌注后血腦屏障破壞與多因素調控有關。
[1] Nordal RA,Wong CS.Molecular targets in radiation-induced blood-brain barrier disruption[J].Int J Radiat Oncol Biol Phys,2005,62(1):279-287.
[2] Begley DJ,Brightman MW.Structural and functional aspects of the blood-brain barrier[J].Prog Drug Res,2003,61(1):39-78.
[3] Asahi M,Wang X,Mori T,et al.Effects of matrix metalloproteinase-9 gene knock-out on the proteolysis of blood-brain barrier and white matter components after cerebral ischemia[J].J Neurosci,2001,21(19):7724-7732.
[4] 胡芳弟,封士蘭,趙健雄,等.HPLC法測定黃芪中黃酮類成分和黃芪甲苷的含量[J].分析測試技術與儀器,2003,9(3):173-177.
[5] 黃惠,王嶺,李艷,等.黃芪注射液對大鼠腦缺血再灌注損傷的保護作用研究[J].卒中與神經疾病,2014,21(1):19-22.
[6] 曲友直,趙燕玲,李敏,等.黃芪甲苷對腦缺血再灌注后血腦屏障的保護作用及occludin蛋白表達的影響[J].卒中與神經疾病,2010,17(2):92-93, 96.
[7] Longa EZ,Weinstein PR,Carlson S,et al.Reversible middle cerebral artery occlusion without craniectomy in rats[J].Stroke,1989,20(1):84-91.
[8] 陳新云.炎癥因子在大鼠腦缺血后MMP和TIMP-1致腦損傷中的作用[J].中山大學學報(醫學科學版),2013,34(2):230-234.
[9] Gu Z,Cui J,Brown S,et al.A highly specific inhibitor of matrix metalloproteinase-9 rescues laminin from proteolysis and neurons from apoptosis in transient focal cerebral ischemia[J].J Neurosci,2005,25(27):6401-6408.
[10]Li M,Qu YZ,Zhao ZW,et al.Astragaloside IV protects against focal cerebral ischemia/reperfusion injury correlating to suppression of neutrophils adhesion-related molecules[J].Neurochem Int,2012,60(5):458-465.
(2016-04-19收稿 2016-05-10修回)
Protective effects of astragaloside IV on blood-brain barrier and the content of IL-1β and expression of MMP-9 protein after cerebral ischemic reperfusion
QuYouzhi,YangZhen,LiMin,etal.
DepartermentofNeurosurgery,TangduHospital0fFourthMilitaryMedicalUniversity,Xi’an710038
Objective To investigate the protective effects of astragaloside IV on blood-brain barrier and the content of IL-1β, expression of MMP-9 protein after cerebral ischemic reperfusion.Methods 72 SD rats were divided randomly into four groups: sham-operated group, normal- saline contral group, group treated by low dose of astragaloside IV(10 mg/kg),group treated by high dose of astragaloside IV(20 mg/kg).Evans Blue(EB) leakage, the content of IL-1β,expression of MMP-9 protein were respectively detected by spectrophotometry, ELISA and immunohistochemistry.Results Compared with sham-operated group, EB leakage,the content of IL-1β and expression of MMP-9 protein were higher in normal- saline contral group (P<0.01).Compared with normal saline contral group, EB leakage,the content of IL-1β and expression of MMP-9 protein were lower in group treated by low dose of astragaloside Ⅳ and group treated by high dose of astragaloside Ⅳ(P<0.05). There was no statistical difference between group treated by low dose of astragaloside Ⅳ and group treated by high dose of astragaloside Ⅳ(P>0.05).Conclusion Astragaloside Ⅳ could have protective effects on blood-brain barrier after cerebral ischemic reperfusion. Its mechanisms may be associated with down-regulation of the content of IL-1β and expression of MMP-9 protein.
Astragaloside Ⅳ Cerebral ischemic reperfusion Blood-brain barrier IL-1β MMP-9
國家自然科學基金(30600841)
710038 西安,第四軍醫大學唐都醫院神經外科
R743
A
1007-0478(2016)06-0389-03
10.3969/j.issn.1007-0478.2016.06.001

