前列腺癌多參數MRI計算機輔助診斷系統的構建
高 歌,王成彥,趙 凱,徐康潔,王慧慧,胡 娟,張 玨,王霄英
1. 北京大學第一醫院醫學影像科,北京 100034;2. 北京大學工學院生物醫學工程系,北京大學前沿交叉學科研究院,北京 100871
前列腺癌多參數MRI計算機輔助診斷系統的構建
高 歌1,王成彥2,趙 凱1,徐康潔1,王慧慧1,胡 娟1,張 玨2,王霄英1
1. 北京大學第一醫院醫學影像科,北京 100034;2. 北京大學工學院生物醫學工程系,北京大學前沿交叉學科研究院,北京 100871

高歌,博士研究生。現在北京大學第一醫院醫學影像科進行科學研究學習,研究方向為腹部影像診斷。博士期間主要從事前列腺多參數MRI計算機輔助診斷研究,對計算機輔助診斷技術、圖像特征提取分析及前列腺多參數磁共振診斷標準有較深入的研究。曾多次赴國際會議進行學術交流及展示。
多參數磁共振成像(multiparametric MRI,mpMRI)已成為前列腺癌檢出、分期、指導活檢及治療后隨訪最常用的影像學方法。由于MRI技術的復雜性,診斷具有較強的經驗依賴性。計算機輔助診斷(computer-aided diagnosis,CAD)技術可進行多變量分析,提高疾病的臨床診斷效能,近年來廣泛應用于醫學圖像分析。基于mpMRI的前列腺癌CAD系統近幾年取得了較大進展并顯現出良好的應用前景,本文結合本單位實際經驗,簡要介紹CAD在前列腺癌mpMRI診斷中的進展。
計算機輔助診斷;磁共振成像;前列腺癌
前列腺多參數磁共振成像(multiparametric MRI,mpMRI)已成為前列腺癌臨床診斷的常規手段[1-2],包括T1WI、T2WI,以及功能MRI (functional MRI,fMRI)如擴散加權成像(diffusionweighted imaging,DWI)、動態增強MRI(dynamic contrast-enhanced MRI,DCE-MRI)、磁共振波譜(magnetic resonance spectroscopy,MRS)等。T1WI 和T2WI具有較高的軟組織分辨率,能提供前列腺解剖信息。DWI和DCE-MRI可反映前列腺組織中水分子擴散和微血管灌注情況,為前列腺癌的檢出提供更多診斷信息[3]。但前列腺mpMRI診斷的準確性較多依賴影像科醫師的個人經驗[4],閱片者之間的一致性也欠佳。因此,計算機輔助診斷(computer-aided diagnosis,CAD)成為近年來前列腺mpMRI的研究熱點之一。
1 前列腺癌CAD的發展過程
自1994年CAD首次應用于前列腺癌診斷以來[5],發展快速,廣泛應用于前列腺癌診斷。20世紀90年代初,前列腺癌CAD主要基于臨床數據,如直腸指診(digital rectal examination, DRE)、血清前列腺特異性抗原(prostate-specific antigen,PSA)等指標進行疾病預測。近年來,隨著MRI在前列腺癌診斷中的重要性不斷提高,基于mpMRI的前列腺癌CAD系統大量涌現。目前,基于mpMRI的前列腺癌CAD系統主要包括兩大類別,分別是計算機輔助檢出(computer-aided detection,CADe)和計算機輔助診斷(computeraided diagnosis,CADx)。前者主要用于前列腺可疑癌灶的檢出,對病灶進行高亮標示,并輸出病灶為癌的可能性;后者則用于鑒別前列腺癌灶與非癌灶[6]。雖然上述兩類CAD的輸出結果形式不同,但CAD系統的結構大致相同(圖1)。
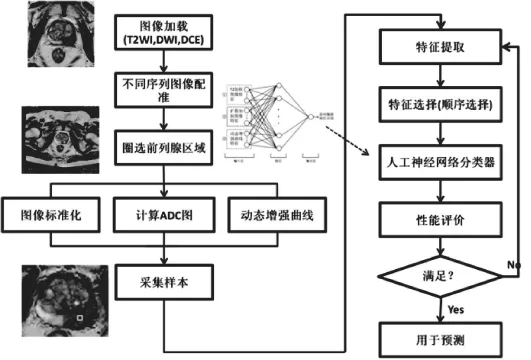
圖1 前列腺癌CAD系統流程圖
CAD能綜合多個參數對圖像進行多變量分析,有效避免醫師基于單一指標的判斷,或過度依賴個人經驗的主觀判斷。不僅使診斷過程更客觀,還能縮短診斷時間,提高診斷效能。符合臨床需求的前列腺CAD系統需具備以下特征:在不依賴閱片醫師的個人經驗和縮短閱片時間的情況下,達到滿足臨床需求的診斷準確性。
2 前列腺癌mpMRI 的CAD構建
2.1 圖像預處理
由于被檢者或成像技術原因,前列腺在MRI中的位置和信號強度存在一定差異。因此,首先要對原始圖像數據進行均勻性矯正和標準化處理,改善圖像質量,提高CAD圖像特征提取和分析的準確性。通過預處理,矯正成像過程中由于脈沖序列和線圈(不均勻性、穿透性)、操作環境及MRI設備自身原因所致的腺體內不同區域及各序列之間圖像信號灰度均值和方差的偏差[6],避免MRI圖像灰度值的不均勻性對后期圖像分割和病灶識別的影響。
2.2 圖像分割
前列腺MRI圖像分割獲得的腺體輪廓可為后續臨床處理提供參考,如前列腺靶向穿刺、近距離放射治療及其他局部治療等[7]。前列腺分割還可在不同成像方法之間的圖像融合中發揮作用,如MRI與超聲圖像融合[8],從而提高直腸超聲引導下穿刺活檢的陽性率。在CAD系統中,對前列腺MRI圖像進行準確分割是下一步圖像特征提取和識別的基礎,其效能直接影響后續病灶識別的準確性。T2WI可清楚顯示解剖,因此是進行前列腺分割的主要序列,在圖像配準后分割結果可自動擴展至其他序列。
傳統手工分割一方面對軟件使用者個人經驗的依賴性較強,存在主觀性、可重復性差、不易實現三維分割等缺陷;另一方面,手動分割過程繁瑣,大大增加了CAD系統的分析時間。因此,有效的自動或半自動圖像分割技術的實現,對提高系統的可操作性及診斷性能具有重要臨床價值。受限于MRI的成像原理,傳統的基于邊緣[9]或區域[10]的圖像分割方法效能有限。近年來,基于形變模型的分割方法研究成為前列腺分割研究領域的熱點[11]。但前列腺MRI自動分割仍處于初步研究階段,其分割準確性尚未達到臨床應用的要求,需對算法進行優化。
2.3 圖像配準
mpMRI要求綜合不同序列的圖像信息進行判斷,因此不同序列之間圖像配準成為CAD系統的基本組成部分。基于mpMRI的前列腺癌CAD圖像配準包括:消除被檢者體位改變造成的前列腺位置變動;糾正不同成像序列的圖像變形;解決不同序列之間顯示野(field of view,FOV)不一致的問題。
圖像配準的效能很大程度上取決于MRI掃描參數的設定。在MRI數據采集過程中,應保持各序列之間FOV一致,盡可能縮短掃描時間減少運動偽影,優化序列參數減少變形偽影,均可提高圖像配準的準確性,減少配準步驟的耗時。
2.4 圖像特征提取
圖像特征的提取可基于體素提取[12-14],也可基于感興趣區(region of interest,ROI)[15-16]。
基于體素的圖像特征提取方法,通過不同體素之間信號強度的差別識別前列腺癌灶,因此信號強度相關統計量是基于體素圖像特征提取的主要特征之一。邊緣特征也常被用來檢測體素之間信號強度的改變,提供更多圖像信息[17]。紋理特征主要為前列腺癌組織與非癌組織的辨別提供圖像信息,最常用的紋理特征提取方法為灰度共生矩陣(gray level co-occurrence matrix,GLCM)及其相關統計量。另有研究表明,人類視覺系統對粗糙度和凹凸度的感知與分形維度(fractal dimension, FD)具有密切聯系,因此可利用圖像區域的分形維度來描述特定圖像區域的紋理特征[18-19]。此外,不同體素在前列腺內的位置也可作為圖像特征之一被提取。
基于ROI的圖像特征提取,首先要構建整個圖像每個體素的特征圖譜,然后通過勾畫ROI從體素圖譜中提取某一區域的圖像特征相關統計量,用于鑒別癌與非癌組織。常用的統計量為百分比及均數、標準差、峰度和偏度等統計矩[20]。Litjens等[15]提出圖像對稱相關特征也屬于此類,由圖像中呈鏡像對稱ROI的圖像特征均數相比而獲得。解剖相關圖像特征,如體積、致密度和球形相關圖像特征也可用于前列腺組織良惡性鑒別。灰度直方圖是對圖像所包含的全部像素的灰度進行統計獲得的圖像特征,包含兩大類:一類與圖像信號強度相關,另一類則為方向梯度直方圖。前者的統計特征包括均數、標準差、偏度、峰度、能量和熵[21],后者可通過梯度向量分布描述ROI的形狀。此外,分形分析也可作為基于ROI的圖像特征進行提取,主要通過反映組織成分復雜性的分形維度特征參數進行分析[19]。
DCE作為前列腺mpMRI的常規序列,其圖像特征提取在前列腺癌的檢出中具有一定臨床價值。目前,DCE序列常用的圖像特征主要是基于時間-信號強度曲線的半定量參數,通過一系列幅值及其對應的時間特征來反映前列腺組織的微血管灌注情況[22]。此外,基于不同藥代動力學模型對濃度-時間曲線進行數學處理獲得的定量模型參數,如對比劑容積轉移常量(Ktrans)、滲漏空間(Ve)和速度常量(Kep)等也可作為特征參數進行提取[23]。
圖像特征的提取和選擇直接影響CAD系統的診斷效能。雖然多數學者將研究重點集中于分類器的研發,但事實上作為分類器輸入項的圖像特征的提取和選擇比分類器的選擇更為重要。提取圖像特征參數并非越多越好,若一味追求提取參數的數量而忽視有效參數的篩選,不僅無助于CAD效能的提高,反而會增加軟件運行時間,降低效率。鑒于此,有效的圖像特征選擇對提高CAD診斷效能具有重要的臨床價值。
前列腺的MRI技術繁多,第2版前列腺影像報告和數據系統(Prostate Imaging Reporting and Data System,PI-RADS)推薦T2WI+DWI/ ADC+DCE-MRI聯合的mpMRI進行前列腺癌檢出,因此基于上述MRI序列建立前列腺癌CAD系統。Peng等[20]研究結果顯示,聯合T2WI灰度直方圖特征、表觀擴散系數(apparent diffusion coefficient,ADC)均數、ADC十分位數及基于Tofts模型[24]的Ktrans值建立的前列腺CAD系統進行前列腺癌檢出,可獲得受試者工作特征(receiver operating characteristic,ROC)曲線的下面積(area under the curve, AUC)達0.95±0.02的診斷效能,是目前所報道研究中效能最高的CAD系統。
2.5 分類器
近年來,隨著機器學習理論的發展,出現了很多先進的學習方法。其中,以選擇癌和非癌訓練集間最大分類間隔的最優超平面的支持向量機(support vector machine,SVM)的效能最高,在解決小樣本、非線性和高維的機器學習問題中表現出許多優勢[25]。Niaf等[17]基于T2WI、DWI和DCE-MRI圖像,比較SVM、線性判別分析(linear discriminant analysis,LDA)、樸素貝葉斯(Na?ve Bayes,NB)分類器和K最鄰近算法(K-nearest neighbor algorithm,KNN),對前列腺外周帶癌灶檢出的效能,結果顯示SVM的效能最高。Vos等先后基于DCE序列[26]和T2WI+DCE序列[27],將SVM應用于前列腺外周帶病灶分析中,均獲得了較高效能。
近年來,隨機森林(random forest, RF)算法被逐步用于醫學圖像分析中,并在處理一些醫學問題中獲得了滿意結果[28]。RF是一個組合分類器,由多個決策樹作為構成RF的基礎分類器,能有效處理大數據集,且無需對輸入變量進行過多處理,同樣獲得了較好的效能。Tiwari等[29]將RF算法應用于T2WI+MRS的前列腺癌診斷中,結果顯示對于不同屬性數據,RF具有較高的整合能力。
雖然SVM和RF兩種算法在解決前列腺癌mpMRI診斷中具有相對較高的效能,但兩者仍存在局限和不足,尚需大樣本研究對算法進行改進和優化。
本單位研發的前列腺CAD系統提取的圖像特征包括T2WI和DWI/ADC的灰度統計、灰度直方圖和灰度共生矩陣特征,以及DCE-MRI時間-信號強度曲線的半定量和定量參數。采用3層結構的前饋性人工神經網絡作為分類器[30],將進行了均勻化矯正和標準化處理的MRI圖像中提取的特征和臨床信息作為輸入參數,輸出為前列腺癌的預測結果(介于0~1之間的預測值)和預測圖,具體CAD軟件設計見圖2。
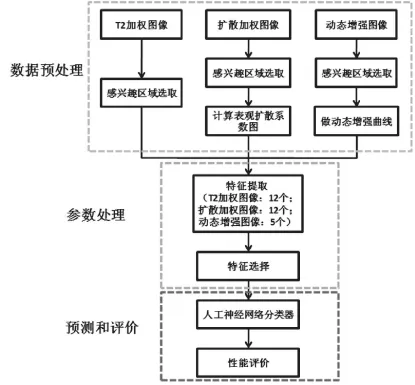
圖 2 本單位構建的前列腺癌CAD系統結構
3 前列腺癌mpMRI 的CAD臨床效能研究
CAD系統常用效能評價方法為ROC曲線,通過AUC反映系統的效能。目前,基于1.5T MRI 的CAD系統AUC為0.71~0.97,而基于3.0T MRI的CAD系統效能稍有提高,AUC為0.77~0.95[31]。此外,靈敏度、特異度能為CAD系統效能評價提供更多信息,1.5T MRI CAD系統的靈敏度和特異度為0.74~1.0、0.43~0.93,而3.0T MRI CAD系統的靈敏度和特異度為0.60~0.90、0.66~0.99。通常3.0T MRI CAD系統能獲得較高效能,且不同版本軟件之間效能差異較小。
盡管不同CAD系統之間測試數據集和效能評價方法不統一,妨礙了不同CAD系統之間的效能比較,但大量研究顯示,基于mpMRI的CAD系統的效能相對于基于單一序列的CAD系統有一定程度的提高。Viswanath等[32]將T2WI、DWI和DCE序列聯合,CAD系統效能由基于單序列的0.62~0.65提高至0.77。Litjens等[15]的研究得到相同結論,整合了T2WI、DWI和DCE序列的mpMRI CAD系統相對于各單一序列的CAD系統,診斷效能由0.71~0.76提升至0.89。另有研究顯示,聯合的MRI序列越多,CAD系統獲得的效能越高[14]。
4 前列腺癌mpMRI 的CAD展望
隨著信息技術的發展,基于mpMRI的前列腺癌CAD系統的診斷效能不斷提高。 CAD能顯著提高缺乏前列腺癌MRI診斷經驗影像科醫師的診斷準確率,并獲得與診斷經驗豐富的影像科醫師相當的診斷效能[33]。但如何將CAD系統整合入前列腺癌影像學診斷流程尚需深入研究。
此外,軟件運行模式的限制也是制約CAD臨床推廣的關鍵因素。近年來,隨著信息通訊技術及移動互聯網的不斷發展,移動應用軟件(application,App)已成為高效處理日常事務的主要手段,采用App進行疾病診斷、預防、監測及患者自我健康管理也逐漸被醫師和患者接受[34]。嘗試通過App實現CAD指令和數據的輸入、輸出,將會成為未來CAD與日常臨床工作實現無縫化鏈接的重要手段。
[1] PANEBIANCO V, BARCHETTI F, SCIARRA A,et al. Multiparametric magnetic resonance imaging vs. standard care in men being evaluated for prostate cancer: a randomized study [J]. Urol Oncol, 2015, 33(1): e1-e7.
[2] FüTTERER J J, BRIGANTI A, D E VISSCHERE P,et al. Can clinically significant prostate cancer be detected with multiparametric magnetic resonance imaging? A systematic review of the literature [J]. Eur Urol, 2015,68(6): 1045-1053.
[3] WANG R, WANG H, ZHAO C, et al. Evaluation of multiparametric magnetic resonance imaging in detection and prediction of prostate cancer [J]. PLoS One, 2015,10(6): e0130207.
[4] RUPRECHT O, WEISSER P, BODELLE B, et al. MRI of the prostate: interobserver agreement compared with histopathologic outcome after radical prostatectomy [J]. Eur J Radiol, 2012, 81(3): 456-460.
[5] SNOW P B, SMITH D S, CATALONA W J. Artificial neural networks in the diagnosis and prognosis of prostate cancer: a pilot study [J]. J Urol, 1994, 152(5 Pt 2): 1923-1926.
[6] GIGER M L, CHAN H P, BOONE J. Anniversary paper: History and status of CAD and quantitative image analysis: the role of Medical Physics and AAPM [J]. Med Phys, 2008, 35(12): 5799-5820.
[7] JOLESZ FA, NABAVI A, KIKINIS R. Integration of interventional MRI with computer-assisted surgery [J]. J Magn Reson Imaging, 2001, 13(1): 69-77.
[8] GHOSE S, OLIVER A, MARTI R, et al. A survey of prostate segmentation methodologies in ultrasound,magnetic resonance and computed tomography images [J]. Comput Methods Programs Biomed, 2012, 108(1): 262-287.
[9] VIKAL S, HAKER S, TEMPANY C, et al. Prostate contouring in MRI guided biopsy [J]. Proc SPIE Int Soc Opt Eng, 2009, 7259: 72594A.
[10] KLEIN S, VAN DER HEIDE U A, LIPS I M, et al. Automatic segmentation of the prostate in 3D MR images by atlas matching using localized mutual information [J]. Med Phys, 2008, 35(4): 1407-1417.
[11] TSAI A, YEZZI A JR, WELLS W, et al. A shape-based approach to the segmentation of medical imagery using level sets [J]. IEEE Trans Med Imaging, 2003, 22(2): 137-154.
[12] ARTAN Y, HAIDER M A, LANGER D L, et al. Prostate cancer localization with multispectral MRI using cost-sensitive support vector machines and conditionalrandom fields [J]. IEEE Trans Image Process, 2010, 19(9):2444-2455.
[13] VISWANATH S, BLOCH B N, GENEGA E, et al. A comprehensive segmentation, registration, and cancer detection scheme on 3 Tesla in vivo prostate DCE-MRI [J]. Med Image Comput Assist Interv, 2008, 11(Pt 1):662-669.
[14] OZER S, LANGER D L, LIU X, et al. Supervised and unsupervised methods for prostate cancer segmentation with multispectral MRI [J]. Med Phys, 2010, 37(4): 1873-1883.
[15] LITJENS G, DEBATS O, BARENTSZ J, et al. Computer-aided detection of prostate cancer in MRI [J]. IEEE Trans Med Imaging, 2014, 33(5): 1083-1092.
[16] VOS P C, BARENTSZ J O, KARSSEMEIJER N, et al. Automatic computer-aided detection of prostate cancer based on multiparametric magnetic resonance image analysis [J]. Phys Med Biol, 2012, 57(6): 1527-1542.
[17] NIAF E, ROUVIERE O, MEGE-LECHEVALLIER F,et al. Computer-aided diagnosis of prostate cancer in the peripheral zone using multiparametric MRI [J]. Phys Med Biol, 2012, 57(12): 3833-3851.
[18] LOPES R, AYACHE A, MAKNI N, et al. Prostate cancer characterization on MR images using fractal features [J]. Med Phys, 2011, 38(1): 83-95.
[19] LV D, GUO X, WANG X, et al. Computerized characterization of prostate cancer by fractal analysis in MR images [J]. J Magn Reson Imaging, 2009, 30(1):161-168.
[20] PENG Y, JIANG Y, YANG C, et al. Quantitative analysis of multiparametric prostate MR images: differentiation between prostate cancer and normal tissue and correlation with Gleason score-a computer-aided diagnosis development study [J]. Radiology, 2013, 267(3): 787-796.
[21] ZHAO K, WANG C, HU J, et al. Prostate cancer identification: quantitative analysis of T2-weighted MR images based on a back propagation artificial neural network model [J]. Sci China Life Sci, 2015, 58(7): 666-673.
[22] PUECH P, BETROUNI N, MAKNI N, et al. Computer-assisted diagnosis of prostate cancer using DCE-MRI data: design, implementation and preliminary results [J]. Int J Comput Assist Radiol Surg, 2009, 4(1):1-10.
[23] CAI W, LI F, WANG J, et al. A comparison of arterial spin labeling perfusion MRI and DCE-MRI in human prostate cancer [J]. NMR Biomed, 2014, 27(7): 817-825.
[24] TOFTS P S. Modeling tracer kinetics in dynamic Gd-DTPA MR imaging [J]. J Magn Reson Imaging, 1997,7(1): 91-101.
[25] BURGES C J C. A tutorial on support vector machines for pattern recognition [J]. Data Min Know Dis, 1998,2(2): 121-167.
[26] VOS P C, HAMBROCK T, HULSBERGEN-VAN DE KAA C A, et al. Computerized analysis of prostate lesions in the peripheral zone using dynamic contrast enhanced MRI [J]. Med Phys, 2008, 35(3): 888-899.
[27] VOS P C, HAMBROCK T, BARENSTZ J O, et al. Computer-assisted analysis of peripheral zone prostate lesions using T2-weighted and dynamic contrast enhanced T1-weighted MRI [J]. Phys Med Biol, 2010,55(6): 1719-1734.
[28] CRIMINISI A, SHOTTON J, KONUKOGLU E. Decision forests: A unified framework for classification,regression, density estimation, manifold learning and semi-supervised learning [J]. Foun Trend Comput Graph Vis, 2012, 7(2-3): 81-227.
[29] TIWARI P, VISWANATH S, KURHANEWICZ J,et al. Multimodal wavelet embedding representation for data combination (MaWERiC): integrating magnetic resonance imaging and spectroscopy for prostate cancer detection [J]. NMR Biomed, 2012, 25(4): 607-619.
[30] 呂冬姣, 張玨, 王霄英, 等. 人工神經網絡在前列腺癌診斷中的應用 [J]. 北京大學學報(醫學版), 2009, 41(4):469-473.
[31] LEMAITRE G, MARTI R, FREIXENET J, et al. Computer-aided detection and diagnosis for prostate cancer based on mono and multi-parametric MRI: a review [J]. Comput Biol Med, 2015, 60(5): 8-31.
[32] VISWANATH S, BLOCH B N, CHAPPELOW J,et al. Enhanced multi-protocol analysis via intelligent supervised embedding (EMPrAvISE): Detecting prostate cancer on multi-parametric MRI [J]. Proc SPIE Int Soc Opt Eng, 2011, 7963: 79630U.
[33] HAMBROCK T, VOS P C, HULSBERGEN-VAN DE KAA C A, et al. Prostate cancer: computer-aided diagnosis with multiparametric 3-T MR imaging-effect on observer performance [J]. Radiology, 2013, 266(2):521-530.
[34] SILVA B M, RODRIGUES J J, DE LA TORRE DIEZ I,et al. Mobile-health: A review of current state in 2015 [J]. J Biomed inform, 2015, 56(8): 265-272.
Setup of computer-aided diagnosis system for prostate cancer on multiparametric MRI
GAO Ge1, WANG Chengyan2, ZHAO Kai1, XU Kangjie1, WANG Huihui1, HU Juan1, ZHANG Jue2, WANG Xiaoying1
(1. Department of Medical Imaging, Peking University First Hospital, Beijing 100034, China; 2. Department of Biomedical Engineering,College of Engineering; Academy for Advanced Interdisciplinary Studies, Peking University, Beijing 100871, China)
Correspondence to: WANG Xiaoying E-mail: cjr.wangxiaoying@vip.163.com
Multiparametric MRI (mpMRI) has been considered as the method of choice for prostate cancer detection,staging, guidance for biopsy and treatment follow-up. However, effectiveness of mpMRI is usually affected by personal experience and expertise. Computer-aided diagnosis (CAD) system shows promise for improved prostate cancer diagnosis. This article aims to review the technique advance and effectiveness comparison of the state-of-the-art CADs for prostate cancer on mpMRI.
Computer-aided diagnosis; Magnetic resonance imaging; Prostate cancer
R445.2
A
1008-617X(2016)02-0117-06
王霄英 E-mail:cjr.wangxiaoying@vip.163.com
2016-06-12)

