幽門螺桿菌lpp20基因在食品級乳酸菌中的表達及免疫活性鑒定*
孫 楠,張榮光,段廣才,陳帥印,彭曉燕,范清堂,郗園林
鄭州大學公共衛生學院流行病學教研室; 河南省分子醫學重點實驗室 鄭州 450001
?
幽門螺桿菌lpp20基因在食品級乳酸菌中的表達及免疫活性鑒定*
孫楠,張榮光#,段廣才#,陳帥印,彭曉燕,范清堂,郗園林
鄭州大學公共衛生學院流行病學教研室; 河南省分子醫學重點實驗室 鄭州 450001
摘要目的:構建分泌表達幽門螺桿菌lpp20基因的重組乳酸乳球菌菌株,并鑒定其免疫活性,為研究安全高效的幽門螺桿菌口服疫苗奠定基礎。方法:采用PCR法從幽門螺桿菌基因組DNA中擴增lpp20基因,將lpp20先與T載體(pMD19-T)連接,進而經雙酶切與表達載體pNZ8149-SPusp45連接,用電穿孔法將重組質粒轉入食品級乳酸乳球菌菌株NZ3900中,并用Nisin誘導Lpp20表達,表達產物通過Western blot法鑒定免疫活性。結果:lpp20基因的PCR擴增產物大小約為540 bp,重組質粒的酶切、PCR和測序鑒定結果符合預期;在菌體和培養基中均檢出表達的Lpp20蛋白,重組表達的Lpp20蛋白相對分子質量約為20 000,且具有與小鼠抗幽門螺桿菌血清反應的免疫活性。結論:成功構建了能夠分泌表達幽門螺桿菌Lpp20抗原的乳酸乳球菌菌株,該重組菌株在口服疫苗研究中具有應用潛力。
幽門螺桿菌(Helicobacterpylori,H.pylori)是人體胃炎、消化性潰瘍和胃癌等胃部疾病的主要病原體[1-2]。我國自然人群H.pylori感染率為56.22%[3],雖然臨床治療H.pylori感染目前仍以三聯療法為主,但由于藥物治療的不良反應嚴重和根除率逐年下降,且無法達到群體防治的效果[4],所以疫苗研究將在H.pylori感染防治中具有廣闊應用前景。食品級乳酸乳球菌(Lactococcuslactis,L.lactis)NZ3900菌株以其安全可靠性而成為備受關注的口服疫苗表達載體[5-6]。Lpp20是一種免疫活性較強且氨基酸序列高度保守的H.pylori保護性抗原[7],目前以L.lactisNZ3900為 Lpp20表達宿主菌的口服疫苗研究尚少有報道。該研究構建表達Lpp20抗原的重組L.lactis菌株,并鑒定其作為H.pylori疫苗菌株的免疫活性。
1材料與方法
1.1質粒與菌株L.lactisNZ3900菌株和質粒載體pNZ8149購自荷蘭NIZO食品研究所;H.pyloriHp27菌株為河南省分子醫學重點實驗室保種菌株,分離自鄭州市慢性萎縮性胃炎患者;質粒載體pNZ8149-SPusp45由河南省分子醫學重點實驗室前期構建;質粒載體pMD19-T購自大連寶生物公司。
1.2主要試劑pMD19-T克隆載體、質粒提取試劑盒、凝膠DNA回收試劑盒、T4 DNA連接酶、限制性內切酶及DL2000 Marker和pyrobest DNA 聚合酶購自TaKaRa公司,誘導劑Nisin為美國Sigma公司產品。
1.3H.pylorilpp20基因的PCR擴增用堿裂解法提取H.pyloriHp27菌株的基因組DNA。擴增lpp20基因的PCR引物由上海生工生物工程有限公司合成,引物序列:5’-CGAGTCGCATGCATGAAAAATCAAGTTA-3’(上游),5’-GCTCTAGACTACTTTTTAACCATGCCCAA-3’(下游)。在上游和下游引物中分別含有SphⅠ和XbaⅠ酶切位點。采用pyrobest DNA聚合酶和上述引物,以Hp27 基因組DNA為模板,PCR擴增lpp20基因,PCR反應條件為:預變性94 ℃5 min,94 ℃變性30 s,55 ℃退火30 s;72 ℃終延伸5 min。
1.4H.pylorilpp20基因克隆和鑒定將PCR產物用10 g/L瓊脂糖凝膠進行電泳分析,并用凝膠回收試劑盒回收,將回收的基因片段與質粒載體pMD19-T連接后,用于轉化E.coliDH5α感受態細胞。通過藍白斑篩選得到陽性轉化子,用試劑盒從轉化子中提取質粒,經PCR和酶切鑒定后,將重組質粒pMD19-T-lpp20交由上海生工生物工程有限公司測序。
1.5表達載體的構建和L.lactis的轉化分別將pMD19-T-lpp20和L.lactis質粒載體pNZ8149-SPusp45用SphⅠ+XbaⅠ進行雙酶切,用試劑盒回收lpp20基因和載體pNZ8149-SPusp45的酶切片段,以T4 DNA連接酶于室溫連接2 h,將10 μL連接產物與100 μLL.lactisNZ3900感受態細胞混勻后,轉入預冷的電擊杯進行電轉化[8]。電擊參數:脈沖25 μF、電阻200 Ω、電壓1 250 V,電擊后加入1 mL預冷的GM17MC恢復培養基,將菌液轉入1.5 mL的離心管中,冰上靜置5 min,30 ℃、體積分數5%CO2條件下靜止恢復培養2 h, 取100 μL恢復培養的菌液接種到Elliker選擇固體培養基上[8],在30 ℃、體積分數5%CO2條件下靜止培養過夜,陽性克隆子為黃色菌落。提取重組菌質粒,通過PCR、酶切、測序進行鑒定。
1.6Lpp20的誘導表達參照文獻[8],將L.lactisNZ3900/pNZ8149-SPusp45和L.lactisNZ3900/pNZ8149-SPusp45-lpp20單菌落分別接種于10 mL GM17液體培養基中,30 ℃、體積分數5%CO2條件下靜止培養過夜。次日取過夜培養的菌液2 mL加入到50 mL的GM17液體培養基中,在菌液OD600nm=0.3~0.4時,加入Nisin液至終濃度為25 mg/L,誘導5 h,將菌液4 ℃離心,分別收集上清和菌體,上清中加入終體積分數為10%的三氯乙酸于4 ℃過夜,次日收集沉淀,-20 ℃貯存備用;用原菌液0.1倍體積的磷酸緩沖液重懸菌體,加溶菌酶37 ℃水浴,1 h后用超聲細胞壁儀破壁,4 ℃離心收集上清,即為菌體蛋白,-20 ℃貯存備用。
1.7Western blot檢測采用120 g/L分離膠和50 g/L濃縮膠進行SDS-PAGE分析,重組菌株的菌體可溶性蛋白和培養液上清蛋白樣品按每孔20~50 μg上樣。電泳約3 h,凝膠用考馬斯亮藍R250染色,脫色,待蛋白條帶清晰后,用凝膠圖像分析儀進行分析。重組乳酸菌表達產物經SDS-PAGE電泳后,用濕轉法轉膜,采用課題組前期自制的小鼠抗H.pylori血清作為一抗,辣根過氧化物酶標記的羊抗鼠IgG為二抗,根據需要量將增強型發光劑和穩定劑混合配置為化學發光檢測底物,進行Western blot分析。
2結果
2.1H.pylorilpp20基因的PCR擴增以H.pyloriHp27菌株基因組DNA為模板,lpp20基因的PCR產物電泳結果見圖1。
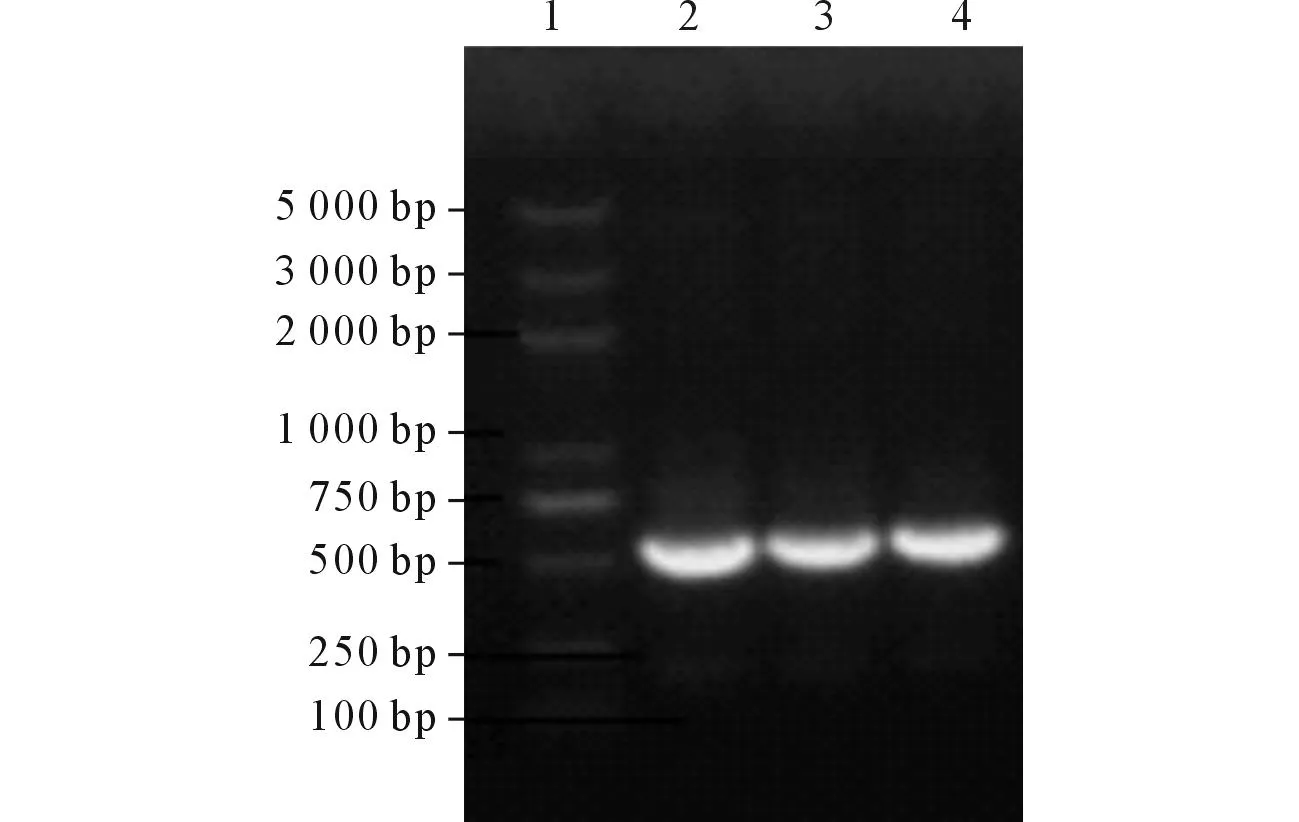
1:DNA Marker;2、3、4:lpp20 PCR產物。圖1 H. pylori lpp20基因的PCR擴增
2.2H.pylorilpp20基因克隆和鑒定構建的重組質粒pMD19-T-lpp20的PCR和雙酶切鑒定結果正確(圖2),測序結果與GenBank 報道Hp27 lpp20基因序列(GI:31540586)同源性為97%,對應的氨基酸序列相同。
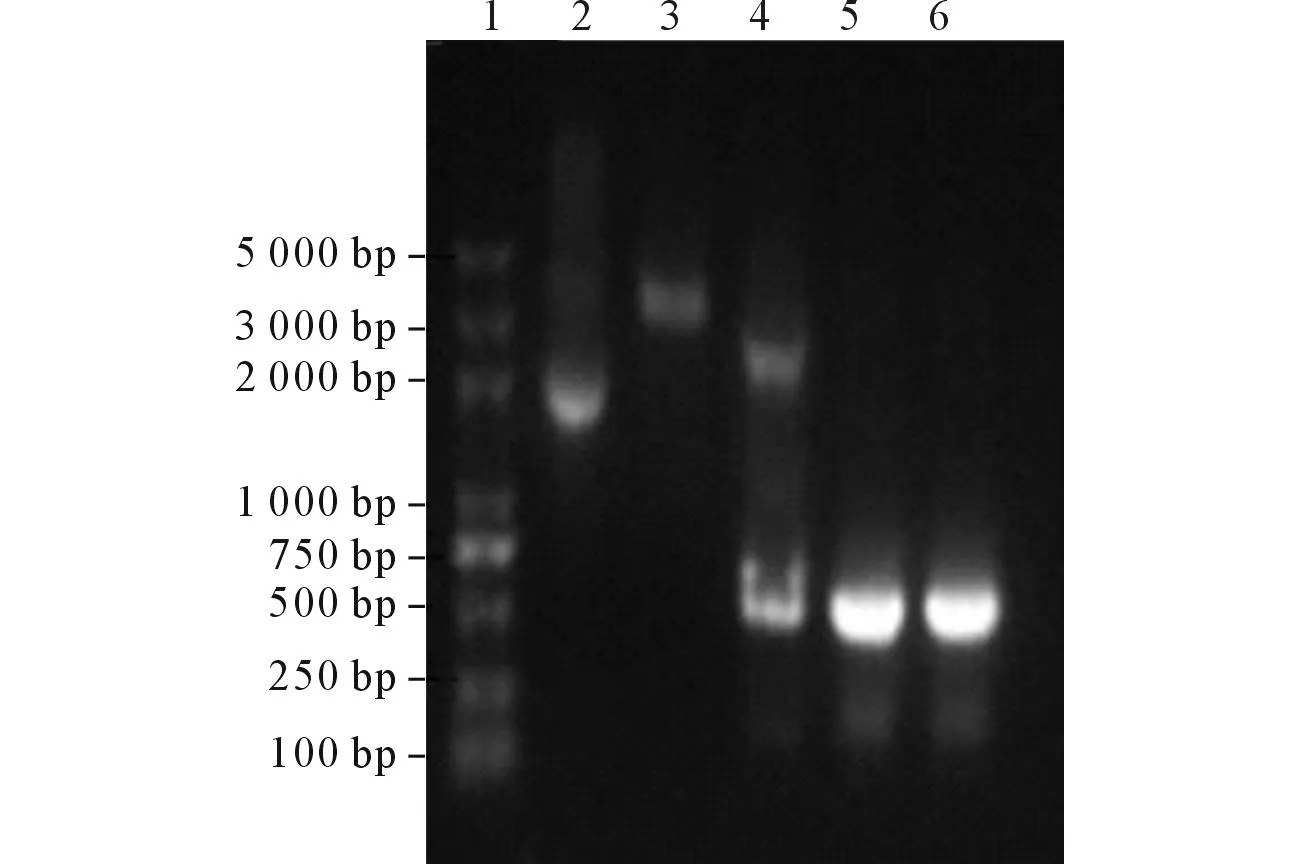
1:DNA Marker;2:pMD19-T-lpp20質粒;3:質粒pMD19-T-lpp20單酶切;4:質粒pMD19-T-lpp20雙酶切;5:以重組質粒為模板lpp20 PCR產物;6:以H. pylori基因組DNA為模板lpp20 PCR產物。圖2 重組質粒pMD19-T-lpp20的PCR和酶切鑒定
2.3重組質粒pNZ8149-SPusp45-lpp20的構建L.lactis經電轉化后,在Elliker篩選培養板生長出金黃色陽性菌落,菌落經培養后提取質粒,重組質粒的PCR、酶切鑒定(圖3)及測序結果符合預期。
2.4重組L.lactis菌株表達產物鑒定L.lactis菌株誘導表達產物的SDS-PAGE分析結果顯示重組菌株與原菌株蛋白條帶差異不明顯。Western blot分析結果顯示,重組菌株菌體總蛋白和培養液上清蛋白樣品中均檢出相對分子質量約為20 000的Lpp20表達產物,重組表達的Lpp20蛋白與小鼠抗H.pylori免疫血清發生明顯的陽性反應(圖4、5)。
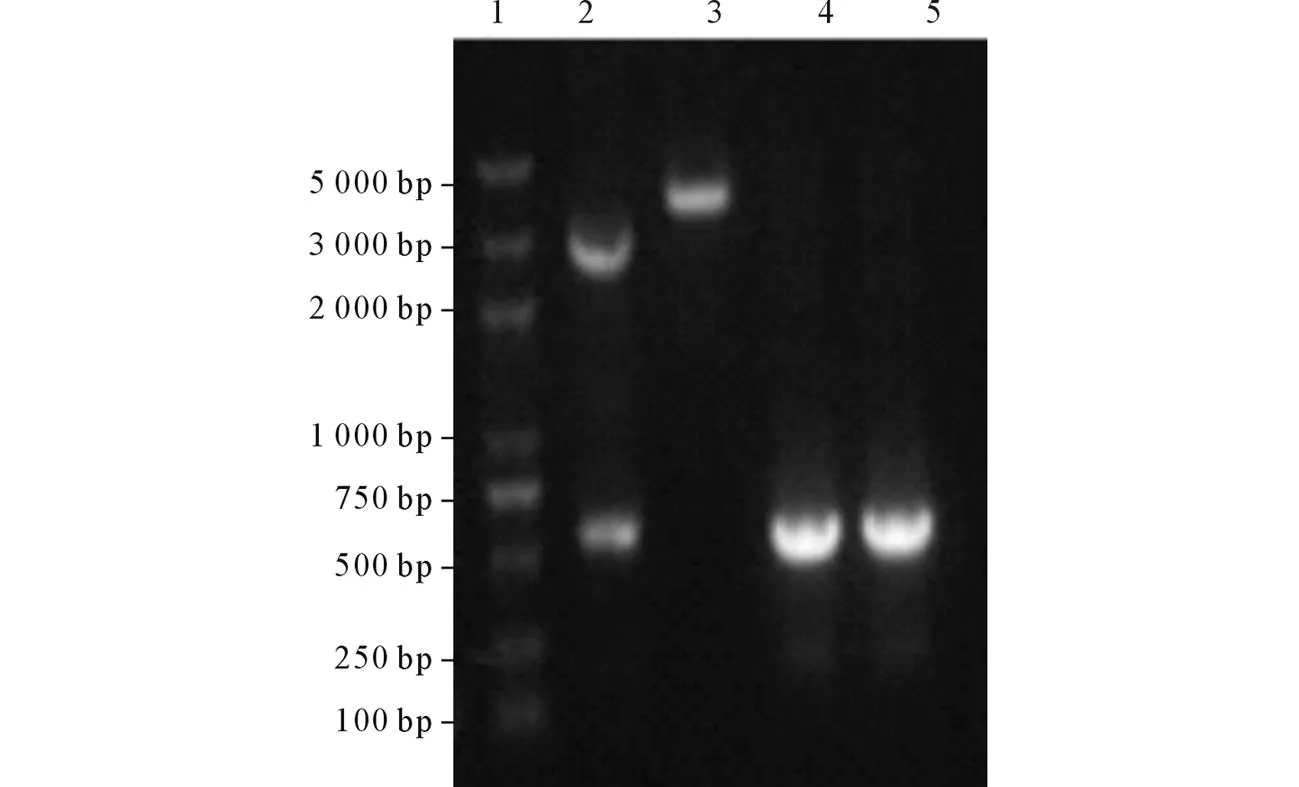
1: DNA Marker;2:質粒pNZ8149-SPusp45-lpp20雙酶切;3:質粒pNZ8149-SPusp45-lpp20單酶切;4:以重組質粒為模板lpp20基因的 PCR產物;5:以H. pylori全基因組為模板lpp20 PCR產物。圖3 重組質粒pNZ8149-SPusp45-lpp20的PCR和酶切鑒定

1:蛋白Marker;2:L.lactis NZ3900/pNZ8149-SPusp45-lpp20菌體總蛋白;3:L.lactis NZ3900/pNZ8149-SPusp45菌體總蛋白。 圖4 L.lactis 重組菌株菌體蛋白樣品的Western blot結果

1:蛋白Marker;2:L.lactis NZ3900/pNZ8149-SPusp45-lpp20 培養基上清蛋白;3:L.lactis NZ3900/pNZ8149-SPusp45培養基上清蛋白。圖5 L.lactis 重組菌株培養基上清樣品的Western blot結果
3討論
臨床上常用抗生素治療H.pylori的感染,對這類疾病頻繁采用抗生素治療可致使細菌耐藥性增加,而且對重復感染無預防作用[9],所以更有效的防治只能寄希望于疫苗研究的成功。在疫苗研究中,口服疫苗以其免疫途徑安全、方便、合理等優點而受到關注,然而,缺乏安全有效的疫苗載體阻礙了口服疫苗研究發展。現有研究[10]多采用減毒傷寒沙門氏菌作為口服疫苗載體,由于沙門氏菌屬于致病菌,減毒株不僅仍具有一定的毒性,而且還存在遺傳穩定性問題,應用于人體時其安全性難以保證。而且這類疫苗應用于人體時,檢測不到或僅引起微弱的免疫反應,免疫效果遠低于動物實驗[11]。因此,有必要探討更安全有效的口服疫苗載體。
L.lactis是乳酸菌類的一個菌種,在食品加工中的應用已有悠久的歷史,屬于食品級的益生菌,安全性十分可靠,且其生長迅速,易于培養,遺傳背景和調控機制相對清楚,作為口服疫苗載體具有很大潛力。在基因工程領域,已建立一系列基于乳酸菌的遺傳轉化系統,應用這些系統定向生產人類所需要的產品將成為熱點。乳酸菌遺傳轉化系統中應用較多的是NICE系統。L.lactisNZ3900/pNZ8149是NICE系統中的一種,其誘導劑、篩選標記和宿主均為食品級,是食品級安全的外源基因表達系統,在安全性方面的優勢十分突出[5-6,12]。作者所在的實驗室前期為了擴大該系統表達外源基因的功能,通過在pNZ8149核苷酸序列中插入編碼信號肽的SPusp45序列,以期得到能分泌表達外源基因的pNZ8149-SPusp45。該研究結果表明,pNZ8149-SPusp45能夠在L.lactisNZ3900中分泌表達外源基因Lpp20,為口服疫苗研究提供了一種新的抗原表達載體系統。
從H.pylori疫苗保護性抗原的研究進展上看, 理想的疫苗候選抗原應該具有特異性、保守性、低毒性、能夠定位于病原的表面等特征,H.pylori的Lpp20蛋白是定位于細菌外膜上的一種高度保守的脂蛋白,現有研究[13]顯示Lpp20是一種理想的疫苗候選抗原。雖有研究[7]表明,分離自菌體外膜囊泡的Lpp20蛋白具有良好的免疫原性和免疫保護性,但由于采用這種方法制備疫苗抗原較困難,Lpp20抗原在疫苗方面應用研究受到限制。該研究構建的L.lactis重組表達系統為Lpp20制備提供了一種新的方法。
該研究構建的重組菌株L.lactisNZ3900/pNZ8149-SPusp45-lpp20中除H.pylori疫苗抗原基因lpp20外,其余成分均具有食品級安全性,極大限度地提高了該工程菌株作為疫苗菌株的安全性[6]。該實驗結果表明該菌株能夠分泌表達Lpp20蛋白,且表達的Lpp20蛋白與小鼠抗H.pylori血清發生較強的免疫反應。
綜上所述,重組菌株L.lactisNZ3900/pNZ8149-SPusp45-lpp20不僅具有作為口服疫苗的應用潛力,而且有望作為發酵菌株,用于食品加工,尤其是乳制品發酵工藝中,生產具有防治幽門螺桿菌感染及相關胃腸疾病作用的保健食品,產生可觀的社會經濟效益。
參考文獻
[1]DA COSTA DM,PEREIRA EDOS S,RABENHORST SH.What exists beyond cagA and vacA?Helicobacterpylorigenes in gastric diseases[J].World J Gastroenterol,2015,21(37):10563
[3]張萬岱,胡伏蓮,蕭樹東,等.中國自然人群幽門螺桿菌感染的流行病學調查[J].現代消化及介入診療,2010,15(5):265
[4]楊鈺欣,李丹丹.幽門螺桿菌疫苗相關研究進展[J].中國免疫學雜志,2012,28(5):478
[5]ZHANG XJ,FENG SY,LI ZT,et al.Expression ofHelicobacterpylorihspA gene inLactococcuslactisNICE system and experimental study on its immunoreactivity[J].Gastroenterol Res Pract,2015,2015:750932
[7]KEENAN J,OLIARO J,DOMIGAN N,et al.Immune response to an 18-kilodalton outer membrane antigen identifies lipoprotein 20 as aHelicobacterpylorivaccine candidate[J].Infect Immun,2000,68(6):3337
[8]CHEN S,ZHANG R,DUAN G,et al.Food-grade expression ofHelicobacterpyloriureB subunit inLactococcuslactisand its immunoreactivity[J].Curr Microbiol,2011,62(6):1726
[9]KRISTENSEN D,CHEN D.Strategies to advance vaccine technologies for resource-poor settings[J].Vaccine,2013,31(Suppl 2):B157
[10]GUNN BM,WANDA SY,BURSHELL D,et al.Construction of recombinant attenuated Salmonella enterica serovar
typhimurium vaccine vector strains for safety in newborn and infant mice[J].Clin Vaccine Immunol,2010,17(3):354
[11]ANDERL F,GERHARD M.Helicobacterpylorivaccination: is there a path to protection?[J].World J Gastroenterol,2014,20(34):11939
[12]MIERAU I,KLEEREBEZEM M.10 years of the nisin-controlled gene expression system (Nice) inLactococcuslactis[J].Appl Microbiol Biotechnol,2005,68(6):705
[13]岳俊杰,李北平,周圍,等.幽門螺桿菌Lpp20蛋白的生物信息學分析[J].生物技術通訊,2009,20(5):651
(2015-12-11收稿責任編輯李沛寰)
doi:10.13705/j.issn.1671-6825.2016.04.011
#通信作者:張榮光,男,1968年5月生,博士,副教授,研究方向:分子流行病學,E-mail:zrg@zzu.edu.cn;段廣才,男,1958年8月生,博士,教授,研究方向:分子流行病學,E-mail: gcduan@zzu.edu.cn
中圖分類號R183
關鍵詞乳酸菌;lpp20基因;幽門螺桿菌;分泌表達;食品級
Expression of Helicobacter pylori lpp20 gene in food-grade Lactococcus lactis and its immunoreactivity
SUN Nan,ZHANG Rongguang,DUAN Guangcai,CHEN Shuaiyin,PENG Xiaoyan,FAN Qingtang,XI Yuanlin
DepartmentofEpidemiology,CollegeofPublicHealth,ZhengzhouUniversity;HenanKeyLaboratoryofMolecularMedicine,Zhengzhou450001
Key wordsLactococcus lactis;lpp20 gene;Helicobacter pylori;secretary expression;food-grade
AbstractAim: To construct a food-grade expression system of Helicobacter pylori(H. pylori) lpp20 gene in Lactococcus lactis(L.lactis) and evaluate its immunoreactivity with aim to establish basis for development of safe and efficient orally administrable vaccine against H. pylori. Methods: The lpp20 gene was obtained by PCR amplification from the genomic DNA of H. pylori, and ligated to plasmid pMD19-T and then to the expression vector pNZ8149-SPusp45. The recombinant pNZ8149-SPusp45-Lpp20 was electrotransformed into L.lactis NZ3900. The resultant recombinant strains were induced to express the exogenous gene with Nisin, and the expression products were assessed by Western blot. Results: The length of the amplified lpp20 gene by PCR was estimated 540 bp. The gene fragments were correctly inserted into the vector as identified by enzyme digestion, PCR and gene sequencing. The expression product of lpp20 gene was detected both in the bacterium digestion and the culture media samples, and with a relative molecular weight of 20 000,which was immunoreactive to anti-H. pylori mouse sera. Conclusion: The recombinant strain of L.lactis capable of secretary expression of H. pylori antigen Lpp20 has been successfully constructed and, shows potential for being an anti-H. pylori vaccine candidate.
*中國博士后科學基金資助項目20070410252

