蒙脫石對水溶液中甘氨酸的吸附特性及機理
郭玉婷,董發勤,劉明學,秦永蓮,周青,吳傳龍,宗美榮,黃婷,劉媛媛
(1. 西南科技大學 生命科學與工程學院,四川 綿陽,621010;2. 西南科技大學 固體廢物處理與資源化教育部重點實驗室,四川 綿陽,621010;3. 西南科技大學 材料科學與工程學院,四川 綿陽,621010)
蒙脫石對水溶液中甘氨酸的吸附特性及機理
郭玉婷1,董發勤2,劉明學1,秦永蓮2,周青2,吳傳龍3,宗美榮2,黃婷1,劉媛媛1
(1. 西南科技大學 生命科學與工程學院,四川 綿陽,621010;2. 西南科技大學 固體廢物處理與資源化教育部重點實驗室,四川 綿陽,621010;3. 西南科技大學 材料科學與工程學院,四川 綿陽,621010)
研究蒙脫石對不同濃度甘氨酸在水溶液中的吸附特性及機理。采用X線衍射(XRD)、全反射傅里葉變換紅外光譜(ATR-FTIR)和等離子體發射光譜(ICP-AES)等手段對吸附樣品進行性質表征。研究結果表明:蒙脫石平衡吸附量隨甘氨酸濃度升高而增加,在甘氨酸濃度為0.01~0.20 mol/L范圍內,蒙脫石吸附甘氨酸符合Freundlich等溫吸附模型。蒙脫石層間陽離子解吸總量小于其對甘氨酸的平衡吸附量,且蒙脫石 d(001)由 1.528 nm 減小到1.446 nm,揭示蒙脫石吸附甘氨酸是通過層間陽離子交換機制,但陽離子交換非惟一方式。蒙脫石吸附甘氨酸存在陽離子交換和端面吸附2種機制:通過COO-與蒙脫石端面正電基團間的靜電作用力吸附甘氨酸兩性離子;通過與蒙脫石層間基面氧原子形成氫鍵吸附甘氨酸正離子。
蒙脫石;甘氨酸;端面吸附;陽離子交換;全反射傅里葉變換紅外光譜
目前,對于黏土礦物表面與氨基酸相互作用的研究已深入到廣泛的領域,如水地球化學[1]、土壤科學[2]和生命起源探索[3]等。早在 1987年,HEDGES等[1]的研究已證實自然界的水體和沉積物中均存在可檢測的溶解性游離氨基酸,其遷移過程與自然條件下的吸附作用密切相關。生命起源以前,地殼中大量存在著黏土礦物,其在生命起源的化學演化過程中的作用至關重要。從氨基酸小分子到多肽的生命進化過程中,SiO2,Al2O3和黏土礦物等都起到了重要的催化作用。也有相關研究表明氨基酸與黏土礦物間存在的鍵合作用能較好地解釋生命起源以前氨基酸的化學演化[4-5]。生命出現后,氨基酸作為多肽、蛋白質的基本結構單元,廣泛存在于自然界的各生命體中。因此,研究黏土礦物對可溶性氨基酸的吸附行為及其機制對闡明黏土礦物與氨基酸分子在生命進化過程中的相關反應至關重要。氨基酸作為一種兩性物質,其解離狀態與溶液pH密切相關。目前已有報道稱氨基酸的活性基團可以通過靜電吸引、疏水作用、共價鍵合以及氫鍵等方式與黏土或氧化物發生吸附作用[3, 6]。現有研究發現由于黏土礦物的陽離子交換性,通常其對堿性氨基酸的吸附較中性和酸性氨基酸強[4, 7-8]。而且黏土礦物的層間陽離子類型也會對其吸附氨基酸造成影響。有關黏土礦物對自然環境中氨基酸的吸附研究多在實驗室可控條件下進行,但主要是對吸附條件、吸附量等的研究,而且其結果受黏土和氨基酸種類以及具體實驗條件的影響也較大[9]。鑒于黏土礦物和氨基酸在生命演化中的重要地位以及環境中二者的相互作用機制仍不明確等現狀,本文作者借助XRD,ATR-FTIR以及ICP-AES等分析手段對蒙脫石與甘氨酸在水溶液中的吸附特性進行探討。
1 實驗部分
1.1材料與試劑
蒙脫石樣品購自浙江三鼎科技有限公司,采用XRD和定量 X線熒光(XRF)光譜法測定其物相和成分。經XRF定量分析可知,各元素組分含量(質量分數,下同)分別為SiO259.33 %,Al2O319.91 %,CaO 1.86%,MgO 3.64%,K2O 0.59%,Fe2O31.68%,Na2O 1.00%,LOI 9.98%;經XRD分析可知蒙脫石純度較高,d(001)為1.528 nm(d為距離),d(300)為0.149 nm,該蒙脫石樣品為鈣基蒙脫石。在吸附實驗中,甘氨酸和蒙脫石樣品不再經任何加工處理。實驗所用甘氨酸、無水乙醇、HCl、NaOH和茚三酮均為分析純試劑,所有用水均為去離子水。
1.2吸附實驗方法
為了確定蒙脫石對甘氨酸吸附平衡時間和吸附最合適pH,首先進行時間和pH影響蒙脫石吸附甘氨酸的批量吸附實驗。準確量取20 mL濃度為0.05 mol/L的氨基酸水溶液,于 50 mL錐形瓶中,加入蒙脫石0.2 g,分別吸附2~24 h后終止反應。
采用1 mol/L NaOH和1 mol/L HCl調節上述甘氨酸水溶液pH在1~10之間,準確量取不同pH的甘氨酸水溶液20 mL于50 mL錐形瓶中,分別加入0.2 g蒙脫石,吸附12 h后終止反應(時間影響吸附的實驗中蒙脫石對甘氨酸的吸附于12 h達到平衡,下同)。在上述吸附實驗中,同時設置氨基酸水溶液染菌對照組,且處理組和對照組均重復3次(下同)。
確定了吸附條件之后,進行了甘氨酸濃度對蒙脫石吸附甘氨酸的影響實驗。配制濃度為 0.01,0.05,0.10,0.15和0.20 mol/L的甘氨酸水溶液,調節pH為3(pH影響吸附的實驗中pH在2~4范圍吸附較好),量取不同濃度甘氨酸水溶液20 mL于50 mL錐形瓶中,加入蒙脫石0.2 g,同時設置對照組(20 mL去離子水+0.2 g蒙脫石,pH=3)和氨基酸水溶液染菌對照組。吸附12 h后終止反應。
上述吸附實驗的整個吸附過程均在溫度為25 ℃、轉速為120 r/min的恒溫振蕩器中進行,恒溫振蕩平衡相應時間后,取反應終止液于4 000 r/min離心20 min,并將上清液用0.22 μm微孔濾膜過濾,獲得的上清液用于測定剩余氨基酸濃度、pH和元素溶出;沉淀物用去離子水洗滌3次,自然干燥后進行XRD分析。
1.3表征方法
1.3.1甘氨酸濃度、元素溶出及pH測定
將吸附實驗中獲得的上清液進行甘氨酸濃度、元素溶出及pH測定。甘氨酸濃度測定采用經典的茚三酮顯色法[10]進行測定。根據標準曲線法計算溶液中氨基酸濃度,平衡時的吸附量 qe按下式計算:qe=10-3V(ρ0-ρe)/m。其中:qe為吸附劑吸附氨基酸平衡吸附量,mg/g;ρ0為氨基酸初始質量濃度,mg/L;ρe為吸附平衡時氨基酸質量濃度,mg/L;V為溶液體積,mL;m為吸附劑的質量,g。
溶出元素采用等離子發射光譜儀(iCAP6500,美國Thermo Fisher公司)進行測定,所得結果以處理組減去對照組來表示。
1.3.2XRD測定
將吸附實驗中獲得的蒙脫石干燥沉淀物采用荷蘭帕納科公司的X’Pert Pro 型X線衍射儀進行XRD分析。分析條件:輻射源為Cu靶,Kα(Kα1=1.540 598× 10-10m,Kα2=1.544 426×10-10m),管電壓為40 kV,管電流為 40 mA,掃描范圍為 2θ=3°~80°,步長為0.03°,用X'Pert HighScore Plus軟件對XRD圖譜進行分析。
1.3.3ATR-FTIR測定
1.3.3.1溶液中甘氨酸的ATR-FTIR測定
配制濃度為0.05 mol/L的甘氨酸水溶液,調節pH 為4.33,6.18和9.07,對不同pH下的甘氨酸水溶液進行ATR測試,獲得的譜圖與水的譜圖作差譜,得到水溶液中甘氨酸的譜圖。
1.3.3.2蒙脫石吸附甘氨酸的ATR-FTIR測定
準確量取上述不同pH的甘氨酸水溶液5 mL于10 mL反應管中,分別加入準確稱量好的蒙脫石0.05 g,同時設置對照組(5 mL去離子水+0.05 g蒙脫石)。將混合體系置于25 ℃,120 r/min的恒溫振蕩器中進行吸附,恒溫振蕩吸附12 h后,取部分反應混合液直接進行ATR測試,獲得的圖譜分為4部分:被吸附的甘氨酸、未被吸附的甘氨酸、蒙脫石和水。為了只得到被吸附到蒙脫石上的甘氨酸的譜圖,將剩余反應液于4 000 r/min離心20 min,并將上清液用0.22 μm微孔濾膜過濾,所得的上清液進行ATR測試,得到未被吸附甘氨酸的譜圖;將對照組進行ATR測試,獲得蒙脫石和水的譜圖。將混合液譜圖與上清液和對照譜圖作差譜,最終獲得被吸附甘氨酸的譜圖。
在紅外吸收光譜儀(Nicolet-5700,美國尼高力儀器公司)的ATR附件上進行ATR測試,測試條件:譜圖采集范圍為400~4 000 cm-1,分辨率為4 cm-1,掃描次數為64次。紅外譜圖處理包括基線校準、平滑等,作差譜時差減因子為 0.95~1.00,通過 OMIC軟件完成。
2 結果與討論
2.1蒙脫石吸附甘氨酸的定量分析
甘氨酸是一種中性非極性氨基酸,是組成多肽、蛋白質結構的最小單元。甘氨酸是一種兩性電解質,等電點pI為5.97,存在酸式和堿式電離2種方式,解離方程式如圖1所示。圖2所示為甘氨酸在不同pH下各離子的摩爾分數。
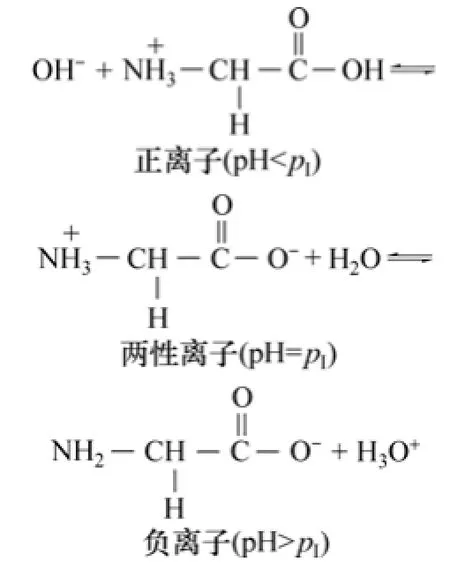
圖1 甘氨酸的酸式和堿式解離方程式Fig. 1 Acid and alkaline dissociation equation of glycine
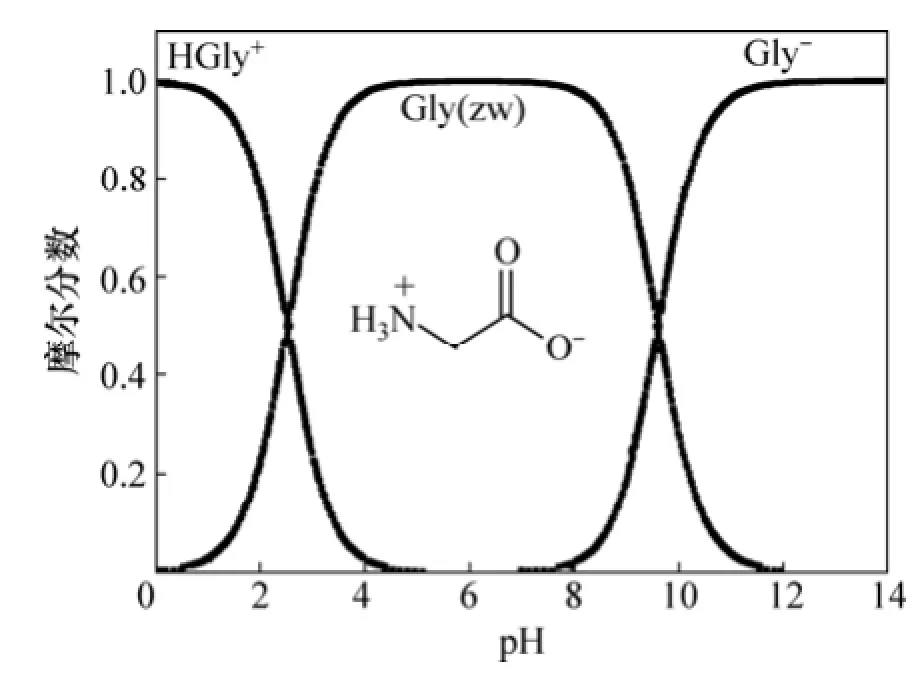
圖2 甘氨酸在不同pH下各離子的摩爾分數Fig. 2 Mole fraction of different dissociation states of dissolved glycine as function of pH
當溶液pH<pI時,甘氨酸為堿式電離,隨著pH降低,甘氨酸正離子逐漸增加,兩性離子逐漸減少;當溶液pH>pI時,甘氨酸為酸式電離,隨著pH升高,甘氨酸兩性離子逐漸減少,負離子逐漸增加;當溶液pH=pI時,甘氨酸主要以兩性離子形式存在(圖2[11])。因此甘氨酸電離出的不同離子種類的相對量與不同pH下的甘氨酸的電離狀態密不可分。蒙脫石對甘氨酸的吸附在不同pH范圍有所不同,主要由甘氨酸的電離特性和蒙脫石的結構性質共同決定。
在時間和pH影響蒙脫石吸附甘氨酸的批量吸附實驗中(在吸附前后,染菌對照組的甘氨酸濃度無變化表明吸附中沒有染菌現象發生,下同),不同吸附時間蒙脫石對甘氨酸的吸附如圖3所示。吸附0~8 h時,蒙脫石對甘氨酸的平衡吸附量隨時間增加較快; 吸附8~12 h之間時,蒙脫石對甘氨酸的平衡吸附量隨時間增長較緩;吸附12 h后趨于穩定。因此,蒙脫石對甘氨酸的吸附于12 h左右達到平衡。蒙脫石在不同pH條件下對甘氨酸的平衡吸附量如圖4所示。當pH為1~3時,蒙脫石對甘氨酸的平衡吸附量較大;當pH為3~5時,蒙脫石對甘氨酸的平衡吸附量較 pH為 1~3有所降低;當pH為5~9時,蒙脫石對甘氨酸的平衡吸附量大大減少,且趨于穩定,表明酸性條件下,蒙脫石對甘氨酸的吸附較佳。且有學者指出在酸性條件下,尤其是pH為3時對蒙脫石吸附甘氨酸最有利[11]。因此,根據上述結果確定了本研究的吸附條件:pH為3,吸附時間為12 h。
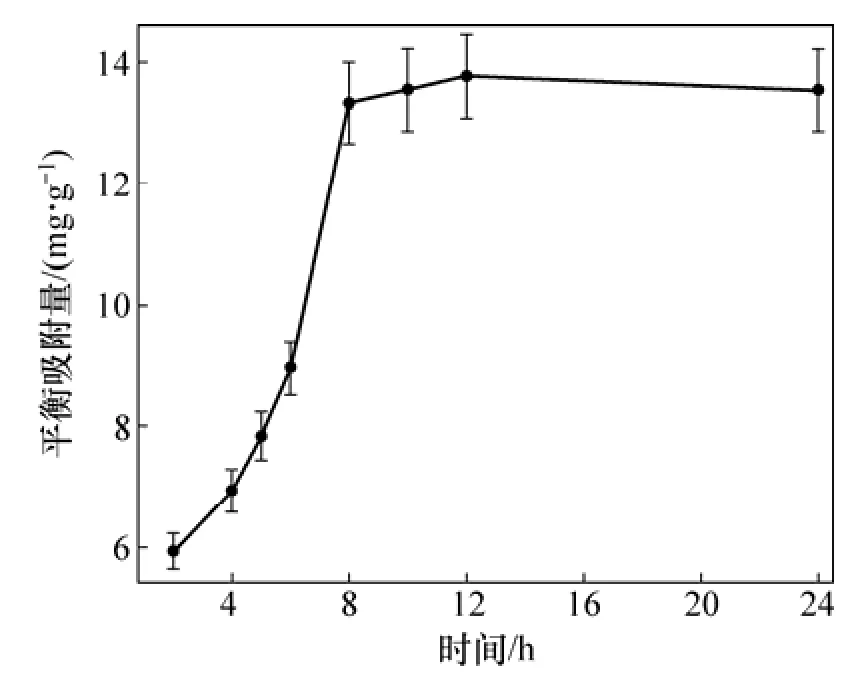
圖3 蒙脫石對甘氨酸的平衡吸附量隨時間變化曲線Fig. 3 Equilibrium adsorption quantity of glycine onto montmorillonite as the function of time
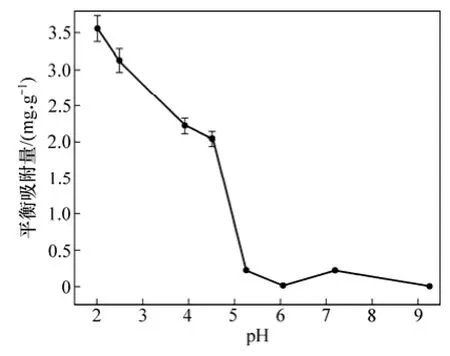
圖4 不同初始pH下蒙脫石對甘氨酸的平衡吸附量Fig. 4 Equilibrium adsorption quantity glycine onto montmorillonite at different initial pH values
在蒙脫石對不同濃度甘氨酸的吸附特性研究實驗中,圖5所示為蒙脫石對不同濃度甘氨酸的平衡吸附量和 Freundlich吸附等溫式。 隨著甘氨酸濃度升高,蒙脫石對甘氨酸的平衡吸附量逐漸增大,線性相關性較好,線性關系為:y =850.05x-6.089 8,R2=0.97。在甘氨酸濃度范圍內(0.01~0.20 mol/L),蒙脫石的平衡吸附量并未達到最大值(圖5)。為了明確蒙脫石對甘氨酸的吸附特性,本研究采用Freundlich等溫吸附模型對蒙脫石吸附不同濃度甘氨酸進行擬合,公式為logqe=logKf+(1/n)logρe,其中:qe為蒙脫石對甘氨酸的平衡吸附量;Kf為與最大吸附能有關的常數[12]。在所研究濃度范圍內,蒙脫石對甘氨酸的吸附基本符合Freundlich等溫吸附模型,其中log Kf=-3.85,n=0.67,R2=0.91。該吸附實驗結果與RAMOS等[11]對甘氨酸的吸附研究結果(log Kf=-0.18,n=0.69,R2=0.97)一致,表明在所研究的甘氨酸濃度范圍內蒙脫石對甘氨酸的吸附機制相同。但PARBHAKAR等[4]在對蒙脫石吸附賴氨酸的研究中發現,在較低賴氨酸濃度(0.025 mol/L)下,蒙脫石對賴氨酸的吸附不符合Freundlich等溫吸附模型,表明蒙脫石對賴氨酸的吸附與甘氨酸有所差異。
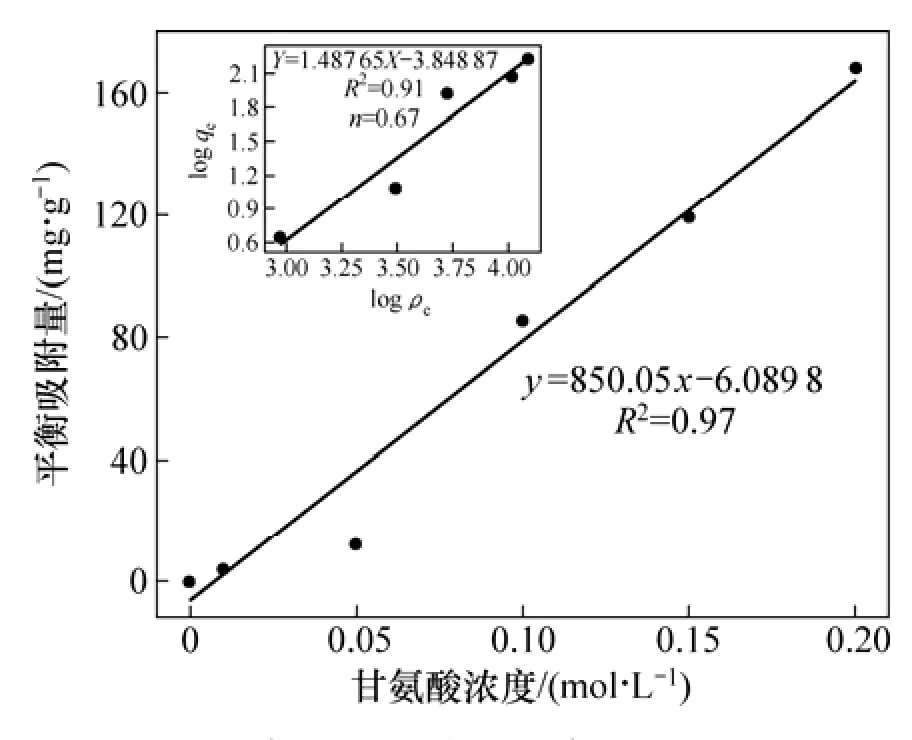
圖5 蒙脫石對甘氨酸的等溫吸附模型Fig. 5 Isotherm adsorption of glycine on montmorillonite
吸附平衡后溶液體系中蒙脫石層間陽離子解吸和甘氨酸平衡吸附量對比如圖6所示。從圖6可知:對比分析蒙脫石對甘氨酸的平衡吸附量和反應后溶液體系中層間主要陽離子(Ca2+,Mg2+和K+)解吸情況發現,隨著甘氨酸濃度升高,3種主要層間陽離子濃度呈現增加趨勢,Ca2+解吸量最多,Mg2+次之,解吸最少的是K+,這可能與3種陽離子在蒙脫石層間的質量分數有關。在甘氨酸的所有處理濃度下,蒙脫石的3種層間陽離子的解吸總量均低于甘氨酸平衡吸附量(圖6),表明蒙脫石吸附甘氨酸可能與層間陽離子交換機制有關,而且還必然涉及到一些其他機制,這與PARBHAKAR等[4]以及RAMOS等[11]的研究結果一致。
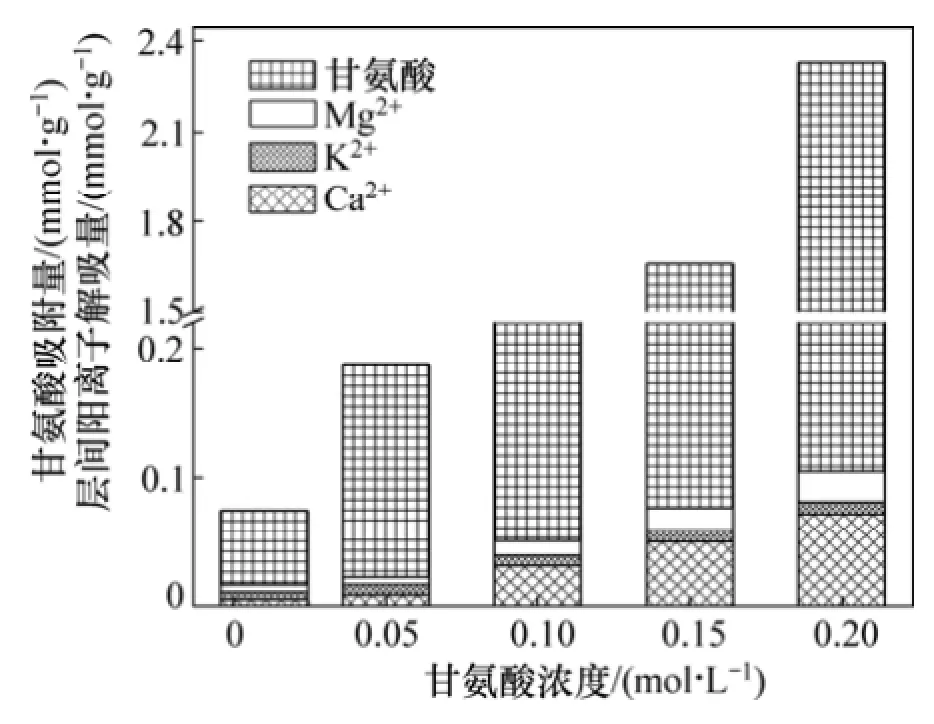
圖6 蒙脫石層間陽離子解吸量與甘氨酸平衡吸附量對比Fig. 6 Comparison of cations desorbed from montmorillonite interlayer and equilibrium adsorption quantity of glycine
另外,蒙脫石與不同濃度甘氨酸吸附平衡后溶液體系pH變化如表1所示。甘氨酸溶液初始pH約為3,吸附平衡之后,不同甘氨酸濃度下pH均有所升高。溶液體系pH增大是H+與蒙脫石層間陽離子發生交換的直接證據。相關研究證實蒙脫石吸附氨基酸可以通過蒙脫石表面與氨基酸間的靜電相互作用、與氨基酸兩性離子間的氫鍵作用力或通過陽離子交換等機制實現[8]。本研究中層間陽離子的解吸暗示蒙脫石吸附氨基酸可能是通過陽離子交換機制,因為在pH為3時,甘氨酸主要以正離子形式存在(圖2)。但是陽離子解吸總量低于甘氨酸平衡吸附量,一方面是因為能與蒙脫石層間陽離子發生交換的不只是甘氨酸正離子,還有可能是溶液體系中的H+;另一方面,3種陽離子的解吸總量與被吸附甘氨酸不同表明層間陽離子交換機制并不是蒙脫石吸附甘氨酸的惟一方式,還可能通過端面吸附的方式,這在蒙脫石吸附甘氨酸的ATR-FTIR分析中將得到證實。另外,也有相關研究發現蒙脫石對甘氨酸的吸附可能存在陽離子交換和端面吸附2種方式[11]。
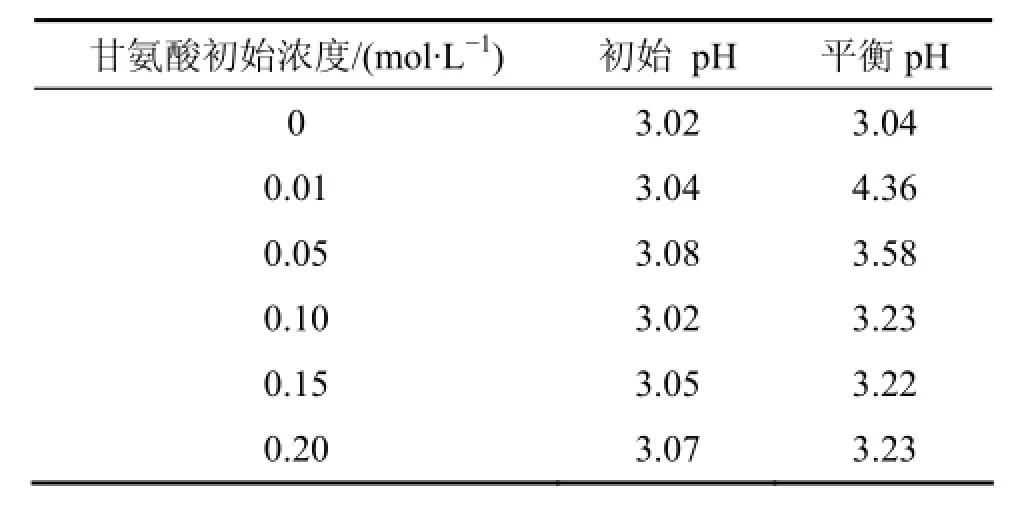
表1 蒙脫石吸附甘氨酸前后溶液的pH變化Table 1 pH value of suspensions of montmorillonite in glycine solutions before and after adsorption
2.2蒙脫石的XRD分析
圖7所示為蒙脫石與不同濃度甘氨酸作用后XRD變化圖。不同初始濃度甘氨酸與蒙脫石吸附平衡后,同對照組相比,處理組蒙脫石d(001)峰的強度、位置和形狀都與甘氨酸初始濃度密切相關(圖7)。
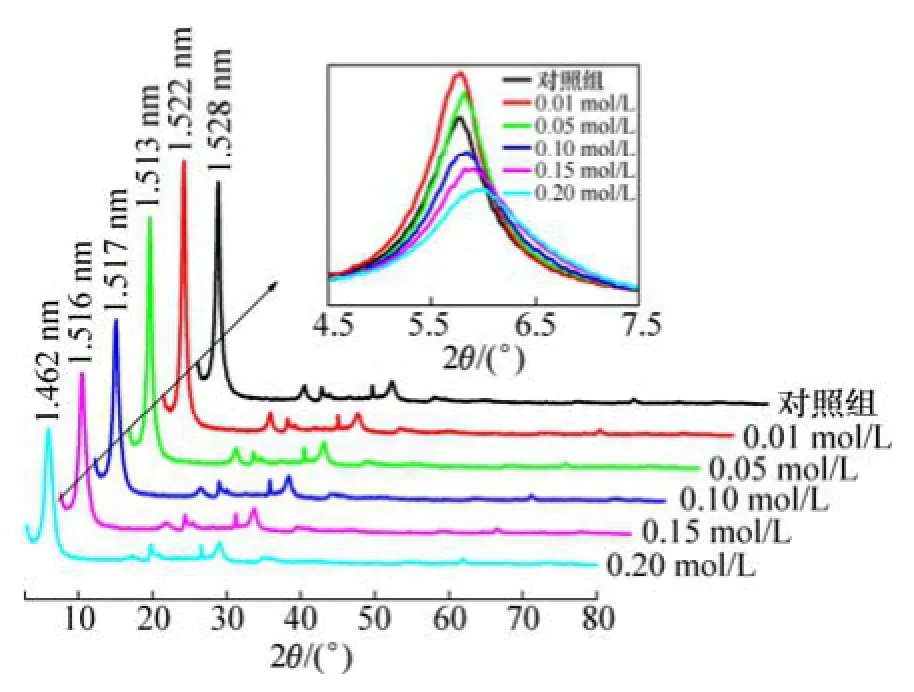
圖7 蒙脫石與不同濃度甘氨酸作用后XRD圖譜Fig. 7 XRD patterns of glycine adsorbed on montmorillonite at different glycine concentrations
隨著甘氨酸初始濃度增加,d(001)由對照組的1.528 nm減小到1.446 nm,表明蒙脫石吸附甘氨酸后層間距減小;且蒙脫石的d(001)衍射峰位隨甘氨酸濃度增加均往高角度方向偏移(由5.78°偏移至6.04°),衍射角變大反映出蒙脫石晶面間距有所減小。當甘氨酸濃度較低(0.01和0.05 mol/L) 時,吸附平衡后蒙脫石的 d(001)峰強度明顯增強;當甘氨酸濃度大于0.1 mol/L時,蒙脫石的d(001)衍射峰強度明顯降低,同時半高峰較對照組明顯增大,說明低濃度和高濃度甘氨酸對蒙脫石d(001)峰的影響存在差異,較高濃度的甘氨酸處理下蒙脫石的晶面間距發生了變化,反映出晶格畸變引起的結晶度下降現象。
蒙脫石吸附甘氨酸后使其自身結構發生了一定程度的改變。一方面,d(001)變小是由于甘氨酸溶液中H+與晶層層間域中可交換陽離子發生交換作用[13]。因為H+半徑小于K+和Ca2+等陽離子半徑,因而發生陽離子交換后蒙脫石的晶層厚度減小[14]。另一方面,有研究表明氨等小分子在蒙脫石表面吸附后,將取代蒙脫石的物理吸附水,由于氨分子動力學直徑(0.26 nm)小于水分子直徑(0.40 nm),導致層間距減小,d(001)降低[15]。因此,甘氨酸被蒙脫石吸附后可能進入了蒙脫石層間取代水分子,由于甘氨酸分子動力學直徑與水分子直徑(0.40 nm)相近,所以,對蒙脫石晶層厚度的改變不明顯。王生新等[16]研究發現蒙脫石在吸附之后,晶層間距未增大,說明膠粒吸附在晶層端面。因此,本研究也有可能由于蒙脫石對甘氨酸的吸附以端面吸附為主,而甘氨酸對蒙脫石層間陽離子的交換吸附為輔,從而對晶層厚度的改變也有限。
2.3蒙脫石吸附甘氨酸的ATR-FTIR分析
為了進一步揭示甘氨酸與蒙脫石相互作用的本質,對比分析了甘氨酸在水溶液和被吸附到蒙脫石上的基團變化情況。
圖8(a)所示為甘氨酸水溶液在 pH為 4.33,6.18和8.07下測得的ATR-FTIR圖譜;圖8(b)所示為在對應pH處理下蒙脫石吸附甘氨酸的ATR-FTIR圖譜。在不同pH下,甘氨酸在水溶液中的ATR吸收峰型非常相似,這是因為在所研究的 pH范圍內,甘氨酸的熱力學解離狀態主要是以甘氨酸兩性離子形式存在(圖2)。表2所示為本研究對甘氨酸的基團解譜對比。
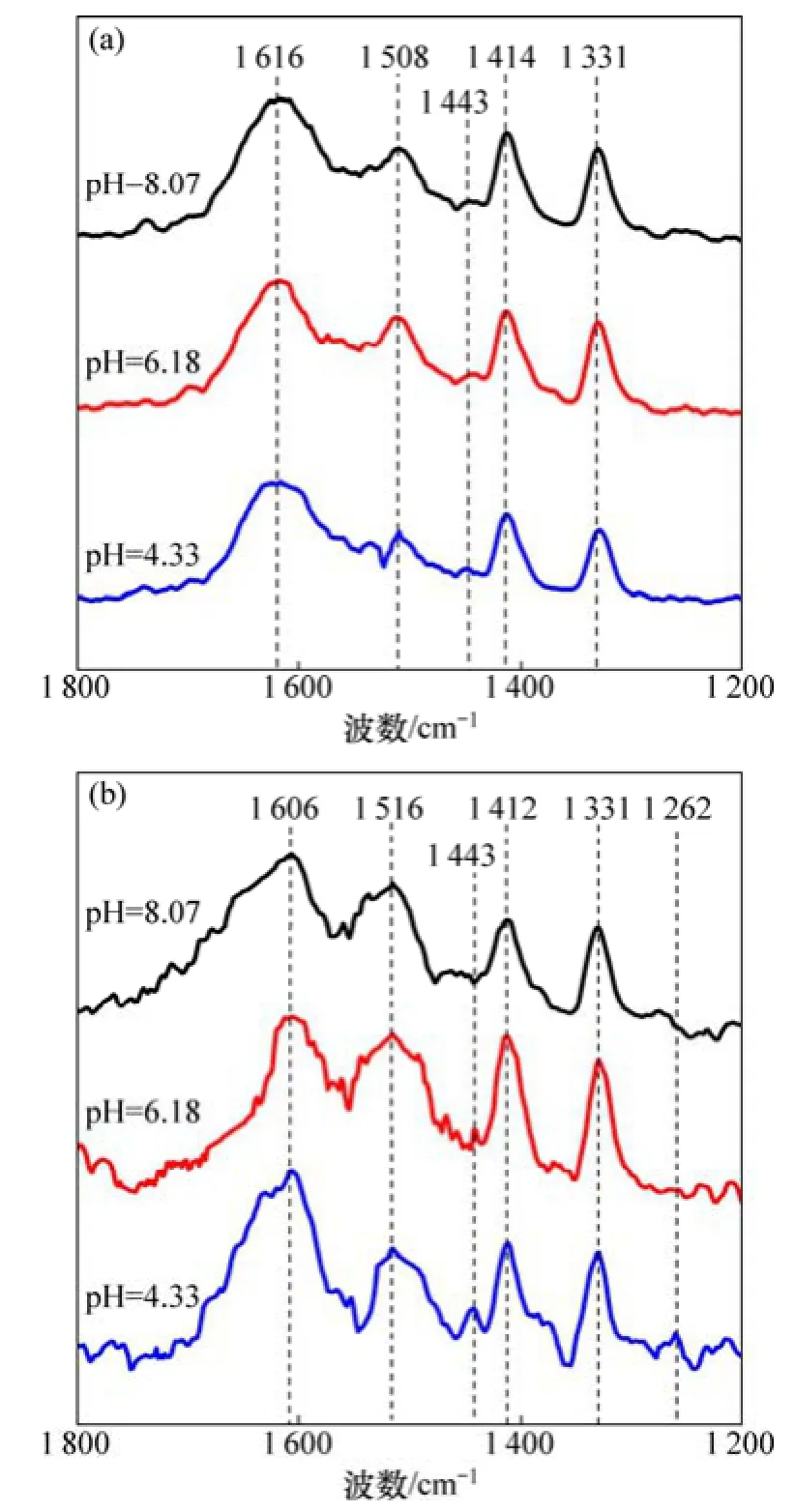
圖8 蒙脫石與不同pH甘氨酸相互作用的FTIR-ATR分析Fig. 8 ATR-FTIR spectra of glycine interacting with montmorillonite at different pH values
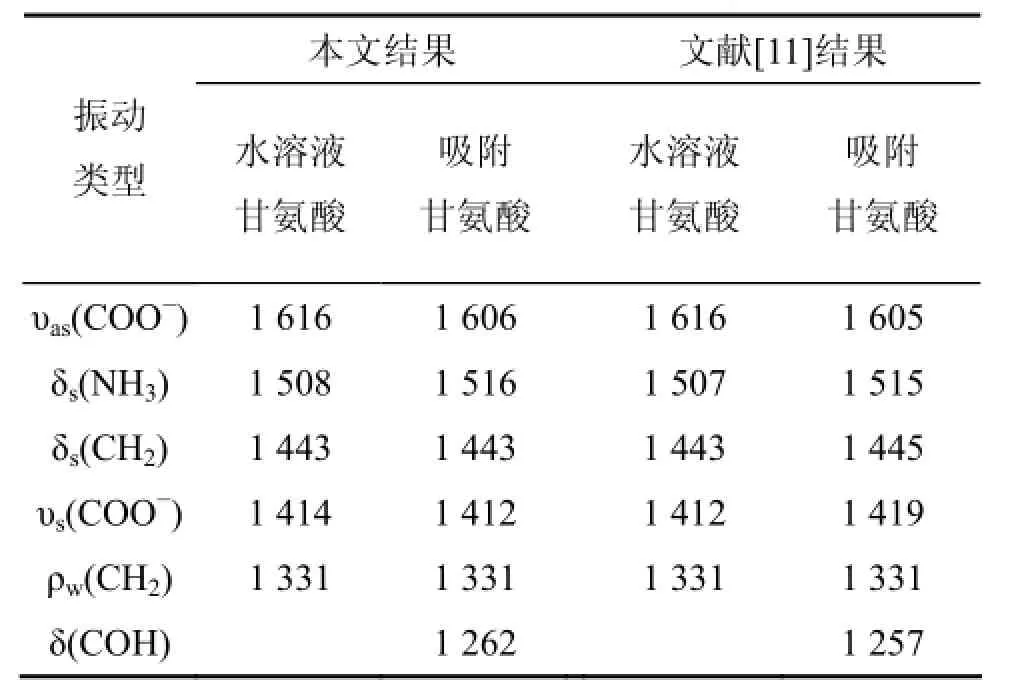
表2 水溶液中氨基酸和蒙脫石吸附氨基酸在1 800~1 200 cm-1范圍的紅外吸收Table 2 Assignments of main aqueous and adsorbed glycine IR bands in 1 800~1 200 cm-1region 波數/cm-1
由圖8可知:蒙脫石吸附的甘氨酸的ATR圖譜8(b)中的吸收峰型與甘氨酸水溶液圖8(a)很相似,表明甘氨酸兩性離子被吸附到了蒙脫石上。對比分析圖8(a)和圖8(b)可見:蒙脫石吸附的甘氨酸相應吸收峰位發生了明顯偏移,這是甘氨酸與蒙脫石發生吸附作用的直接證據。在不同pH條件下,δs(NH3)由1 508 cm-1偏移到較高波數1 516 cm-1,表明甘氨酸的質子化氨基與蒙脫石之間存在相互作用;υas(COO-)由 1 616 cm-1偏移到低波數1 606 cm-1以及υs(COO-)由1 414 cm-1偏移到1 412 cm-1,反映了甘氨酸去質子化的羧基與蒙脫石之間存在吸附作用。這一結果與一些黏土礦物對其他氨基酸吸附研究的FTIR分析結果一致[17]。目前針對蒙脫石與氨基酸相互作用的研究認為:氨基酸能通過 NH3+與蒙脫石層間基面氧原子上的殘余負電荷由于庫侖力而形成氫鍵,發生相互作用[4]。本研究中被吸附到蒙脫石上的甘氨酸ATR-FTIR光譜中主要基團的對應峰位發生的變化再次驗證了上述相互作用機制。δs(NH3)由1 508 cm-1偏移到較高波數1 516 cm-1是氨基與蒙脫石層間基面氧原子存在吸附作用的直接證據,也有關于石英吸附甘氨酸的相關研究表明,二者的吸附機制在于甘氨酸的氨基與石英表面基團形成了氫鍵[18]。另外也有研究表明,蒙脫石對氨基酸的吸附在較低濃度(0.15 mmol/L)下主要是端面吸附,在高濃度時端面吸附達飽和后,還存在陽離子交換吸附機制[11]。
本研究的平衡吸附量與層間陽離子解吸量不一致已證實陽離子交換并不是吸附的惟一機制。而在ATR-FTIR結果中,υas(COO-)由1 616 cm-1偏移到低波數1 606 cm-1以及υs(COO-)由1 414 cm-1偏移到1 412 cm-1,這一現象是甘氨酸通過去質子化的COO-與蒙脫石發生端面吸附作用的直接體現。酸性體系中COO-能和蒙脫石端面發生吸附主要取決于2個因素:1) 產生于蒙脫石硅氧四面體片的基面和硅氧四面體片、鋁氧八面體片的端面破鍵正電荷;2) 鋁氧八面體片中離子離解形成的正電荷。故甘氨酸兩性離子能與蒙脫石帶正電的端面因靜電作用力發生吸附作用。且RAMOS等[11, 19]已證實靜電作用主要產生于COO-與之間。
此外,從圖8(b)可見:當pH為4.33時,在1 262 cm-1處存在吸收峰,該吸收峰為羧基中COH的變形振動δ(COH)。該振動只有在羧基為質子化形式時才會出現,表明盡管在pH為4.33時甘氨酸的解離形態為正離子的存在形式極少(圖2),但是被吸附到蒙脫石上的甘氨酸也有正離子形式。結合δs(NH3)由1 508 cm-1偏移到較高波數1 516 cm-1可推斷,甘氨酸正離子由于氨基質子化使其成為正一價離子而進入了蒙脫石層間域中,進一步為甘氨酸通過陽離子交換被吸附到蒙脫石層間提供了證據。
因此,蒙脫石吸附甘氨酸主要是通過甘氨酸的氨基和羧基實現。圖9所示為蒙脫石與水溶液中甘氨酸相互作用示意圖(忽略比例和定量關系)。二者的相互作用較復雜,蒙脫石對甘氨酸兩性離子存在端面吸附,主要通過 COO-與蒙脫石端面正電基團之間的靜電作用力實現;甘氨酸正離子與蒙脫石層間陽離子也存在交換吸附,正離子進入蒙脫石層間后主要是通過NH3+與蒙脫石層間基面氧原子形成氫鍵進行吸附。此外,溶液體系中還存在著H+與層間陽離子的交換效應,這也就增加了對自然界中蒙脫石吸附氨基酸的定量研究難度。另外,常溫條件下沒有發現甘氨酸低聚反應的發生。因為在ATR-FTIR結果中,并未觀察到酰胺鍵的存在,說明蒙脫石吸附甘氨酸后沒有肽鍵出現。這表明:在一般條件下即使有黏土礦物的參與,氨基酸的聚合也較難發生。BUJDAK等[20]采用不同成分的黏土礦物研究了一些氨基酸的聚合,結果發現只有質量分數為 1.5%的甘氨酸在蒙脫石的參與下發生了聚合反應,因此,氨基酸在一般條件下聚合率很低。
3 結論
1) 在甘氨酸濃度0.01~0.20 mol/L范圍內,蒙脫石對甘氨酸的吸附隨甘氨酸濃度增加而增加,呈現出較好的線性關系,且符合Freundlich等溫吸附模型。
2) 蒙脫石吸附甘氨酸后,其層間距減小、d(001)峰位發生偏移主要因為 H+的陽離子交換效應對蒙脫石d(001)減小的影響強于甘氨酸陽離子交換對層間吸附水的取代效應。
3) 蒙脫石對甘氨酸的宏觀吸附、蒙脫石XRD分析以及ATR-FTIR結果證實蒙脫石對甘氨酸的吸附機制有2種:一個是對甘氨酸兩性離子的端面吸附機制,通過 COO-與蒙脫石端面正電基團之間的靜電作用力實現;另一個是甘氨酸正離子與蒙脫石層間陽離子的交換吸附機制,通過NH3+與蒙脫石層間基面氧原子形成氫鍵進行吸附。
4) 蒙脫石對甘氨酸的吸附實驗揭示了自然界中黏土礦物的存在對可溶性游離氨基酸的分布和遷移具有重要影響。
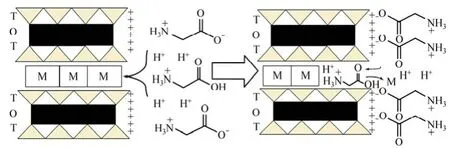
圖9 蒙脫石與水溶液中甘氨酸相互作用示意圖Fig. 9 Schematic diagram of montmorillonite/glycine interaction in aqueous solutions
[1] HEDGES J I, HARE P E. Amino acid adsorption by clay minerals in distilled water[J]. Geochimica et Cosmochimica Acta,1987, 51(2): 255-259.
[2] SENWO Z N, TABATABAI M A. Amino acid composition of soil organic matter[J]. Biology and Fertility of Soils, 1998, 26(3):235-242.
[3] LAMBERT J F. Adsorption and polymerization of amino acids on mineral surfaces: a review[J]. Origins of Life and Evolution of the Biosphere, 2008, 38(3): 211-242.
[4] PARBHAKAR A, CUADROS J, SEPHTON M A, et al. Adsorption of L-lysine on montmorillonite[J]. Colloids and Surfaces A Physicochemical and Engineering Aspects, 2007, 307:142-149.
[5] RAMOS M E, HUERTAS F J. Adsorption of lactate and citrate on montmorillonite in aqueous solutions[J]. Applied Clay Science, 2014, 90: 27-34.
[6] TAKANO Y, HORIUCHI T, MARUMO K, et al. Vertical distribution of amino acids and chiral ratios in deep sea hydrothermal sub-vents of the Suiyo Seamount, Izu-Bonin Arc,Pacific Ocean[J]. Organic Geochemistry, 2004, 35(10):1105-1120.
[7] CUADROS J, ALDEGA L, VETTERLEIN J, et al. Reactions of lysine with montmorillonite at 80 ℃: implications for optical activity, H+transfer and lysine-montmorillonite binding[J]. Journal of Colloid and Interface Science, 2009, 333(1): 78-84.
[8] KITADAI N, YOKOYAMA T, NAKASHIMA S. In situ ATR-IR investigation of L-lysine adsorption on montmorillonite[J]. Journal of Colloid and Interface Science, 2009, 338(2): 395-401.
[9] DASHMAN T, STOTZKY G. Physical properties of homoionic montmorillonite and kaolinite complexed with amino acids and peptides[J]. Soil Biology and Biochemistry, 1985, 17(2):189-195.
[10] 楊遠帆, 倪輝, 吳黎明. 茚三酮法測定蜂蜜及果葡糖漿中的氨基酸含量[J]. 中國食品學報, 2013, 13(2): 171-176. YANG Yuanfan, NI Hui, WU Liming. Determination of amino acid in honey and high fructose corn syrup (HFCS) by the method of ninhydrin colorization[J]. Journal of Chinese Institute of Food Science and Technology, 2013, 13(2): 171-176.
[11] RAMOS M E, HUERTAS F J. Adsorption of glycine on montmorillonite in aqueous solutions[J]. Applied Clay Science,2013, 80/81(8): 10-17.
[12] 馮其明, 王倩, 劉琨, 等. 纖蛇紋石吸附Cu(Ⅱ)的動力學及熱力學研究[J]. 中南大學學報(自然科學版), 2011, 42(11):3225-3231. FENG Qiming, WANG Qian, LIU Kun, et al. Adsorption kinetics and thermodynamics of copper (Ⅱ) on chrysotile[J]. Journal of Central South University (Science and Technology),2011, 42(11): 3225-3231.
[13] BIBI I, SINGH B, SILVESTER E. Dissolution of illite in saline-acidic solutions at 25 ℃[J]. Geochimica et Cosmochimica Acta, 2011, 75(11): 3237-3249.
[14] NIETO F, MELLINI M, ABAD I. The role of H3O+in the crystal structure of illite[J]. Clays and Clay Minerals, 2010, 58(2):238-246.
[15] 劉冬, 袁鵬, 劉紅梅, 等. 利用氨吸附漫反射紅外光譜法探測蒙脫石的固體酸性[J]. 礦物學報, 2010, 30(1): 33-39. LIU Dong, YUAN Peng, LIU Hongmei, et al. A Study on the acidity of montmorillonite by using ammonia DRIFT spectroscopy[J]. Acta Mineralogica Sinica, 2010, 30(1): 33-39.
[16] 王生新, 呂擎峰, 王得楷, 等. 水玻璃固化黏土礦物的試驗研究[J]. 中南大學學報(自然科學版), 2013, 44(7): 2656-2662. WANG Shengxin, Lü Qingfeng, WANG Dekai, et al. Experimental study of clay minerals solidified by sodium silicate[J]. Journal of Central South University (Science and Technology), 2013, 44(7): 2656-2662.
[17] BENETOLI L O B, DE SOUZA C M D, DA SILVA K L, et al. Amino acid interaction with and adsorption on clays: FT-IR and Mossbauer spectroscopy and X-ray diffractometry investigations[J]. Origins of Life and Evolution of Biospheres,2007, 37(6): 479-493.
[18] STIEVANO L, PIAO L Y, LOPES I, et al. Glycine and lysine adsorption and reactivity on the surface of amorphous silica[J]. European Journal of Mineralogy, 2007, 19(3): 321-331.
[19] ROZALéN M, BRADY P V, HUERTAS F J. Surface chemistry of K-montmorillonite: ionic strength, temperature dependence and dissolution kinetics[J]. Journal of Colloid and Interface Science, 2009, 333(2): 474-484.
[20] BUJDAK J, RODE B M. The effect of smectite composition on the catalysis of peptide bond formation[J]. Journal of Molecular Evolution, 1996, 43(4): 326-333.
(編輯 羅金花)
Adsorption characteristics and mechanism of glycine on montmorillonite in aqueous solutions
GUO Yuting1, DONG Faqin2, LIU Mingxue1, QIN Yonglian2, ZHOU Qing2,WU Chuanlong3, ZONG Meirong2, HUANG Ting1, LIU Yuanyuan1
(1. School of Life Science and Engineering, Southwest University of Science and Technology, Mianyang 621010, China;2. Key Laboratory of Solid Waste Treatment and Resource Recycle of Ministry of Education,Southwest University of Science and Technology, Mianyang 621010, China;3. School of Materials Science and Engineering,Southwest University of Science and Technology, Mianyang 621010, China)
Adsorption characteristics and mechanism of different concentrations of glycines adsorbed on the surface of montmorillonite from aqueous solutions were studied. The reaction products were characterized using X-ray diffraction (XRD) and attenuated total reflectance Fourier-transform infrared (ATR-FTIR) spectroscopy and inductively coupled plasma-atomic emission spectrometry (ICP-AES). The results show that the equilibrium amount of glycine adsorbed by montmorillonite increases with the variable glycine concentrations from 0.01 to 0.20 mol/L. And the dependence of glycine adsorption with its aqueous concentration fits for a Freundlich equation at the studied concentration range of glycine. The total amount of the desorbed interlayer cations is less than the equilibrium amount of glycine adsorbed by montmorillonite, and the cation exchange reaction produces a decrease of the montmorillonite interlayer space from1.528 to 1.446 nm, demonstrating that the glycine adsorbed by montmorillonite mainly through cation exchange mechanism, but the cation exchange is not the only adsorption way. ATR-FTIR results confirm two adsorption mechanisms, one is the glycine cation exchange through hydrogen bonding between thegroup and the basal oxygen of the interlayer surface, and the other mechanism is edge adsorption by electrostatic force between the COO-group and the positively charged groups at the edge surface of montmorillonite.
montmorillonite; glycine; edge adsorption; cation exchange; attenuated total reflection Fourier-transform infrared spectroscopy
P575.4;P592
A
1672-7207(2016)04-1092-08
10.11817/j.issn.1672-7207.2016.04.002
2015-04-13;
2015-06-20
國家自然科學基金資助項目(41130746,41272371);國家重點基礎研究發展規劃(973計劃)項目(2014CB46003);西南科技大學研究生創新基金資助項目(14ycx073)(Projects (41130746, 41272371) supported by the National Natural Science Foundation of China;Project (2014CB46003) supported by the National Basic Research Development Program (973 Program) of China; Project (14ycx073) supported by Postgraduate Innovation Fund Project by Southwest University of Science and Technology)
董發勤,教授,博士生導師,從事生態環境材料、礦物環境研究;E-mail:fqdong@swust.edu.cn

