水楊醛衍生物縮2-氨甲基苯并咪唑Schiff堿合成、與DNA相互作用及其生物活性研究*1
(1.浙江師范大學浙江省固體表面反應化學重點實驗室,浙江金華 321004;2.浙江師范大學化學與生命科學學院,浙江金華 321004)
水楊醛衍生物縮2-氨甲基苯并咪唑Schiff堿合成、與DNA相互作用及其生物活性研究*1
林秋月1,2, 魏瓊1,2, 程建平2, 陸夢迪2
(1.浙江師范大學浙江省固體表面反應化學重點實驗室,浙江金華321004;2.浙江師范大學化學與生命科學學院,浙江金華321004)
合成了3種水楊醛衍生物縮2-氨甲基苯并咪唑Schiff堿化合物(HL),通過元素分析、紅外光譜、紫外光譜和核磁共振氫譜進行了表征,分別為:HL1=水楊醛縮2-氨甲基苯并咪唑,C15H13ON3;HL2=5-氯水楊醛縮2-氨甲基苯并咪唑,C15H12ON3Cl;HL3=鄰香蘭素縮2-氨甲基苯并咪唑,C16H15O2N3.通過紫外光譜法、熒光光譜法和黏度法檢測了3種Schiff堿與DNA相互作用的情況.結果顯示:隨著DNA的加入,3種Schiff堿的紫外吸收光譜出現減色效應和紅移現象;對溴化乙錠-DNA復合體系的熒光有較強的猝滅作用;隨著Schiff堿的加入,DNA的黏度減小.表明3種Schiff堿與DNA之間能以部分插入模式發生較強烈的相互作用,且強度按HL1,HL3和HL2的順序依次增強.HL2和HL3對人體外結腸癌細胞(COLO205)和人乳腺癌細胞(MCF-7)的增殖均有較強的抑制作用,且HL2的抑制活性高于HL3.同時,3種Schiff堿有較好的抑菌活性,其中HL2對大腸桿菌的抑菌效果最顯著.
2-氨甲基苯并咪唑;水楊醛;Schiff堿;DNA;相互作用;生物活性
Schiff堿是一類含亞胺基(==CN)官能團的有機化合物,具有抑菌、消炎、抗癌等生物活性,有關方面的研究一直是化學和生物學界關注的熱點[1-2].水楊醛衍生物的Schiff堿在抗真菌、抗病毒和促進DNA水解等方面有重要的作用,是藥物和其他有機試劑的中間體[3].苯并咪唑為雜環化合物,含苯并咪唑的小分子藥物能與DNA雙螺旋中的AT堿基系列特異性地結合[4],具有多方面的生物和藥理活性,廣泛應用于藥物中間體的制備[5].將有生物活性的苯并咪唑引入到水楊醛衍生物Schiff堿中,符合藥物拼合原理及藥物設計理念.通常,將2種藥物的活性結構拼合在一起,所形成的藥物兼具兩者的性質,顯示的藥效作用理應得到強化.因此,研究苯并咪唑的水楊醛衍生物Schiff堿的合成和生物活性是一個新穎而富有意義的課題.
目前,本課題組已報道了5-氯水楊醛縮2-氨甲基苯并咪唑Schiff堿的合成和結構[6].有關水楊醛縮2-氨甲基苯并咪唑Schiff堿的研究已有少量的報道[7].本研究首次合成了鄰香蘭素縮2-氨甲基苯并咪唑Schiff堿,并通過紫外和熒光光譜法、黏度法系統地研究了3種水楊醛衍生物縮2-氨甲基苯并咪唑Schiff堿化合物(HL)與生物大分子(DNA)的相互作用,進一步測試了Schiff堿化合物對人結腸癌細胞(COLO205)和人乳腺癌細胞(MCF-7)體外增殖的抑制活性,并且檢測了3種化合物對金黃色葡萄球菌、枯草桿菌、大腸桿菌和白色念珠菌4種受試菌的抑菌活性.
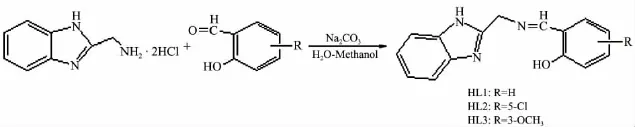
圖1 Schiff堿化合物HL1,HL2和HL3的合成
1 材料與方法
1.1試劑和儀器
小牛胸腺DNA(ct-DNA)購自北京華美公司. ct-DNA溶液(ρ=200μg·mL-1,c=3.72×10-4mol·L-1)用0.1 mol·L-1NaCl溶液配制,置4℃保存,經純度測定A260/A280=1.8~2.0.三羥甲基氨基甲烷(Tris)購自國藥集團化學試劑有限公司,Tris-HCl緩沖液pH為7.4.溴化乙錠(EB)購自Fluka公司.除水楊醛、鄰香蘭素為化學純外,其余試劑均為分析純.實驗用水為二次蒸餾水.人體結腸癌細胞株(COLO205)和人體乳腺癌細胞株(MCF-7)購自中國科學院上海細胞庫.金黃色葡萄球菌(Staphylococcus aureus)、枯草桿菌(Bacillus subtilis)、大腸桿菌(Escherichia coli)和白色念珠菌(Canidia albicans)均由浙江省金華市中心醫院提供.
Vario ELⅢ元素分析儀;NEXUS-670 FT-IR紅外光譜儀;UV-2501PC紫外可見分光光度計;Brucker Avance 400 MHz核磁共振儀;烏氏黏度計;LS-55型熒光光度計.
1.2Schiff堿化合物HL的合成
HL的合成路線見圖1.其中:HL1=水楊醛縮2-氨甲基苯并咪唑;HL2=5-氯水楊醛縮2-氨甲基苯并咪唑;HL3=鄰香蘭素縮2-氨甲基苯并咪唑.
1.2.12-氨甲基苯并咪唑的合成
2-氨甲基苯并咪唑鹽酸鹽參照文獻[8]的方法合成:稱取甘氨酸 0.067 mol,鄰苯二胺0.05 mol,加入75 mL 4 mol·L-1鹽酸,于130℃左右油浴,攪拌回流72 h.溶液由粉紅色變棕黃色,直至為藍綠色.反應完畢后,將反應液蒸發至25 mL左右,置冰箱中(約0℃)過夜后過濾,將沉淀溶于30 mL 95%乙醇和3 mL水的混合溶劑中進行重結晶,真空干燥,得到白色粉狀固體.
1.2.2HL的合成
水楊醛縮2-氨甲基苯并咪唑Schiff堿(HL1)參照文獻[9]的方法合成:將2-氨甲基苯并咪唑鹽酸鹽5 mmol溶于15 mL水中,用碳酸鈉溶液調節pH至弱酸性,室溫下滴加8mL含5mmol水楊醛的甲醇溶液,滴加完畢后繼續攪拌4 h,有大量的黃色沉淀生成,過濾,沉淀分別用水、石油醚充分洗滌后再用乙腈重結晶,得到黃色粉狀固體.
5-氯水楊醛縮2-氨甲基苯并咪唑 Schiff堿(HL2)的合成:HL2的合成方法與HL1相似,用5-氯水楊醛[10]5 mmol代替水楊醛反應,將所得黃色固體用體積比為1∶1的乙腈-甲醇混合溶劑重結晶,得到黃色粉狀固體.
鄰香蘭素縮 2-氨甲基苯并咪唑 Schiff堿(HL3)的合成:將2-氨甲基苯并咪唑鹽酸鹽5 mmol溶于15 mL體積比為1∶4的甲醇-水混合溶劑中,用碳酸鈉溶液調節pH至弱酸性,室溫下滴加8 mL含5 mmol鄰香蘭素的甲醇溶液,滴加完畢后繼續攪拌4 h,產生大量的黏性黃色沉淀.將所得沉淀用水、石油醚充分洗滌后,用無水乙醇重結晶得到黃色粉狀固體.
所得產物均經真空干燥后置于硅膠干燥器中保存,備用.
1.3化合物HL與DNA相互作用的檢測
1.3.1紫外光譜法
固定化合物HL的濃度為6.0×10-5mol·L-1,分別加入一系列不同量的3.72×10-4mol·L-1DNA溶液,用Tris-HCl緩沖溶液(pH=7.4)定容至10.00 mL,室溫下作用30 min后,以對應濃度的DNA溶液作參比,對200~400 nm波長的紫外吸收光譜進行掃描.
1.3.2熒光光譜法
將2.00 mL Tris-HCl緩沖溶液(pH=7.4),10μL 2.0×10-3mol·L-1溴化乙錠(EB)溶液和2.00 mL 200μg·mL-1DNA溶液置于比色管中,室溫下作用1 h后,分別加入不同量的HL溶液,以Tris-HCl緩沖液稀釋并定容至10.00 mL,繼續作用2 h后,以激發波長(λex)為520 nm掃描體系在發射波長為530~700 nm的熒光光譜.
1.3.3黏度法
黏度用烏氏黏度計測定.固定DNA的濃度為3.72×10-4mol·L-1,依次增加化合物HL的濃度(0~3.33×10-6mol·L-1),恒溫在25℃,每次作用30 min后測定溶液流經毛細管的時間.相對黏度(η)按下式[11]計算:
η=(t-t0)/t0.
式中:t0為緩沖溶液流經毛細管所需的時間;t為含有不同濃度HL的DNA溶液流經毛細管的時間.以(η/η0)1/3對結合比率r(r=cHL/cDNA)作圖,其中η0和η分別為未加HL和加入不同量HL的DNA溶液的相對黏度.
1.4化合物HL的抑菌活性實驗
將化合物HL用二甲基亞砜(DMSO)溶解并配制成濃度分別為1.0×10-3mol·L-1和1.0× 10-2mol·L-1的溶液,滅菌后備用.在培養皿中,往牛肉膏蛋白胨培養基中加入200μL菌懸液,將牛津杯豎直放置于培養基中,并將一定濃度的待測樣品注入牛津杯中,蓋好培養皿.將平皿放在37℃培養箱中倒置培養,18 h后觀察結果,測定牛津杯周圍產生的抑菌圈直徑.用同樣的方法接種只含溶劑的瓊脂平皿作為空白對照.所有實驗均重復3次.按照上述方法分別測定了化合物HL 對4種受試菌:金黃色葡萄球菌(S.aureus)、枯草桿菌(B.subtilis)、大腸桿菌(E.coli)和白色念珠菌(C.albicans)的抑菌活性.
2 結果與討論
2.1化合物HL的表征
2.1.1HL的組成和性質
室溫下,HL1,HL2和HL3在固相時均很穩定,但在液相中因水解或氧化顏色逐漸加深.它們難溶于水,能溶于多數有機溶劑,其中HL3幾乎能溶于除石油醚外的一切常見有機溶劑.表1列出了3種Schiff堿化合物HL的元素分析數據,實驗值與理論值基本吻合,誤差在4%之內.因此,推測Schiff堿化合物HL的組成為:HL1=水楊醛縮2-氨甲基苯并咪唑,C15H13ON3;HL2=5-氯水楊醛縮2-氨甲基苯并咪唑,C15H12ON3Cl;HL3=鄰香蘭素縮2-氨甲基苯并咪唑,C16H15O2N3.
2.1.2化合物HL的紅外光譜
采用KBr壓片法測定了Schiff堿化合物HL 在4 000~400 cm-1的紅外光譜.3種Schiff堿的紅外光譜圖極為相似,HL3的紅外光譜見圖2.由紅外光譜圖可見:Schiff堿官能團中的亞胺基σC=N特征吸收峰[12]出現在1 628~1 638 cm-1,HL1為1 632 cm-1,HL2為1 638 cm-1,HL3為1 628 cm-1;苯環的σPh—OH吸收峰,HL1為1 276 cm-1,HL2為1 275 cm-1,HL3為1 253 cm-1.
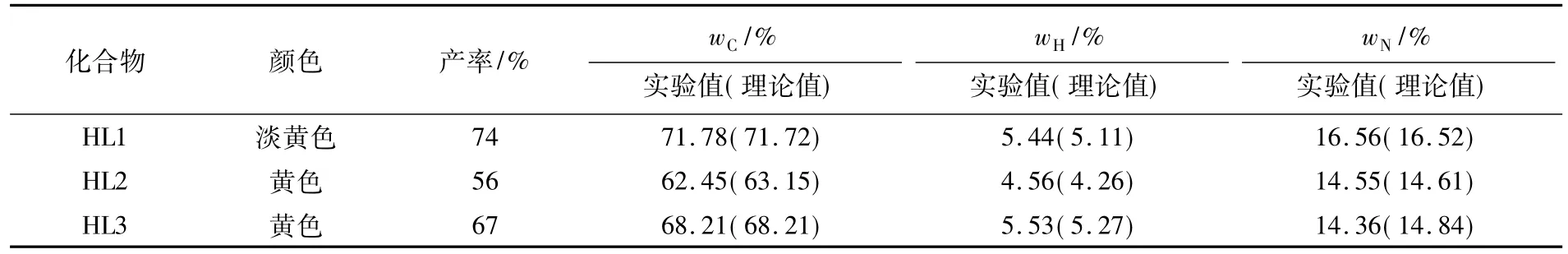
表1 化合物HL的元素分析數據
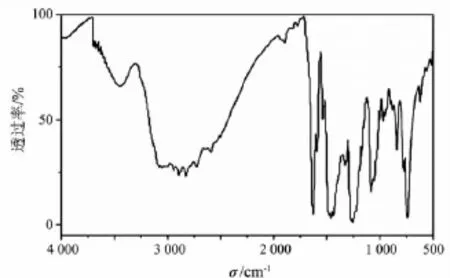
圖2 Schiff堿化合物HL3的紅外光譜圖
2.1.3化合物HL的紫外光譜
配制1×10-4mol·L-1Schiff堿化合物HL的甲醇溶液,測定了3種Schiff堿化合物在200~400 nm波長的紫外吸收光譜,所得數據見表2.其中:在281,274,250和224 nm左右的4個強吸收峰可歸屬于HL中的苯環和咪唑環的π-π*電子躍遷吸收;330 nm左右的弱吸收峰歸屬于亞氨基官能團中氮原子上的孤電子對向共軛雙鍵的n-π*躍遷吸收[13].
2.1.4化合物HL的核磁共振氫譜
3種化合物HL在DMSO中的核磁共振氫譜圖形十分相似.表3為HL1,HL2和HL3的核磁共振氫譜數據.
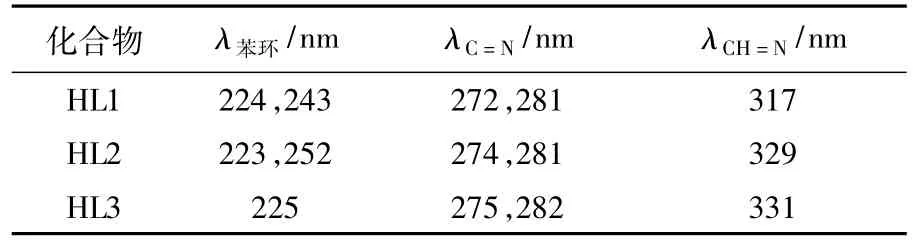
表2 化合物HL的紫外光譜數據
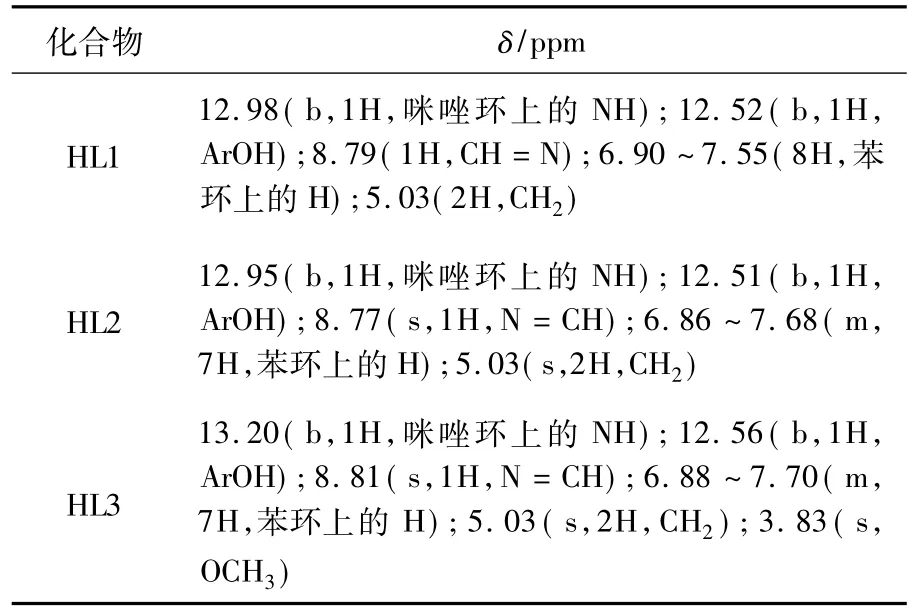
表3 化合物HL的1H NMR數據
從表3可以看出,3種化合物具有類似的化學位移,證明它們具有相似的結構.而3種化合物均在8.79~8.81有化學位移,說明Schiff堿官能團亞胺氫(--CH==N--)的存在.
綜上所述,2-氨甲基苯并咪唑與3種水楊醛衍生物的Schiff堿化合物HL均已生成.
2.2化合物HL與DNA的相互作用
2.2.1DNA對HL紫外吸收光譜的影響
紫外-可見吸收光譜是研究小分子化合物與DNA相互作用的一種簡便而有效的方法.當小分子化合物以插入方式與DNA結合時,其吸收光譜出現減色效應,并伴隨一定程度的紅移;而以其他方式結合時,光譜沒有明顯的變化[14].
圖3顯示了DNA對HL紫外吸收光譜的影響.由圖3可見:在Tris緩沖溶液中,3種化合物在320 nm和400 nm附近出現的弱吸收峰對應于Schiff堿的酚亞胺基團的躍遷吸收帶;在230~300 nm出現較強的吸收峰,歸屬于苯環或苯并咪唑環的π-π*躍遷吸收帶.對照表2中化合物HL的紫外光譜數據,可以說明:在化合物HL生物性質的實驗濃度范圍內,HL是穩定的,并未發生解離;隨著DNA濃度的增加,以上吸收峰均出現有規律的減色,并伴隨微弱的紅移.由此推測,化合物HL的芳環部分插入到DNA堿基對之間而發生了一定程度的相互作用[15].
為了定量比較化合物HL與DNA結合能力的強弱,可通過如下方程[16]計算結合常數:
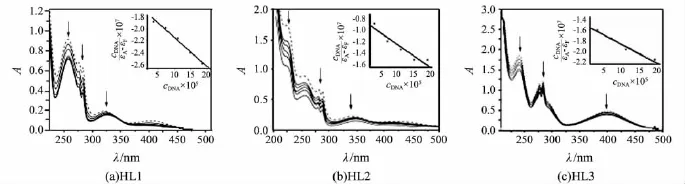
圖3 DNA對HL1,HL2和HL3紫外吸收光譜的影響
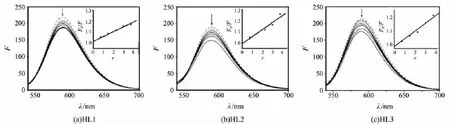
圖4 HL1,HL2和HL3對EB-DNA復合體系的熒光猝滅
式中:cDNA表示DNA溶液的濃度;εA,εB和εF分別表示表觀、游離和與DNA鍵合飽和時化合物的摩爾吸光系數;以cDNA/(εA-εF)對cDNA作圖(見圖3中插圖),所得直線的斜率與截距的比值即為化合物與DNA的結合常數Kb.計算得到結合常數Kb/(L·mol-1)分別為:3.14×103(HL1),6.27×103(HL2)和5.25×103(HL3),表明化合物HL與DNA發生了較強烈的相互作用,強度順序為:HL2最強,HL3次之,HL1最弱.
2.2.2化合物HL對EB-DNA體系的熒光猝滅
溴化乙錠(EB)為具有共軛平面的熒光探針分子,能專一性地插入DNA雙螺旋內部的堿基對之間,使自身的熒光強度較在純水溶液中有顯著增強.當EB從與DNA的結合態中被置換出來或DNA雙螺旋減少時,將發生熒光猝滅.因而,化合物對EB-DNA體系熒光猝滅的程度可以說明該化合物與DNA插入作用的強弱[17].圖4顯示了化合物HL對EB-DNA復合體系的熒光猝滅程度.隨著HL的加入,EB-DNA體系的熒光發射強度發生了明顯的下降.根據Stern-Volmer方程[18]
F0/F=1+Ksqr,
式中:F0和F分別為加入化合物前后EB-DNA復合體系的熒光強度;Ksq為化合物對EB-DNA體系的動態猝滅常數;r=cHL/cDNA.所得數據以F0/F 對r進行線性擬合(見圖4中插圖),求得化合物的熒光猝滅常數 Ksq分別為1.16(HL1),1.53 (HL2)和1.45(HL3),且強度以HL1,HL3和HL2的順序遞增.這種對EB-DNA體系的熒光猝滅作用可以歸結為:HL中的平面芳香苯并咪唑環與DNA堿基對的平面芳香環發生π-π堆積結合作用,即發生了類似于EB的插入作用,并進一步取代EB而與DNA結合,導致能量轉移,從而引發EB-DNA復合體系熒光強度的降低[19].
2.2.3化合物HL對DNA黏度的影響及作用模式
在缺乏晶體結構數據的情況下,對DNA在溶液中長度變化敏感的流體動力學方法被認為是測試化合物與DNA作用模式的最嚴謹的方法[20].若小分子化合物以插入方式與DNA作用,將導致DNA雙螺旋伸長而使黏度增加;若以靜電和溝面等非插入方式與DNA作用,DNA溶液的黏度無明顯變化;而若以部分插入方式與DNA作用,可能使DNA雙螺旋扭結而表現為黏度減小[21].
為了進一步確定Schiff堿化合物HL分子與DNA作用的模式,測定了它們在25℃時對DNA黏度的影響,結果見圖5.由圖5可見,隨著HL濃度的增加,DNA的相對黏度均逐步降低,這一現象表明3種化合物與DNA的主要作用模式均為部分插入模式.這可能是由于Schiff堿分子的苯并咪唑環與水楊醛基的苯環并未處于同一平面,使其只能部分插入到 DNA堿基對之間,導致DNA的雙螺旋結構發生了扭曲,有效長度減小之故.同時,DNA黏度降低幅度亦隨HL1,HL3和HL2順序增大,表明化合物HL的作用強度依次增強.這與光譜法研究的結果一致.從組成上看,這可能與前兩者的水楊醛苯環上分別引入了氯原子和甲氧基團對分子產生了電子效應有關.
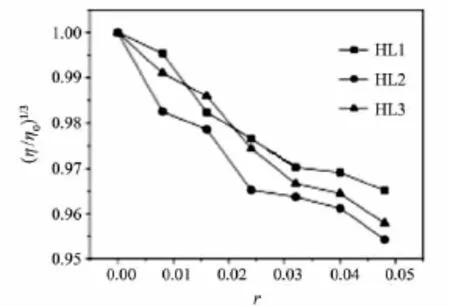
圖5 25℃時HL1,HL2和HL3對DNA黏度的影響
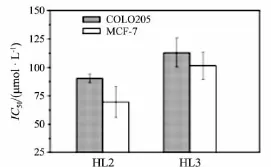
圖6 HL2和HL3與COLO205和MCF-7作用的半數抑制濃度IC50

圖7 HL1,HL2和HL3與COLO205和MCF-7作用的濃度-抑制率曲線
2.3化合物HL對人體外癌細胞增殖的抑制活性
化合物HL對受試的人體結腸癌細胞(COLO205)和人體乳腺癌細胞(MCF-7)增殖(72 h)的半數抑制濃度(IC50)示于圖6,HL與腫瘤細胞的體外作用濃度-抑制率曲線示于圖7.由于HL1對2種癌細胞均沒有明顯的抑制作用,故不討論.HL2和HL3能有效地抑制2種癌細胞的增殖生長,且其活性隨濃度的增加而逐步增強.當濃度達到200μmol·L-1時,HL2和HL3對結腸癌的抑制率已分別達到了65%和45%,而對乳腺癌的抑制率均已超過65%.IC50值亦表明HL2和HL3對乳腺癌MCF-7細胞的抑制活性高于對結腸癌COLO205細胞的抑制活性.說明化合物HL的抑制作用對癌細胞具有較高的選擇性.對于同一癌細胞株而言,HL2的抑制活性高于HL3.3種Schiff堿化合物組成的差別在水楊醛基團上,依活性順序為:5-氯水楊醛(HL2)>鄰香蘭素(HL3)>水楊醛(HL),說明在水楊醛芳環上引入氯原子(HL2)或甲氧基(HL3)將促進化合物對癌細胞的抑制作用.同時,抗癌活性的強弱順序與化合物HL同DNA相互作用的強度順序基本一致,也預示了DNA可能是該類Schiff堿化合物抗癌作用的靶分子之一.
2.4化合物HL的抑菌活性
選擇2種革蘭氏陽性菌(金黃色葡萄球菌S. aureus和枯草桿菌B.subtilis)、一種革蘭氏陰性菌(大腸桿菌E.coli)和一種真菌(白色念珠菌C.albicans)作為受試菌進行抑菌活性實驗.溶劑DMSO和3種Schiff堿化合物HL的抑菌活性實驗結果見表4.結果表明:HL1,HL2和 HL3對4種受試菌株均有較好的抑制作用,且具有相同的選擇性,對不同菌株的抑菌活性強度順序為大腸桿菌>金黃色葡萄球菌>白色念珠菌>枯草桿菌,且隨著HL濃度的增大,抑菌活性也增強;HL2 和HL3的抑菌活性大于HL1,當濃度為1.0× 10-2mol·L-1時,HL2對大腸桿菌的抑菌效果最顯著;溶劑DMSO對4種受試菌的抑制作用很小. 以DMSO為對照,化合物HL2分別對大腸桿菌和金黃色葡萄球菌的抑菌實驗結果見圖8.

表4 化合物HL對4種受試菌的抑菌活性
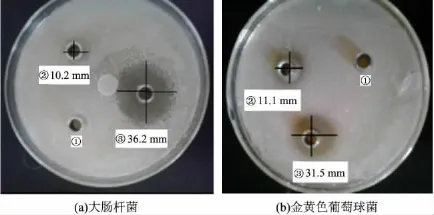
圖8 HL2對大腸桿菌和金黃色葡萄球菌的抑菌實驗結果
3 結論
本研究合成了3種水楊醛衍生物縮2-氨甲基苯并咪唑Schiff堿化合物:水楊醛縮2-氨甲基苯并咪唑(HL1)、5-氯水楊醛縮2-氨甲基苯并咪唑(HL2)和鄰香蘭素縮2-氨甲基苯并咪唑(HL3),其中HL3為首次報道,并對它們的結構進行了表征.通過紫外光譜法、熒光光譜法和黏度法研究了3種Schiff堿化合物與DNA的相互作用,結果顯示,它們能與DNA發生部分插入模式的較強烈的相互作用,且強度按HL1,HL3和HL2依次增強.同時,測試了3種Schiff堿化合物對人結腸癌細胞(COLO205)和人乳腺癌細胞(MCF-7)體外增殖的抑制活性,結果表明HL2和HL3有較強的增殖抑制活性,而HL1對2種癌細胞幾乎沒有抑制活性.實驗還表明,3種Schiff堿化合物對金黃色葡萄球菌(S.Aureus)、枯草桿菌(B.subtilis)、大腸桿菌(E.coli)和白色念珠菌(C.albicans)有較好的抑菌活性,其中HL2對大腸桿菌的抑菌效果最顯著.
致謝:衷心感謝浙江省醫學科學院藥物研究所在測試化合物對人體外癌細胞的增殖抑制活性方面給予的幫助!
[1]Sinha D,Tiwari A K,Singh S,et al.Synthesis,characterization and biological activity of Schiff base analogues of indole-3-carboxaldehyde[J]. Eur JMed Chem,2008,43(1):160-165.
[2]Bindu P,Kurup M R P,Satyakeerty T R.EPR,cyclic voltammetric and biological activities of copper(Ⅱ)complexes of salicylaldehyde N(4)substituted thiosemicarbazone and heterocyclic bases[J].Polyhedron,1999,18(3/4):321-331.
[3]Shi Lei,Ge Huiming,Tan Shuhua,et al.Synthesis and antimicrobial activities of Schiff bases derived from 5-chloro-salicylaldehyde[J].Eur J Med Chem,2007,42(4):558-564.
[4]Parkinson JA,Barber J,Douglas K T.Minor-groove recognition of the self-complementary duplex d(CGCGAATTCGCG)2by Hoechst33258:a high-field NMR study[J].Biochemistry,1990,29(44):10181-10190.
[5]Wright JB.The chemistry of the benzimidazoles[J].Chem Rev,1951,48(3):397-541.
[6]Cheng Jianping,Lin Qiuyue,ZhuWenzhong,etal.Synthesis,crystal structure and DNA interaction of N-(benzimidazol-2-ylmethyl)-5-chlorosalicylideneimine[J].Struc Chem,2009,28(2):235-239.
[7]Mohamed G G,Abd El-Wahab Z H.Salicylidene-2-aminobenzimidazole Schiff base complexes of Fe(Ⅲ),Co(Ⅱ),Cu(Ⅱ),Zn(Ⅱ)and Cd(Ⅱ)[J].JTherm Anal Calorim,2003,73(1):347-359.
[8]Cescon L A,Day A R.Preparation of some benzimidazolylamino acids.Reactions of amino acids with o-phenylenediamines[J].JOrg Chem,1962,27(2):581-586.
[9]Maurya M R,Kumar A,Ebel M,et al.Synthesis,characterization,reactivity,and catalytic potential ofmodel vanadium(Ⅳ,Ⅴ)complexes with benzimidazole derived ONN donor ligands[J].Inorg Chem,2006,45(15):5924-5937.
[10]柳翠英,趙全芹.2-羥基-5-氯苯甲醛的合成[J].中國醫藥工業雜志,2001,32(1):37-40.
[11]Wu Huilu,Wang Kaitong,Liu Bin,etal.Synthesis,characterization,crystal structure and DNA-binding studies of two zinc(Ⅱ)complexeswith the V-shaped bis(benzimidazole)-thiapropane and its derivative ligand[J].Inorg Chim Acta,2012,384(1):302-308.
[12]Gümüs F,Algül O,Eren G,et al.Synthesis,cytotoxic activity on MCF-7 cell line and mutagenic activity of platinum(Ⅱ)complexes with 2-substituted benzimidazole ligands[J].Eur JMed Chem,2003,38(5):473-480.
[13]Gaballa A S,Asker M S,Barakat A S,etal.Synthesis,characterization and biological activity of some platinum(Ⅱ)complexeswith Schiff bases derived from salicylaldehyde,2-furaldehyde and phenylenediamine[J].Spectrochim Acta Part A,2007,67(1):114-121.
[14]Chetana P R,Rao R,Roy M,et al.New ternary copper(Ⅱ)complexes of L-alanine and heterocyclic bases:DNA binding and oxidative DNA cleavage activity[J].Inorg Chim Acta,2009,362:4692-4698.
[15]林秋月,賀新前,王東航,等.N-取代吡啶酰胺與DNA作用的研究[J].浙江師范大學學報:自然科學版,2009,32(2):189-195.
[16]Arjmand F,Aziz M.Synthesis and characterization of dinuclear macrocyclic cobalt(Ⅱ),copper(Ⅱ)and zinc(Ⅱ)complexes derived from 2,2,2,2-S,S[bis(bis-N,N-2-thiobenzimidazolyloxalato-1,2-ethane)]:DNA binding and cleavage studies[J].Eur JMed Chem,2009,44 (2):834-844.
[17]Liu Jie,Zhang Tixiang,Lu Tongbu,et al.DNA-binding and cleavage studies ofmacrocyclic copper(Ⅱ)complexes[J].J Inorg Biochem,2002,91(1):269-276
[18]Uma V,Castineiras A,Nair B U.Copper(Ⅱ)complexes of N4 tetradentate ligandswith flexible alkyl spacers:Crystal structure,DNA binding and cleavage studies[J].Polyhedron,2007,26(13):3008-3016.
[19]Zhang Fan,Zheng Xiaoliang,Lin Qiuyue,et al.Two novel cadmium(Ⅱ)complexes with demethylcantharate and polypyridyl:Crystal structure,interactions with DNA and bovine serum albumin[J].Inorg Chim Acta,2013,394:85-91.
[20]Goeda K R S,Naik H SB,Kumar B V,et al.Synthesis,antimicrobial,DNA-binding and photonuclease studies of cobalt(Ⅲ)and nickel(Ⅱ)Schiff base complexes[J].Spectrochim Acta Part A,2013,105:229-237.
[21]杜芳園,林秋月,齊慶遠,等.2-取代咪唑與去甲斑蝥酸過渡金屬配合物的合成、結構及生物活性表征[J].中國科學:B輯 化學,2015,45(10):1050-1064.
(責任編輯薛榮)
Synthesis,DNA interaction and biological activity of N-(benzim idazol-2-ylmethyl)-salicylideneim ine Schiff base
LIN Qiuyue1,2, WEIQiong1,2, CHENG Jianping2, LU Mengdi2
(1.Zhejiang Key Laboratory for Reactive Chemistry on Solid Surfaces,Zhejiang Normal University,Jinhua 321004,China;2.Collegeof Chemistry and Life Sciences,Zhejiang Normal University,Jinhua 321004,China)
Three Schiff bases,N-(benzimidazol-2-ylmethyl)-salicylideneimine(HL1,C15H13ON3),N-(benzimidazol-2-ylmethyl)-5-chloro-salicylideneimine(HL2,C15H12ON3Cl)and N-(benzimidazol-2-ylmethyl)-ovallineneimine(HL3,C16H15O2N3)were synthesized and characterized by elemental analysis,IR,UV-spectra and1H NMR.The interaction between compounds and DNA was studied by ultraviolet absorption spectra,fluorescence spectra and viscositymeasurements.As increasing concentration of DNA,the absorption bands of the compoundswere affected,resulting in hypochromicity and slight red shift.The compounds to the EB-DNA solutions caused significant reduction in emission intensities.The relative viscosity of DNA steadily decreasedafter adding compounds.The results showed that the compounds could bind to DNA with stronger intensity via partial intercalativemode.The binding ability followed the trend from low to high:L1,L3 and L2.Meanwhile,the antiproliferative activities tests showed that HL2 and HL3 had greater activities againsthuman colon cancer cells(COLO205)and human breast cancer cells(MCF-7)in vitro,in which HL2 had stronger inhibition ratios compared to HL3.The antibacterial activities of title compounds against Staphylococcusaureus,Bacillus subtilis,Escherichia coli,Canidia albicans were tested respectively.The results showed that HL2 had stronger inhibition against E.Coli.
2-aminomethylbenzimidazole;salicylaldehyde;Schiff base;DNA;interaction;biological activity
O626
A
1001-5051(2016)02-0179-08
10.16218/j.issn.1001-5051.2016.02.010
*收文日期:2015-07-02;2015-11-23
浙江省新苗人才計劃項目(2015R404007);浙江師范大學研究生創新項目(ZC323015055)
林秋月(1957-),女,浙江樂清人,教授.研究方向:生物無機化學.

