乳清蛋白乳液界面性質(zhì)及其物理穩(wěn)定性和氧化穩(wěn)定性的研究
陳先鑫,馬曉雨,朱雯婷,湯小明,朱雪梅,*,熊 華,白春清(.南昌大學食品科學與技術國家重點實驗室,江西南昌330047;.江西科技師范大學生命科學學院,江西南昌33003)
乳清蛋白乳液界面性質(zhì)及其物理穩(wěn)定性和氧化穩(wěn)定性的研究
陳先鑫1,馬曉雨1,朱雯婷1,湯小明1,朱雪梅1,*,熊華1,白春清2
(1.南昌大學食品科學與技術國家重點實驗室,江西南昌330047;
2.江西科技師范大學生命科學學院,江西南昌330013)
以乳清蛋白與玉米油為原料,采用高壓均質(zhì)技術制備水包油型(O/W)乳液。探究乳清蛋白濃度(0.45%~3.60%)、離子強度(250 mmol/L NaCl)對乳清蛋白乳液界面特性及其物理穩(wěn)定性和氧化穩(wěn)定性的影響。結果表明:隨著乳清蛋白濃度的增加,乳液的粒徑、乳析指數(shù)、過氧化值(POV)和丙二醛生成物(TBARS)都呈現(xiàn)降低的趨勢,而乳液的界面蛋白濃度、電位隨著蛋白濃度的增加而增加。乳液中加入250 mmol/L NaCl能夠增加乳液的粒徑、乳析指數(shù)、界面蛋白含量、電位值、POV和TBARS值。上述結果表明乳液界面蛋白濃度增多,乳液的物理穩(wěn)定性和氧化穩(wěn)定性得到增強,而乳液中加入NaCl后能夠減弱乳液的物理穩(wěn)定性和氧化穩(wěn)定性。
乳液,乳清蛋白,物理穩(wěn)定性,氧化穩(wěn)定性
乳液通常是指一相以液滴形式均勻分散在另一種與其不相混溶的液體中形成的熱力學不穩(wěn)定分散體系[1]。日常生活中人們所接觸到的各種食品如調(diào)味品、蛋黃醬、湯、牛奶、飲料等[2]均屬于這一體系。由于乳液是熱力學不穩(wěn)定體系,存儲過程中經(jīng)常會出現(xiàn)聚結、奧氏熟化、絮凝和相轉化[3-4]等物理失穩(wěn)現(xiàn)象,除此之外,還會產(chǎn)生乳化劑的水解和油脂氧化衰敗等化學失穩(wěn)現(xiàn)象[5]。上述物理失穩(wěn)現(xiàn)象會導致乳液液滴平均粒徑尺寸增加,并形成大顆粒的聚集,最后導致乳液相分離[6]。
為了解決上述問題,通常的方法是向乳液里添加表面活性劑、抗氧化劑等穩(wěn)定劑。相比于吐溫類、司盤類、陰離子型等普通的小分子類乳化劑,乳清蛋白因為其較高的營養(yǎng)價值、安全性及良好的表面活性和部分抗氧化效能而廣泛地應用在食品乳液中[7]。
近年的研究表明,乳液由于具有較大的表面積,其穩(wěn)定性與界面特性有著緊密的關系。雖然最近有許多關于乳清蛋白乳液穩(wěn)定性的研究,但是多集中于研究其物理穩(wěn)定性,如Kulmyrzaev等[7]只是片面研究了pH及KCl對乳清蛋白乳液物理穩(wěn)定性的影響,沒有深刻分析其物理穩(wěn)定性和氧化穩(wěn)定性與乳液界面特性的關系。此外由于乳液的穩(wěn)定性受蛋白質(zhì)濃度、溫度、pH、離子強度等多種因素的影響[5],關于不同乳清蛋白濃度和NaCl對乳液物理穩(wěn)定性和氧化穩(wěn)定性的研究更是未見報道。因此本文以乳清分離蛋白與玉米油為原料,系統(tǒng)地研究不同乳清蛋白濃度和NaCl對乳液物理穩(wěn)定性和氧化穩(wěn)定性的影響,并揭示了乳液界面蛋白濃度與乳液物理化學穩(wěn)定性之間的關系,以期為該類型乳清蛋白乳液的工業(yè)化生產(chǎn)提供理論依據(jù)和技術支持。
1 材料與方法
1.1材料與儀器
玉米油當?shù)爻校蝗榍宸蛛x蛋白蛋白含量91%~92%,Glanbia公司;氯化鈉、鹽酸、甲醇、正丁醇、異辛烷、異丙醇、硫代巴比妥酸、三氯乙酸等試劑分析純。
BS 224S型電子天平北京賽多利斯科學儀器有限公司;GYB 30-6S高壓均質(zhì)機上海東華高壓均質(zhì)機廠;NICOMP 380/ZLS激光納米粒度儀美國PSS公司;JB-3型磁力攪拌器、PHS-3精密pH計上海雷磁新徑儀器有限公司;熒光倒置顯微鏡重慶光學儀器廠;T6紫外可見分光光度計北京普析通用儀器有限公司;Ultra Turrax T25高速分散機德國IKA公司。
1.2實驗方法
1.2.1乳液的制備乳液的制備參考Shao等[8]的方法。具體步驟為:將準確稱量的乳清蛋白溶于10 mmol/L磷酸緩沖液中,配制兩組不同濃度(0.45%、0.90%、1.80%、3.60%,w/v)的乳清蛋白分散液,然后于室溫下磁力攪拌5 h,并添加0.02%(w/v)疊氮化鈉充當抗菌劑,溶解充分后在4℃的冰箱中水化12 h,使乳清蛋白充分的溶解。
將預先溶解的乳清蛋白溶液從冰箱取出,室溫下放置。一組乳清蛋白分散液不進行任何預處理,作為空白;另外一組乳清蛋白分散液,待其恢復到室溫后,加入250 mmol/L的NaCl后調(diào)至pH為7.0,待用。然后分別向上述兩組乳清蛋白分散液中加入10%(v/v)玉米油,用高速分散機在12000 r/min條件下分散2 min,再用高壓均質(zhì)機于40 MPa均質(zhì)三個循環(huán),即得新鮮制備乳液,均質(zhì)溫度控制在25℃。
1.2.2乳液微觀結構的觀察采用熒光倒置顯微鏡觀察乳液的微觀結構。具體方法為:將50 μL乳液樣品和5 μL的1%尼羅紅染液均勻混合于載玻片上,然后將載玻片置于載物臺上,目鏡放大10倍,物鏡放大10倍進行觀察,CCD照相機連接電腦顯示樣品的顯微圖片。
1.2.3平均粒度和Zeta電位的測定用去離子水將新制備的乳液稀釋100倍,采用激光納米粒度儀對新制備的各組乳液粒度和Zeta電位進行測定。
1.2.4界面蛋白含量的測定乳液界面吸附蛋白含量的測定根據(jù)Shao等[8]的方法。
1.2.5乳液的儲存穩(wěn)定性將乳液置于室溫下儲藏,于0、20、30 d測量其粒徑,觀察其儲存穩(wěn)定性。
1.2.6乳析指數(shù)的測定將乳液置于室溫下儲藏,乳液在儲存期間內(nèi)乳析指數(shù)的測定參考王金梅等[9]的方法。
1.2.7乳液過氧化值(POV)的測定將制備的新鮮乳液,立即分裝到50 mL的玻璃試管中,于45℃電熱恒溫培養(yǎng)箱中放置以促進氧化反應,并于1、3、6、11、13、15、19、22 d拿出分裝小樣進行氧化實驗的測定。過氧化值的測定,采用硫氰化鐵法,測定方法參考Wan等[10]的方法。
1.2.8次級氧化產(chǎn)物-丙二醛生成物(TBARS)的測定TBARS生成量的測定由Zhao等[11]的方法略微改動而成。具體步驟:TBA(硫代巴比妥酸)試劑的配制:將0.375 g硫代巴比妥酸,15 g三氯乙酸,1.76 mL 12 mol/L HCl,82.9 mL去離子水均勻混合。將1 mL去離子水,2 mL TBA試劑混合于15 mL試管中,漩渦30 s。將試管在沸水中加熱25 min后在室溫下冷卻20 min,隨后2500 r/min離心20 min,室溫條件放置15 min后,將上層清液用0.22 μm的水系微孔濾膜進行過濾,532 nm下測定濾液的吸光度。根據(jù)1,1,3,3-四乙氧基丙烷標準曲線計算乳液中TBARS的濃度。
1.3數(shù)據(jù)分析
所有實驗均重復3次,采用Origin 8.0和SPSS 16.0對實驗數(shù)據(jù)進行統(tǒng)計分析,樣品平均值之間的差異性通過Duncan法比較(p<0.05)。
2 結果與分析
2.1新鮮乳液微觀結構的觀察
由圖1可以看出乳液顆粒分散得比較均勻,粒徑較小,液滴之間沒有出現(xiàn)明顯聚結。對比圖1A~D和圖1E~H,可以發(fā)現(xiàn)無論乳液是否加入NaCl,含有0.45%乳清蛋白的乳液的粒徑最大,隨著乳清蛋白含量的不斷增加,乳液粒徑不斷減小,這主要是因為隨著乳清蛋白濃度的升高,它的乳化能力不斷增強,更多的乳清蛋白吸附到界面維持乳液穩(wěn)定,最終形成粒徑較小的液滴[8]。此外,當乳液中加入了250 mmol/L NaCl后,可以看出乳液出現(xiàn)了部分的聚集現(xiàn)象,這一特點在0.45%乳清蛋白含量的乳液中表現(xiàn)得較為明顯,如圖1E所示;對比圖1A、B和圖1E、F可以發(fā)現(xiàn),加入250 mmol/L NaCl后乳液的粒徑比沒有加入NaCl的乳液的粒徑大,這是因為靜電屏蔽作用使得液滴間靜電排斥力減小,進一步增大了液滴間的相互吸引作用,增大了乳液的聚集程度,使得乳液的平均粒徑有所增加;而對比圖1C、D和圖1G、H可以發(fā)現(xiàn),當乳清蛋白含量在1.80%以上時,和空白組相比,NaCl僅輕微增加了液滴的平均粒徑,進一步說明乳液在較高濃度蛋白含量時較為穩(wěn)定。

圖1 新鮮乳液的熒光倒置顯微圖Fig.1 Inverted fluorescence micrographs of fresh emulsions
2.2乳液的粒徑分布分析
圖2A和圖2B分別為不加NaCl和加入250 mmol/L NaCl的乳液粒徑分布圖,可以看出各乳液都呈現(xiàn)較好的單分散性,表明各乳液都形成了均一穩(wěn)定的體系;此外可以看出隨著乳清蛋白含量的增加,乳液粒度分布的峰值均傾向于往較小粒徑方向移動,說明乳液的平均粒徑逐漸降低[9],與上述新鮮乳液微觀結構的觀察結果一致。這是由于隨著乳清蛋白濃度的升高,它的乳化能力不斷增強,乳清蛋白逐漸吸附到界面維持乳液穩(wěn)定,最終形成粒徑較小的液滴[8]。對比圖2A和圖2B還可以發(fā)現(xiàn),當乳液加入250 mmol/L NaCl后,乳液粒度分布的峰值均傾向于往較大粒徑方向移動,說明乳液的平均粒徑逐漸增加[9],與上述新鮮乳液微觀結構的觀察結果一致。這是因為鹽離子存在條件下乳液界面的靜電屏蔽作用使得乳液的電位絕對值降低,導致液滴間的排斥力下降,液滴間發(fā)生部分聚結[8]。對比圖2A和圖2B可以發(fā)現(xiàn),圖2A中各乳液峰值強度分布都集中在10%~12%之間,圖2B中除了0.90%蛋白含量的乳液外,其他的乳液峰值強度分布都集中在18%~20%之間,表明乳液加入NaCl后較大粒徑的液滴數(shù)量增加,具體表現(xiàn)為乳液的平均粒徑增加,與上述結果吻合;而圖2B中0.90%蛋白含量的乳液峰值強度突然降低至10%,分布開始變寬,出現(xiàn)該現(xiàn)象的原因有待于進一步的研究。
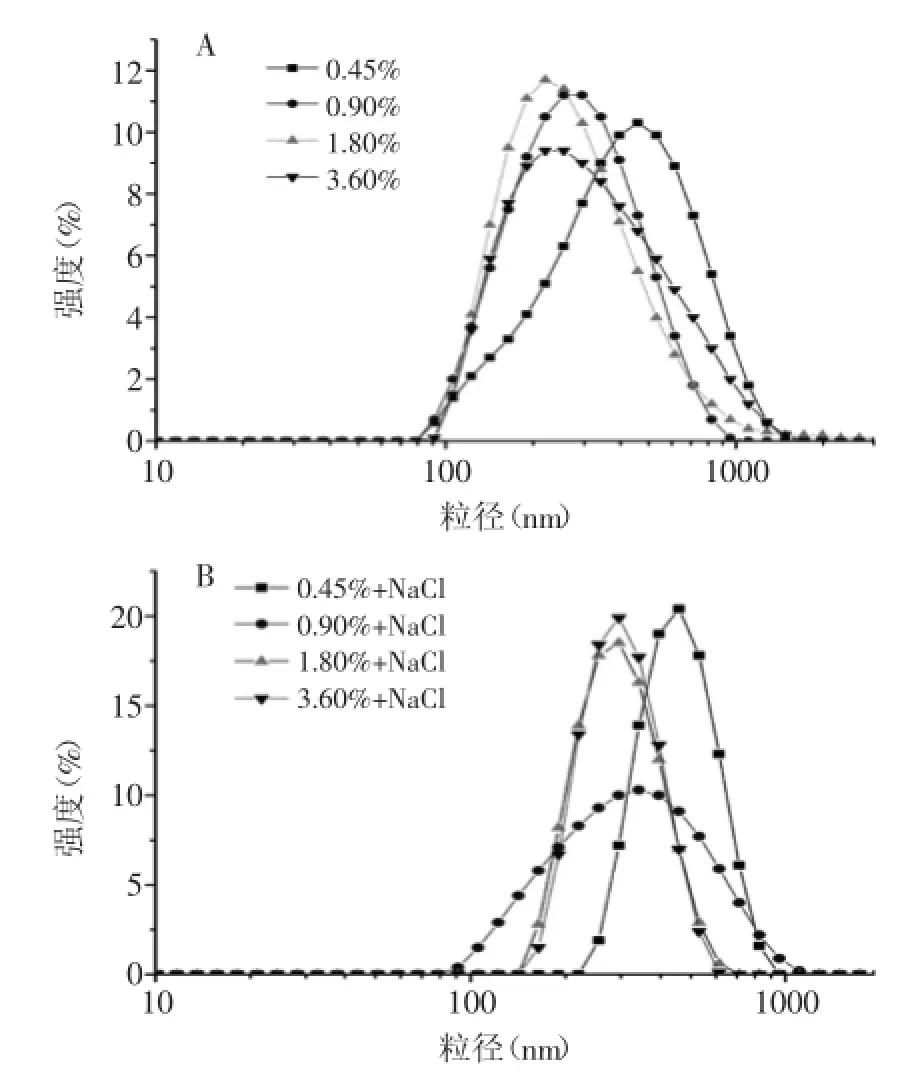
圖2 新鮮乳液的粒徑分布圖Fig.2 Droplet size distribution of fresh emulsions
2.3乳液的電位分析
油滴的表面電荷量決定油滴間排斥作用力的大小,一般可以通過Zeta-電位來體現(xiàn)液滴表面電荷量[8]。其中靜電排斥對穩(wěn)定乳液,阻止液滴聚合有著非常重要的作用[11]。通過圖3可以發(fā)現(xiàn)所有乳液的電位都呈現(xiàn)負值,這是因為乳液的pH在7.0左右,高于蛋白質(zhì)的等電點。一般而言,當乳液中Zeta電位的絕對值大于30 mV時,乳液較穩(wěn)定[5]。由圖3可以看出所有乳液的電位值介于-30~-50 mV之間,表明乳液系統(tǒng)較穩(wěn)定。除了0.45%乳清蛋白含量的乳液外,對于所有乳液來說隨著乳清蛋白濃度的增加,電位值增加,即Zeta-電位絕對值均顯著降低(p<0.05),而上述新鮮乳液微觀結構的觀察和粒徑分布的結果表明隨著乳清蛋白濃度的增加,乳液平均粒徑逐漸降低,這說明蛋白乳液的物理穩(wěn)定性除了和乳液界面的電位相關外,蛋白質(zhì)在油相和水相之間形成的空間位阻同樣對穩(wěn)定乳液有重要作用[9]。當乳液中加入了250 mmol/L NaCl后,乳液的電位值均增加,以0.90%和1.80%乳清蛋白含量的乳液為例,沒有加入NaCl之前,其電位值分別為-48.40 mV和-45.11 mV,加入NaCl后其電位值分別增加到-41.11 mV和-37.72 mV,即電位絕對值都降低了,產(chǎn)生這種現(xiàn)象的主要原因是鹽離子加入后在乳液界面產(chǎn)生了靜電屏蔽現(xiàn)象。
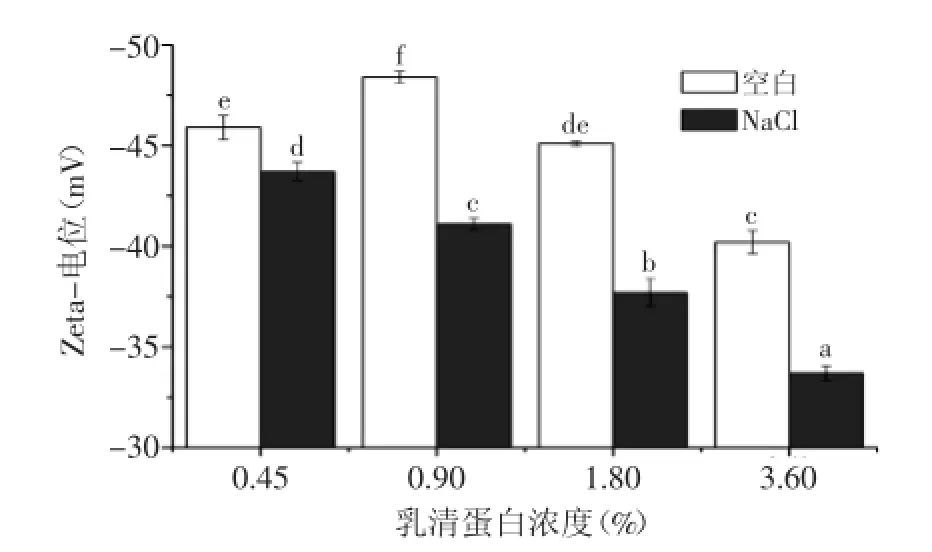
圖3 新鮮乳液的電位圖Fig.3 Zeta potential of fresh emulsions
2.4乳液的界面蛋白含量的測定
界面蛋白濃度是表征乳液穩(wěn)定性的重要參數(shù)之一,一般而言,界面蛋白濃度越高,乳液就越穩(wěn)定[8]。圖4揭示了不同蛋白濃度和鹽處理對于乳液的界面蛋白濃度的影響。由圖4可知,隨著蛋白含量的不斷增加,乳液中吸附至液滴界面的蛋白含量越多,這一變化規(guī)律與乳液微觀結構的觀察結果和粒徑分布的變化趨勢一致,這表明乳液界面蛋白濃度和蛋白質(zhì)的乳化能力之間存在關聯(lián)性。當乳液中加入了250 mmol/L NaCl后,乳液中界面吸附的蛋白含量也有所增加,與粒徑等結果有差異,表明盡管靜電屏蔽作用有利于蛋白質(zhì)吸附至液滴界面,但是乳液的穩(wěn)定性是受多種因素共同影響的[8]。此外,分析發(fā)現(xiàn)本文中高濃度蛋白含量時乳液的界面蛋白濃度明顯高于邵云等[8]的結果,如本文中乳清蛋白含量為3.60%時,其界面吸附量接近13 mg/m2,遠高于邵云等的3.84 mg/m2的最高界面蛋白濃度,這可能是蛋白質(zhì)和油的種類不同造成的。
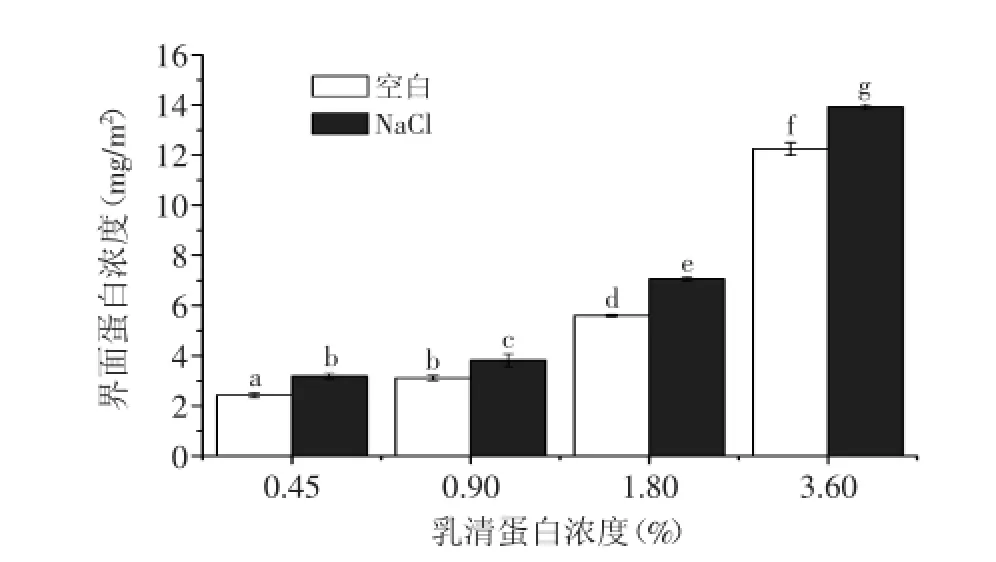
圖4 乳液的界面蛋白含量Fig.4 Interfacial protein concentration of emulsions
2.5乳液的物理儲存穩(wěn)定性
乳液置于室溫環(huán)境下儲存一個月的粒徑變化趨勢見表1。從表1可以看出乳液置于室溫下時,0.45%乳清蛋白含量的乳液的粒徑最大,隨著乳清蛋白含量的不斷增加,粒徑不斷減小,這一結果與前面的粒徑分布圖等結果一致。加入250 mmol/L NaCl后,乳液的粒徑顯著增加(p<0.05)。隨著儲存時間的不斷延長,乳液的粒徑都有不同程度的增加,0.45%乳清蛋白含量的乳液的粒徑增長速度最快,未加入NaCl和加入NaCl的0.45%乳清蛋白含量的乳液的最初平均粒徑分別為332.11 nm和415.12 nm,30 d后其粒徑分別增加至480.89 nm和859.95 nm,再次證明該乳液的物理穩(wěn)定性最差;0.90%乳清蛋白含量的乳液的粒徑增長速度僅次于0.45%乳清蛋白含量的乳液,未加入NaCl和加入NaCl的0.90%乳清蛋白含量的乳液的最初平均粒徑分別為249.20 nm和286.19 nm,30 d后其粒徑分別增加至321.58 nm和374.46 nm;1.80%乳清蛋白含量的乳液的粒徑增長速度較緩慢,最初平均粒徑為243.72 nm,30 d后其粒徑僅增加至299.54 nm,該乳液加入250 mmol/L NaCl后,粒徑增長速度增加,最初平均粒徑為291.16 nm,30 d后其粒徑增加至369.67 nm;未加入NaCl和加入NaCl的3.60%乳清蛋白含量的乳液的最初平均粒徑分別為240.27 nm和293.37 nm,一個月后其粒徑分別增加至289.27 nm和310.14 nm,其增長速度最緩慢。上述結果表明隨著乳液中乳清蛋白濃度的增加,乳液中界面蛋白濃度逐漸增加,更多的的乳清蛋白吸附到乳液界面維持乳液穩(wěn)定,乳液的儲存穩(wěn)定性逐漸增強,而乳液加入NaCl后,由于鹽離子條件下乳液界面的靜電屏蔽作用使得乳液的電位絕對值下降,導致液滴間的排斥力降低,液滴間發(fā)生部分聚集,使得乳液平均粒徑增加,儲存穩(wěn)定性變差。
2.6乳液乳析指數(shù)的測定
乳液的乳析指數(shù)是關于乳液中油相和連續(xù)相之間平衡穩(wěn)定狀態(tài)的指標,是評價乳液物理穩(wěn)定性的一個非常重要的參數(shù)[12]。表2反映了乳液儲存120 d內(nèi)乳析指數(shù)的變化情況。分析發(fā)現(xiàn),儲存60 d后,未加入NaCl和加NaCl的0.45%蛋白含量的乳液的乳析指數(shù)分別增加到7.69%和20.51%,乳液經(jīng)過鹽處理后,其乳析指數(shù)顯著增加(p<0.05),這是因為鹽離子存在條件下乳液油滴界面的靜電屏蔽作用使得液滴間發(fā)生聚結,造成了乳液失穩(wěn),從而加快了乳液油、水兩相的分層[8];其他乳液都未發(fā)現(xiàn)乳液分層的情況。乳液儲存120 d后,所有乳液都出現(xiàn)分層的情況,且隨著蛋白濃度的增加,乳液的乳析指數(shù)不斷降低。乳液加入NaCl后,與空白組相比0.45%蛋白含量的乳液中乳析指數(shù)增加較為顯著,而其他較高蛋白濃度乳液的乳析指數(shù)雖有所增加,但是幅度不大,說明乳清蛋白濃度較高時對乳液脂肪上浮有抑制作用。這些結論和前面的粒徑等結果一致,并與邵云等[8]的研究發(fā)現(xiàn)基本一致。
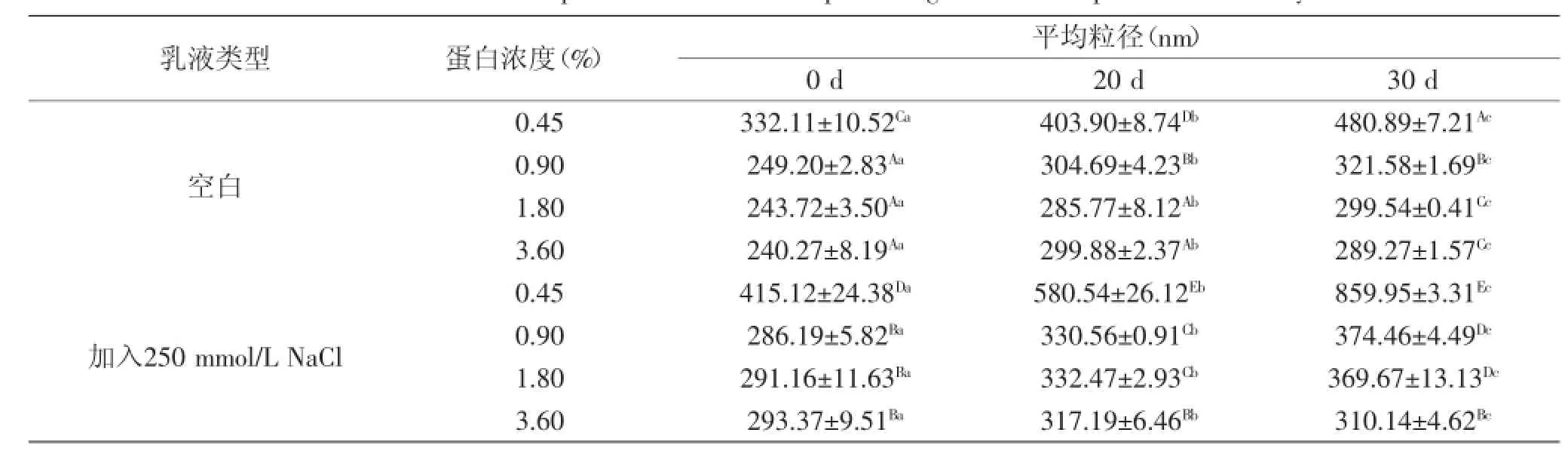
表1 乳液室溫儲存30 d的粒徑變化趨勢Table 1 Evolution of droplet size of emulsions upon storage at room temperature for 30 days
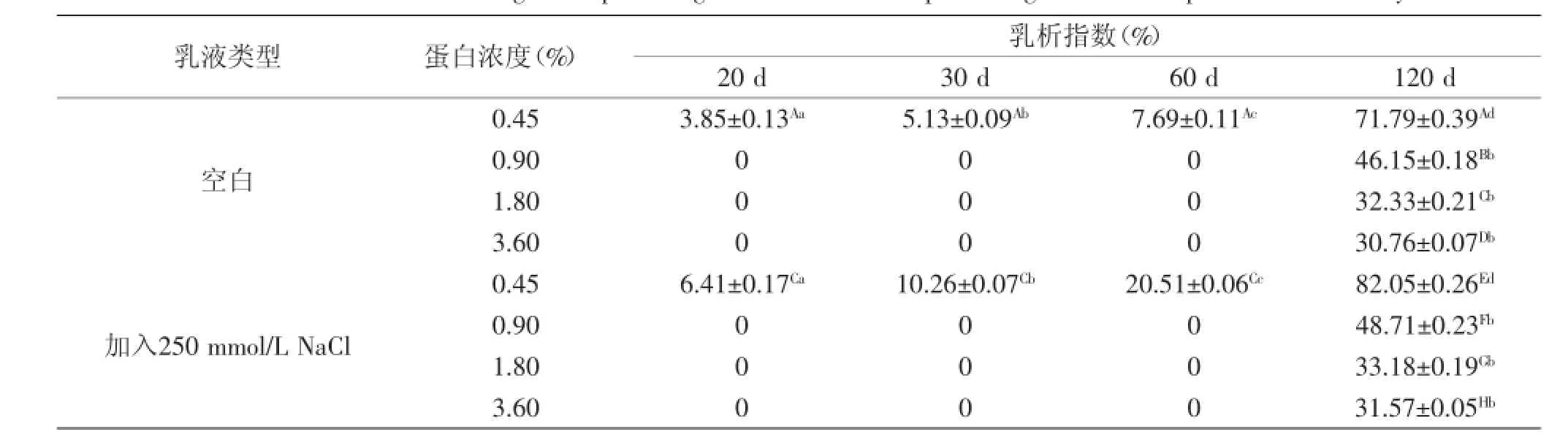
表2 乳液室溫儲存120 d內(nèi)乳析指數(shù)的變化趨勢Table 2 Evolution of creaming index percentage of the emulsions upon storage at room temperature for 120 days
2.7乳液的氧化穩(wěn)定性的測定
圖5揭示了不同乳清蛋白濃度和NaCl對乳液POV值的影響。由圖5可以看出所有乳液的POV值隨著儲存時間的增加而增大,而且蛋白濃度為0.45%的乳液中油脂的氧化速度最快,22 d后乳液中POV值達到了60.58 mmol/kg oil,而22 d后蛋白含量為0.90%~3.60%的乳液POV值分別為22.29、17.76、17.55 mmol/kg oil。上述結果表明一定范圍內(nèi),隨著乳液中乳清蛋白含量的增加,更多的蛋白質(zhì)吸附到界面維持乳液穩(wěn)定,在水相和油相之間形成空間位阻,此外,乳液中的蛋白質(zhì)吸附在油滴表面后形成一層粘彈性蛋白膜,該蛋白膜可以螯合金屬離子和清除自由基,可以起到抑制油脂氧化的作用[8],所以乳液的氧化穩(wěn)定性得到提高;當?shù)鞍缀砍^1.80%時,POV值降低趨勢不明顯。乳液中加入了NaCl后,其POV變化趨勢與未加入NaCl的基本一致,22 d后,蛋白含量為0.45%~ 3.60%的乳液POV值分別為65.47、27.24、25.17、23.66 mmol/kg oil,表明乳液中加入NaCl后,乳液的氫過氧化物生成量增加,氧化穩(wěn)定性降低,與前述乳液物理穩(wěn)定性的結果一致。
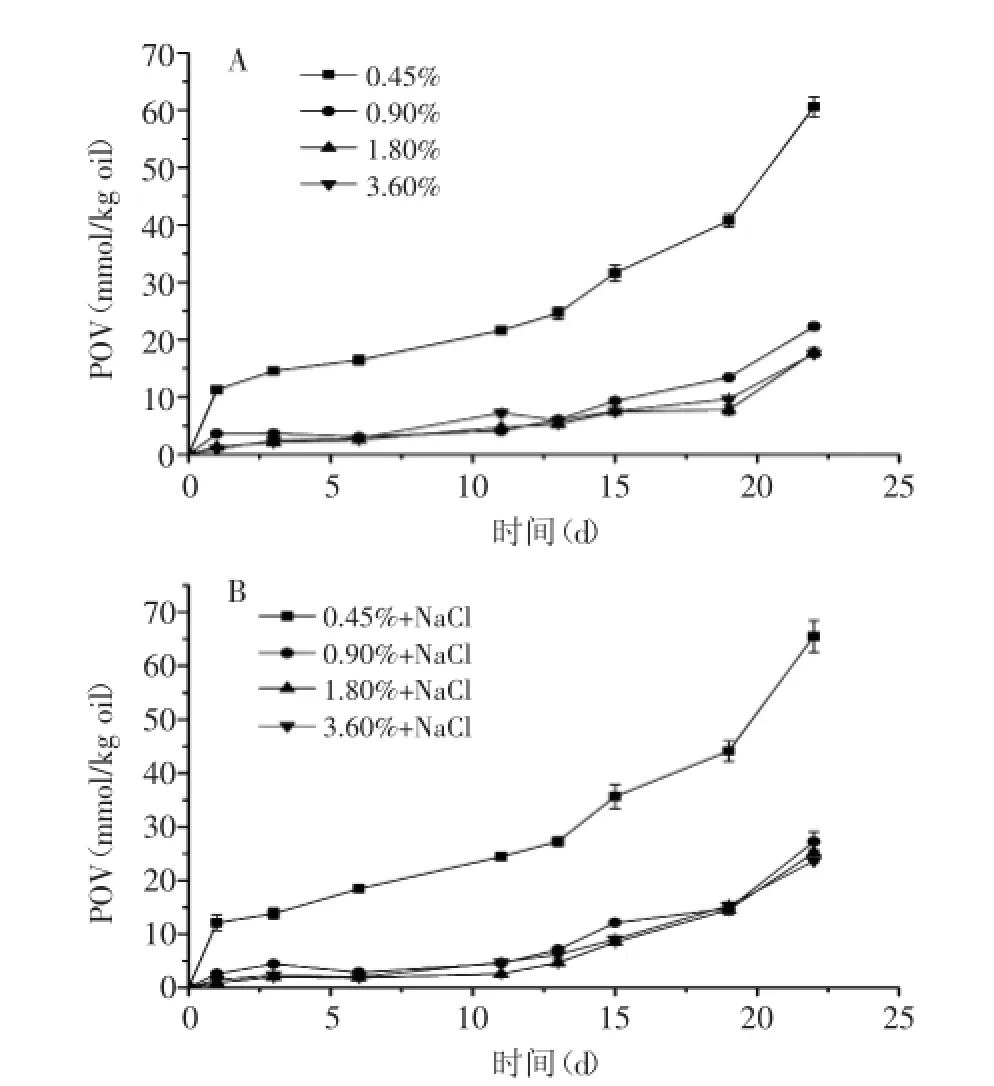
圖5 乳液的POV變化趨勢圖Fig.5 Evolution of POV of emulsions
TBARS值是表征脂質(zhì)次級氧化程度的指標之一,一般將TBARS值與POV值相結合,來共同分析油脂的氧化進程。由圖6可以看出,乳液儲存22 d后,0.45%蛋白含量的乳液中TBARS含量仍然是最高的,隨著蛋白含量增加,TBARS值先降低再逐漸升高,與POV的結果稍有不同,表明蛋白質(zhì)抑制油脂初級氧化的原理和抑制次級氧化的原理稍有差異。此外,乳液中加入NaCl后,TBARS都顯著增加(p<0.05),這一結果和POV的結論一致。
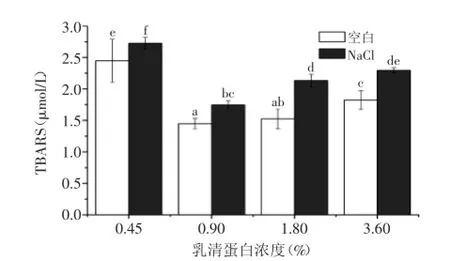
圖6 乳液的TBARS變化趨勢圖Fig.6 Evolution of TBARS of emulsions
綜合乳液POV和TBARS的分析結果,可以看出0.45%蛋白含量的乳液氧化穩(wěn)定性最差,增加蛋白質(zhì)濃度后,更多的蛋白質(zhì)吸附到界面維持乳液穩(wěn)定,POV和TBARS減少,乳液的氧化穩(wěn)定性得到提高。乳液中加入NaCl后POV和TBARS都增加,表明乳液的氧化穩(wěn)定性降低,與粒徑、乳析指數(shù)等結果吻合。
3 結論
本文究了不同乳清蛋白濃度和NaCl對于乳液界面性質(zhì)和物理化學穩(wěn)定性的影響。結果表明:增加乳清蛋白的濃度,乳液的粒徑、Zeta-電位絕對值、乳析指數(shù)、POV值和TBARS值都呈現(xiàn)降低的趨勢,而乳液的界面蛋白濃度呈現(xiàn)增加的趨勢。加入250 mmol/L NaCl到乳液后能夠增加乳液的粒徑、乳析指數(shù)、界面蛋白含量、POV和TBARS值,但降低了乳液的Zeta-電位絕對值。以上實驗結果說明一定范圍內(nèi)增加乳液中乳清蛋白濃度后,更多的蛋白質(zhì)吸附到乳液的界面,形成一種天然屏障,空間位阻增強,從而減少水相和油相間,液滴與液滴間的接觸,抑制了乳液的氧化速率和液滴間的聚集,所以乳液的物理穩(wěn)定性和氧化穩(wěn)定性得到提高。而NaCl加入乳液后,由于靜電屏蔽作用使得靜電排斥力減小,進一步增強了液滴間的相互吸引作用,增大了乳液的失穩(wěn)程度,使得乳液的物理穩(wěn)定性和氧化穩(wěn)定性降低。
[1]Falkeborg M,Guo Z.Dodecenyl succinylated alginate(DSA)as a novel dual-function emulsifier for improved fish oil-inwater emulsions[J].Food Hydrocolloids,2015(46):10-18.
[2]Huck-Iriart C,Rincón-Cardona J A,Herrera M L.Stability of whey protein concentrate/sunflower oil emulsions as affected by sucrose and xanthan Gum[J].Food and Bioprocess Technology,2014,7(9):2646-2656.
[3]Liang Y,Gillies G,Patel H,et al.Physical stability,microstructure and rheology of sodium-caseinate-stabilized emulsions as influenced by protein concentration and nonadsorbing polysaccharides[J].Food Hydrocolloids,2013,36(2):245-255.
[4]Cui Z,Kong X,Chen Y,et al.Effects of rutin incorporation on the physical and oxidative stability of soy protein-stabilized emulsions[J].Food Hydrocolloids,2014,41(20):1-9.
[5]盧錦麗.食品級純膠O/W乳液穩(wěn)定性及流變特性研究[D].杭州:浙江工商大學,2013.
[6]田大志.檸檬精油乳液的物理化學穩(wěn)定性研究[D].武漢:湖北工業(yè)大學,2014.
[7]Kulmyrzaev A A,Schubert H.Influence of KCl on the physicochemical properties of whey protein stabilized emulsions [J].Food Hydrocolloids,2004,18(1):13-19.
[8]Shao Y,Tang C H.Characteristics and oxidative stability of soy protein-stabilized oil-in-water emulsions:Influence of ionic strength and heat pretreatment[J].Food Hydrocolloids,2014,37 (2):149-158.
[9]王金梅.大豆蛋白熱聚集行為及界面、乳化性質(zhì)研究[D].廣州:華南理工大學,2012.
[10]Wan Z L,Wang J M,Wang L Y,et al.Complexation of resveratrol with soy protein and its improvement on oxidative stability of corn oil/water emulsions[J].Food Chemistry,2014,161(6):324-331.
[11]Zhao Q,Selomulya C,Wang S,et al.Enhancing the oxidative stability of food emulsions with rice dreg protein hydrolysate[J]. Food Research International,2012,48(2):876-884.
[12]李薇.米渣蛋白酶解物壁材特性及其微膠囊化研究[D].南昌:南昌大學,2011.
Study on the interfacial property,physical and oxidative stability of emulsions stabilized by whey protein
CHEN Xian-xin1,MA Xiao-yu1,ZHU Wen-ting1,TANG Xiao-ming1,ZHU Xue-mei1,*,XIONG Hua1,BAI Chun-qing2
(1.State Key Laboratory of Food Science and Technology,Nanchang University,Nanchang 330047,China;2.College of Life Science,Jiangxi Science and Technology Normal University,Nanchang 330013,China)
In this study,whey protein and corn oil were used to prepare oil-in-water(O/W)emulsions using high-pressure homogenization.The effects of whey protein concentration(0.45%~3.60%)and ionic strength (250 mmol/L NaCl)on the interfacial property,physical and oxidative stability of emulsions were investigated. The results showed that increasing whey protein concentration lead to decrease in the particle size,creaming index,peroxide value(POV)and thiobarbituric acid reactive substances(TBARS),and increase in interfacial protein concentration and potential.Addition of 250 mmol/L NaCl contributed to increase in the particle size,creaming index,interfacial protein concentration,potential,POV and TBARS values of the emulsions.These findings indicated that the physical and oxidative stability of the emulsions could be improved by increasing the interfacial protein concentration or decreasing ionic strength.
emulsion;whey protein;physical stability;oxidative stability
TS201.1
A
1002-0306(2016)04-0155-06
10.13386/j.issn1002-0306.2016.04.022
2015-07-06
陳先鑫(1990-),男,碩士研究生,研究方向:食品營養(yǎng),E-mail:994821760@qq.com。
朱雪梅(1982-),女,博士,副教授,主要從事功能性油脂和油脂化學方面的研究,E-mail:zhuxuemei@ncu.edu.cn。
南昌大學科研訓練(創(chuàng)新學分)項目(14001748);國家“十二五”農(nóng)村領域科技計劃項目(2013AA102203-05)。

