酸性KI溶液被空氣中O2氧化的數字化實驗研究
顧曄
摘要:碘離子在酸性條件下容易被空氣中的O2氧化,而碘量法滴定常常處于酸性環境中,空氣中氧氣是否會對滴定終點產生影響?為了解決上述問題,利用數字化實驗手段研究了碘離子在酸性條件下被空氣中的O2氧化的情況,得到0.6 mol/L KI溶液在不同pH環境下的吸光度隨時間變化圖像,并由此判斷常規碘量法定量實驗過程中可以忽略氧氣對滴定終點的影響。
關鍵詞:KI;碘量法滴定;氧化;酸度;色度傳感器
文章編號:1005–6629(2016)8–0055–03 中圖分類號:G633.8 文獻標識碼:B
KI固體、標準溶液等常用于物質組成、樣品濃度等定量分析,如碘量法、沉淀法等,而I-離子在溶液中具有一定的還原性(I2+2e-=2I-,φθ=+0.5355V[1]),滴定過程中溶液中的I-離子可能直接被空氣中的O2(O2+4e-+4H+=2H2O,φθ=+1.229V[2])氧化,這樣就會對最終的分析結果產生影響。果真如此嗎?碘量法是經典的定量實驗方法,其終點的準確性是不是受酸度的影響?根據Nernst方程可知“凡有H+參加的電極反應,酸度對電極電勢的影響都是很大的[3]”,那么酸度在怎樣的區間可以忽略空氣中氧氣對滴定的影響?帶著這些疑問,筆者嘗試了碘化鉀溶液在不同酸度環境下被O2氧化的相關實驗。
1 相關文獻研究
人教版高中化學選修4(化學反應原理)模塊第二章第二節的[科學探究]欄目探究了反應“4I-+ O2+4H+=2I2+2H2O”中溶液出現藍色的時間和溫度的關系(提供1 mol/L KI溶液、0.1 mol/L H2SO4溶液和淀粉溶液);2010年朱正德老師研究了敞開體系中上述實驗中出現藍色的時間和溫度的關系[4](觀色法);謝慶群在此基礎上采用平行對比試驗研究了密閉體系下溫度的影響[5](觀色法),兩位老師均采用課本中給予的0.1 mol/L H2SO4溶液控制了酸度變量;2012年李桂林等研究了酸度對碘量法滴定的影響,提出弱酸性的KI淀粉溶液能作為測定KIO3的試劑的觀點[6];后來也有老師探討了酸堿性環境對該反應的影響:2013年李曉明等探討了碘化鉀與空氣反應的酸堿性條件得出“在堿性溶液中碘離子也可以被O2氧化,且隨著pH的減小碘離子的氧化越容易[7]”的結論;隨后2015年吳朝輝老師借助實驗條件和理論計算分析了不同pH條件下氧化、歧化速率的相對大小和影響因素,提出“KI和O2的反應,受KI的狀態、溶液的pH以及氧的分壓等因素影響[8]”。
顯然,除了溫度,酸度對該反應的影響也是非常明顯的,而滴定過程中涉及KI的體系均需控制在中性或堿性環境中嗎?2012年江蘇卷19題就出現了酸性條件下的類似滴定:“……為確定加入鋅灰(主要成分為Zn、ZnO,雜質為鐵及其氧化物)的量,實驗中需測定除去H2O2后溶液中Cu2+的含量。實驗操作為:準確量取一定體積的含有Cu2+的溶液于帶塞錐形瓶中,加適量水稀釋,調節溶液pH=3~4,加入過量的KI,用Na2S2O3標準溶液滴定至終點。……”。此處pH=3~4對滴定終點判斷沒有影響嗎?過量的KI是否會被空氣中的O2氧化?僅憑視覺觀察加入淀粉后有無藍色出現可能不太可靠,不同人的辨色能力有差異,同一個人看不同樣品也不能做到完全一致。分光光度計是適用于解決此類問題的,但連續的吸光度變化需要若干數據作工作曲線,于是筆者嘗試采用色度傳感器做數字化實驗。
2 實驗部分
2.1 實驗試劑和器材
試劑:0.6 mol/L KI溶液、0.5%淀粉溶液(新配)、1.0 mol/L H2SO4、0.10 mol/L H2SO4、10-2 mol/L H2SO4、10-3 mol/L H2SO4、10-4 mol/L H2SO4、10-5 mol/L H2SO4、10-6 mol/L H2SO4
器材:色度傳感器、比色皿、數據采集器(Venier LoggerPro)、計算機等
2.2 實驗步驟
(1)相關溶液的配制(略)。
(2)向1~8號試管中分別加入3mL 0.6 mol/L的KI溶液,滴入1滴新配制的0.5%淀粉溶液。
(3)向1~7號試管中分別加入3mL 1.0 mol/L、0.10 mol/L、10-2 mol/L、10-3 mol/L、10-4 mol/L、10-5 mol/L、10-6 mol/L硫酸,振蕩均勻后,取適量液體于比色皿中,用色度傳感器(吸收波長選擇565nm)測量各試管中溶液的吸光度隨時間的變化曲線。
(4)在8號試管中再加入3mL的蒸餾水,同樣方法測量其吸光度隨時間的變化曲線。
(5)分析數據,記錄各混合液吸光度達到0.15(A)時所需的顯色時間。
2.3實驗數據采集和分析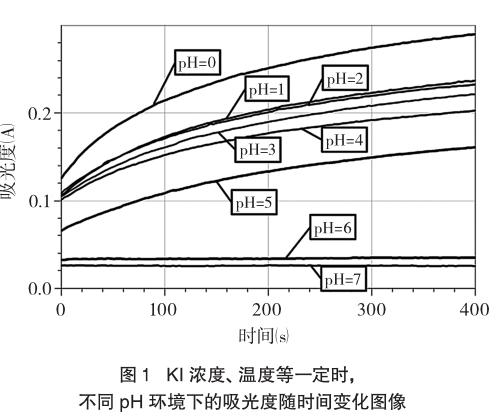
取實驗條件為室溫13.3℃,記錄1~8組(其中第8組為參比組)、實驗吸光度達15%的顯色時間(從圖1獲取或直接從LogPro軟件中讀取),結果如表1。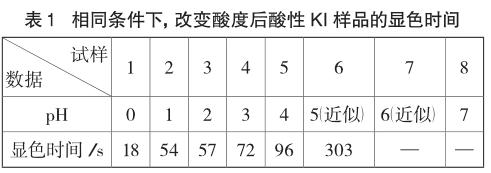
可見,在控制溫度、氣壓、吸光度等變量時,顯色時間隨pH的增大而延長。只有在c(H+)=1 mol·L-1時(實驗室溫度13.3℃)溶液才在短短18s內被迅速氧化。表1數據說明強酸性條件下碘離子很快被氧化成I2,較弱的酸性條件下該反應是較慢的,故在酸性不是很強的介質中,碘離子被空氣中氧氣氧化的因素可以忽略。也正因為如此,在間接碘量法滴定銅離子、鐵離子時,往往有一個調節pH的環節,如中國化學會第26屆全國高中生化學競賽(省級賽區)試卷第3題測定Cu2+離子時有“冷卻后加入2g KI固體(過量)和適量Na2CO3,溶液變為棕色并生成沉淀”的操作,其中Na2CO3的加入與調節反應體系pH不無關系。
3 結論與討論
3.1 結論
結合文獻給出的電極電勢數據:“I2+2e-=2I-,φθ=+0.5355V,O2+4e-+4H+=2H2O,φθ=+1.229V”,不難發現該反應“4I-+O2+4H+=2I2+2H2O”進行的趨勢是較為明顯的,但反應的限度是熱力學問題,能否立即發生是動力學問題,表1數據說明較弱的酸性條件下該反應是很慢的,到肉眼可觀察到明顯變色所需時間更長,故文章開始引用的2012年江蘇卷19題調節pH至3~4是較為合理的。強酸性條件(pH<2)下,才需考慮空氣中氧氣對滴定終點的影響,否則經典的“碘量法”為何時至今日仍在使用呢?當然,為了力求實驗結果的準確性,我們在碘量法滴定過程中也應該避免滴定時間過長,將氧氣的影響降到最小。
3.2 實驗技術反思
以色度傳感器為主要技術支撐的數字實驗在該實驗中起到了記錄連續時間范圍內的吸光度變化數值,為數據篩選提供了較大的數據樣本和方便的采集途徑,同時也有利于控制肉眼較難判斷的顏色深淺的程度。當然,限于比色皿的空間和操作規則,本實驗還有一個遺憾,表1中的pH是計算得出的,部分數據不夠精確,若能配合pH傳感器和溶解氧傳感器給出pH和溶解氧的實時變化數據,相信實驗結論將更加完善。
3.3 對教學的啟發
反應“4I-+O2+4H+=2I2+2H2O”是一個很好的探究溫度對化學反應速率影響的實驗素材,但不妨將之拓展:(1)氧氣量(溶解氧傳感器和壓強傳感器)對顯色時間的影響;(2)酸度對顯色時間的影響;(3)KI濃度對顯色時間的影響(控制酸度變量,配制0.1~2.0 mol/L的KI溶液)。這樣學生對這個重要反應的認識便更加深刻,同時對影響速率的因素認識也將更加全面。
致謝:感謝南京師范大學教師教育學院研究生韋存容、葛春洋等在實驗技術、器材等方面給予的支持和幫助!
參考文獻:
[1][2]武漢大學等.無機化學(上)(第三版)[M].北京:高等教育出版社,1994:500~502.
[3]華彤文等.普通化學原理(第3版)[M].北京:北京大學出版社,2009:213.
[4]朱正德.淀粉碘化鉀酸性溶液在空氣中出現藍色與溫度的關系實驗研究[J].中學化學教學參考,2010,(6): 46~47.
[5]謝慶群.淀粉碘化鉀酸性溶液變為藍色的實驗條件再探究[J].化學教學,2014,(8):69.
[6]李桂林.碘量法在中學化學實驗中的應用和探究[J].化學教學,2012,(2):48~50.
[7]李曉明,管廷河. KI溶液遇空氣氧化變質原因的探究[J].化學教學,2013,(5):47~48.
[8]吳朝輝.碘化鉀淀粉溶液遇氧氣是否變色的原因探析[J].化學教學,2015,(8):53~55.

