非特殊型浸潤性乳腺癌HER-2檢測方法的對比研究
成玉霞 赫淑倩 董賀 孫青
·論著·
非特殊型浸潤性乳腺癌HER-2檢測方法的對比研究
成玉霞 赫淑倩 董賀 孫青★
目的應用實時定量PCR技術(quantitive real-time PCR,qPCR)檢測石蠟包埋非特殊型浸潤性乳腺癌標本的HER-2表達狀況,與免疫組織化學技術(immunohistochemistry,IHC)和熒光原位雜交技術(fluorescence in situ hybridization,FISH)相應檢測結果進行比較,以驗證qPCR技術檢測HER-2方法的可靠性和實用性。方法采用FISH和qPCR技術對IHC檢測結果分別為HER-2(0、1+、2+、3+)的乳腺癌標本各100例進行檢測,用kappa檢驗分析三者的一致性。結果100例HER-2(0)和HER-2(1+)的標本FISH和qPCR的檢測結果均無擴增,符合率100%;IHC檢測HER-2(2+)的標本,FISH和qPCR檢測結果之間k=0.731(P<0.001),二者一致性強;IHC檢測HER-2(3+)的標本,FISH與qPCR檢測結果k=0.634(P<0.001),二者具有較好的一致性,與IHC檢測結果也具有較強的一致性。三者對乳腺癌患者的臨床病理指標反應具有較好的一致性。結論qPCR方法簡便、實用、有效,檢測乳腺癌HER-2基因狀況可與FISH法互為補充。
非特殊型浸潤性乳腺癌;HER-2;IHC;FISH;qPCR
近年來,我國乳腺癌的發病率和死亡率逐年上升,且日趨年輕化,成為威脅女性健康的幾大惡性腫瘤之一。據文獻報道,約20%~25%的乳腺癌患者呈人類表皮生長因子受體-2(human epidermal grow th factor receptor 2,HER-2)過表達或基因擴增[1],而HER-2高表達的浸潤性乳腺癌分化低,易發生淋巴結轉移,且復發早,預后差[2-3]。2002年,美國食品和藥品管理局(Food and Drug Administration,FDA)批準赫賽汀用于HER-2過表達的乳腺癌[4]。大量臨床研究也表明,HER-2高表達的乳腺癌患者使用赫賽汀治療后,其無病生存率和總生存期大大延長;相反,HER-2低表達患者使用赫賽汀治療不能獲益。因此標準化檢測HER-2受體已成為赫賽汀靶向治療的重要部分[5]。
目前,美國FDA批準應用于評估HER-2狀態的技術為免疫組織化學(immunohistochemistry,IHC)和熒光原位雜交(fluorescence in situ hybridization,FISH)2種。然隨著實時定量PCR技術(quantitive real-time PCR,qPCR)的發展和日趨成熟,RNA水平的HER-2檢測變得更加簡便、快捷,其能否替代FISH技術作為IHC檢測的補充,有待進一步的研究確證[6-7]。本研究分別用IHC、FISH和qPCR 3種技術檢測400例非特殊性浸潤性乳腺癌石蠟組織的HER-2狀態,將三者結果進行比較,并對比三者結果與患者臨床病理特征之間的聯系,以驗證qPCR技術的可靠性和實用性及其替代FISH技術的可行性。
1 材料與方法
1.1 標本來源
選取2010年1月至2014年6月我院手術切除病理明確診斷的非特殊性浸潤性乳腺癌患者的石蠟腫瘤組織,重新切片進行IHC檢測,由病理診斷醫師重新評估,從中選取HER-2免疫組化結果0、1+、2+和3+各100例分別行FISH基因擴增和qPCR檢測。患者均為女性,年齡最小為26歲,最大為83歲,中位年齡53.1歲。回顧入組患者ER、PR及Ki-67的免疫組化結果,并統計分析HER-2結果與各指標表達之間的關系。
1.2 IHC法
腫瘤蠟塊切片3~4μm,粘附載玻片貼片,常規65℃烘烤過夜,平行加陰陽性對照。使用美國羅氏VENTANA Bench Mark全自動免疫組化染色機和VENTANA抗HER-2蛋白的單克隆抗體,克隆號4b5。IHC標記的操作關鍵步驟依次為VENTANA脫蠟液EZ 75℃脫蠟4 m in;95℃PH8.0抗原修復30min;緩沖液中漂洗,過氧化物酶阻滯液中孵育4 min;隨后加入HER-2一抗,37℃孵育16m in;二抗UV HRP孵育8m in;DAB顯色8m in,蘇木素復染,返藍液返藍,最后漂洗封片。
1.3 FISH法
切片準備同IHC,平行加做陰陽性對照。Path-Vysion HER-2 DNA探針試劑盒購自美國Vysis公司,熒光顯微鏡型號為德國萊佧LeiCa DM 4000B。操作步驟:充分脫蠟至水,蒸餾水煮沸20 min,晾干后37℃胃酶消化15 m in,漂洗后梯度酒精脫水晾干,加10μL雜交液蓋片并用蠟膠封邊,85℃變性5 m in,37℃雜交過夜。第2天將切片置于雜交后洗液(2×SSC,0.3%NP-40)中漂浮蓋玻片,組織片入雜交后洗液72℃2 m in,再將其放置在暗處室溫干燥,滴加10μL DAPI顯色液在組織片靶區域,蓋玻片封片,熒光顯微鏡觀察結果。使用德國萊佧Leica CW 4000 FISH分析軟件進行拍照并計數。
1.4 qPCR法
1.4.1 組織準備
組織進行切片,厚度8~10μm,對照相應組織的HE切片選取腫瘤區域進行顯微切割,根據癌細胞量多少使用2~3片進行檢測,切片后盡快進行RNA的提取,如不能及時提取要存放于-20℃,以減少RNA的降解。
1.4.2 RNA的提取
提取組織總RNA使用的是微量組織總RNA快速提取試劑盒(江蘇默樂生物科技有限公司),采用胍鹽裂解的柱式離心法從石蠟組織切片中提取。每例吸取2μL作為模板進行下游實驗,剩余可以放入冰箱-20℃保存。
1.4.3 擴增檢測
HER-2核酸檢測試劑盒(熒光PCR法)購自江蘇默樂生物科技有限公司,采用逆轉錄聚合酶鏈式反應(reverse transcription ploymerase chain reaction,RT-PCR)結合Taqman熒光探針技術對乳腺癌患者腫瘤組織樣本中HER-2基因表達進行鑒別,每個樣本同時進行管家基因的檢測,實現基因的相對定量,熒光信號的收集定為FAM(HER-2)、HEX(VIC)。同一批次加入陰陽性質控品,儀器為美國ABI公司PCR儀7500。擴增體系為25μL,其中包括RT-PCR buffer 18.1μL,酶m ix 0.4μL,引物探針m ix 4.5μL,RNA(cDNA)模板2.0μL。擴增條件為45℃15 m in;95℃1 m in;然后95℃15 s,58℃1 m in擴增40個循環。
1.5 結果判定標準
HER-2 IHC和FISH檢測結果判斷標準均為2013年美國臨床腫瘤學會/美國病理學家學會2007版乳腺癌HER-2檢測指南基礎上的更新版本[8]以及我國《乳腺癌HER-2檢測指南(2014版)》[9]。
qPCR HER-2檢測結果判斷標準按照試劑盒說明推薦:陽性質控品ΔCt≥23,且陰性質控品其突變管與參照管均無Ct值,或未出現典型擴增曲線,檢測樣本的CtHER-2和Ct管家基因都有典型S型擴增曲線,提示本次檢測有效,否則無效。ΔCt= 20-(CtHER-2-Ct管家基因),ΔCt≥23,HER-2表達陽性;ΔCt≤21,HER-2表達陰性;21<ΔCt<23,應重新檢測,若ΔCt>21,則為HER-2表達陽性,否則為陰性。
對于3種方法差異顯著的病例,重復進行檢測,確保結果真實可靠。
1.6 統計學方法
應用SPSS 11.5統計學分析軟件,3種方法檢測結果的一致性采用Kappa檢驗,P<0.05為差異具有統計學意義;用χ2和Fisher's Exact test來分析HER-2結果與患者臨床病理特征之間的關系。
2 結果
2.1 乳腺癌患者HER-2、ER、PR、Ki-67免疫組織化學染色
乳腺癌腫瘤細胞中ER、PR和Ki-67免疫組織化學染色陽性表達均定位于細胞核,HER-2的表達位于細胞膜(圖1)。患者ER表達結果為:陰性80例,15例1+,45例2+,260例3+;PR表達結果為:陰性145例,50例1+,60例2+,145例3+;Ki-67表達結果為:≤5%45例,>5%且≤30%220例,>30%且≤50% 70例,>50%65例;HER-2結果如表1所示。
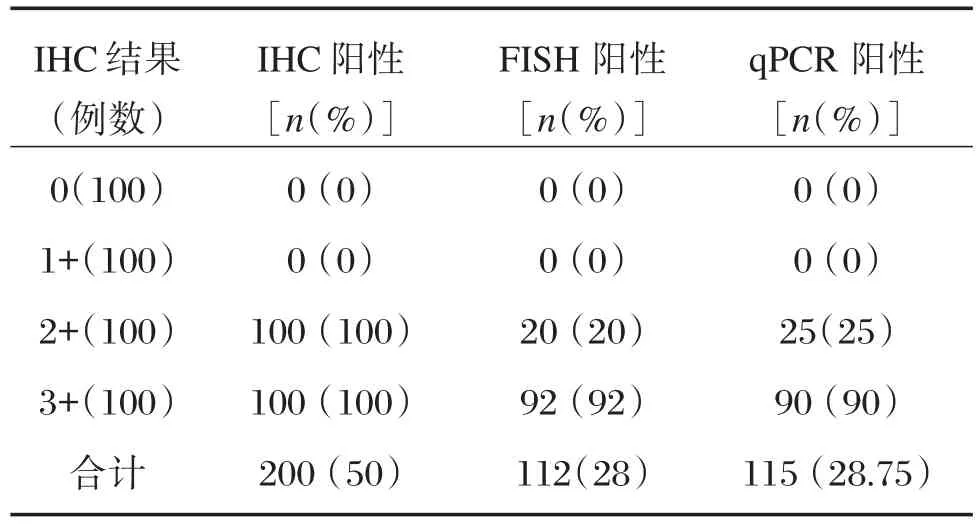
表1 浸潤性乳腺癌中FISH、qPCR和IHC檢測HER-2的結果比較Table 1 Comparison of HER-2 results by FISH,qPCR and IHC
2.2 乳腺癌患者HER-2基因擴增的FISH檢測結果
400例標本中,FISH檢測結果為:HER-2基因擴增112例,擴增率28%(112/400);無HER-2基因擴增者285例,占檢測總例數的71.3%(291/400);不能確定者3例,占0.075%(3/400),該3例后經qPCR檢測,證實其中2例存在HER-2的擴增,另1例未擴增。腫瘤組織中FISH 3種表達的情況如圖2所示。
2.3 乳腺癌患者HER-2基因qPCR檢測結果
400例標本中,檢測有擴增的115例,擴增率28.8%(115/400),另外285例標本沒有擴增,占到檢測總例數的71.25%(285/400),見表1。
2.4 乳腺癌患者HER-2基因不同檢測方法間的區別與聯系
200例IHC檢測分別為0/1+的標本中,FISH和qPCR檢測無一例擴增,符合率100%;在IHC檢測HER-2結果為2+的標本中,FISH的陽性檢出率為20%,qPCR的陽性檢出率為25%,其中FISH和qPCR結果共同陰性者71例(73%,71/97),FISH和qPCR結果共同陽性者17例(18%,17/97),qPCR陽性而FISH結果陰性的病例6例(6%,6/97),FISH結果陽性而qPCR檢測為陰性的有3例(3%,3/97),經Kappa檢驗,在IHC 2+的乳腺癌中FISH和qPCR的檢測結果k=0.731(P<0.000 1)(表2,圖3)。例2例(2%,62/100),FISH結果陽性而qPCR檢測為陰性的有4例(4%,4/100),經Kappa檢驗,在IHC 3+的乳腺癌中FISH和qPCR的檢測結果k= 0.634(P<0.000 1)(表3,圖4)。
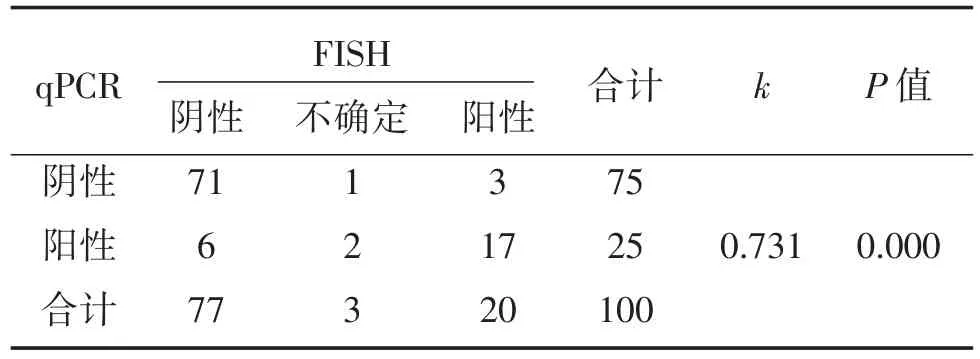
表2 乳腺癌中HER-2表達2+標本qPCR和FISH表達結果的比較Table 2 Comparison of HER-2 results by qPCR and FISH in IHC(2+)
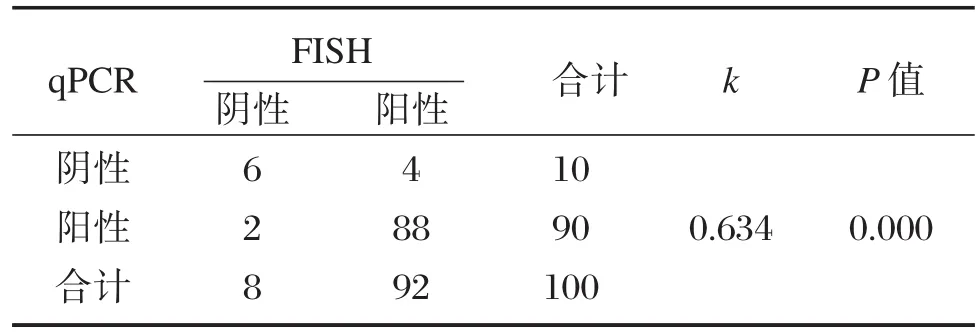
表3 乳腺癌中HER-2表達3+標本qPCR和FISH表達結果的比較Table 3 Comparison of HER-2 resultsby qPCR and FISH in IHC(3+)
在IHC檢測表達為3+的腫瘤組織中,FISH檢測的整體陽性率為92%,qPCR的陽性檢出率為90%,其中FISH和qPCR結果共同陽性者88例(88%,88/100),FISH和qPCR結果共同陰性者6例(6%,6/100),qPCR陽性而FISH結果陰性的病
2.5 乳腺癌中IHC、qPCR和FISH檢測HER-2結果與臨床病理特征的聯系
病理學分級I級的有40例,Ⅱ級的有295例,Ⅲ級的有65例;淋巴結轉移的有175例,無淋巴結轉移的有225例;臨床分期T1有180例,T2有175例,T3有20例,T4有25例。
IHC和qPCR檢測的HER-2結果陽性率均與組織的病理學分級、ER、PR以及Ki67的表達這幾個因素密切相關(P<0.05),而與患者年齡、淋巴結轉移情況、臨床分期關系不密切,分別見表4、表6;而FISH檢測的HER-2結果陽性率與患者的組織的病理學分級、臨床分期、ER、PR以及Ki67的表達這幾個因素亦密切相關(P<0.05),而與患者的淋巴結轉移情況關系不密切(表5)。
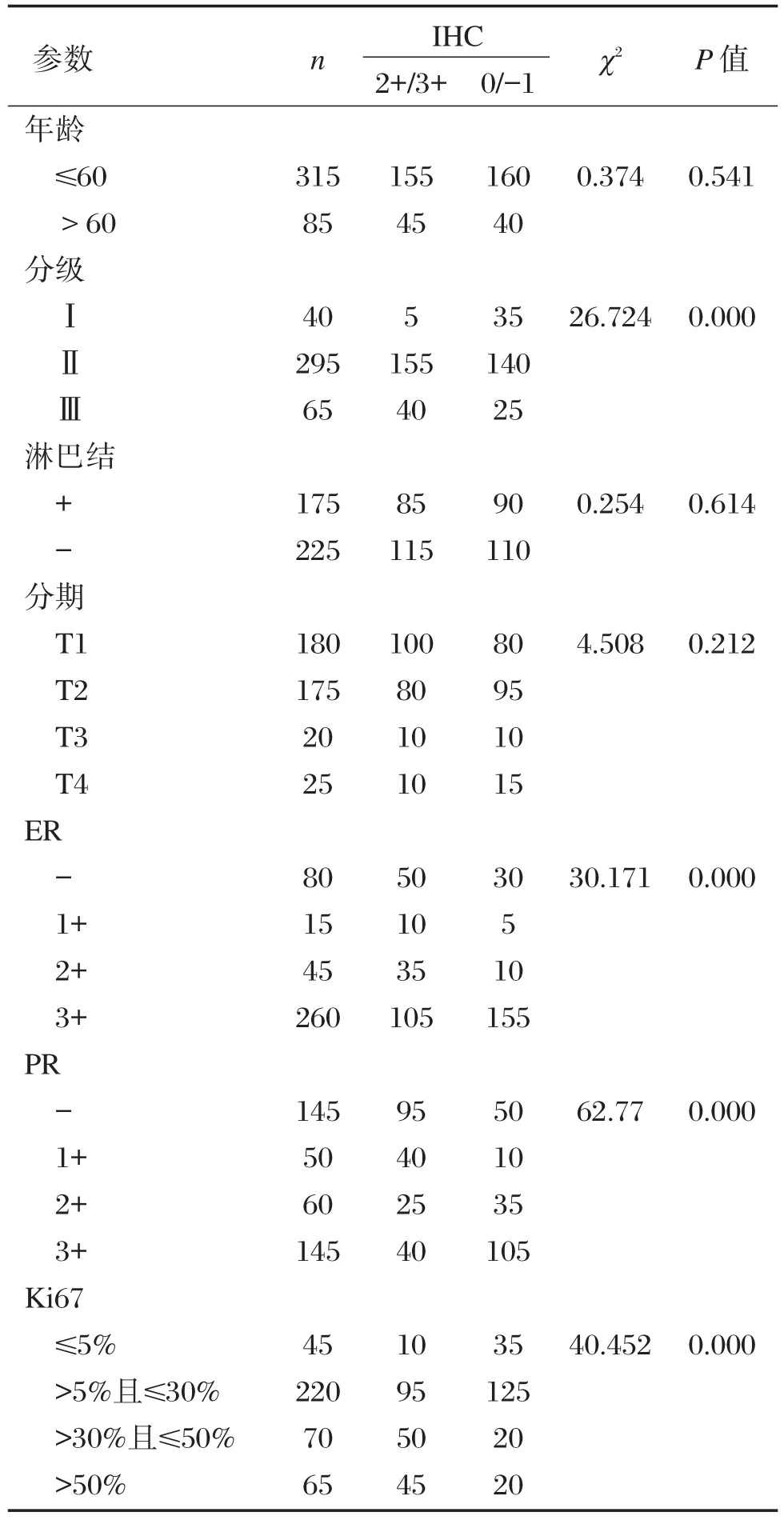
表4 用免疫組織化學(IHC)方法檢測的HER-2表達的結果與臨床病理特征Table 4 Expression of HER-2 by IHC and clinicopathological parameters
3 討論
HER-2/neu或HER-2基因定位于人第17號染色體的長臂(17q21.1),其編碼的產物HER-2在乳腺癌組織中有25%~30%存在異常高表達[10]。HER-2高表達或其基因的擴增與乳腺癌的發生、發展、預后及治療等有著重要的聯系[11]。HER-2基因擴增的乳腺癌患者對內分泌治療及常規化療藥物不敏感、預后差,而對HER-2的靶向藥物赫賽汀的敏感性較好。2002年,赫賽汀已通過美國FDA認證,但必須在IHC檢測HER-2(3+)和/或FISH法檢測結果為陽性時才能使用[12],自此,HER-2檢測有了巨大的臨床價值[5]。
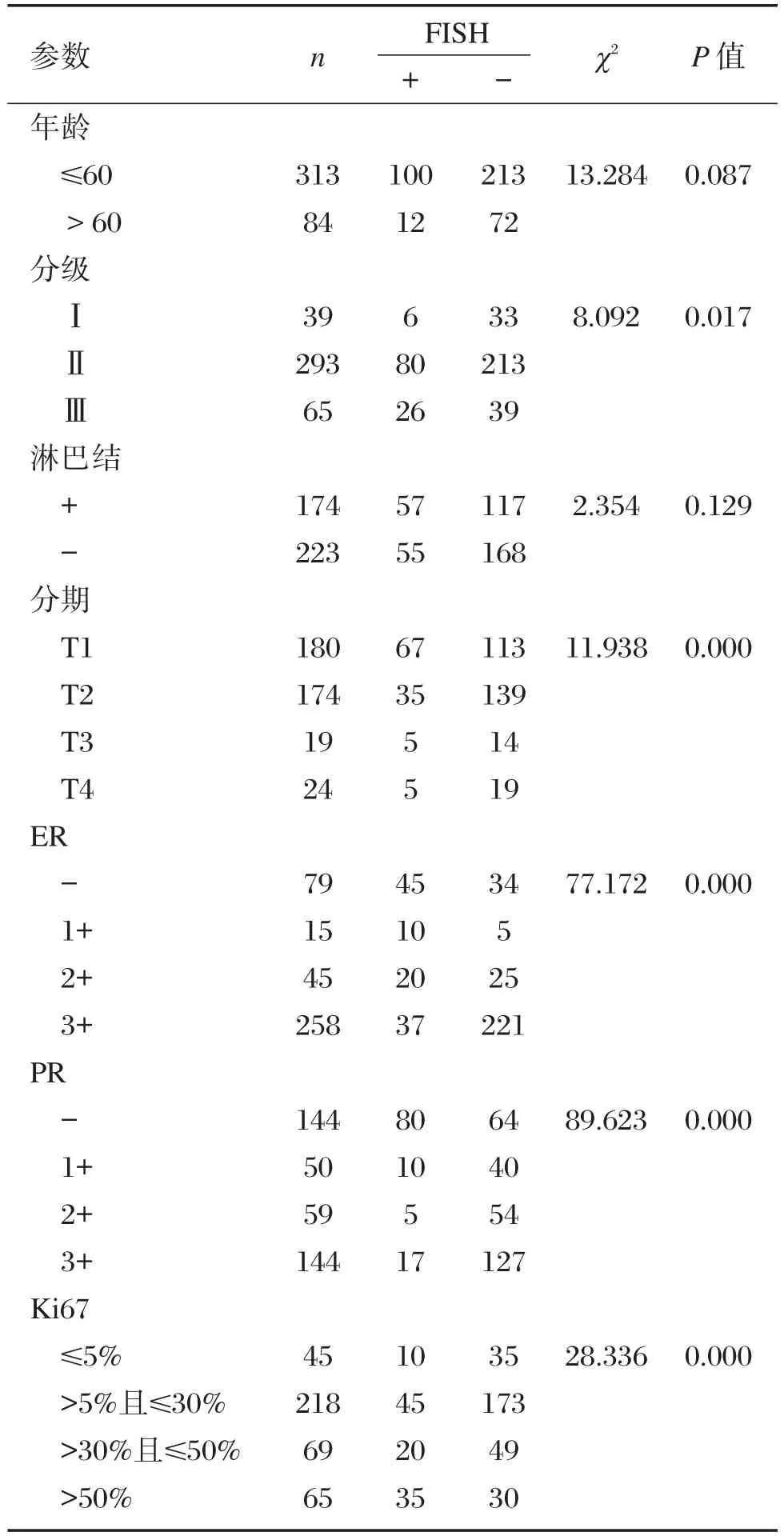
表5 用熒光原位雜交(FISH)方法檢測的HER-2表達的結果與臨床病理特征Table 5 Expression of HER-2 by FISH and clinicopathological parameters
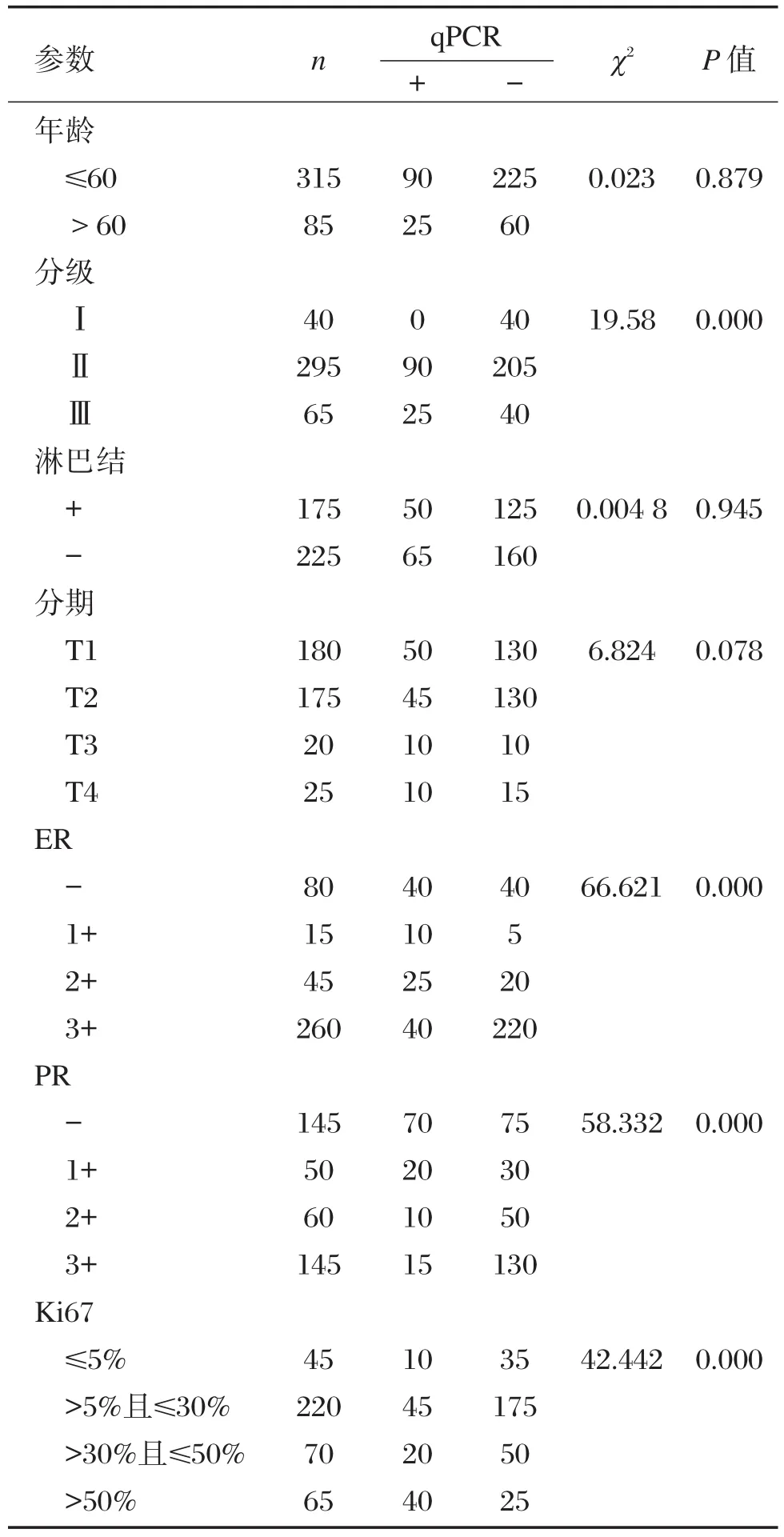
表6 用實時定量PCR(qPCR)方法檢測的HER-2表達的結果與臨床病理特征Table 6 Expression of HER-2 by qPCR and clinicopathological parameters
目前,國內外常用的HER-2檢測方法有IHC、FISH、顯色原位雜交[13](chromosome in situ hybridization,CISH)、銀染原位雜交(silver in situ hybridization,SISH)和qPCR[14]等,但qPCR尚未作為常規應用。IHC是目前臨床上常用的檢測乳腺癌HER-2蛋白表達的方法,該方法操作簡便、費用低廉、可重復性好。然而由于標記蛋白在組織固定后其抗原活性會下降或消失,從而導致假陰性;抗原修復可提高其敏感性,但修復過度會產生假陽性;另一方面,抗體的差異、結果主觀判斷差異等原因,均使得IHC結果假陽性或假陰性問題無法避免。全自動免疫組化機的應用,最大程度去除了染色過程中人為因素的影響;但是標本離體時間的長短,之后能否及時有效固定及其標準化的組織處理對于IHC檢測結果的準確與否至關重要。FISH是用于檢查17號染色體著絲粒和HER-2/neu基因擴增情況的技術,染色體的穩定性比蛋白質好得多,故此技術的敏感性和特異性較高,并可以避免17號染色體的非整倍體現象導致的IHC結果的假陽性,已被公認為檢測HER-2基因過表達的金標準。但在進行FISH檢測時也會受到一些因素的影響,比如蛋白消化不當、烤片溫度過高等,可使熒光信號減弱或無信號;熒光容易淬滅,需要暗視野觀察并計數等,使得結果判定容易受人為因素影響;FISH方法試劑成本高,操作繁瑣,需要配置特殊的熒光顯微鏡及專門的軟件觀察等,無疑給檢測帶來困難。
qPCR[15]方法是檢測RNA的最好選擇,更接近于RNA定量,qPCR方法敏感可靠。Chariyalertsak等[16]的研究顯示,qPCR方法能簡單又精確地檢測出石蠟組織中的HER-2表達狀況。Barberis等[17]認為qPCR能有效檢測HER-2且成本較低,Bossard等[18]也有類似的發現,與IHC相比,qPCR的敏感性和特異性能達到87.5%和100%,與FISH相比,qPCR的敏感性和特異性能達到89.5%和92%。本次實驗中我們用實時熒光定量PCR的方法檢測HER-2mRNA的表達,研究結果表明無論在HER-2(0,1+)的乳腺癌患者中,還是HER-2(2+,3+)的患者中qPCR檢測結果和FISH基因檢測結果都出現較高的一致性,(k=0.731,k=0.634,P均<0.001),由此我們認為qPCR檢測結果與金標準FISH的檢測結果一致性好,其他研究也得出過類似的結論[19-20]。qPCR方法具有操作簡便、經濟省時以及可以批量操作的優點,其成本比IHC高,但僅為FISH成本的1/4左右,將來若能應用于臨床檢測,可為IHC(2+)的患者提供更為經濟的選擇。
本研究中,IHC、FISH和qPCR檢測的HER-2結果陽性率均與組織的病理學分級、ER、PR以及Ki67的表達等因素密切相關(P<0.05),而與患者年齡、淋巴結轉移情況、臨床分期關系不密切,說明在反應臨床病理特征方面三者具有一致性,從側面證實了3種檢測方法結果的一致性。Zhu等[21]在應用qPCR技術在檢測胃癌HER-2也得到了同樣的結論。未來qPCR技術有望在乳腺癌HER-2檢測中應用于臨床與FISH方法互為補充。
本研究中IHC(2+,3+)標本中的陽性率與國內外大多數研究結果一致,但在IHC(0,1+)的標本中未曾檢測出陽性,這除了與標本及時充分固定,處理恰當和使用全自動免疫組化染色機染色等因素有關外,還可能與我們使用新的評判標準有關。在我們的研究中應用舊的免疫組化HER-2判讀標準有1例判為1+、更新的判讀標準為2+的標本,經FISH和qPCR檢測示均有HER-2基因擴增,說明更新的判讀標準較舊標準避免了漏檢,具有更好的參考價值。對于IHC(3+)而FISH(-)或qPCR(-)的患者選擇使用赫賽汀靶向藥物的療效尚需進一步大樣本的研究和臨床隨診驗證。
[1]Demonty G,Bernard-Marty C,Puglisi F,et al.Progress and new standards of care in the management of HER-2 positive breast cancer[J].Eur J Cancer,2007,43(3):497-509.
[2]Mandusic V,Dim itrijevic B,Nikolic-Vukosavljevic D,et al.Different associations of estrogen receptor βisoforms,ERβ1 and ERβ2,expression levels with tumor size and survival in early-and late-onset breast cancer[J].Cancer Lett,2012,321(1):73-79.
[3]Berghoff AS,Bago-Horvath Z,Dubsky P,et al.Impact of HER-2-targeted therapy on overall survival in patients with HER-2 positive metastatic breast cancer[J].Breast J,2013,19(2):149-155.
[4]Bayoudh L,Afrit M,Daldoul O,et al.Trastuzumab(herceptin)for themedical treatment of breast cancer[J].TunisMed,2012,90(1):6-12.
[5]Petersen ER,Srensen PD,Jakobsen EH,et al.Serum HER-2 predicts response and resistance to trastuzumab treatment in breast cancer[J].Clin Chem Lab Med,2013,51(7):1483-1492.
[6]Nistor A,Watson PH,Pettigrew N,et al.Real-time PCR complements immunohistochem istry in the deter mination of HER2/neu status in breast cancer[J]. BMCClin Pathol,2006,6:2-5.
[7]Specht K,Richter T,Müller U,et al.Quantitative gene expression analysis in microdissected archival formalin-fixed and paraffin-embedded tumor tissue[J]. Am JPathol,2001,158(2):419-429.
[8]Wolff AC,Hammond ME,Schwartz JN,et al.Recommendations for human epidermal grow th factor receptor 2 Testing in Breast Cancer:American Society of Clinical Oncology/College of American Pathologists Guideline update[J].JClin Oncol,2013,31(31):3997-4013.
[9]《乳腺癌HER2檢測指南(2014版)》編寫組.乳腺癌HER2檢測指南(2014版)[J].中華病理學雜志,2014,43(4):262-266.
[10]Slamon DJ,Godolphin W,Jones LA,et al.Studies of the HER-2/neu proto-oncogene in human breast and ovarian cancer[J].Science,1989,244(4905):707-712.
[11]Ross JS,Slodkowska EA,Symmans WF,et al.The HER-2 receptor and breast cancer:ten years of targeted anti-her-2 therapy and personalized medicine[J]. The Oncologist,2009,14(4):320-368.
[12]Tariq M,Muniba A,Waseem I,et al.Status of HER-2 amplification,polysomy17 and histopathological features of 425 pakistani breast cancer patients[J].Asian Pac JCancer Prev,2011,12(11):3069-3073.
[13]Kiyose S,Igarashi H,Nagura K,et al.Chromogenic in situ hybridization(CISH)to detect HER2 gene amplification in breast and gastric cancer:comparison with immunohistochemistry(IHC)and fluorescence in situ hybridization(FISH)[J].Pathol Int,2012,62(11):728-734.
[14]Garuti A,Rocco I,Cirmena G,et al.Quantitative real time PCR assessment of hormonal receptors and HER2 status on fine-needle aspiration pre-operatory specimens from a prospectively accrued cohort of omen with suspect breastmalignant lesions[J].GynecolOncol,2014,132(2):389-396.
[15]Ma GF,Liu YM,Gao H,et al.HER2 mRNA status contributes to the discrepancy between gene amplification and protein overexpression in gastric cancer[J]. Dig Dis Sci,2014,59(2):328-335.
[16]Chariyalertsak S,Purisa W,Vinyuvat S.Her-2/neu amplification deter m ined by real-time quantitative PCR and its association with clinical outcome of breast cancer in Thailand[J].Asian Pac JCancer Prev,2011(12):1703-1706.
[17]Barberis M,PellegriniC,Cannone M,etal.Quantitative PCR and Her2 testing in breast cancer:a technical and cost-effec-tiveness analysis[J].Am JClin Pathol,2008,129(4):563-570.
[18]Bossard C,Bieche I,Le Doussal V,et al.Real-time RT-PCR:a complementary method to detect Her-2 status in breast carcinoma[J].Anticancer Res,2005(25):4679-4683.
[19]Pazhoomand R,Keyhani E,Banan M,et al.Detection of HER2 status in breast cancer:comparison of current methods with MLPA and real-time RT-PCR[J].Asian Pac JCancer Prev.2013;14(12):7621-7628.
[20]Pu T,Guo P,Qiu Y,etal.Quantitative real-time polymerase chain reaction is an alternative method for the detection of HER-2 amplification in formalin-fixed paraffin-embedded breast cancer samples[J].Int J Clin Exp Pathol,2015 Sep 1;8(9):10565-10574.
[21]Zhu GJ,Xu CW,Fang MY,etal.Detection of Her-2/ neu expression in gastric cancer:quantitative PCR versus immunohistochemistry[J].Exp Ther Med,2014,8(5):1501-1507.
Com parison of different methods for HER-2 status detection in non-special invasive breast carcinoma
CHENG Yuxia,HEShuqian,DONG He,SUN Qing★
(Department of Pathology,Qianfoshan Hospital,Jinan,Shandong,China,250014)
Objective To compare quantitative polymerase chain reaction(qPCR)with immunohistochemistry(IHC)and fluorescence in situ hybridization(FISH)for the detection of HER-2 in non-special invasive breast carcinoma.Methods HER-2 expression levels in carcinoma tissue were detected using IHC,and the HER-2 gene expression levels were determined by FISH and qPCR.According to IHC results,all patients were divided into 4 groups[(HER-2(0),HER-2(1+),HER-2(2+)and HER-2(3+)]with 100 cases in each. The kappa test was used to measure the consistency among the results of IHC,FISH and qPCR.Results In HER-2(0)and HER-2(1+)groups,there were no differences between the results of qPCR and FISH.In HER-2(3+)group,a few discrepancies were found between qPCR and FISH[k=0.634(P<0.001)].In HER-2(2+)group,the diagnostic consistency was good between qPCR and FISH[k=0.731(P<0.001)].Using FISH test,there was consistency in correlation between HER-2 expression and clinicopathological parameters in the results of qPCR,FISH and IHC.Conclusion qPCR is a convenient,objective and efficient method,which may be used as an alternative to FISH,for the detection of HER-2 gene state of non-special invasive breastcarcinoma.
Non-special invasive breast carcinoma;HER-2;IHC;FISH;qPCR
國家自然科學基金(81272420);山東省自然科學基金(ZR2012HM085)
山東省千佛山醫院病理科,山東,濟南250014
★通訊作者:孫青,E-mail:qingsw99@163.com

