槲皮素與6-O-α-D-麥芽糖-β-環糊精包合物的理化表征
李 赟,汪 芳,鄒 偉,王雪松,蔡紅燕,陳 軒,孫 威,沈汪洋,3,*
(1.武漢輕工大學食品科學與工程學院,湖北 武漢 430023;2.武漢凱迪工程技術研究總院有限公司,湖北 武漢 430023;3.大宗糧油精深加工省部共建教育部重點實驗室,湖北 武漢 430023)
槲皮素與6-O-α-D-麥芽糖-β-環糊精包合物的理化表征
李 赟1,汪 芳2,鄒 偉1,王雪松1,蔡紅燕1,陳 軒1,孫 威1,沈汪洋1,3,*
(1.武漢輕工大學食品科學與工程學院,湖北 武漢 430023;2.武漢凱迪工程技術研究總院有限公司,湖北 武漢 430023;3.大宗糧油精深加工省部共建教育部重點實驗室,湖北 武漢 430023)
采用相溶解度法研究6-O-α-D-麥芽糖-β-環糊精(6-O-α-D-maltosyl-β-cyclodextrin,Mal-β-CD)和β-環糊精(β-cyclodextrin,β-CD)對槲皮素的包合效果,利用溶劑法制備Mal-β-CD與槲皮素的包合物,借助紫外光譜分析、紅外光譜分析、掃描電子顯微鏡、X射線衍射、熱重及差示掃描量熱聯用等分析手段研究該包合物的理化性質,并采用分子對接法建立了該包合物的超分子結構。結果表明:Mal-β-CD包合槲皮素的能力高于母體β-CD。分子對接結果表明,槲皮素是沿Mal-β-CD的大口端方向進入其疏水空腔形成包合物,二者間是通過氫鍵相連接的。較之母體β-CD,Mal-β-CD與槲皮素的包合效果更好,且包合后槲皮素的物相發生重大變化,熱穩定性提高。
槲皮素;6-O-α-D-麥芽糖-β-環糊精;包合物;理化性質;分子對接
槲皮素是一種多功能性的天然膳食類黃酮[1],廣泛存在于蘋果、葡萄、草莓、洋蔥、花生、大豆、土豆、西蘭花、茶及紅酒中[2-4]。研究表明,槲皮素具有抗花粉癥、抗糖尿病、抗癌、抗病毒、抗炎、抗氧化、螯合金屬離子、清除自由基、保護神經等多種特性[5-11],對由腺苷二磷酸、膠原或凝血酶引起的血小板聚集及血栓有抑制作用[12]。但槲皮素水溶性低(<7 μg/mL)、穩定性低,導致其生物利用率低,從而限制了其在食品行業中的應用[13-14]。目前提高槲皮素水溶性的途徑主要有形成微脂囊、膠團、環糊精包合等[15-17],本研究采用與環糊精(cyclodextrin,CD)包合的途徑來提高槲皮素的水溶性,從而提高其利用率。
CD是由數個葡萄糖殘基以α-1,4糖苷鍵連接而成的環式低聚糖,由Villiers教授在1891年發現[18]。CD具有疏水中腔和親水外表面的特殊結構,這一特殊結構使其能夠與多種無機或有機分子形成主客體復合物[19],通過CD包合,客體分子的水溶性、化學穩定性可有效提高,且毒性有所降低。最常見的CD是分別由6、7、8 個葡萄糖殘基組成的α-、β-和γ-CD。β-CD因具有價格低廉和可與客體分子完美契合的空腔尺寸(空腔深度為0.78 nm,直徑為0.78 nm)的優點而在CD的包合中應用最為廣泛[20]。然而,有研究顯示,β-CD能夠與膽固醇、磷脂形成穩定的復合物,產生溶血作用,從而對細胞造成傷害,因此β-CD被禁止用于非腸道吸收方式給藥[21]。
6-O-α-D-麥芽糖-β-環糊精(6-O-α-D-maltosyl-βcyclodextrin,Mal-β-CD)是利用化學或生物酶法將麥芽糖基接枝到母體β-CD的6位羥基而得到的分支環糊精。該產物保留了母體β-CD的包合性能,且具有較母體β-CD更高的水溶性和安全性[22]。
本實驗采用相溶解度法研究β-CD和Mal-β-CD對槲皮素的包合效果,利用溶劑法制備槲皮素的包合物,借助紫外光譜分析、紅外光譜分析、掃描電子顯微鏡、X射線衍射、熱重法及差示掃描量熱法、核磁共振等分析手段研究包合物的理化特征,以期擴大槲皮素在食品和醫藥領域中的應用。
1 材料與方法
1.1 材料與試劑
槲皮素(純度98%)、β-CD(純度≥97%,相對分子質量為1 134.98)、Mal-β-CD(純度98%,相對分子質量為1 459.27) 美國Sigma公司;其他試劑均為分析純。
1.2 儀器與設備
RET Basic 型恒溫磁力攪拌器 廣州儀科實驗室技術有限公司;LGJ-10型冷凍干燥機 北京松源華興科技發展有限公司;1260型高效液相色譜儀 美國Agilent公司;TU-1810PC型紫外-可見光光度計 北京普析通用儀器有限責任公司;NEXUS670型傅里葉紅外光譜儀 美國尼高力儀器公司;S-3000N型掃描式電子顯微鏡 日本日立公司;7000型X射線衍射儀 日本島津制作所;AscendTM 600MHZ型核磁共振波譜儀德國Bruker公司;STA449F3型熱重/差熱綜合分析儀德國耐馳儀器制造有限公司。
1.3 方法
1.3.1 槲皮素/Mal-β-CD相溶解度的測定
槲皮素/Mal-β-CD相溶解度的測定參考文獻[23]進行。稱取5 mg槲皮素分別加入到不同濃度的β-CD和Malβ-CD溶液(0~10 mmol/L)中,制得混合溶液。將混合液在30 ℃條件下水浴振蕩72 h,使反應達到動態平衡。取上清液,用孔徑為0.45 μm的微孔濾膜過濾,上清液中槲皮素的濃度采用高效液相色譜法進行測定。用槲皮素濃度對CD濃度作圖,得到包合物的相溶解度圖。依據Higuchi-Connors方程計算得到表觀穩定常數Ks。
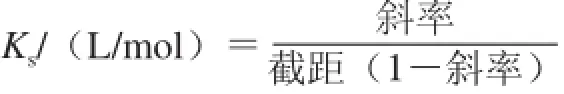
1.3.2 槲皮素/Mal-β-CD包合物的制備
稱取1.824 1 g(1.25 mmol)Mal-β-CD,用40 mL 30%甲醇溶解,待其完全溶解后,加入0.075 6 g(0.25 mmol)槲皮素,30 ℃條件下水浴振蕩72 h,之后4 000 r/s離心15 min,取上清液,除去甲醇,冷凍干燥,制得淺黃色固體,即為槲皮素/Mal-β-CD包合物。
1.3.3 槲皮素/Mal-β-CD物理混合物的制備
稱取0.075 6 g槲皮素、1.824 1 g Mal-β-CD,室溫條件下研磨攪拌均勻,制得槲皮素/Mal-β-CD物理混合物。
1.3.4 槲皮素/Mal-β-CD紫外光譜分析
稱取適量的槲皮素、Mal-β-CD、槲皮素與Mal-β-CD物理混合物及包合物溶于甲醇中,在300~400 nm波長處測其紫外吸收光譜。
1.3.5 槲皮素/Mal-β-CD紅外光譜分析
將適量槲皮素、Mal-β-CD、槲皮素與Mal-β-CD物理混合物及包合物用溴化鉀壓片,用傅里葉紅外光譜儀記錄其紅外光譜。
1.3.6 槲皮素/Mal-β-CD掃描電子顯微鏡觀察
將適量槲皮素、Mal-β-CD、槲皮素與Mal-β-CD物理混合物及包合物依照掃描電子顯微鏡操作要求制片后置于顯微鏡下觀察。
1.3.7 X射線衍射分析
取適量槲皮素、Mal-β-CD、槲皮素與Mal-β-CD物理混合物及包合物在Cu靶/石墨單色器,管壓40 kV,管流40 mA,在掃描范圍為10~60 °條件下進行X射線衍射分析。
1.3.8 槲皮素/Mal-β-CD熱重及差示掃描量熱同步分析
取5 mg左右槲皮素、Mal-β-CD、槲皮素與Mal-β-CD包合物均勻平鋪在坩堝中,用熱重及差示掃描量熱同步儀記錄樣品的熱重及差示掃描量熱曲線,測定條件為:氮氣流速20 mL/min,掃描溫度范圍40~500 ℃,掃描速率10 ℃/min。
1.3.9 分子對接
在Hyperchem 8.0軟件中構造槲皮素分子,結構運用分子力學方法MM+和半經驗的量子化學方法AM1進行優化,Mal-β-CD的構建參考文獻[24]進行,在β-CD小口端引入一個麥芽糖基。利用AUTODOCK4.2分子模擬軟件對槲皮素和Mal-β-CD進行分子對接,設定autogrid box參數為60 ?×60 ?×60 ?,格間距參數為0.375 ?;采用拉馬克遺傳算法進行計算,其他參數均默認設置,對接20 次。
2 結果與分析
2.1 槲皮素/Mal-β-CD相溶解度實驗分析
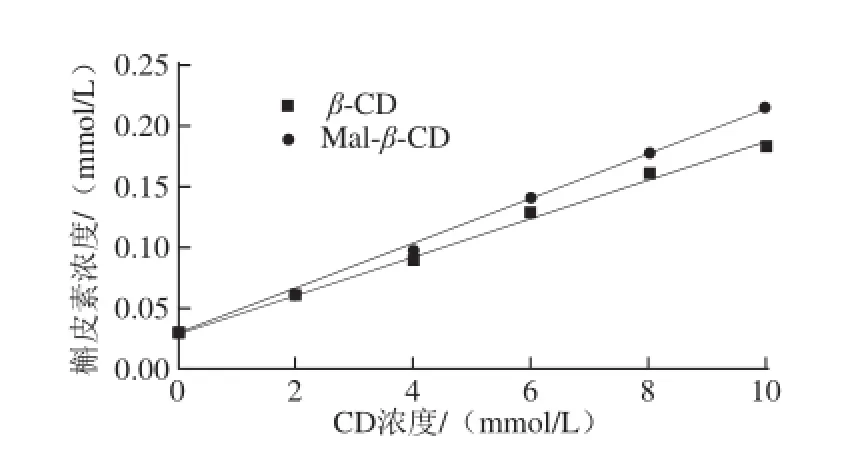
圖1 槲皮素與CD的相溶解度Fig. 1 Phase-solubility diagrams of inclusion complexes formed from quercetin and CDs
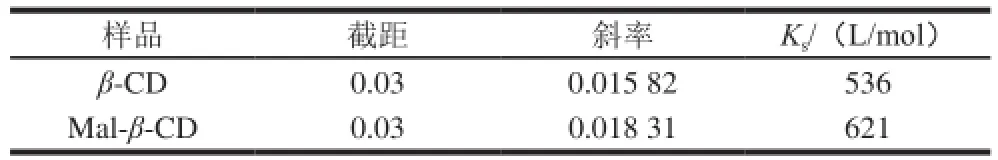
表1 槲皮素與CD間包合作用的表觀穩定常數Table 1 Apparent stability constants of the inclusion complex between quercetin and cyclodextrins
由圖1可知,槲皮素溶解度與CD濃度呈線性關系,同濃度的Mal-β-CD對槲皮素的溶解性要大于β-CD。根據Higuchi-Connors原理,槲皮素與CD的結合比為1∶1,Mal-β-CD與槲皮素的Ks(621 L/mol)高于β-CD與槲皮素的Ks(536 L/mol),表明Mal-β-CD包合槲皮素的能力高于母體β-CD,這一現象可能是由于Mal-β-CD在水溶液中的穩定性高于β-CD引起。由于Mal-β-CD對槲皮素的溶解性和穩定性均優于β-CD,其對槲皮素的包合能力較好,又具有較高的安全性,所以選擇Mal-β-CD與槲皮素進行包合。
2.2 槲皮素/Mal-β-CD紫外吸收光譜分析
由圖2可知,槲皮素在370 nm波長處有紫外特征吸收峰,Mal-β-CD沒有不飽和鍵,紫外吸收很弱,沒有特征峰,槲皮素與Mal-β-CD的物理混合物的紫外吸收光譜與槲皮素相同,而二者包合物的紫外吸收特征峰與槲皮素紫外吸收特征峰相比,發生了藍移,這可能是由于Mal-β-CD對槲皮素進入其空腔產生空間位阻使槲皮素分子結構的共軛效應減小導致的,由此表明槲皮素的共軛體系與Mal-β-CD之間發生了包合作用,兩種物質間并不是簡單的物理混合。

圖2 槲皮素(a)、Mal-β-CD(b)、Mal-β-CD與槲皮素的物理混合物(c)及包合物(d)的紫外光譜Fig. 2 Ultraviolet-visible spectroscopy quercetin(a), Mal-β-CD(b), and their mixture(c) and complex(d)
2.3 槲皮素/Mal-β-CD紅外光譜分析
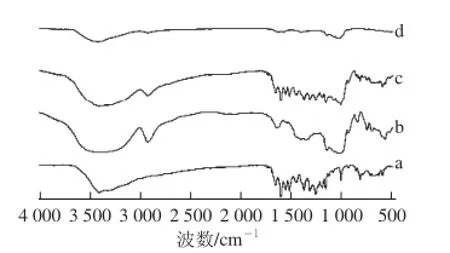
圖3 槲皮素(a)、Mal-β-CD(b)、Mal-β-CD與槲皮素的物理混合物(c)及包合物(d)的紅外光譜Fig. 3 Infrared spectroscopy of quercetin (a), Mal-β-CD(b), and their mixture (c) and complex (d)
由圖3可知,槲皮素具有羥基(3 409.25 cm-1)、羰基(1 662.49 cm-1)和C—H伸縮振動(1 262.74 cm-1)的特征吸收峰,Mal-β-CD具有羥基(3 409.37 cm-1)、亞甲基(2 928.04 cm-1)和糖苷鍵(1 026.77 cm-1)的特征吸收峰,槲皮素與Mal-β-CD的物理混合物的紅外光譜為二者紅外光譜的疊加,表明二者未發生相互作用,而槲皮素與Mal-β-CD的包合物在400~1 500 cm-1之間的紅外光譜發生明顯變化,其他掃描范圍內未出現新的吸收峰,由此表明槲皮素與Mal-β-CD在形成包合物的過程中并未產生新的共價鍵。
2.4 槲皮素/Mal-β-CD掃描電子顯微鏡分析
掃描電子顯微鏡是利用電子與物質之間相互作用來測定樣品的表面形態。槲皮素、Mal-β-CD、槲皮素與Mal-β-CD的物理混合物及包合物的表面形態如圖4所示。
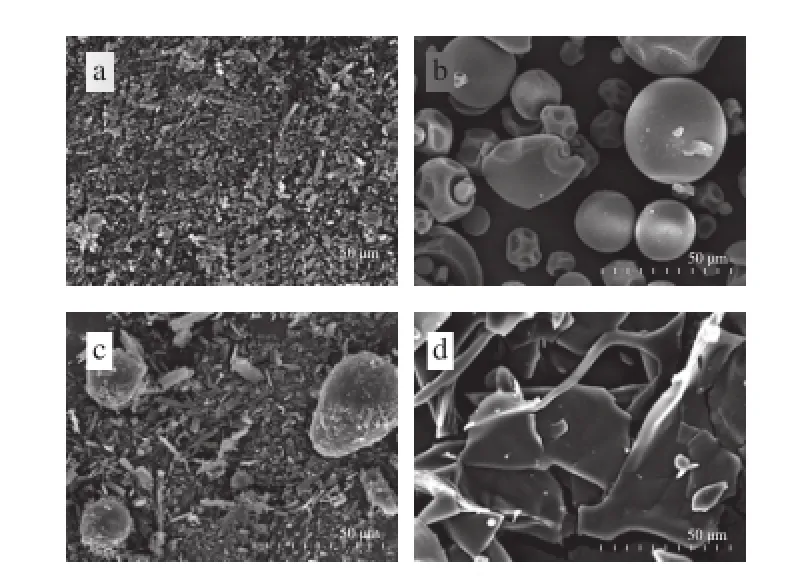
圖4 槲皮素(a)、Mal-β-CD(b)、Mal-β-CD與槲皮素的物理混合物(c)及包合物(d)的電子顯微鏡圖Fig. 4 Scanning electron micrographs of quercetin(a), Mal-β-CD(b), and their mixture(c) and complex(d)
由圖4可知,槲皮素的表面形態為針狀結晶,Mal-β-CD則呈現出多孔的球狀形態,在槲皮素與Mal-β-CD的物理混合物中,兩種形態均能被觀察到,而二者的包合物的表面形態則發生明顯變化,呈無定形狀態。
2.5 槲皮素/Mal-β-CD X射線衍射分析
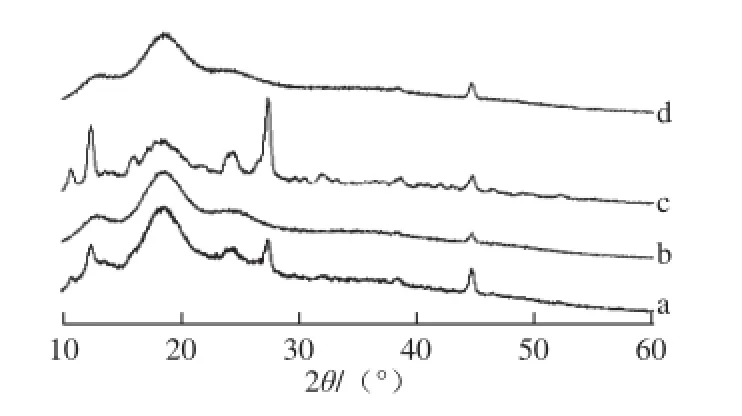
圖5 槲皮素(a)、Mal-β-CD(b)、Mal-β-CD與槲皮素的物理混合物(c)及包合物(d)的X射線衍射Fig. 5 X-ray diffractometry patterns of quercetin (a), Mal-β-CD (b), and their mixture (c) and complex (d)
由圖5可知,槲皮素的衍射峰較為尖銳,表明其形態為結晶狀,而Mal-β-CD在13°和18°附近具有兩個寬大的吸收峰,說明其結構中不含晶體結構,槲皮素與Mal-β-CD的物理混合物中,槲皮素的尖銳結晶衍射峰和Mal-β-CD的寬大衍射峰均有呈現,而二者的包合物中,槲皮素的尖銳結晶峰消失,其衍射圖譜與Mal-β-CD類似,這說明包合物中槲皮素的物相發生重大變化,已完全分散于Mal-β-CD中。
2.6 槲皮素/Mal-β-CD熱重及差示掃描量熱同步分析
熱重及差示掃描量熱同步分析方法可同時測定樣品在升溫過程中的質量變化和吸放熱[25]。槲皮素的熱重及差示掃描量熱分析結果如圖6a所示。由熱重曲線可知,槲皮素在100 ℃之前質量有少量損失,溫度繼續升高時,質量仍然下降,對應的差示掃描量熱曲線有兩個很大的吸熱峰,峰值溫度分別為107.21 ℃和314.81 ℃,而槲皮素的熔點在314 ℃左右,由此說明槲皮素在其熔融之前已部分分解,熔融之后再進一步降解。Mal-β-CD的熱重及差示掃描量熱分析結果如圖6b所示。由熱重曲線可知,Mal-β-CD在300 ℃之前基本上沒有質量損失,說明該吸熱峰是由于樣品水分揮發引起,在300~400 ℃之間質量損失嚴重,對應的差示掃描量熱曲線在300~400 ℃之間有一個明顯的吸熱峰,峰值溫度為314.02 ℃,由此可知該質量損失是由Mal-β-CD含碳分解物揮發引起,400 ℃之后樣品質量基本穩定,說明Mal-β-CD降解完成。槲皮素與Mal-β-CD的包合物的熱重及差示掃描量熱分析結果如圖6c所示,該包合物的熱重和差示掃描量熱曲線與Mal-β-CD的相同,槲皮素的差示掃描量熱曲線的特征吸熱峰消失,說明其不再以晶體形態存在,而是完全分散在Mal-β-CD中。在溫度升至300 ℃時,包合物的質量開始發生嚴重損失,說明通過Mal-β-CD包合,槲皮素的熱穩定性顯著提高。
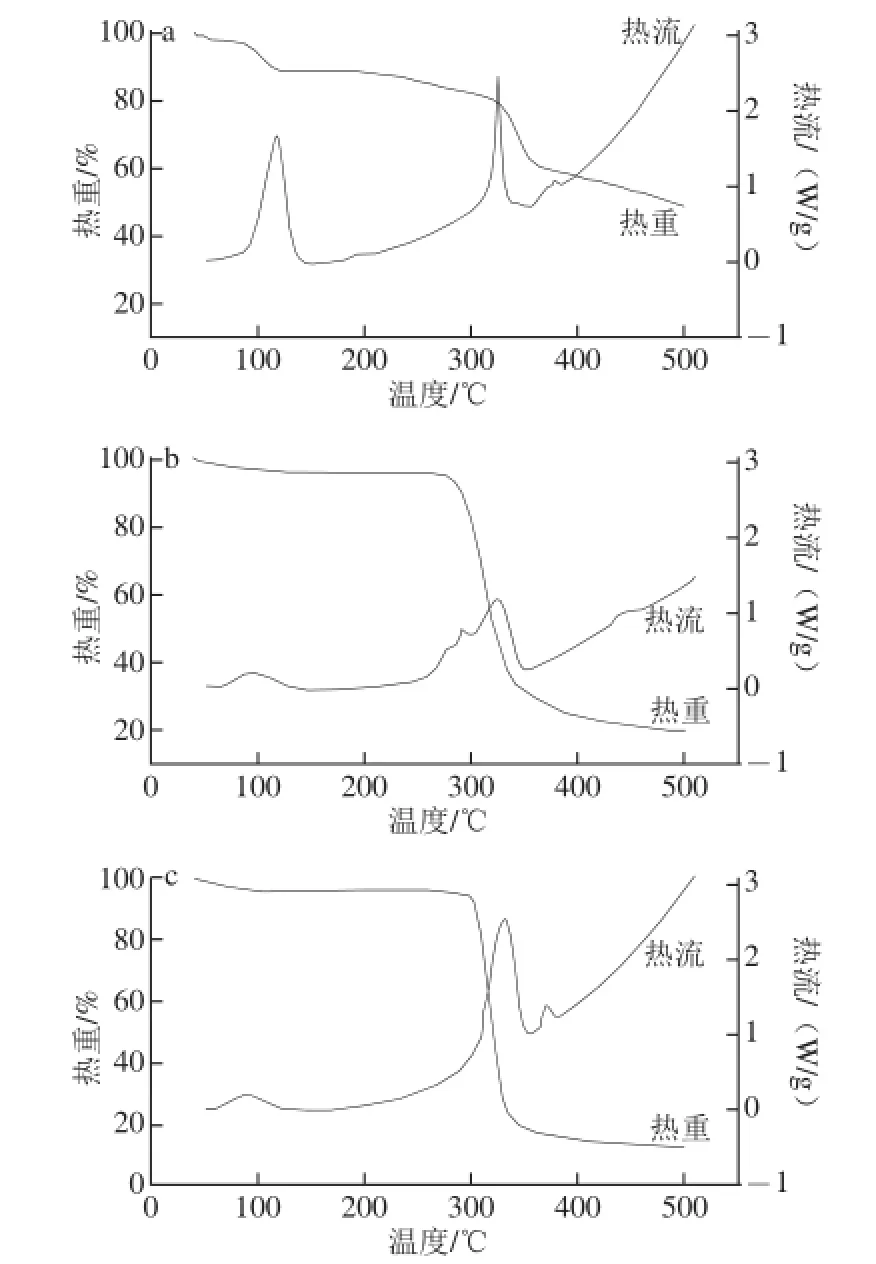
圖6 槲皮素(a)、Mal-β-CD(b)、Mal-β-CD與槲皮素包合物(c)的熱重及差示掃描量熱圖Fig. 6 Thermogravimetric/differential scanning calorimetry curves of quercetin (a), Mal-β-CD (b) and their complex (c)
2.7 分子對接分析
本研究中,Mal-β-CD和槲皮素分別作為受體和配體,二者包合物的三維超分子結構利用分子模擬對接的方法獲得(圖7)。結果表明:槲皮素沿Mal-β-CD的大口端方向進入其疏水性空腔,其C環在空腔內,A環位于大口端處,B環位于小口端處,二者之間以分子間氫鍵來維持該超分子結構。
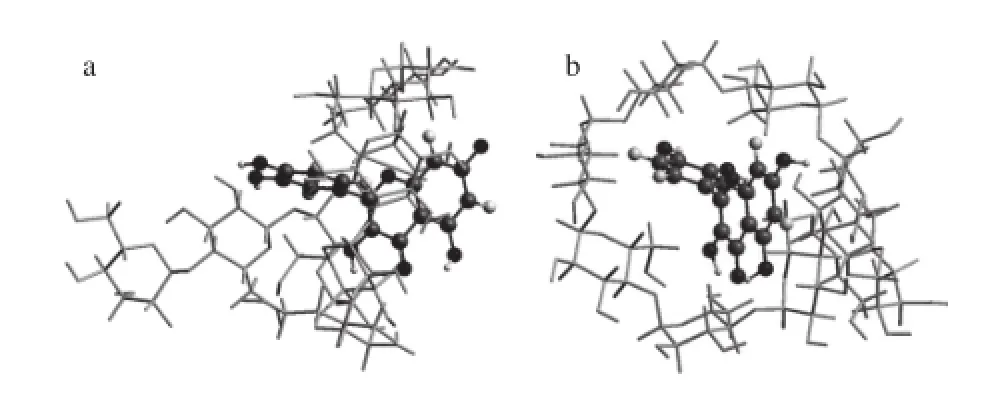
圖7 槲皮素/Mal-β-CD復合物的三維超分子結構Fig. 7 Three-dimensional supermolecular structure of quercetin/Mal-β-CD complex
3 結 論
研究結果表明Mal-β-CD對槲皮素的溶解性及穩定性均優于β-CD,對槲皮素具有較好的包合能力。通過溶劑法制得的槲皮素與Mal-β-CD的包合物不是簡單的物理混合,而是槲皮素的共軛體系與Mal-β-CD之間發生了包合作用形成的,二者之間是以氫鍵來維持分子結構的。槲皮素與Mal-β-CD在形成包合物的過程中并未產生新的共價鍵,但包合物的表面形態及物相均發生了明顯變化。經過包合,槲皮素的熱穩定性也得到顯著提高。
[1] HARISH S, VIKASH K, AMIT K S, et al. Isocitrate lyase of Mycobacterium tuberculosis is inhibited by quercetin through binding at N-terminus[J]. International Jounal of Biological Macromolecules, 2015, 78: 137-141. DOI:10.1016/j.ijbiomac.2015.04.005.
[2] GWI N C, JI H K, JI H K, et al. Effect of quercetin on learning and memory performance in ICR mice under neurotoxic trimethyltin exposure[J]. Food Chemistry, 2012, 132(2): 1019-1024. DOI:10.1016/ j.foodchem.2011.11.089.
[3] ESTHER P, áNGEL M, HAYLEY E, et al. Production of watersoluble quercetin formulations by antisolvent precipitation and supercritical drying[J]. The Journal of Supercritical Fluids, 2015, 104: 281-290. DOI:10.1016/j.supflu.2015.07.006.
[4] MOHAMED L T, SAMEHA M, BRUNO B, et al. Quercetin alleviates predator stress-induced anxiety-like and brain oxidative signs in pregnant rats and immune count disturbance in their offspring[J]. Pharmacology, Biochemistry and Behavior, 2013, 107(6): 1-10. DOI:10.1016/j.pbb.2013.03.009.
[5] BALABOLKIN I I, GORDEEVA G F, FUSEVA E D, et al. Use of vitamins in allergic illnesses in children (in Russian)[J]. Voprosy Meditsinskoi Khimii, 1992, 38(5): 36-40.
[6] COSKUN O, KANTER M, KORKMAZ A, et al. Quercetin, a flavonoid antioxidant, prevents and protects streptozotocin-induced oxidative stress and β-cell damage in rat pancreas[J]. Pharmacological Research, 2005, 51(2): 117-123. DOI:10.1016/j.phrs.2004.06.002.
[7] ZHANG X, XU Q, SAIKI I. Quercetin inhibits the invasion and mobility of murine melanoma B16-BL6 cells through inducing apoptosis via decreasing Bcl-2 expression[J]. Clinical & Experimental Metastasis, 2000, 18(5): 415-421. DOI:10.1023/A:1010960615370.
[8] SANYOG J, AMIT K J, MILIND P, et al. Novel self-emulsifying formulation of quercetin for improved in vivo antioxidant potential: implications for drug-induced cardiotoxicity and nephrotoxicity[J]. Free Radical Biology and Medicine, 2013, 65: 117-130. DOI:10.1016/ j.freeradbiomed.2013.05.041.
[9] JAFAR E N D, AHAD M, SEYED M G, et al. Synthesis, characterization and antioxidant property of quercetin-Tb(III) complex[J]. Advanced Pharmaceutical Bulletin, 2014, 4(2): 101-104. DOI:10.5681/apb.2014.016.
[10] YASUSHI N, HIROYUKI T. Quantitative analysis of quercetin using Raman spectroscopy[J]. Food Chemistry, 2011, 126(2): 751-755. DOI:10.1016/j.foodchem.2010.11.059.
[11] LU J, ZHENG Y L, LUO L, et al. Quercetin reverses D-galactose induced neurotoxicity in mouse brain[J]. Behavioural Brain Research, 2006, 171(2): 251-260. DOI:10.1016/j.bbr.2006.03.043.
[12] 邵偉, 王金山, 王春香, 等. 槲皮素-β-環糊精包合物的研究[J].高等學校化學學報, 1998, 19(7): 1101-1103. DOI:10.3321/ j.issn:0251-0790.1998.07.039.
[13] SURAYA J, OYAIS A C, GHULAM M R, et al. Investigation of antioxidant activity of quercetin (2-(3,4-dihydroxyphenyl)-3,5,7-trihydroxy-4H-chromen-4-one) in aqueous micellar media[J]. Food Research International, 2013, 51(1): 294-302. DOI:10.1016/ j.foodres.2012.12.022.
[14] 翟廣玉, 馬巖, 閆臻, 等. 槲皮素包合物的研究進展[J]. 化學與黏合, 2010, 32(4): 52-57. DOI:10.3969/j.issn.1001-0017.2010.04.015.
[15] PRALHAD T, RAJENDRAKUMAR K. Study of freeze-dried quercetin-cyclodextrin binary systems by DSC, FT-IR, X-ray diffraction and SEM analysis[J]. Journal of Pharmaceutical and Biomedical Analysis, 2004, 34(2): 333-339. DOI:10.1016/S0731-7085(03)00529-6.
[16] LIU W, GUO R. Interaction between flavonoid, quercetin and surfactant aggregates with different charges[J]. Journal of Colloid and Interface Science, 2006, 302(2): 625-632. DOI:10.1016/ j.jcis.2006.06.045.
[17] LANDI-LIBRANDI A P, CHRYSOSTOMO T N, MARZOCCHIMA CHADO C M, et al. Study of quercetin-loaded liposomes as potential drug carries: in vitro evaluation of human complement activation[J]. Journal of Liposome Research, 2012, 22(2): 89-99. DOI:10.3109/0898 2104.2011.615321.
[18] LORENZ R T, CYSEWSKI G R. Commercial potential for Haematococcus microalgae as a natural source of astaxanthin[J]. Trends in Biotechnology, 2000, 18(4): 160-166. DOI:10.1016/S0167-7799(00)01433-5.
[19] ARUMUGAM S P, JEYACHANDRAN S, BASKARALINGAM V, et al. Improvement on dissolution rate of inclusion complex of Rifabutin drug with β-cyclodextrin[J]. International Journal of Biological Macromolecules, 2013, 62: 472-480. DOI:10.1016/ j.ijbiomac.2013.09.006.
[20] PARAMASIVAGANESH K, SRINIVASAN K, MANIVEL A, at al. Studies on inclusion complexation between 4,4’-dihydroxybiphenyl and β-cyclodextrin by experimental and theoretical approach[J]. Journal of Molecular Structure, 2013, 1048: 399-409. DOI:10.1016/ j.molstruc.2013.04.072.
[21] BELLRINGER M E, SMITH T G, READ R, et al. β-Cyclodextrin: 52-week toxicity studies in the rat and dog[J]. Food and Chemical Toxicology, 1995, 33(5): 367-376. DOI:10.1016/0278-6915(94)00149-I.
[22] 崔波. 麥芽糖基-β-環糊精的酶法合成及其性質和應用研究[D]. 無錫: 江南大學, 2011: 7.
[23] LIU B, LI W, ZHAO J, et al. Physicochemical characterisation of the supramolecular structure of luteolin/cyclodextrin inclusion complex[J]. Food Chemistry, 2013, 141(2): 900-906. DOI:10.1016/ j.foodchem.2013.03.097.
[24] EID E E M, ABDUL A B, SULIMAN F E O, et al. Characterization of the inclusion complex of zerumbone with hydroxypropylβ-cyclodextrin[J]. Food Chemistry, 2011, 83(4): 1707-1714. DOI:10.1016/j.carbpol.2010.10.033.
[25] 劉本國, 張瑞婷, 吳曉楠, 等. 橙皮苷/羥丙基-β-環糊精包合物的理化性質研究[J]. 現代食品科技, 2013, 29(10): 2349-2352. DOI:10.13982/j.Mfst. 1673-9078. 2013.10.023.
Physicochemical Properties of Inclusion Complex of Quercetin with 6-O-α-D-Maltosyl-β-Cyclodextrin
LI Yun1, WANG Fang2, ZOU Wei1, WANG Xuesong1, CAI Hongyan1, CHEN Xuan1, SUN Wei1, SHEN Wangyang1,3,*
(1. College of Food Science and Engineering, Wuhan Polytechnic University, Wuhan 430023, China; 2. Wuhan Kaidi General Research Institute Engineering&Technology Co. Ltd., Wuhan 430023, China; 3. Key Laboratory of the Deep Processing of Bulk Grain and Oil Authorized, Ministry of Education, Wuhan 430023, China)
In this study, the inclusion efficiency of 6-O-α-D-maltosyl-β-cyclodextrin (Mal-β-CD) and β-cyclodextrin (β-CD) for quercetin was studied by the phase solubility method, and the inclusion complex of quercetin with Mal-β-CD was prepared by the solvent method. The physicochemical properties of the inclusion complex were studied by ultravioletvisible spectroscopy, infrared spectroscopy, scanning electron microscope, X-ray diffractometry, and thermogravimetric/ differential scanning calorimetry. The molecular docking method was also applied to study the three-dimensional supermolecular structure of the complex. The results showed that the inclusion efficiency of Mal-β-CD was superior to β-CD. The results of molecular docking showed that quercetin could enter the hydrophobic cavity from the wide rim of G2-β-CD to form a super-molecular structure. Quercetin and Mal-β-CD were connected by hydrogen bonds. Compared with β-CD, Mal-β-CD exhibited higher inclusion efficiency, resulting in significantly changed physicochemical properties and improved stability of quercetin.
quercetin; 6-O-α-D-maltosyl-β-cyclodextrin; inclusion complex; physicochemical property; molecular docking
10.7506/spkx1002-6630-201621007
TS201.2
A
1002-6630(2016)21-0038-05
李赟, 汪芳, 鄒偉, 等. 槲皮素與6-O-α-D-麥芽糖-β-環糊精包合物的理化表征[J]. 食品科學, 2016, 37(21): 38-42.
DOI:10.7506/spkx1002-6630-201621007. http://www.spkx.net.cn
LI Yun, WANG Fang, ZOU Wei, et al. Physicochemical properties of inclusion complex of quercetin with 6-O-α-D-maltosylβ-cyclodextrin[J]. Food Science, 2016, 37(21): 38-42. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201621007. http://www.spkx.net.cn
2016-03-02
國家自然科學基金青年科學基金項目(31301415)
李赟(1990—),女,碩士研究生,研究方向為食品生物化學。E-mail:shuang7061234@163.com
*通信作者:沈汪洋(1978—),男,副教授,博士,研究方向為食品生物化學。E-mail:whwangyangshen@126.com

