氧化苦參堿干預(yù)TGF-β1誘導(dǎo)A549細(xì)胞上皮-間質(zhì)轉(zhuǎn)化作用研究*
沈陽軍區(qū)總醫(yī)院呼吸科(沈陽110016) 劉 蕾 馬 壯 謝 華 孫文武
?
·論著·基礎(chǔ)研究·
氧化苦參堿干預(yù)TGF-β1誘導(dǎo)A549細(xì)胞上皮-間質(zhì)轉(zhuǎn)化作用研究*
沈陽軍區(qū)總醫(yī)院呼吸科(沈陽110016) 劉 蕾 馬 壯 謝 華 孫文武
目的:探討氧化苦參堿(Oxy)對轉(zhuǎn)化生長因子β1(TGF-β1)誘導(dǎo)肺泡上皮細(xì)胞間質(zhì)轉(zhuǎn)化的干預(yù)作用,期望為肺纖維化治療提供新的候選藥物。方法:選用0.25、0.5、1 mg/ml氧化苦參堿預(yù)處理A549細(xì)胞30 min后,再給與(5 ng/ml)TGF-β1共孵育培養(yǎng)48 h,MTT法檢測細(xì)胞增殖變化,光鏡下觀察細(xì)胞形態(tài)變化,Western blot檢測TGF-β1下游信號分子Smad2/3磷酸化變化和EMT標(biāo)志分子E-candherin、N-cadherin和Vimentin表達(dá)變化。結(jié)果:氧化苦參堿能有效干預(yù)TGF-β1誘導(dǎo)A549細(xì)胞細(xì)胞增殖、細(xì)胞形態(tài)變化,抑制TGF-β1介導(dǎo)的Smad2/3磷酸化和E-candherin表達(dá)下調(diào)、N-cadherin和Vimentin表達(dá)上升。結(jié)論:氧化苦參堿能有效抑制TGF-β1誘導(dǎo)A549細(xì)胞上皮-間質(zhì)轉(zhuǎn)化,氧化苦參堿可以作為抗肺纖維化治療的候選藥物。
肺纖維化(Pulmonary fibrosis,PF)是各種不同病因所致肺部疾病的共同結(jié)局,包括特發(fā)性肺纖維化(Idiopathic pulmonary fibrosis,IPF)、結(jié)節(jié)病、塵肺、過敏性肺炎、藥物和放射線導(dǎo)致肺纖維化以及與膠原血管病有關(guān)的致肺纖維化肺泡炎等。肺纖維化的致死率高,5年生存率僅次于肺癌,且其發(fā)病率正呈逐年上升趨勢[1]。肺纖維化的發(fā)病機制復(fù)雜,目前研究認(rèn)為上皮細(xì)胞受損后發(fā)生上皮-間質(zhì)轉(zhuǎn)化(Epithelial-mesenchymal transition,EMT)轉(zhuǎn)變?yōu)槌衫w維細(xì)胞,同時成纖維細(xì)胞發(fā)生異常增殖是肺纖維化形成的兩個主要環(huán)節(jié)[2]。轉(zhuǎn)化生長因子β1(Transforming growth factor,TGF-β1)是一種重要的致纖維化生長因子,能夠通過其下游TGF-β受體以及Smads蛋白刺激成纖維細(xì)胞增殖和膠原的合成,促進(jìn)膠原蛋白、纖維連接蛋白、透明質(zhì)酸、蛋白聚糖等在細(xì)胞外基質(zhì)中沉淀,減少細(xì)胞外基質(zhì)的降解,在很多器官纖維化疾病中都被認(rèn)為是纖維化的“總開關(guān)”[3]。研究報道指出,TGF-β1介導(dǎo)的肺泡上皮細(xì)胞EMT是介導(dǎo)肺纖維化的主要機制之一[4]。氧化苦參堿(Oxymatnine, Oxy),又稱苦參堿,是從豆科植物苦參(Sophora flavescens ait)或萍科植物廣豆根(Sophora subprostrata)中分離出來的生物堿。研究表明其能夠直接抑制乙型肝炎的復(fù)制,并能夠阻斷肝細(xì)胞的凋亡同時抑制肝纖維化的發(fā)生[5]。本研究中,我們體外培養(yǎng)人肺泡II型上皮細(xì)胞A549,TGF-β1誘導(dǎo)其發(fā)生EMT,使用氧化苦參堿干預(yù)處理,觀察對細(xì)胞增殖、細(xì)胞形態(tài)、細(xì)胞EMT發(fā)生的影響,期望為肺纖維化治療提供新的候選藥物,有效提高肺纖維化患者的治療效果和生存率。
材料和方法
1 實驗材料 人肺泡II型上皮細(xì)胞A549購自北京協(xié)和醫(yī)學(xué)研究所細(xì)胞庫;TGF-β1重組蛋白購自 Sigma公司(純度分別 >99%);氧化苦參堿購自Baomanbio公司(純度分別>99%);兔抗人Smad2/3、p-Smad2/3、E-candherin、N-cadherin、Vimentin和β-actin 多克隆抗體和HRP 標(biāo)記羊抗兔 IgG 購自沈陽萬類科技有限公司;ECL 化學(xué)發(fā)光試劑盒為 Pierce 公司產(chǎn)品;DMEM培養(yǎng)培養(yǎng)基為 Gibco 公司產(chǎn)品,細(xì)胞培養(yǎng)所用胎牛血清購自Hyclone公司;其他生化試劑為國產(chǎn)分析純。
2 實驗方法
2.1 細(xì)胞培養(yǎng): 人肺泡A549細(xì)胞培養(yǎng)于含10%胎牛血清的DMEM培養(yǎng)液中,置于飽和濕度,5%CO2的細(xì)胞培養(yǎng)箱中培養(yǎng),隔天換液,每天用倒置顯微鏡觀察細(xì)胞形態(tài)以及細(xì)胞生長情況,待細(xì)胞長至80%融合時進(jìn)行消化傳代。
2.2 實驗分組: 對數(shù)生長期A549細(xì)胞隨機分為5組:A:對照組(Control);B:TGF-β1處理組(TGF-β1);C:TGF-β1+氧化苦參堿低劑量組(TGF-β1+L-Oxy);D:TGF-β1+氧化苦參堿中劑量組(TGF-β1+M-Oxy);E:TGF-β1+氧化苦參堿高劑量組(TGF-β1+H-Oxy)。氧化苦參堿預(yù)處理30 min后,再給與(5 ng/ml)TGF-β1共孵育培養(yǎng)48 h,氧化苦參堿參考劑量分別為0.25、0.5、1 mg/ml。
2.3 MTT法檢測氧化苦參堿干預(yù)對TGF-β1誘導(dǎo)A549細(xì)胞增殖的影響: 選擇對數(shù)生長期的A549細(xì)胞,胰酶消化后制成單細(xì)胞懸液,按2000/孔的密度接種于96孔板,待細(xì)胞貼壁后換液為無血清培養(yǎng)液繼續(xù)培養(yǎng)24 h,分別加入濃度為0、0.25、0.5、1 mg/ml氧化苦參堿預(yù)處理30 min后,再給與(5 ng/ml)TGF-β1共孵育48 h,每組設(shè)置5個復(fù)孔,置于細(xì)胞培養(yǎng)箱中培養(yǎng),48 h后分別加入5 g/L的MTT 20 μl,繼續(xù)孵育4 h,棄去上清,加入DMSO 150 μl,充分震蕩20 min,于酶標(biāo)儀上測定其在490 nm處的吸光度值。
2.4 Western blot檢測各組細(xì)胞TGF-β信號通路以及EMT相關(guān)指標(biāo)的表達(dá): 收集各組細(xì)胞后加入蛋白裂解液及PMSF,冰上放置40 min,4℃ 12000 rpm/min離心40 min,取上清,BCA法定量蛋白。取20 μg蛋白樣品,于10%聚丙烯酰胺凝膠上行SDS-PAGE,電泳結(jié)束后100 V電轉(zhuǎn)印至PVDF膜上。將PVDF膜放入封閉液中37℃封閉1 h,稀釋一抗4℃孵育過夜。PBS洗膜4次,加入堿性磷酸酶標(biāo)記的稀釋二抗孵育,37℃震搖1 h,洗膜。ECL發(fā)光法曝光成像,掃描入電腦并進(jìn)行灰度分析。
3 統(tǒng)計學(xué)方法 采用SPSS17.0統(tǒng)計學(xué)軟件。各組實驗測試指標(biāo)經(jīng)Shapiro-Wilk檢驗呈正態(tài)分布,以平均值±標(biāo)準(zhǔn)差表示,經(jīng)F檢驗證實方差齊。采用單因素方差分析,組間的兩兩比較均采用LSD-t檢驗,P<0.05為差異有統(tǒng)計學(xué)意義。
結(jié) 果
1 氧化苦參堿干預(yù)TGF-β1誘導(dǎo)A549細(xì)胞增殖 MTT法檢測細(xì)胞增殖,測量OD490值代表細(xì)胞數(shù)的多少,體現(xiàn)細(xì)胞增殖能力的變化。按照實驗分組干預(yù)處理48h得到氧化苦參堿(Oxy)干預(yù)后,TGF-β1誘導(dǎo)A549細(xì)胞增殖能力逐漸減弱,低中高Oxy干預(yù)組與TGF-β1處理組相比,差異均具有統(tǒng)計學(xué)意義(P<0.01);與正常對照組相比無統(tǒng)計學(xué)差異(P>0.05)。表明Oxy能有效抑制TGF-β1誘導(dǎo)的A549細(xì)胞增殖,見表1。
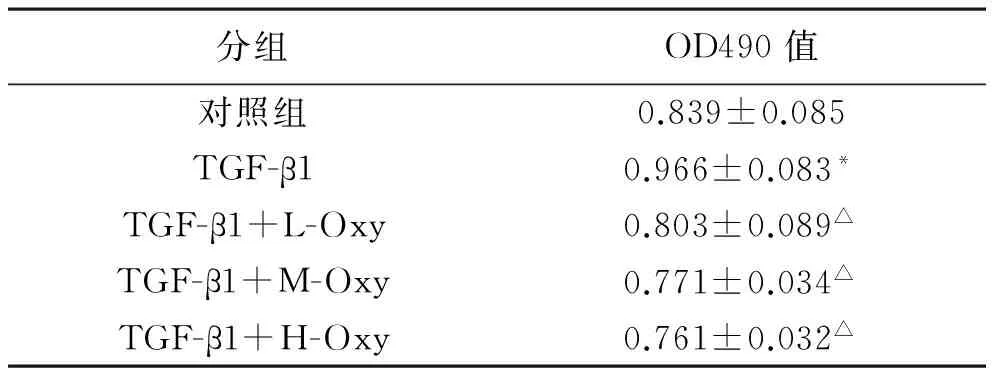
表1 氧化苦參堿干預(yù)TGF-β1誘導(dǎo)A549細(xì)胞增殖的影響
2 氧化苦參堿干預(yù)TGF-β1誘導(dǎo)A549細(xì)胞形態(tài)變化 熒光顯微鏡下觀察細(xì)胞形態(tài)學(xué)變化,得到與對照組細(xì)胞相比,TGF-β1處理細(xì)胞與鄰近細(xì)胞分離,細(xì)胞形態(tài)從鵝卵石狀轉(zhuǎn)變?yōu)殚L梭形,由上皮性細(xì)胞轉(zhuǎn)化為間充質(zhì)細(xì)胞狀。低中高濃度Oxy干預(yù)后,細(xì)胞形態(tài)變化有所緩解,其中高濃度Oxy干預(yù)效果最佳,細(xì)胞形態(tài)與對照組相比未有明顯改變(圖1)。表明Oxy能有效抑制TGF-β1誘導(dǎo)的A549細(xì)胞間充質(zhì)狀轉(zhuǎn)化。
3 氧化苦參堿干預(yù)TGF-β1誘導(dǎo)A549細(xì)胞上皮-間質(zhì)轉(zhuǎn)化 TGF-β1活化Smad2/3信號調(diào)控上皮細(xì)胞EMT發(fā)生。Western blot 法檢測Smad2/3、p-Smad2/3表達(dá)得到,TGF-β1處理后 p-Smad2/3表達(dá)上調(diào),使用Oxy干預(yù)后,能有效抑制p-Smad2/3,高濃度Oxy作用后p-Smad2/3表達(dá)下調(diào)最明顯(圖2A)。表明Oxy能有效干預(yù)TGF-β1/Smad2/3信號活化。同時檢測EMT標(biāo)記分子的表達(dá)變化,得到TGF-β1處理后,A549細(xì)胞上皮標(biāo)記分子E-candherin表達(dá)降低,間質(zhì)標(biāo)記分子N-cadherin和Vimentin的表達(dá)上調(diào),Oxy干預(yù)能有效恢復(fù)E-candherin表達(dá),降低N-cadherin和Vimentin的表達(dá),高濃素Oxy作用效果更明顯(圖2B)。表明氧化苦參堿能有效抑制TGF-β1誘導(dǎo)的A549細(xì)胞上皮-間質(zhì)轉(zhuǎn)化,其可能的機制為干預(yù)TGF-β1/Smad2/3信號活化。
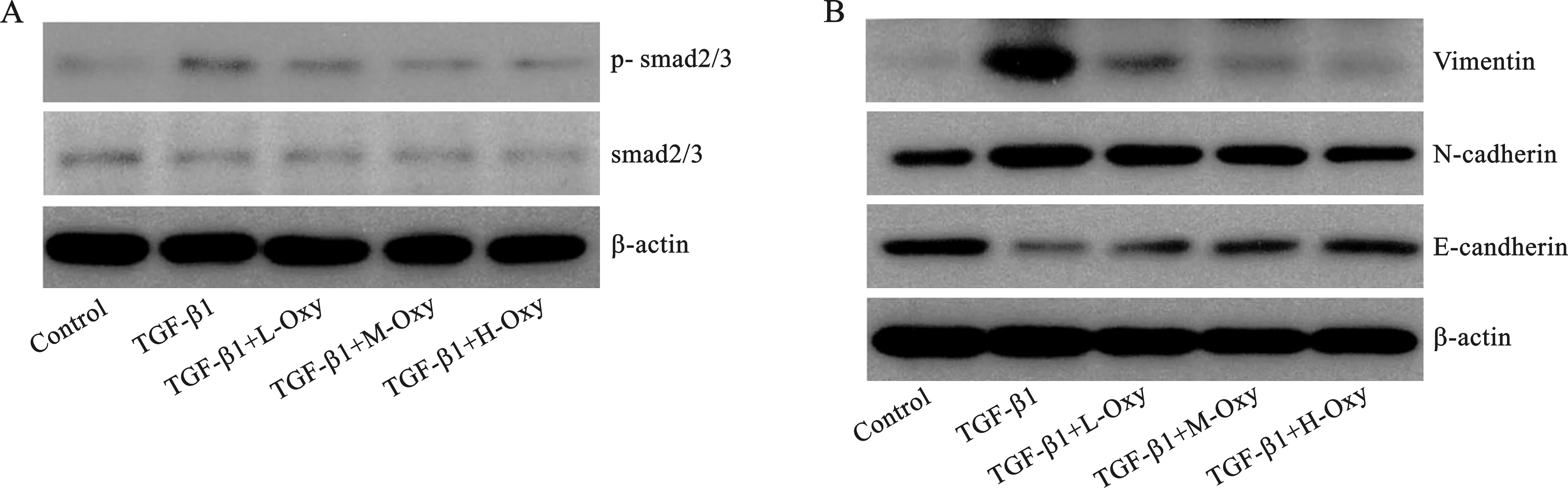
圖2 氧化苦參堿干預(yù)TGF-β1誘導(dǎo)A549細(xì)胞上皮-間質(zhì)轉(zhuǎn)化[A:Western blot 法檢測TGF-β1下游信號Smad2/3的活化(p- Smad2/3的表達(dá));B:Western blot 法檢測細(xì)胞上皮-間質(zhì)轉(zhuǎn)化的標(biāo)志分子E-candherin、N-cadherin和Vimentin的表達(dá)]
討 論
EMT在肺纖維化發(fā)生中發(fā)揮重要作用,抑制EMT發(fā)生有助于緩解肺纖維化[6]。本研究通過使用TGF-β1體外處理肺泡Ⅱ型上皮細(xì)胞A549,誘導(dǎo)細(xì)胞EMT發(fā)生;通過氧化苦參堿干預(yù),得到氧化苦參堿能夠有效抑制TGF-β1誘導(dǎo)的細(xì)胞增殖、細(xì)胞形態(tài)的改變;并檢測得到氧化苦參堿能夠有效抑制TGF-β1下游信號分子Smad2/3的磷酸化,抑制間質(zhì)細(xì)胞標(biāo)志分子N-cadherin和Vimentin的表達(dá),恢復(fù)E-candherin的表達(dá)。這些提示氧化苦參堿可能通過干預(yù)TGF-β1介導(dǎo)的Smad2/3的活化,抑制A549細(xì)胞EMT;氧化苦參堿可以作為抗肺纖維治療獲選藥物。
研究顯示,在多種肺疾病中,例如哮喘、慢性阻塞性肺病、先天性肺纖維化、博來霉素誘導(dǎo)的肺纖維化等病理損害誘導(dǎo)肺泡Ⅱ型上皮細(xì)胞向肌成纖維母細(xì)胞分化通過上皮-間質(zhì)轉(zhuǎn)化,喪失正常表皮完整性,細(xì)胞粘附分子E-candherin和ZO-1表達(dá)丟失;增加間質(zhì)表型分子的表達(dá)如N-cadherin和Vimentin,增強細(xì)胞外基質(zhì)產(chǎn)生能力,介導(dǎo)肺纖維化的發(fā)生[7]。在PF早期階段肺泡巨噬細(xì)胞數(shù)量和活性增多,合成釋放大量具有多種活性的細(xì)胞因子、前炎性介質(zhì)、趨化因子及蛋白酶類;TGF-β1是關(guān)鍵的纖維相關(guān)因子,其能有效誘導(dǎo)上皮性細(xì)胞發(fā)生EMT轉(zhuǎn)化,增殖分化為肌成纖維細(xì)胞母細(xì)胞,誘導(dǎo)肺纖維組織的細(xì)胞外基質(zhì)大量產(chǎn)生,當(dāng)肺泡Ⅱ型上皮細(xì)胞慢性接觸TGF-β1后細(xì)胞將經(jīng)歷EMT[8]。研究發(fā)現(xiàn)TGF-β1在百草枯處理的大鼠血清和肺組織增加,TGF-β1 mRNA表達(dá)水平逐漸增加在第7天達(dá)到一個峰值,且TGF-β1增加在羥基脯氨酸和膠原蛋白增加之前,干預(yù)TGF-β1/Smads信號活化后將有效抑制肺纖維化,上皮間質(zhì)轉(zhuǎn)化的發(fā)生[11]。本研究中,體外培養(yǎng)肺泡Ⅱ型上皮細(xì)胞A549,使用TGF-β1處理,觀測得到TGF-β1處理能有效促進(jìn)細(xì)胞增殖、細(xì)胞形態(tài)發(fā)生變化,細(xì)胞間粘附減少,細(xì)胞呈長梭形,表現(xiàn)間質(zhì)樣表型;同時檢測細(xì)胞EMT標(biāo)記分子得到E-candherin表達(dá)降低、N-cadherin和Vimentin表達(dá)增加。表明已成功建立TGF-β1誘導(dǎo)肺泡Ⅱ型上皮細(xì)胞的EMT轉(zhuǎn)化。
氧化苦參堿具有廣泛的抗腫瘤、抗心律失常、抗炎以及抗病毒等多種藥理作用,苦參堿及其制劑的開發(fā)與應(yīng)用已成為近年來藥學(xué)領(lǐng)域的熱門課題之一[10]。馬鵬等[11]報道,氧化苦參堿能夠改善晚期肝癌患者肝功能,降低AFP、CEA和CA125,延長患者生存時間。張靜等[12]報道,氧化苦參堿可使慢性中度乙肝患者肝功能復(fù)常,膠原纖維下降及凝血酶原活動度恢復(fù)得到明顯改善。已有的研究提示氧化苦參堿能夠通過抑制TGF-β1誘導(dǎo)的Smad3的磷酸化和核轉(zhuǎn)移有效抑制瘢痕纖維母細(xì)胞膠原蛋白的表達(dá)[13],通過抑制NF-κB通路減少炎性細(xì)胞因子生成,進(jìn)而抑制腎纖維化[14]。我們的前期研究證實氧化苦參堿能夠通過有效緩解小鼠肺纖維化,抑制炎癥反應(yīng)和氧化應(yīng)激損傷,下調(diào)炎癥因子TNF-α和IL-6的表達(dá),降低MPO活性和MDA水平,并能有效抑制TGF-β1的表達(dá)及其下游信號分子Smad2/3的活化[15]。本研究中,通過使用高、中、低三個濃度的氧化苦參堿干預(yù)TGF-β1誘導(dǎo)的肺泡Ⅱ型上皮細(xì)胞的EMT轉(zhuǎn)化,得到氧化苦參堿能有效抑制TGF-β1誘導(dǎo)的增殖、細(xì)胞形態(tài)的間質(zhì)變化,恢復(fù)E-candherin的表達(dá),降低N-cadherin和Vimentin表達(dá),且可能的機制亦與干預(yù)Smad2/3的活化有關(guān)。表明氧化苦參堿能有效干預(yù)TGF-β1誘導(dǎo)的肺泡Ⅱ型上皮細(xì)胞上皮機制轉(zhuǎn)化,可能成為有效的抗肺纖維化藥物。
[1] 曾慶富, 牛海艷. 肺纖維化機制的研究進(jìn)展[J]. 中華病理學(xué)雜志, 2001, 30(5): 371-373.
[2] 梁冠男, 胡永斌, 周建華. 肺纖維化中上皮-間質(zhì)轉(zhuǎn)型信號轉(zhuǎn)導(dǎo)機制研究進(jìn)展[J]. 國際病理科學(xué)與臨床雜志, 2008, 28(6): 9-503.
[3] Kang HR, Cho SJ, Lee CG,etal. Transforming growth factor (TGF)-beta1 stimulates pulmonary fibrosis and inflammation via a Bax-dependent, bid-activated pathway that involves matrix metalloproteinase-12[J]. The Journal of Biological Chemistry,2007, 282(10):7723-32.
[4] Xie L, Zhou D, Xiong J,etal. Paraquat induce pulmonary epithelial-mesenchymal transition through transforming growth factor-beta1-dependent mechanism[J]. Experimental and Toxicologic Pathology : Official Journal of the Gesellschaft fur Toxikologische Pathologie, 2016, 68(1):69-76.
[5] Ling JY, Zhang GY, Cui ZJ,etal. Supercritical fluid extraction of quinolizidine alkaloids from Sophora flavescens Ait. and purification by high-speed counter-current chromatography[J]. Journal of Chromatography A,2007, 1145(1-2):123-7.
[6] Wang J, Zhu Y, Tan J,etal. Lysyl oxidase promotes epithelial-to-mesenchymal transition during paraquat-induced pulmonary fibrosis[J]. Molecular Bio Systems, 2016, 12(2):499-507.
[7] Milara J, Peiro T, Serrano A,etal. Epithelial to mesenchymal transition is increased in patients with COPD and induced by cigarette smoke[J]. Thorax, 2013, 68(5):410-20.
[8] Chen T, Nie H, Gao X,etal. Epithelial-mesenchymal transition involved in pulmonary fibrosis induced by multi-walled carbon nanotubes via TGF-beta/Smad signaling pathway[J]. Toxicology Letters, 2014, 226(2):150-62.
[9] Han YY, Shen P, Chang WX. Involvement of epithelial-to-mesenchymal transition and associated transforming growth factor-beta/Smad signaling in paraquat-induced pulmonary fibrosis[J]. Molecular Medicine Reports, 2015, 12(6):7979-84.
[10] Zhang Y, Piao B, Hua B,etal. Oxymatrine diminishes the side population and inhibits the expression of beta-catenin in MCF-7 breast cancer cells[J]. Med Oncol, 2011, 28 Suppl 1:S99-107.
[11] 馬 鵬,孟存英,劉鵬飛,等.氧化苦參堿對晚期肝癌患者AFP、CEA和CA125影響研究[J].陜西中醫(yī),2015,36(11):1445-1448.
[12] 陳 晨,金 玉.氧化苦參堿防治慢性腎纖維化機理實驗研究[J].陜西中醫(yī),2014,35(1):106-109.
[13] Fan DL, Zhao WJ, Wang YX,etal. Oxymatrine inhibits collagen synthesis in keloid fibroblasts via inhibition of transforming growth factor-beta1/Smad signaling pathway[J]. International Journal of Dermatology, 2012, 51(4):463-72.
[14] 陳 晨, 金 玉. 氧化苦參堿防治慢性腎纖維化機理的實驗研究[J]. 陜西中醫(yī), 2014,35(1):106-109.
[15] Liu L, Lu W, Ma Z,etal. Oxymatrine attenuates bleomycin-induced pulmonary fibrosis in mice via the inhibition of inducible nitric oxide synthase expression and the TGF-beta/Smad signaling pathway[J]. International Journal of Molecular Medicine, 2012, 29(5):815-22.
(收稿:2016-01-14)
Effect of oxymatnine on TGF-β1 inducing A549 epithelial to mesenchymal cell transition Department of Respiratory Diseases,Shenyang Military Region General Hospital
(Shen yang 110016) Liu Lei Ma Zhuang Xie Hua et al
Objective: We investigated the effect of Oxymatnine (Oxy) on TGF-β1 inducing alveolar epithelial to mesenchymal cell transition, and hope to provide a new candidate for the treatment of pulmonary fibrosis. Methods: After treatment with 0.25, 0.5, 1 mg/ml Oxy separately for 30 min , A549 cells were co-incubation with TGF-β1 (5 ng/ml) for 48h to detecte the cell proliferation changes by MTT, observed the cell morphological changes through microscopy, and analyzed the expression of phosphorylation of Smad2/3and EMT marker molecules E-candherin, N-cadherin and Vimentin by Western blotting. Results: Oxy could effectively interfere with the cellular proliferation and cell morphological changes, inhibited the expression phosphorylation of Smad2/3, E-candherin down-regulated,and N-cadherin and Vimentin up-regulated mediated by TGF-β1. Conclusion: Oxymatrine could inhibit TGF-β1 induced A549 cells epithelial - mesenchymal transition, Oxymatrine could been used as a new candidate drugs for treatment of pulmonary fibrosis.
Oxymatrine Pulmonary fibrosis/physiopathology Transforming growth factor beta 1 Epithelial cells Cell line,transformed
*遼寧省博士啟動基金資助項目(20141175)
氧化苦參堿 肺纖維化/病理生理學(xué) 轉(zhuǎn)化生長因子β1 上皮細(xì)胞 細(xì)胞系,轉(zhuǎn)化
R364.7
A
10.3969/j.issn.1000-7377.2016.11.001

