擬南芥SNC1基因突變對植株細胞分生和抗氧化性狀的影響
莫旭東,鄧東京,覃 磊,才桑吉,莫 祎,夏石頭*
(1 植物激素與生長發育湖南省重點實驗室,長沙 410128; 2 湖南農業大學生物科學技術學院,長沙 410128;3 湖南農業大學國際學院,長沙 410128)
?
擬南芥SNC1基因突變對植株細胞分生和抗氧化性狀的影響
莫旭東1,2,鄧東京3,覃 磊1,2,才桑吉2,莫 祎2,夏石頭1,2*
(1 植物激素與生長發育湖南省重點實驗室,長沙 410128; 2 湖南農業大學生物科學技術學院,長沙 410128;3 湖南農業大學國際學院,長沙 410128)
以擬南芥snc1突變體、其抑制子突變體mos4snc1和Col-0野生型植株為材料,研究了SNC1基因突變對植株細胞分生和抗氧化性狀的影響。結果表明,snc1植株平均比Col-0植株矮65.05%,其第3、4片真葉平均長度比Col-0的短53%,葉片平均寬度比Col-0的窄51%,角果莢平均短9.48%,平均種子數量少20.69%。與Col-0野生型植株相比,snc1植株第1、2片真葉細胞數目平均減少53.14%,而第3、4葉細胞數目平均減少61.88%;snc1突變體的SOD、POD、CAT酶活性和植株中花青素積累量均極顯著高于Col-0野生型植株的,而snc1的抑制子突變體mos4snc1則恢復了野生型表型,其SOD、POD酶活性和花青素含量與Col-0野生型植株的沒有顯著差異。這說明SNC1基因突變嚴重影響了擬南芥植株的細胞分生和抗氧化性能力,導致細胞數目大幅度減少,株型矮小。
擬南芥;SNC1;細胞分生;抗氧化性狀
植物抗性(Resistance,R)基因編碼蛋白能有效針對病原菌快速誘導防御反應,從而保證植株的正常生長發育[1]。植物和病原菌的相互識別會誘導產生活性氧,由于病原菌的無毒基因和植株抗性基因識別后的型號傳遞激活了各類防衛反應,活性氧(Reactive oxygen species,ROS)迸發是過敏性反應的特征,因此,植物的抗病性一定程度上會影響到植物的抗氧化性。在沒有病原菌攻擊時,抗性蛋白水平須受嚴格控制,以防止抗性途徑不必要激活而導致自身免疫的潛在傷害與生長缺陷[1]。在正常生長狀態下,植物體內存在一個完備的清除ROS的防御機制,其體內ROS的產生和清除會維持在一個動態平衡之中[2]。然而當植物遇到脅迫時,這種動態平衡會被破壞,而隨著植物受到脅迫時間的延長和受脅迫程度加重,體內ROS清除系統的功能會逐漸降低,ROS會逐漸累積而導致細胞膜脂過氧化并發生自由基鏈式反應,使細胞膜流動性下降,膜功能受到傷害[3]。ROS酶促清除系統主要是超氧化物歧化酶(SOD)、過氧化物酶(POD)、過氧化氫酶(CAT)等,通過這些酶活性的高低可以在一定程度上反應出植物抗性的強弱。花青素也是一種自由基清除劑,它能和蛋白質結合防止其過氧化,在同等生長情況下花青素的含量也能一定程度上反應出植株的抗氧化性[4]。
擬南芥SNC1(suppressorofnpr1-1,constitutive1)是植物細胞內的一種TIR-NB-LRR (Toll/interleukin-1 receptor-Nucleotide Binding-Leucine Rich Repeat)類R蛋白編碼基因,其序列中的一個堿基點突變導致SNC1蛋白氨基酸序列中的一個谷氨酸(Glu)變成了賴氨酸(Lys),從而組成型激活了病程相關蛋白如PR1和PR2的持續高表達,導致snc1突變體植株株型矮小,葉片卷曲,屬于獲得功能型突變體[5]。進一步的研究發現,snc1的一個抑制子突變可部分抑制其抗病途徑的組成型激活與SNC1介導的抗病表型,使mos4 (modifierofsnc1-1,4)植株恢復野生型表型[6,7]。為進一步深入探討SNC1基因持續激活對植株生長發育的影響,本研究以擬南芥snc1突變體、其抑制子突變體mos4snc1和野生型Col-0植株為材料,通過檢查其生長表型、葉片細胞數目、超氧化物歧化酶(SOD)、過氧化物酶(POD)和過氧化氫酶(CAT)酶活性與花青素含量,一定程度上反映出SNC1基因突變對snc1植株細胞分生增殖與抗氧化性能的影響。
1 材料與方法
1.1 材料與試劑
供試材料為野生型擬南芥(Col-0生態型);snc1突變體和mos4snc1雙突變體,由加拿大UBC李昕實驗室惠贈。
NBT(Nitro Blue Tetrazolium Chloride,硝基四氮唑藍)、MET(L-Methionine,L-甲硫氨酸)、愈創木酚等購自博美生物科技有限責任公司;碘化丙啶(PI)、四鹽酸精胺購自Sigma公司;正丙醇、核黃素、MES(Methyl Methanesulfonate,甲磺酸甲酯)、纖維素酶(cellulose R10)、離析酶(macerozyme R10)、甘油和β-巰基乙醇購自鵬程生物有限公司;其他常規藥品均購自國藥集團化學試劑有限公司。
實驗所需試劑:種子消毒液使用15%NaClO + 0.1% Tween20進行配置。0.1 mol/L磷酸緩沖液(pH6.0),首先配置好AB貯備液,分別為貯備液A:0.2 mol/L NaH2PO4溶液,貯備液B:0.2 mol/L Na2HPO4溶液,然后分別取貯備液A 87.7 mL與貯備液B 12.3 mL,充分混勻并稀釋定容至200 mL。POD反應混合液的配置是使用0.1 mol/L磷酸緩沖液(pH6.0)50 mL,過氧化氫(H2O2)28 μL和愈創木酚19 μL充分混勻得到。0.1 mol/L磷酸緩沖液(pH7.8)的配置是分別取貯備液A 8.5 mL與貯備液B 91.5 mL,充分混勻并稀釋至200 mL。其他使用到的藥劑還有0.026 mol/L蛋氨酸(Met)磷酸鈉緩沖液;7.5×104mol/L硝基四氮唑藍(NBT)溶液;2×10-5mol/L核黃素溶液含1.0 μmol/L EDTA;0.05 mol/L pH7.8磷酸鈉溶液;0.05 mol/L Tris-HCl緩沖液(pH7.0)等。花青素提取液的配置是由正丙醇∶鹽酸∶水=18∶1∶81混合;0.05 mol/L pH7.0磷酸緩沖液;0.2 mol/L H2O2溶液:30% H2O211.36 mL溶于磷酸緩沖液中,定量至250 mL。細胞數目檢測用到的試劑按照文獻[8]方法配制。
1.2 種子的播種與管理
按照Xia等[9,10]的方法,將適量擬南芥種子用種子消毒液殺菌消毒3~5 min后,用蒸餾水清洗兩次,加入0.1%的瓊脂糖使種子重懸,在4℃下避光春化3~4 d。分散種入培養缽后再將培養缽放置在光照培養室中培養,培養條件為16 h光照(23℃) + 8 h(21℃)黑暗、濕度40%~50%。
當幼苗長出2~3片真葉時,將幼苗移栽至小培養缽中,每缽4株,并根據土壤水分蒸發情況,每隔2~3 d澆一次水,保持土壤濕潤,移盆后約35 d可進行各種生理指標檢測。
1.3 細胞數目測定方法
取苗齡約35 d的擬南芥真葉葉片,參照文獻[8]的方法用流式細胞儀進行細胞數量檢測。
1.4 酶活性檢測方法
過氧化物酶(POD)的測定參照文獻[11]方法略作修改。幼苗移栽后約35 d,選取長勢、大小、形態一致的snc1、mos4snc1和Col-0野生型植株幼苗,每株取第3~8片新鮮真葉共約0.2 g放入研缽中,加入1 mL 0.05 mol/L pH7.8磷酸緩沖液,在冰上將其研磨成勻漿,用移液器將勻漿轉移到2 mL離心管中,再以1 mL 0.05 mol/L pH7.8磷酸緩沖液沖洗研缽,一并轉入同一EP管中。4000 rpm離心5 min,再取上清1 mL至5 mL離心管中,加入3 mL pH7.8磷酸緩沖液,顛倒混勻。而后取1 mL酶液和3 mL POD反應液置于石英比色皿中混勻,反應5 min后測定OD470的光密度值。
超氧化物歧化酶(SOD)的測定參照文獻[12]方法略作修改。選取長勢、大小、形態較為一致、移栽后約35 d的snc1、mos4snc1和Col-0野生型植株幼苗,每株取第3~8片新鮮真葉共約0.2 g置于研缽中,加入1 mL 0.05 mol/L pH7.8磷酸緩沖液,于冰上將其研磨成勻漿,用移液器將勻漿轉移至2 mL離心管中,再用1 mL 0.05 mol/L pH7.8磷酸緩沖液沖洗研缽,一并轉入2 mL離心管。然后用冷凍離心機在4℃10 000 g離心30 min,取上清定容至4 mL。然后取潔凈且干燥的5 mL的微燒杯編號,按表1的順序加入酶液及各試劑,反應系統總體積為3 mL。充分混勻后,取1個不加酶液的微燒杯對照組置于暗處,作為空白對照調零,再取2個對照組與試驗組微燒杯一塊放在溫度為25℃,光強為6500 Lux的光照箱內,照光處理20 min,然后立即遮光終止反應。在560 nm波長下用暗處理的溶液調零,測定試驗組光密度值。

表1 反應系統中各試劑及酶液的加入量(mL)Table 1 The amount of each reagent and enzyme liquid for the reaction system (mL)
過氧化氫酶(CAT)含量的測定參照文獻[11]方法略作修改。幼苗移栽后約35 d,選取長勢、大小、形態較為一致的snc1,mos4snc1和Col-0野生型植株幼苗,每株取第3~8片新鮮真葉共約0.2 g放入研缽中,加入1 mL 0.05 mol/L pH7.0磷酸緩沖液,在冰上將其研磨成勻漿,用移液器將勻漿轉移到2 mL離心管中,再用1 mL 0.05 mol/L pH7.0磷酸緩沖液沖洗研缽,一并轉入2 mL離心管中。4000 rpm離心5 min,取上清1 mL至5 mL離心管中,加入3 mL pH7.0磷酸緩沖液,顛倒混勻。取0.1 mL酶液,加入0.05 mol/L pH 7.0磷酸鉀緩沖液1.4 mL和40 mmol/L H2O21.5 mL,于石英比色皿中,立即在波長240 nm處檢測光密度值,每30 s讀數一次,共測定4 min。以不含酶液的待測液作為空白對照。
花青素含量的測定參照Shan等[13]方法稍作修改。幼苗移栽后約35 d,選取長勢、大小、形態較為一致的snc1、mos4snc1和Col-0野生型植株,去根,清洗去泥沙,再用濾紙吸干多余水分。取10株植物做為一個樣品,稱重后放入2 mL帶扣的防爆離心管中。加入1 mL提取液,100℃水浴3 min(當心爆管),用鑷子取出樣品,遮光暗處理至少12 h。用分光光度計測定樣品的A535與A650光密度值。
1.5 數據分析
運用DPS數據處理系統進行統計分析。
2 結果與分析
2.1 Col-0野生型、snc1和mos4snc1突變體植株形態特征
在同樣培養條件下,snc1突變體植株幼苗與Col-0野生型和其抑制子突變體mos4snc1植株幼苗明顯不同,snc1突變體幼苗株型矮小,葉片卷曲,成株果莢較Col-0野生型的短,種子較少。而snc1的抑制子突變體mos4snc1植株恢復了其野生型表型(圖1)。
為量化這種差異特征,統計分析了移栽后約60 d的Col-0野生型、snc1和mos4snc1突變體植株的株高,葉片長度、寬度,果莢長度和每果莢種子數目等。結果snc1植株比Col-0植株平均矮65.05%,其第3、4片真葉平均長度比Col-0的短53%,葉片

圖1 Col-0野生型、snc1和mos4snc1突變體幼苗的形態Fig.1 Morphology of wild type (Col-0),snc1 and mos4 snc1 seedlings
平均寬度比Col-0的窄51%,角果莢平均短9.48%,平均種子數量少20.69%(表2)。而snc1的抑制子突變體mos4snc1則恢復了野生型表型,與Col-0野生型植株沒有顯著差異。說明snc1基因突變嚴重影響了擬南芥植株生長發育,導致植株矮小,葉片變小,果莢變短等表型。
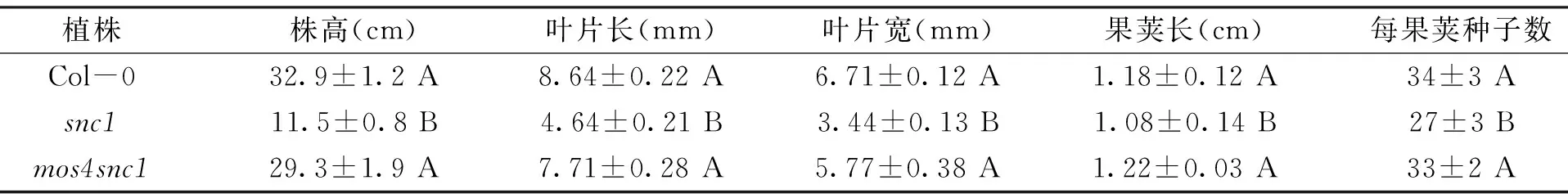
表2 Col-0野生型、snc1和mos4snc1突變體植株的形態指標比較Table 2 Morphological parameters of the wild type Col-0,snc1 and mos4snc1 plants
2.2 SNC1基因突變對snc1植株細胞分生增殖的影響
為進一步檢測snc1突變體植株的矮小株型主要是細胞數目減少引起的還是由單個細胞體積變小所引起的,分別檢測了植株的第1、2片和第3、4片真葉的細胞數目(圖2)。結果表明,野生型Col-0第1、2片真葉的細胞數目平均約為每葉4.95×104個,snc1突變體平均約為每葉2.32×104個,Col-0野生型植株的第1、2片真葉的平均細胞數目是snc1突變體的2.13倍,而mos4snc1突變體平均約為每葉4.39×104個,與野生型植株的第1、2片真葉的平均細胞數目沒有顯著性差異。Col-0第3、4片真葉的平均細胞數目(平均約為每葉1.12×105)是snc1第3、4片真葉的平均細胞數目(約為每葉4.27×104)的2.62倍,而mos4snc1第3、4片真葉的平均細胞數目約為每葉9.49×104。這表明snc1基因突變導致了葉片細胞數目大幅度減少,其中第1、2葉細胞平均減少了53.14%,而第3、4葉細胞平均減少了61.88%,說明snc1基因突變削弱了植株細胞分裂的增生能力。
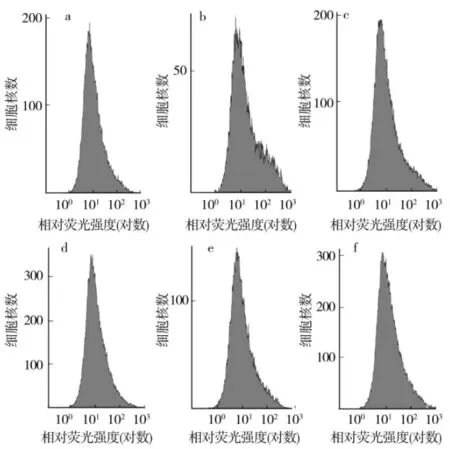
圖2 野生型(Col-0)、snc1和mos4snc1突變體植株真葉細胞核數目Fig.2 Cell nuclei numbers of the leaves in wild type(Col-0),snc1 mutant and mos4snc1 mutant plants
2.3 SNC1基因突變對snc1植株細胞抗氧化脅迫酶活性的影響
植物抗性反應的激活常伴隨著細胞內氧化還原性狀的改變如活性氧迸發。為深入分析SNC1基因突變對植株細胞的抗氧化脅迫性狀的影響,分別檢測了生長約35 d的擬南芥Col-0野生型、snc1和mos4snc1突變體植株葉片的SOD、POD和CAT酶活性,結果如表3。由表3可知,在同樣生長條件下,snc1突變體的SOD、POD、CAT酶活性顯著高于Col-0野生型植株的,表明snc1體內因病程相關蛋白的組成型表達導致持續的氧脅迫,因此在一定程度上需要高活性SOD、POD、CAT酶來清除ROS,以幫助突變體植株適應這種氧化脅迫環境。而mos4snc1突變體則抑制了SNC1的組成型表達,恢復了其野生型表型,植株生長也恢復正常,因此mos4snc1突變體的POD、SOD酶活性與野生型植株的POD、SOD酶活性沒有顯著差別。
2.4 SNC1基因突變對snc1植株細胞花青素積累的影響
植株的抗氧化脅迫能力可能影響到植株體內花青素的積累。統計分析表明,同等生長條件下,snc1、mos4snc1植株中花青素含量顯著高于Col-0植株體內花青素含量,而mos4snc1的花青素含量則低于snc1突變體植株,但兩者之間沒有顯著差別(表3)。

表3 SNC1基因突變植株的POD、SOD、CAT酶活性和花青素含量Table 3 Effects of SNC1 gene mutation on enzyme activities of POD,SOD,CAT and Anthocyanins content
3 結論與討論
擬南芥snc1 (suppressorofnpr1-1,constitutive1)是在研究植物先天免疫反應,篩選npr1(nonexpresserofPRgenes)的抑制子突變體時找到的一個功能獲得型點突變體。該突變體中病程相關蛋白如PR1和PR2等持續高表達,對病原微生物的抗性顯著增強,并導致snc1突變體葉片卷曲,株型矮小[5]。圖位克隆結果表明,該突變基因編碼蛋白是植物中的一種TIR-NB-LRR (Toll/interleukin-1 receptor-Nucleotide Binding-Leucine Rich Repeat)類R蛋白,其基因的突變導致氨基酸序列中的一個谷氨酸(Glu)變成了賴氨酸(Lys),導致SNC1蛋白在snc1突變體中的穩定性增強,從而組成型激活了snc1植株中PR1和PR2等病程相關蛋白高表達。為了探討SNC1基因突變對植株生長發育的影響,本研究以擬南芥野生型Col-0、突變體snc1植株與其抑制子雙突變體mos4snc1為材料,檢測基因突變對植物細胞分生增殖的影響和細胞抗氧化性狀的影響,發現基因突變導致snc1植株第3、4片真葉平均比Col-0野生型植株的第3、4片真葉短53%、窄51%,植株比野生型植株平均矮65.05%,其角果莢平均短9.48%,平均種子數量少20.69%。說明SNC1基因突變嚴重影響了擬南芥植株生長發育,導致葉小,植株矮小,果莢變短。而其抑制子突變體mos4snc1則與Col-0野生型植株沒有顯著差異。
為進一步分析snc1的矮小株型是否由細胞體積變小所引起,本研究通過葉片酶解,細胞裂解和細胞核收集后染色,用流式細胞儀詳細檢測了Col-0野生型、snc1和mos4snc1雙突變體植株的細胞數目,結果顯示Col-0植株的第1、2片真葉平均細胞數目是snc1植株第1、2片真葉平均細胞數目的2.13倍,第3、4片真葉的平均細胞數目是snc1第3、4片真葉的2.62倍。而抑制子植株mos4snc1與野生型植株之間沒有顯著差別,證明SNC1基因突變削弱了植株細胞的分生增殖能力,從而導致細胞數目減少,植株變矮。
[1] Dangl JL,Jones JD.Plant pathogens and integrated defence responses to infection[J].Nature,2001,411:826-833.
[2] Sikka SC,Rajasekaran M,Hellstrom WJG.Role of oxidative stress and antioxidants in male infertility[J].Toxicology Letters,2013,3(2):93-103.
[3] Noctor G,Foyer CH.Ascorbate and glutathione:keeping active oxygen under control[J].Annual Review of Plant Biology,1998,49(4):249-279.
[4] Prior RL,Wu X.Anthocyanins:structural characteristics that result in unique metabolic patterns and biological activities[J].Free Radical Research,2006,40(10):1014-1028.
[5] Zhang Y,Goritschnig S,Dong X,et al.A gain-of-function Mutation in a plant disease resistance gene leads to constitutive activation of downstream signal transduction pathways in suppressor ofnpr1-1,constitutive 1[J].Plant Cell,2003,15(11):2636-2646.
[6] Palma K,Zhao Q,Cheng YT,et al.Regulation of plant innate immunity by three proteins in a complex conserved across the plant and animal Kingdoms[J].Genes & Development,2007,21(12):1484-1493.
[7] Johnson KCM,Xia S,Feng X,et al.The chromatin remodeler SPLAYED negatively regulates SNC1-mediated immunity[J].Plant and Cell Physiology,2015,56(8):1616-1623.
[8] 李依馳,崔 看,程 鵬,等.擬南芥葉片細胞數直接高效檢測體系的建立[J].湖南農業大學學報(自然科學版),2015,41(5):480-485.
[9] Xia ST,Xiao LT,Gannon P,et al.RFC3 regulates cell proliferation and pathogen resistance inArabidopsis[J].Plant Signaling & Behavior,2010,5(2):168-170.
[10]Xia ST,Xiao LT,Bi DL,et al.Arabidopsisreplication factor C subunit 1 plays an important role in embryogenesis[J].Journal of Plant Physiology & Molecular Biology,2007,33(3):179-187.
[11]蕭浪濤,王三根.植物生理學實驗技術[M].北京:中國農業出版社,2008.103-107.
[12]湯章城.現代植物生理學實驗指南[M].北京:科學出版社,1999.314-315.
[13]Shan X,Zhang Y,Peng W,et al.Molecular mechanism for jasmonate-induction of anthocyanin accumulation in Arabidopsis[J].Journal of Experimental Botany,2009,60:3849-3860.
Effects ofSNC1 Gene Mutation on Cell Proliferation and Antioxidation Character inArabidopsisthaliana
MO Xudong1,2,DENG Dongjing3,QIN Lei1,2,CAI Sangji2,MO Yi2,XIA Shitou1,2*
(1 Hunan Provincial Key Laboratory of Phytohormones and Growth Development,Changsha,Hunan 410128,China;2 College of Bioscience and Biotechnology,Hunan Agricultural University,Changsha,Hunan 410128,China;3 International College,Hunan Agricultural University,Changsha,Hunan 410128,China)
Wild type Col-0,snc1 mutant and its suppressormos4snc1 double mutant plants was used as materials to study the effects ofSNC1 gene mutation on cell proliferation and antioxidation character inArabidopsisthaliana.The results showed that the average plant height ofsnc1 was 65.05% shorter than that of Col-0 wild type plants,with the average blade length and width of the third and 4thtrue leaf reduced by 53% and 51%,average silique length and numbers of seeds per silique reduced by 9.48% and 20.69%,respectively.Compared with the wild type plants,cell number of the first and second true leaves decreased 53.14%,and that of the third and 4thleaves insnc1 mutants decreased 61.88%.The activity of superoxide dismutase (SOD),peroxidase (POD) and catalase (CAT) enzyme insnc1 mutants was significantly higher than that of the wild type plants.The accumulation of anthocyanin in snc1 was also significantly higher than that of the wild type plants.The mutated phenotype was restored to wild type inmos4snc1 double mutant.As a result,there is no significant difference for the activity of SOD and POD betweenmos4snc1 double mutant and wild type plants.It is suggested that the cell proliferation and antioxidation character is severely affected bySNC1 gene mutation which leads to the cell number reduction and plant drawf with snc1 gene.
Arabidopsis;SNC1;cell division and proliferation;oxidation resistance
2016-05-05
莫旭東(1989-),男,碩士研究生。 *通信作者:夏石頭,教授,Email:xstone0505@163.com。
湖南省自然科學杰出青年基金項目(11JJ1007)。
Q786
A
1001-5280(2016)05-0557-06
10.16848/j.cnki.issn.1001-5280.2016.05.18

