環(huán)磷腺苷葡胺致不良反應(yīng)文獻(xiàn)分析
洪文英,王述蓉(1.成都市溫江區(qū)人民醫(yī)院臨床藥學(xué)室,成都 610000;2.西南醫(yī)科大學(xué)藥學(xué)院,四川瀘州646000;3.西南醫(yī)科大學(xué)附屬醫(yī)院藥學(xué)部,四川瀘州 646000)
環(huán)磷腺苷葡胺致不良反應(yīng)文獻(xiàn)分析
洪文英1,2*,王述蓉3#(1.成都市溫江區(qū)人民醫(yī)院臨床藥學(xué)室,成都610000;2.西南醫(yī)科大學(xué)藥學(xué)院,四川瀘州646000;3.西南醫(yī)科大學(xué)附屬醫(yī)院藥學(xué)部,四川瀘州646000)
目的:探討環(huán)磷腺苷葡胺致不良反應(yīng)(ADR)發(fā)生的特點(diǎn)、一般規(guī)律,為臨床安全合理用藥提供參考。方法:以“環(huán)磷腺苷葡胺”“不良反應(yīng)”為檢索詞,檢索中國(guó)期刊全文數(shù)據(jù)庫(kù)、萬(wàn)方數(shù)據(jù)庫(kù)、維普中文科技期刊數(shù)據(jù)庫(kù),自數(shù)據(jù)庫(kù)建庫(kù)至2016年2月,按納入與排除標(biāo)準(zhǔn)進(jìn)行文獻(xiàn)篩選,對(duì)得到的病例資料進(jìn)行提取和統(tǒng)計(jì)分析。結(jié)果:共納入17篇文獻(xiàn),涉及20例患者,男女比例為1∶1;≥60歲患者居多,共有11例(占55.00%);ADR大多在用藥30 min內(nèi)發(fā)生(18例,90.00%);14例(70.00%)為聯(lián)合用藥;ADR可累及多個(gè)器官/系統(tǒng),以全身性損害(12例,27.91%)和皮膚及其附件損害(11例,25.58%)最常見(jiàn),嚴(yán)重者可致過(guò)敏性休克(7例)。結(jié)論:臨床應(yīng)重視環(huán)磷腺苷葡胺引發(fā)的ADR,嚴(yán)格按說(shuō)明書規(guī)定用藥,并關(guān)注其輔料成分,密切防范ADR的發(fā)生。
環(huán)磷腺苷葡胺;藥品不良反應(yīng);文獻(xiàn)分析
環(huán)磷腺苷葡胺為非洋地黃類強(qiáng)心劑,具有正性肌力作用,能增強(qiáng)心肌收縮力,改善心肌泵血功能,有擴(kuò)張血管作用,可降低心肌代謝,保護(hù)缺血缺氧的心肌,還改善竇房結(jié)P細(xì)胞功能,被內(nèi)科臨床廣泛應(yīng)用于心力衰竭、心肌炎、冠狀動(dòng)脈硬化、心肌梗死、心功能不全、中風(fēng)后遺癥、腦動(dòng)脈硬化、肝臟熱缺血、眩暈癥、神經(jīng)性耳聾、白細(xì)胞減少癥、原發(fā)性血小板減少性紫癜等[1]。環(huán)磷腺苷葡胺作為一種應(yīng)用廣泛的藥物,其說(shuō)明書提示的應(yīng)有偶見(jiàn)心悸、心慌、頭暈等癥狀,未提及可能發(fā)生的其他不良反應(yīng)。但是近年來(lái),隨著環(huán)磷腺苷葡胺的廣泛應(yīng)用,該藥的不良反應(yīng)報(bào)道逐漸增多,為研究其致藥品不良反應(yīng)(ADR)的規(guī)律和特點(diǎn),本研究對(duì)國(guó)內(nèi)近年來(lái)關(guān)于環(huán)磷腺苷葡胺致ADR的報(bào)道進(jìn)行整理、統(tǒng)計(jì)和分析,以期為臨床安全合理用藥提供參考。
1 資料與方法
1.1資料來(lái)源
以“環(huán)磷腺苷葡胺”“不良反應(yīng)”為檢索詞,檢索中國(guó)期刊全文數(shù)據(jù)庫(kù)(CJFD)、萬(wàn)方數(shù)據(jù)庫(kù)、維普中文科技期刊數(shù)據(jù)庫(kù)(VIP),檢索時(shí)間范圍均為自數(shù)據(jù)庫(kù)建庫(kù)至2016年2月。
1.2納入與排除標(biāo)準(zhǔn)
納入標(biāo)準(zhǔn):檢索環(huán)磷腺苷葡胺致ADR的文獻(xiàn),研究類型包括個(gè)案報(bào)告、病例系列研究、隊(duì)列研究、類試驗(yàn)、隨機(jī)對(duì)照試驗(yàn)(RCT)。
排除標(biāo)準(zhǔn):ADR描述不清或未描述的;明確無(wú)ADR發(fā)生的;明確不為環(huán)磷腺苷葡胺引起的ADR;重復(fù)發(fā)表的;二次文獻(xiàn)研究;實(shí)驗(yàn)研究、綜述、摘要類文獻(xiàn)。
1.3統(tǒng)計(jì)學(xué)方法
對(duì)納入文獻(xiàn)的相關(guān)信息進(jìn)行提取,并采用回顧性研究方法,按照患者性別、年齡、用藥劑量、發(fā)生時(shí)間、合并用藥、臨床表現(xiàn)及預(yù)后進(jìn)行統(tǒng)計(jì)、分析。
2 結(jié)果
根據(jù)納入與排除標(biāo)準(zhǔn)進(jìn)行文獻(xiàn)篩選,共獲得17篇有效文獻(xiàn),涉及20例患者,分別按照“1.3”項(xiàng)下方法等進(jìn)行統(tǒng)計(jì)、分析。
2.1患者年齡與性別分布
20例環(huán)磷腺苷葡胺致ADR中,男性10例,女性10例,男女比例為1∶1,差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05);年齡最小者36歲,最大者89歲。從年齡分布來(lái)看,主要發(fā)生在60歲以上患者(55.00%)。環(huán)磷腺苷葡胺致ADR發(fā)生的患者年齡與性別分布見(jiàn)表1。
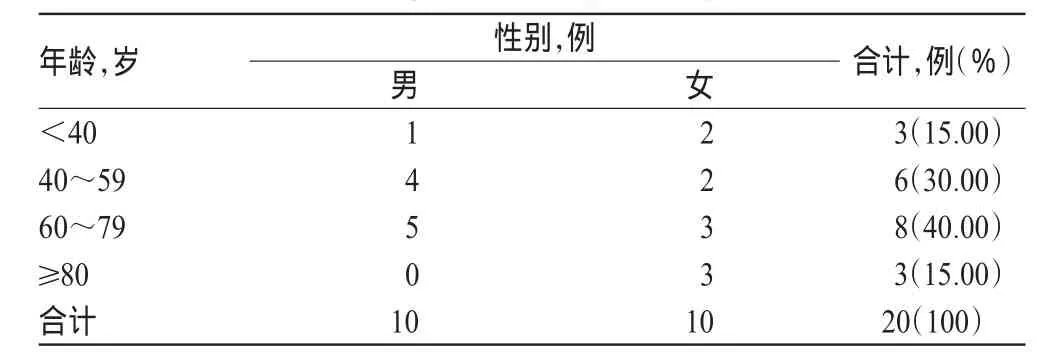
表1 發(fā)生ADR患者的年齡與性別分布Tab 1 Distribution of patient’s age and gender inADR cases
2.2患者藥物過(guò)敏史
20例患者中,3例有藥物過(guò)敏史,分別是對(duì)青霉素、阿莫西林舒巴坦、磺胺類藥物過(guò)敏,11例患者明確既往無(wú)藥物過(guò)敏史,6例未描述藥物過(guò)敏史情況。患者藥物過(guò)敏史分布見(jiàn)表2。
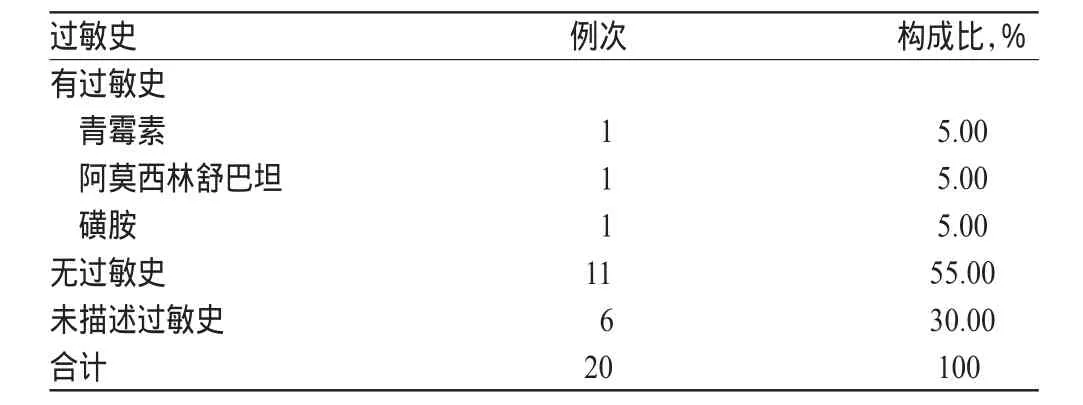
表2 患者藥物過(guò)敏史分布Tab 2 Distribution of allergy history
2.3患者用藥原因分布
20例患者用藥原因中,以心臟疾病為主,有10例(50.00%),其次為外傷骨折伴心電圖異常6例(30.00%)和腦梗死及腦損傷4例(20.00%)。患者用藥原因分布見(jiàn)表3。
2.4ADR發(fā)生時(shí)間分布
20例ADR中,首次用藥即發(fā)生ADR 19例,有1例于用藥次日再次使用時(shí)發(fā)生[2]。ADR多在用藥30 min內(nèi)發(fā)生(90.00%),出現(xiàn)時(shí)間最短為用藥后2 min[1,3-6],最長(zhǎng)為用藥1 d后[7]。ADR發(fā)生時(shí)間分布見(jiàn)表4。

表3 患者用藥原因分布Tab 3 Distribution of medication reasons

表4 ADR發(fā)生時(shí)間分布Tab 4 Distribution of occurrence time ofADR
2.5用藥情況
2.5.1藥物使用劑型和生產(chǎn)廠家分布20例ADR中,應(yīng)用注射用無(wú)菌粉末者9例(45.00%),注射液5例(25.00%),其余6例(30.00%)無(wú)法判斷使用劑型,具體見(jiàn)表5。
2.5.2用法用量20例ADR中,環(huán)磷腺苷葡胺均采取靜脈滴注方式給藥,用量最低為20 mg,最高240 mg,大多按照說(shuō)明書劑量用藥,僅有1例患者超劑量用藥(240 mg)[8];配伍輸液的選擇上,有11例選擇藥品說(shuō)明書推薦的5%葡萄糖注射液,4例選擇0.9%氯化鈉注射液,2例選擇5%葡萄糖氯化鈉注射液,3例未描述溶劑情況。
2.5.3聯(lián)合用藥20例ADR中,2例為單獨(dú)使用環(huán)磷腺苷葡胺過(guò)程中出現(xiàn),4例未描述聯(lián)合用藥情況,其余14例明確有聯(lián)合用藥情況。
2.6ADR累及器官/系統(tǒng)和臨床表現(xiàn)
環(huán)磷腺苷葡胺致ADR以全身性損害為主,主要包括過(guò)敏性休克[2-5,9-11]和嚴(yán)重過(guò)敏樣反應(yīng)[1,12],部分患者出現(xiàn)寒戰(zhàn)、發(fā)熱,其他ADR有呼吸系統(tǒng)損害如不適、咳嗽、胸悶、呼吸困難,心腦血管損害如頭暈、心悸、胸痛,皮膚及附件損害如皮疹、瘙癢、潮紅、多汗等,消化系統(tǒng)損害如惡心、嘔吐、腹痛、腹瀉。根據(jù)國(guó)家ADR監(jiān)測(cè)中心編譯的《WHO藥品不良反應(yīng)術(shù)語(yǔ)集》中規(guī)定的ADR累及器官/系統(tǒng)對(duì)20例ADR進(jìn)行統(tǒng)計(jì),具體見(jiàn)表6(由于1例ADR可累及多個(gè)器官/系統(tǒng),故合計(jì)例次>ADR例數(shù))。

表6 ADR累及器官/系統(tǒng)和臨床表現(xiàn)Tab 6 System/organs involved in ADR and clinical manifestations
2.7治療及轉(zhuǎn)歸
立即停藥,給予吸氧、抗過(guò)敏對(duì)癥治療措施,20例ADR治療及預(yù)后均較好,無(wú)死亡病例報(bào)告。
2.8關(guān)聯(lián)性及嚴(yán)重程度評(píng)價(jià)
根據(jù)原國(guó)家食品藥品監(jiān)督管理局ADR監(jiān)測(cè)中心2005年9月發(fā)布《藥品不良反應(yīng)報(bào)告和監(jiān)測(cè)工作手冊(cè)》中的ADR關(guān)聯(lián)性評(píng)價(jià)標(biāo)準(zhǔn)進(jìn)行初步評(píng)價(jià),評(píng)價(jià)結(jié)果:3例肯定,8例很可能,9例可能;按照國(guó)家ADR監(jiān)測(cè)中心《關(guān)于發(fā)布〈常見(jiàn)嚴(yán)重藥品不良反應(yīng)技術(shù)規(guī)范及評(píng)價(jià)標(biāo)準(zhǔn)〉的通知》的評(píng)價(jià)標(biāo)準(zhǔn)進(jìn)行初步評(píng)價(jià),嚴(yán)重的ADR 9例(包括過(guò)敏性休克7例,嚴(yán)重過(guò)敏樣反應(yīng)2例),其余11例為一般的ADR。
3 討論
3.1環(huán)磷腺苷葡胺致ADR相關(guān)因素分析
3.1.1性別與年齡本研究的20例ADR患者中,男女比例為1∶1,差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05),但本研究病例偏少,不能充分說(shuō)明ADR與性別間的關(guān)系。從年齡分布來(lái)看,60歲以上老年患者居多(55.00%),值得密切關(guān)注,這可能與老年患者體質(zhì)相對(duì)較弱心臟功能負(fù)荷有限有關(guān)。當(dāng)靜脈滴注的藥物刺激性大、滴速控制不當(dāng)時(shí),老年人易出現(xiàn)胸悶、氣短、心率加快等熱原樣反應(yīng),而伴有危重、高敏體質(zhì)、心肺功能不良的老年患者尤為如此。老年人易患多種疾病,常需同時(shí)接受多種藥物的聯(lián)合治療,更易發(fā)生因藥物相互作用導(dǎo)致的ADR[13]。
3.1.2藥物過(guò)敏史及用藥原因20例ADR患者中,3例有藥物過(guò)敏史,提示有藥物過(guò)敏史者用藥要特別謹(jǐn)慎。有藥物過(guò)敏史的患者,對(duì)藥物過(guò)敏的易感性較高[14],較其他患者更易出現(xiàn)ADR。11例患者無(wú)藥物過(guò)敏史,提示無(wú)藥物過(guò)敏史患者也不能放松警惕,還需要注意患者的既往史,早先就有的過(guò)敏癥狀或者慢性蕁麻疹、慢性鼻炎、鼻竇炎等疾病在應(yīng)用某些藥物時(shí)可能會(huì)加重癥狀[15]。6例患者未描述藥物過(guò)敏史情況,提示醫(yī)務(wù)人員的風(fēng)險(xiǎn)意識(shí)有待進(jìn)一步提高。20例ADR患者中10例為心臟疾病,6例為其他疾病伴心電圖異常,其余4例無(wú)心臟和(或)心電異常,說(shuō)明該藥存在擅自擴(kuò)大適應(yīng)證使用現(xiàn)象,臨床應(yīng)嚴(yán)格按適應(yīng)證使用。環(huán)磷腺苷葡胺臨床用于心臟疾病,但也有報(bào)道其可致心肌梗死[16],值得臨床注意。
3.1.3ADR發(fā)生時(shí)間環(huán)磷腺苷葡胺致ADR多在用藥過(guò)程中發(fā)生。本次統(tǒng)計(jì)的20例ADR中,首次用藥即發(fā)生的有19例(95%),其中18例在用藥后30 min中內(nèi)發(fā)生,可能與環(huán)磷腺苷葡胺在用藥后10~20 min后開始起作用有關(guān),提示臨床應(yīng)密切觀察患者在用藥30 min內(nèi)的反應(yīng),以便及時(shí)發(fā)現(xiàn)、處理;有1例在用藥次日出現(xiàn),另1例次日再次用藥時(shí)1 min出現(xiàn),提示不能忽略用藥后及連續(xù)用藥后的觀察。
3.1.4給藥途徑與用法用量環(huán)磷腺苷葡胺的ADR均為靜脈滴注所致,本次所檢索的文獻(xiàn)尚未見(jiàn)到其他給藥方式致ADR的報(bào)道。靜脈用藥時(shí),機(jī)體缺少消化道及其他防御系統(tǒng)的屏障作用,以及靜脈用藥時(shí)可能存在內(nèi)毒素、pH、滲透壓、微粒等直接誘因,使其引起ADR的可能性極大增加[13]。配伍輸液的選擇上,有6例未按照說(shuō)明書推薦選擇溶劑,其中有4例選擇0.9%氯化鈉注射液,2例選擇5%葡萄糖氯化鈉注射液。環(huán)磷腺苷葡胺忌配伍藥物氨茶堿[17],未列出0.9%氯化鈉注射液和5%葡萄糖氯化鈉注射液屬于配伍禁忌,但是環(huán)磷腺苷葡胺的稀釋液不僅要考慮配伍后的穩(wěn)定性,還應(yīng)從臨床疾病方面考慮,患者大多因心臟疾病使用環(huán)磷腺苷葡胺,溶劑應(yīng)盡量避免使用鹽類,以免增加心臟負(fù)擔(dān)。用量方面,僅有1例超出說(shuō)明書規(guī)定的劑量范圍,提示本研究中環(huán)磷腺苷葡胺的ADR可能與用藥劑量關(guān)系較小。但本研究病例數(shù)較少,不能充分確定環(huán)磷腺苷葡胺致ADR的發(fā)生與溶劑、用量的相關(guān)性。
本研究中有14例患者在應(yīng)用環(huán)磷腺苷葡胺前聯(lián)合使用了其他藥物,這些藥物對(duì)于環(huán)磷腺苷葡胺致ADR的發(fā)生究竟起了多大的作用,目前無(wú)從知曉。但2種或2種以上的藥物同時(shí)或先后使用,可能會(huì)產(chǎn)生一定影響,使藥物藥效增強(qiáng)或降低、ADR發(fā)生率增加或產(chǎn)生新的ADR[13]。
3.2環(huán)磷腺苷葡胺致ADR的類型及發(fā)生機(jī)制
環(huán)磷腺苷葡胺致ADR可涉及多個(gè)器官/系統(tǒng),以全身性損害為主,其他依次為皮膚及其附件損害、呼吸系統(tǒng)損害和消化系統(tǒng)損害等。20例ADR中,有19例屬于速發(fā)型過(guò)敏反應(yīng),可能的發(fā)生機(jī)制如下:(1)可能與藥物不純、低分子雜質(zhì)和降解產(chǎn)物與機(jī)體蛋白質(zhì)結(jié)合形成變應(yīng)原。(2)與藥物輔料有關(guān)。20例ADR中3例為無(wú)錫凱夫制藥有限公司生產(chǎn)(商品名:凱緦),5例為湖南五洲通藥業(yè)有限公司生產(chǎn)(商品名:麗智),兩藥說(shuō)明書明確輔料為右旋糖酐40,有報(bào)道右旋糖酐可誘發(fā)過(guò)敏反應(yīng)甚至休克[18];還有2例使用江蘇萬(wàn)邦生物醫(yī)藥有限公司生產(chǎn)的環(huán)磷腺苷葡胺,其說(shuō)明書提示輔料為甘露醇,有研究報(bào)道甘露醇也可導(dǎo)致過(guò)敏反應(yīng)甚至休克[19]。(3)與先前被結(jié)構(gòu)相似的藥物分子致敏有關(guān),如環(huán)磷腺苷。(4)與患者生病時(shí)機(jī)體處于超敏狀態(tài)有關(guān)。
3.3環(huán)磷腺苷葡胺的安全使用建議
(1)嚴(yán)格遵循說(shuō)明書的用法、用量。環(huán)磷酰苷葡胺1日劑量不可超過(guò)180 mg,應(yīng)用該劑量時(shí),應(yīng)至少使用5%葡萄糖注射液250 ml稀釋后靜脈滴注,盡量避免靜脈推注[20]。(2)嚴(yán)格控制滴注速度。環(huán)磷腺苷葡胺滴注不宜太快,用量在150 mg以上時(shí)應(yīng)在90 min以上滴完。剛開始輸注環(huán)磷腺苷葡胺的15 min內(nèi)應(yīng)緩慢靜脈滴注,同時(shí)給予患者增加飲水,避免空腹輸注環(huán)磷腺苷葡胺[20]。(3)環(huán)磷腺苷葡胺中的胺類遇到堿類會(huì)發(fā)生化學(xué)反應(yīng)生成氨,對(duì)肝臟有毒性反應(yīng),因此環(huán)磷腺苷葡胺禁止與氨茶堿同時(shí)靜脈使用,必須單獨(dú)輸注,以避免發(fā)生此配伍禁忌導(dǎo)致的ADR[21]。(4)因該藥過(guò)敏性休克報(bào)道已有7例,所以在不具備良好監(jiān)護(hù)和搶救的條件下,過(guò)敏體質(zhì)和老年人應(yīng)盡量避免使用。(5)環(huán)磷腺苷葡胺用藥時(shí)應(yīng)注意關(guān)注輔料是否含有右旋糖酐和甘露醇,若有該成分,要注意觀察,備好相應(yīng)急救用品。
3.4本研究的缺陷
由于條件限制,本次研究?jī)H檢索CJFD、萬(wàn)方數(shù)據(jù)庫(kù)和VIP,未能向相關(guān)廠家及ADR監(jiān)測(cè)中心等相關(guān)部門查詢環(huán)磷腺苷葡胺致ADR的信息,因而樣本量偏少,在一定程度上影響了本研究的論證強(qiáng)度。
綜上所述,環(huán)磷腺苷葡胺目前在多種疾病中使用,但其發(fā)生的過(guò)敏性休克和嚴(yán)重過(guò)敏樣反應(yīng)不容忽視,臨床使用時(shí)應(yīng)嚴(yán)格按說(shuō)明書規(guī)定的適應(yīng)證和用法用量給藥,控制給藥速度,避免不合理的聯(lián)合用藥;使用前注意詢問(wèn)過(guò)敏史,對(duì)老人和有藥物過(guò)敏史的患者要提高警惕,同時(shí)對(duì)輔料中含右旋糖酐或甘露醇的藥品,要注意觀察ADR,做好急救準(zhǔn)備。
[1]黃岳寧.環(huán)磷腺苷葡胺致過(guò)敏反應(yīng)2例[J].醫(yī)學(xué)信息,2013,26(7):479.
[2]韋又嘉.注射用環(huán)磷腺苷葡胺致嚴(yán)重過(guò)敏反應(yīng)1例[J].中國(guó)藥物警戒,2013,10(8):511.
[3]陳春枚,費(fèi)燕.注射用環(huán)磷腺苷葡胺致過(guò)敏性休克1例[J].中國(guó)醫(yī)院藥學(xué)雜志,2011,31(18):1 566.
[4]宋愛(ài)麗,劉君.環(huán)磷腺苷葡氨致過(guò)敏性休克1例[J].藥物流行病學(xué)雜志,2012,21(10):487.
[5]鄭德泉,董閩田.環(huán)磷腺苷葡胺滴注致速發(fā)過(guò)敏性休克1例[J].臨床軍醫(yī)雜志,2011,39(5):912.
[6]王萍,沈潔,孔飛飛,等.靜脈滴注環(huán)磷腺苷葡胺注射液致過(guò)敏1例[J].藥學(xué)實(shí)踐雜志,2015,33(6):575.
[7]李洪杰.環(huán)磷腺苷葡胺過(guò)敏1例[J].新醫(yī)學(xué),2005,36(11):646.
[8]鮑隆梅,劉俊.注射用環(huán)磷腺苷葡胺致過(guò)敏反應(yīng)1例[J].山西醫(yī)藥雜志,2015,44(4):487.
[9]石壬偉.環(huán)磷腺苷葡甲胺致1例速發(fā)型過(guò)敏型休克[J].藥學(xué)與臨床研究,2011,19(4):365
[10]趙樹芬,唐福愛(ài).1例環(huán)磷腺苷葡胺致過(guò)敏性休克的護(hù)理[J].現(xiàn)代中西醫(yī)結(jié)合雜志,2008,17(3):385.
[11]白楊.環(huán)磷腺苷葡氨致過(guò)敏性休克1例[J].中國(guó)實(shí)用鄉(xiāng)村醫(yī)生雜志,2007,14(1):32.
[12]田增英.靜脈滴注環(huán)磷腺苷葡胺致嚴(yán)重神經(jīng)、心臟不良反應(yīng)1例[J].中國(guó)藥物經(jīng)濟(jì)學(xué),2014,9(11):59.
[13]闞全程.臨床藥學(xué)高級(jí)教程[M].北京:人民軍醫(yī)出版社,2014:456、460、462.
[14]徐慧敏,蔡宏文,李天元,等.磺胺類藥物過(guò)敏和交叉過(guò)敏的研究進(jìn)展[J].中國(guó)藥理學(xué)與毒理學(xué)雜志,2012,26(6):897.
[15]李全生,朱曉明,魏慶宇.2014藥物過(guò)敏的國(guó)際共識(shí)解讀[C]//第七次全國(guó)中西醫(yī)結(jié)合變態(tài)反應(yīng)學(xué)術(shù)會(huì)議、遼寧省首屆中西醫(yī)結(jié)合變態(tài)反應(yīng)學(xué)術(shù)會(huì)議、沈陽(yáng)軍區(qū)首屆免疫學(xué)及變態(tài)反應(yīng)學(xué)術(shù)會(huì)議論文匯編.沈陽(yáng):中國(guó)中西醫(yī)結(jié)合學(xué)會(huì),2015:263.
[16]王井玲,趙東瀛.注射用環(huán)磷腺苷葡胺致急性前壁心肌梗死1例[J].醫(yī)藥導(dǎo)報(bào),2016,35(1):99.
[17]張峻.臨床靜脈用藥調(diào)配方法與配伍禁忌速查手冊(cè)[M].北京:人民衛(wèi)生出版社,2012:56.
[18]楊燕妮,馮雪梅,楚莉輝,等.85例右旋糖酐40注射劑致嚴(yán)重不良反應(yīng)報(bào)道分析[J].臨床合理用藥雜志,2016,9(6C):175.
[19]李奎春.藥源性過(guò)敏性休克300例分析[J].中國(guó)藥物經(jīng)濟(jì)學(xué),2016,11(2):27.
[20]楊麗娟.減少輸注環(huán)磷腺苷葡胺副作用的措施及效果觀察[J].醫(yī)療裝備,2014,27(11):26.
[21]王艷,沈佳炎.靜脈滴注環(huán)磷腺苷葡胺注射液致不良反應(yīng)3例[J].心腦血管病防治,2015,15(3):256.
(編輯:晏妮)
LiteratureAnalysis ofAdverse Drug Reactions Induced by MeglumineAdenosine Cyclophosphate
HONG Wenying1,2,WANG Shurong3(1.Chengdu Wenjiang District People’s Hospital,Chengdu 610000,China;2.College of Pharmacy,Southwest Medical University,Sichuan Luzhou 646000,China;3.Dept.of Pharmacy,the Affiliated Hospital of Southwest Medical University,Sichuan Luzhou 646000,China)
OBJECTIVE:To investigate the characteristics and general regularity of adverse drug reaction(ADR)induced by meglumine adenosine cyclophosphate,and to provide reference for rational drug use in the clinic.METHODS:Using“meglumine adenosine cyclophosphate”and“ADR”as keywords,literature were retrieved and analyzed statistically from CJFD,Wanfang database and VIP database according to inclusion and exclusion criteria until Feb.2016.RESULTS:A total of 17 literatures were included,involving 20 patients,with the ratio of male to female was 1∶1.Most patients aged more than 60 years,accounting for 55.00%(11 cases);ADRs often occurred within 30 min during medication(18 cases,90.00%);14 cases(70.00%)were caused by drug combination;ADRs involved multiple organs/systems,the most common damages were systemic injury(12 cases,27.91%),skin and its appendants(11 cases,25.58%),and the most serious were anaphylactic shock(7 cases).CONCLUSIONS:Clinical staffs should pay attention to ADRs induced by meglumine adenosine cyclophosphate,drug use strictly in accordance with package inserts and its ingredients of excipients,and closely monitor and prevent the occurrence of ADRs.
Meglumine adenosine cyclophosphate;ADR;Literature analysis
R969.3;R972+.1
A
1001-0408(2016)32-4518-04
10.6039/j.issn.1001-0408.2016.32.17
*主管藥師,碩士研究生。研究方向:臨床藥學(xué)。電話:028-82720551。E-mail:Hongyepiao0925@126.com
#副主任藥師,碩士。研究方向:臨床藥學(xué)。電話:0830-3165787。E-mail:wang-shurong@sohu.com
(2016-03-11
2016-08-03)

