利妥昔單抗聯合自體外周血干細胞移植治療中高危及復發彌漫大B細胞淋巴瘤的療效觀察
曹俊杰,陸瀅,馬俊霞,張丕勝,劉旭輝,杜小紅,陳冬,裴仁治
·臨床研究·
利妥昔單抗聯合自體外周血干細胞移植治療中高危及復發彌漫大B細胞淋巴瘤的療效觀察
曹俊杰,陸瀅,馬俊霞,張丕勝,劉旭輝,杜小紅,陳冬,裴仁治
目的觀察利妥昔單抗聯合自體外周血干細胞移植(ASCT)治療中高危及復發彌漫大B細胞淋巴瘤(DLBCL)的臨床療效。方法回顧分析24例接受利妥昔單抗聯合ASCT治療的DLBCL患者的臨床資料。結果初治17例,復發7例;初診時臨床分期Ⅱ期9例,Ⅲ期11例,Ⅳ期4例;生發中心型11例,非生發中心型13例;15例患者伴有B癥狀;IPI評分高危6例,中危18例。所有患者均移植成功,無嚴重不良反應。初治患者移植前3例PR患者移植后均達到CR,復發患者移植前3例PR患者移植后2例PR患者再次達到CR。移植前疾病達CR組復發率低于移植前疾病達PR組(<0.05),且移植前疾病達CR組無病生存高于移植前疾病達PR組(<0.05)。結論利妥昔單抗聯合ASCT作為鞏固治療時,移植前處于CR的患者可獲得了長期生存。
淋巴瘤,彌漫大B細胞;利妥昔單抗;自體外周血干細胞移植
NHL的標準治療[4-5]。復發是移植失敗的主要原因,主要與移植物中及患者體內殘留的腫瘤細胞有關。利妥昔單抗有助于清除患者體內及移植物中殘留的淋巴瘤細胞,減少疾病復發。本文回顧分析利妥昔單抗聯合ASCT治療高危及復發DLBCL的療效及安全性,報道如下。
1 資料與方法
1.1 一般資料選擇2010年1月至
2014年12月在寧波大學附屬鄞州醫院收治的DLBCL患者24例,均經病理確診,無心、肝、肺、腎等重要臟器功能不全。其中男10例,女14例;中位年齡42(23~62)歲;初治17例,復發7例;初診時臨床分期Ⅱ期9例,Ⅲ期11例,Ⅳ期4例;生發中心型11例,非生發中心型13例;15例患者伴有B癥狀;IPI評分高危6例,中危18例。
1.2 移植前治療及狀態17例初治患者接受CHOP±利妥昔單抗4~6個療程化療,其中14例患者達到完全緩解(CR),3例達到部分緩解(PR)。7例復發患者接受3~6個療程二線化療方案,4例患者再次達到CR,3例達到PR。1.3外周血干細胞的動員采用環磷酰胺4 g/m2+利妥昔單抗375 mg/m2化療,白細胞降至最低加用粒細胞集落刺激因子(5~10 g/kg)動員外周血干細胞,當白細胞>4×109/L使用COBESpectra細胞分離機采集外周血造血干細胞。
1.4 預處理方案采用BEAM+R(司莫司汀250mg/m2×1d+阿糖胞苷400mg/m2× 4 d+依托泊苷200 mg/m2×4 d+馬法蘭140 mg/m2×1 d+利妥昔單抗375 mg/m2×―1、+8 d)方案預處理化療。
1.5 隨訪和療效評價移植后第1年每3個月1次、第2年每6個月1次、第3年及以后每年1次對患者進行淺表淋巴結B超、頸部+胸部及全腹部CT或PET/CT、乳酸脫氫酶、2微球蛋白檢查。療效根據WHO的評價標準分為CR、 PR、穩定和進展。總生存(OS)時間從診斷明確開始計算直到患者死亡或最后1次隨訪;無病生存(EFS)時間從疾病緩解直到出現新的進展、復發、死亡或最后1次了解疾病無進展。1.6統計方法使用SPSS 19.0統計軟件進行分析。兩組樣本中位數比較采用Mann-Whitney檢驗;率的比較采用檢驗;生存情況通過Kaplan-Meier方法分析。<0.05為差異有統計學意義。
2 結果
2.1 造血干細胞均采集到足夠的造血干細胞,中位采集次數為2次。采集到單個核細胞(MNC)中位數為7.75(4.23~13.58)×108/kg,CD34+細胞中位數為3.92(1.68~11.26)×106/kg。
2.2 移植后造血功能重建患者均成功植活,中性粒細胞數(ANC)>0.5×109/L,中位時間為11(9~15)d;連續3 d不輸注血小板(PLT)情況下PLT>20×109/L,中位時間為12(10~17)d。
2.3 移植相關并發癥患者在預處理期間均出現不同程度的胃腸道反應,主要表現為惡心、嘔吐,8例患者出現腹瀉,給予對癥處理后均減輕。骨髓抑制期間14例繼發輕中度感染,3例繼發肺部感染,1例臨床診斷肺部真菌感染,1例繼發急性中耳炎,抗感染治療后均治愈。6例發生口腔黏膜炎,應用B族維生素,加強口腔護理等措施均治愈。6例出現輕度肝功能異常。所有患者未出現心、肺、腎等重要臟器的功能損傷,以及利妥昔單抗相關的過敏表現。
2.4 療效評估初治患者移植前3例PR患者移植后均達到CR。復發患者移植前3例達到PR,移植后2例PR患者再次達到CR。患者中位隨訪時間19.5(6~54)個月,5例在移植后3~13個月復發,其中4例在復發后3~6個月死亡;其余19例患者均無病存活,2年OS及EFS分別為83.3%和79.2%。移植前疾病達CR 18例,移植后中位隨訪時間26(6~54)個月,復發1例,其余17例均EFS,中位EFS為26個月。移植前疾病達PR6例,移植后復發4例,中位EFS和OS分別為5.5和11.5個月。移植前疾病達CR組復發率低于移植前疾病達PR組<0.05),且移植前疾病達CR組EFS高于移植前疾病達PR組<0.05)。見圖1。
3 討論
ASCT是治療高危和復發惡性淋巴瘤的有效手段。Ladelto等[6]報道,采用利妥昔單抗聯合造血干細胞移植治療NHL,65%患者獲得臨床和分子生物學緩解,4年的EFS和OS率為67%和85%。本組DLBCL患者IPI評分均為中高危,29.2%為復發患者,2年OS及PFS分別為83.3%和79.2%。提示利妥昔單抗聯合ASCT可以改善患者生存。
移植后復發是嚴重影響患者長期生存的重要因素。復發的原因可能與移植物中或體內殘存的惡性淋巴瘤細胞有關。利妥昔單抗可通過抗體依賴的細胞毒性作用、補體依賴的細胞毒作用誘導腫瘤細胞凋亡及干擾抗凋亡途徑增加淋巴瘤細胞對化療的敏感性等機制來殺傷腫瘤細胞。Galimberti等[7]報道經利妥昔單抗的體內凈化,80%~90%的造血干細胞采集產物檢測不出腫瘤細胞。本研究證實,利妥昔單抗體內凈化對造血干細胞采集量和造血干細胞功能無不良影響。本研究顯示,移植前疾病達CR的18例患者,移植后中位隨訪26個月,僅1例患者復發,當利妥昔單抗聯合ASCT治療時,移植前處于緩解的患者可獲得長期生存,達到了基本治愈水平,提高了治愈率。而移植前疾病達PR的6例患者,移植后5例患者再次達到CR,中位隨訪11.5個月,4例患者再次復發。移植前是否達到CR不但影響患者移植后總體生存率,也是移植后復發的獨立危險因素[8]。本組PR患者移植后PFS和OS低于文獻[9-10]報道,可能與患者移植前反復多次應用利妥昔單抗、腫瘤細胞耐藥有關。
本組患者不良反應主要表現為胃腸道反應、黏膜炎,骨髓抑制期間14例繼發輕中度感染,給予對癥支持治療均能順利完成治療,無治療相關死亡病例發生。利妥昔單抗聯合ASCT能在造血干細胞動員和采集過程中達到體內凈化的目的,在預處理過程中達到清除腫瘤殘留病變的作用。當利妥昔單抗聯合ASCT作為鞏固治療時,移植前處于緩解的患者可獲得了長期生存,提高了治愈率;當利妥昔單抗聯合ASCT作為強化治療,移植前達到PR的患者,自體移植后能使這些患者不用反復化療,提高了生活質量。
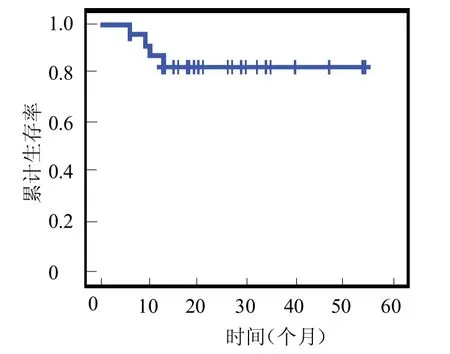
圖1 24例非霍奇金淋巴瘤患者生存曲線
[1]FeugierP,VanHoofA,SebbanC,etal.LongtermresultsoftheR-CHOPstudyinthetreatment of elderly patients with diffuse large B-cell lymphoma:astudyby the Groupe d' EtudedesLymphomesdeL'Adulte[J].JClin Oncol,2005,23(18):4117-4126.
[2]Pfreundschuh M,Trumper L,Osterborg A,et al.CHOP-like chemotherapy plus rituximab versusCHOP-like chemotherapy alone in young patients with goodprognosis diffuse large B-cell lymphoma:a randomizedcontrolledtrial by the MabTheraInternational Trial(MInT)Group[J].Lancet Oncol,2006,7(5):379-391.
[3]Sehn LH,Berry B,Chhanabhai M,et al. The revised International Prognostic Index (R-IPI)isabetter predictorof outcomethan thestandardIPIforpatientswithdiffuselarge B-cell lymphoma treated with R-CHOP [J].Blood,2007,109(5):1857-1861.
[4]Milpied N,DeconinckE,Gaillard F,et al. Initial treatment of aggressive lymphoma withhigh-dose chemotherapy and autolog ousstem-cellsupport[J].NEnglJMed,2004, 350(13):1287-1295.
[5]Dilhuydy MS,Lamy T,Foussard C,et al. Front-line High-Dose Chemotherapy with Rituximab Showed Excellent Long-Term Survival in Adults with Aggressive Large B-Cell Lymphoma:FinalResultsof aPhase II GOELAMS Study[J].Biol Blood Marrow Transplant,2010,16(5):672-677.
[6]LadeltoM,CorradiniP,Vallel S,et al.High rate of clinical and molecular remissions in follicular lymphoma patients receiving high-dose sequential chemotherapy and autograftingatdiagnosis:amulticenter,prospectivestudybythe Gmppoltaliano Trapiante Midollo Osseo(GITMO)[J].Blood, 2002,100(5):1559-1565.
[7]Galimberti S,GuerrinFi,MorabitoF,et al. Quantitative molecular evaluation in auto transplantprogramsforfollicularlymphoma: efficacy of in vivo purging by Rituximab [J].Bone Marrow Transplantation,2003, 32(1):57-63.
[8]梁賾隱,岑溪南,邱志祥,等.利妥昔單抗聯合自體外周血干細胞移植治療彌漫大B細胞淋巴瘤的療效觀察[J].中華血液學雜志,2012,33(12):1033-1037.
[9]蔡宇,王椿,姜杰玲,等.抗CD20單克隆抗體聯合自體外周血干細胞移植治療非霍奇金淋巴瘤的臨床研究[J].白血病·淋巴瘤,2010,19(4):203-206.
[10]HorwitzSM,NegrinRS,BlumeKG,el a1. Rituximab as adjuvant to high-dose therapy andautologous hematopoielic cell transplantationforaggressivenon-HodIgkinlymphmna [J].Blood,2004,103(3):777-783.
10.3969/j.issn.1671-0800.2016.12.004
R733.4
A
1671-0800(2016)12-1556-02彌漫大B細胞淋巴瘤(DLBCL)是成人最常見的非霍奇金淋巴瘤,標準治療方案為R-CHOP,總有效率70%以上[1-2];但仍有超過1/3的患者復發,復發后中位生存期僅3~4個月。淋巴瘤國際預后指數(IPI)評分為中/高危和高危的患者的長期生存率分別是46%和32%[3]。對于復發、初發難治、進展的高度惡性淋巴瘤患者單純放化療效果不佳,高劑量化療聯合自體造血干細胞移植(ASCT)成為對化療敏感的復發或難治侵襲性
2016-10-08
(本文編輯:孫海兒)
315040寧波,寧波大學附屬鄞州醫院
裴仁治,Email:peirz @163.com

