中醫藥調控心衰細胞PKC信號通路的現狀及思考*
薛一濤焦華琛劉 鵬劉廣志陳 煒崔文竹
(1.山東中醫藥大學附屬醫院,山東 濟南 250000;2.山東中醫藥大學,山東 濟南 250000)
·綜 述·
中醫藥調控心衰細胞PKC信號通路的現狀及思考*
薛一濤1焦華琛1劉 鵬2劉廣志2陳 煒2崔文竹2
(1.山東中醫藥大學附屬醫院,山東 濟南 250000;2.山東中醫藥大學,山東 濟南 250000)
近年來,隨著對疾病發生發展機制研究的不斷深入,中醫藥對于心衰的臨床研究已經從單純的臨床觀察,證型分類,逐漸深入到中醫藥對于細胞分子生物學影響的研究上。DAG/PKC信號轉導通路在細胞內信號調控網絡中具有重要作用,是參與細胞生長、增殖、分裂調控的重要信號通路之一。當發生心衰時會不同程度地刺激細胞內PKC信號通路的表達,激活心臟的肥大信號傳導加重心衰。
中醫藥 PKC 信號通路 心衰
心力衰竭(CHF)是指各種心臟結構或功能性疾病導致心室充盈及(或)射血能力受損而引起的一組綜合征[1]。目前認為多種因素參與了心衰的發生發展,如神經內分泌學說、細胞凋亡學說、細胞信號通路等。隨著研究的不斷深入,發現PKC信號通路的過度激活影響著心肌重構加重心衰,但現有研究證據表明PKC信號通路抑制劑多為非特異性,且副作用大,而特異性PKC信號通路抑制劑尚在研究中,且迄今無成功應用到臨床的先例。故應用中藥來干預PKC信號通路的研究正在逐步展開,并且近年來顯示出獨特的優勢并取得了一定成果。現綜述如下。
1 PKC信號轉導途徑結構、激活、表達
1.1 PKC結構 PKC家族絲/蘇氨酸激酶的原型被Nishizuka等在1977年首次發現。PKC參與了大量細胞功能和信號轉導系統,調控細胞的增殖、分化和細胞死亡。其由一條肽鏈組成[2],相對分子質量在80~90 kDa之間,按分子結構分為保守區和可變區,按功能分為調節區和催化區 。目前已發現12種PKC的同工酶,根據其結構特點和輔因子不同可大致分為3類[3](見圖1):1)對Ca2+和DAG兩者均敏感的經典型PKC(cPKC),包括α、βI、βII、γ,依賴磷脂酰絲氨酸(PS)、Ca2+、DAG或其類似物佛波酯(PMA)激活;2)對Ca2+不敏感而對DAG敏感的新型PKC(novel,nPKCs),由δ、ε、η、和θ組成,激活只依賴DAG,不需要Ca2+參與;3)對Ca2+和DAG均不敏感的非典型PKC(atypical aPKCs),由ξ、ι、λ組成,需磷脂類物質激活而不依賴Ca2+、DAG及PMA[4]。
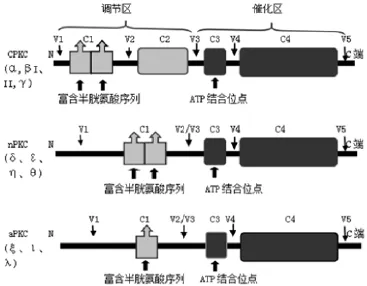
圖1 PKC結構簡圖
1.2 PKC信號通路的激活表達 在生理狀態下PKC主要是由DAG激活[5-6]。它可直接激活PKC,DAG與被激活的PKC的C1位結合,C2位與磷脂酰絲氨酸結合后轉位到細胞膜,在膜磷脂的作用下,構象發生改變,PDK1磷酸化PKC蘇氨酸位點來使PKC的處于激活構象[7]。此時酶被激活,從而細胞內生物信息的代謝,調節基因表達、影響細胞周期和細胞凋亡、控制神經傳導等[8]。然而由PLC催化水解產生的DAG會迅速被代謝掉,用來維持PKC長期效應DAG主要由PLC催化質膜上的磷脂酰膽堿斷裂產生[9]。上述激活過程通常是可逆的。PKC激活后還需要進一步轉位與蛋白激酶C受體(RACKS)等結合來發揮催化作用[10]。每個PKC亞型都有自己的特定RACK序列。此過程可能使PKC處于持續激活狀態,產生長期細胞反應[11]。PKCδ的激活與細胞周期的抑制作用有關,是介導促凋亡信號通路的重要亞型[12]。

圖2 DAG/PKC信號通路激活過程
2 中藥對心衰細胞PKC的影響
已有研究證實,單味中藥及其提取物(如黃芪提取液、人參皂苷、姜黃素[12]等)及一些中藥復方(益氣活血復方、葶藶生脈方、參元丹)對PKC信號通路有良好的抑制作用,能夠提高胞液PKC信號通路活性,降低胞膜PKC信號通路活性,使胞液與胞膜PKC活性比顯著提高,抑制PKC基因過度表達,預防心室重構。
2.1 單味中藥對心衰細胞PKC的影響 近來諸多學者廣泛開展單味中藥提取物對心衰細胞中PKC信號通路影響的研究,并探討其發生機制,發現單味中藥及其提取物能夠通過抑制心肌細胞中PKC各種亞型的過量表達,來改善因藥物及缺血造成的心肌細胞損傷,效果顯著。在充血性心力衰竭中,分布在膜、核-細胞骨架部分的ε、β1和β2-PKC活性明顯增加[13]。在擴張性心肌病和缺血性心肌病引起的心衰中α、β1和β2-PKC活性提高,ε-PKC未見明顯改變[14]。抑制α-PKC其能夠增加心肌收縮力并防止心肌梗死后心力衰竭的發生[15]。β2-PKC參與心衰與心室肥厚的發病中[16-17]。Ferreir等亦發現在人和實驗動物中都發現心肌細胞發生衰竭時β2-PKC活性顯著增加[18]。β2-PKC選擇性抑制劑能夠抑制病理性心臟重構,改善心衰大鼠心臟射血分數,保護心臟的功能[19]。目前基本證實β2-PKC參與心肌肥厚與心衰過程。過去普遍認為ε-PKC參與心肌缺血預處理中心肌保護作用的調節。然而,最近研究表明ε-PKC還參與心室增厚與心衰的發病[20],在心力衰竭進展中ε-PKC與心肌增厚、β2-PKC與心衰有關。如孫宇田等采用結扎左冠狀動脈前降支(LAD)的方法建立心肌梗死后心室重塑模型,將術后24 h存活的36只大鼠分為假手術組 (給予生理鹽水2 mL/d腹腔注射)、模型組(給予生理鹽水2 mL/d腹腔注射)和黃芪治療組(給予黃芪注射液6 g/d,即2 mL/d腹腔注射)。6周后采用Western bloting法檢測心肌細胞中PKCα和PKCε的表達水平,發現黃芪注射液梗死后大鼠的心室重塑具有改善作用,其機制可能通過上調PKCε、抑制PKCα表達而實現的[21]。張英妮通過Langendorff離體灌流裝置,觀察離體心臟在排除神經、體液因素影響的條件下人參皂苷對阿霉素造成的心肌損傷的保護作用,采用RT-PCR對PKC mRNA序列檢測,繼而使用Western Blot方法對其蛋白表達進行檢測,最終得出阿霉素對心肌毒性作用主要表現在使心肌細胞內PKC信號通路介導的鈣離子超負載,造成心肌細胞內原鈣離子的動態平衡被打亂造成心肌損傷,長期作用導致心衰。而人參皂苷對損傷的心肌細胞具有保護作用,并且首次證明了人參二醇皂苷單體Rb1對由阿霉素造成的心肌毒性損傷具有良好的保護[22]。楊競發現白藜蘆醇(Res)對鏈脲佐菌素(STZ)所致糖尿病心肌病的PKC-β2的表達具有抑制作用[23]。陳炬發現白屈菜紅堿 (是傳統天然藥用植物白屈菜的主要有效成分之)能夠抑制高糖誘導的乳鼠心肌細胞形態和功能的改變,并且抑制PKC-α、PKC-β2的表達和活性,對高糖環境中的心肌細胞具有保護作用。與正常心肌細胞比較,心衰肌細胞中PKC的活性明顯增加[24]。
2.2 中藥復方對心衰細胞PKC的影響 同樣研究者通過對臨床治療心衰的經驗效方進行深入研究發現,中藥組方能夠下調PKC水平影響其傳導通路,以此來改善和糾正心衰。研究中藥組方主要集中在益氣、溫陽[25]、活血方面。如張艷采用結扎健康雄性SD大鼠冠狀動脈配合饑餓、游泳等方法造成慢性心衰的動物模型,采用ABC免疫組化方法測定心肌組織中AngⅡ和PKC的含量。結果顯示采用益氣活血復方(黃芪40 g,人參15 g,紅花15 g,丹參15 g,三七5 g,益母草20 g組成)干預的慢性心衰大鼠心肌組織血管緊張素Ⅱ(AngⅡ)和蛋白激酶C(PKC)表達量降低,說明益氣活血復方可能通過降低AngⅡ水平達到抑制RAS系統作用,下調PKC水平影響其傳導通路,以此來改善和糾正心衰[26]。周樺等研究益氣溫陽的葶藶生脈方(紅參、葶藶子、五味子、麥冬、赤芍、生黃芪、益母草、丹參、紅花組成)對心衰大鼠心肌細胞中AT1受體及PKC的影響。以免疫組化法觀察心肌組織中AT1受體和傳導因子PKC的表達,發現葶藶生脈方可以下調心肌組織中AT1與PKC受體的表達,抑制RAS系統的過度激活,以達到抗心力衰竭的作用[27]。尚菊菊等應用免疫組化法觀察PKC及HSP70表達,發現參元丹(黨參、元參、丹參、地龍、土元、水蛙、元胡組成)能夠代替心絞痛的缺血、缺氧的刺激,減小心肌梗死面積,具有心臟保護作用。在假性缺血預處理組的心肌組織中偶見微弱的一處表達。缺血預處理組和藥物預處理+缺血預處理組的大鼠心肌組織中PKC大量的表達,藥物預處理組大鼠心肌組織的PKC表達充分,提示PKC在參元丹的藥理性預適應樣心肌保護過程中起作用[28]。王峰同樣也發現芪桂益脈靈[黃茂、桂枝、黨參、五味子、炒棗仁苦參、三七(單包)、黃連、龍齒等十味中藥組成]能夠提高細胞膜上蛋白激酶C的活性表達,對大鼠心肌缺血再灌注損傷具有保護作用[29]。PKC過度表達降低了心肌收縮功能,導致了心肌肥厚和心力衰竭[30]。在心肌肥厚形成過程中總ε-PKC量增高,過渡為慢性心衰后總PKC顯著減少,PKC抑制劑干預后,PKC趨于恢復正常水平,提示PKC活性增強能促進心肌肥厚的形成,PKC具有刺激“生理性”生長的潛力、維持心肌收縮功能的作用,而在心衰進展中PKC可能起負向調節和保護心臟的作用[31]。
綜上研究表明,單味中藥及其提取物對心肌細胞損傷確實有改善作用,研究者對于各藥物及組方的作用機制也有相應的分析、討論,通過事實證明中藥可以直接或間接抑制心肌細胞中PKC信號通路的表達,與PKC抑制劑的理論符合。例如:燈盞花素(Scutellarin)是一個非競爭性蛋白激酶C抑制劑[32],可抑制心肌細胞的Ca2+內流,同時開放心室肌細胞的K+通道,促進K+外流,心肌細胞產生負性肌力作用,減慢心率,同時可以抑制基因Caspase-3 mRNA的表達,在心肌缺血-再灌注過程中保護心肌細胞。并且有擴張血管、增加血流量、降低外周血管阻力、對抗垂體后葉素所致的心肌缺血缺氧等多種作用。
3 結語與展望
PKC信號通路與心衰的發生發展有著千絲萬縷的聯系,研究PKC信號通路與心衰的相互聯系目的在于臨床應用PKC抑制劑來防治心衰。目前,對PKC信號通路抑制劑的研究取得一定的進展,研究也在不斷深入。但特異性PKC信號通路抑制劑的研究尚在實驗驗證中,非特異性PKC抑制劑副作用大[33],使得長期研究、應用PKC抑制劑受到限制。相比之下,中醫學有著自己獨特的醫療體系,立足于整體觀念,采用辨證論治的方法對機體進行系統全面的調節,來維持人體陰陽平衡。隨著中醫學對于心衰的不斷認識,對心力衰竭的研究已經從單純的臨床觀察,證型分類,逐漸深入到中醫藥對于細胞分子生物學影響的的研究上,發現中醫藥能夠正向影響心衰心肌細胞中分子機制。
心力衰竭的發生發展是一個繁雜的過程,有多種細胞信道轉導途徑協同參與,各種信號途徑之間存在交互聯系,互相影響,各種信號通路之間是如何影響的,是否所有通路可以共同組成一個大的通路來作用于心力衰竭的發病中,有待于深入研究。我們要應用日新月異發展的現代化血管病學理論和技術,繼承開發和研究有效的傳統醫學理論和經驗,以提高臨床醫療水平和科學技術水平,融入世界醫藥學。
[1] 中華醫學會心血管病學分會,中華心血管病雜志編輯委員會.慢性心力衰竭診斷治療指南[J].中華心血管病雜志,2007,36(12):1076-1095.
[2] Azzi A,Boscoboinik D,Hensey C.The protein kinase C family[J].Eur J Biochem 1992,208(3):547-557.
[3] Koya D.Dual protein kinase C alpha and beta inhibitors and diabetic;kidney disease:a revisited therapeutic;target for future clinical trials[J].Diabet Investig,2014,5(2):47-48.
[4] Steinberg SF,Goldberg M.Rybin V0.Protein kinase C isoform diversity in the heart[J].J Mol Cell Cardiol,1995,27:141.
[5] Rosen DM,Das K,Grimes KV.Protein kinase C,an elusive therapeutic;target[J].Nat Rev Drug Discov,2012,11(12):937-957.
[6] Way KJ,Katai N,King GL.Protein kinase C and the development of diabetic;vascular complivations[J].Diabet Med,2001,18(12):941-959.
[7] Bynagari-Settipalli YS,Chari R,Kilpatrick L,et al.Protein kinase C-possible therapeutic target to treat cardiovascular diseases[J].Cardiovasc Hematol Disord Drug Targets,2010,10(4):292-308.
[8] Zheng H,Liu,J,Liu C,et al.Calcium-sensing receptor activating phosphorylation of PKC delta translocation on mitochondria to induce cardiomyocyte apoptosis during ischemia/ reperfusion[J].Molecular and Cellular Biochemistry,2011,358(1-2):335-343.
[9] 何華.心肌肥厚、肥厚-逆轉和慢性心力衰竭心肌中PKCε信號復合物的蛋白質組學研究[J].中國協和醫科大學,2006,48(9):101-102.
[10]陳文政,柏樹令.蛋白激酶C(PKC)與心衰[J].解剖科學進展,2001,7(2):141.
[11]孫宇田,劉聰聰,徐萌,等.黃芪對心肌梗死后大鼠心室重塑的改善作用及其對蛋白激酶C表達的影響[J].吉林大學學報,2015,41(4):769-773.
[12]Zheng H,Liu,J,Liu C,et al.Calcium-sensing receptor activating phosphorylation of PKC delta translocation on mitochondria to induce cardiomyocyte apoptosis during ischemia/ reperfusion[J].Molecular and Cellular Biochemistry,2011,358(1-2):335-343.
[13]Gu X,Sanford PB.Increased protein kinase C and isozyme redistribution in pressure-oberbad cardiac hypertrophy in the rat[J].Circ Res,1994,75:926.
[14]Nancy B,Richard A,Walsh MD,et al.Increased protein kinase C activity and expression of Ca2+-senditive isoforms in failing human heart[J].Circulation,1999,26(3):384
[15]Hambleton M,York A,Sargent MA,et al.lnducible and myocytespecific inhibition of 1PKCalpha enhances cardiac contractility and protests against infarction-induced heart failure[J].Am J 1Physiol Heart Circ Physiol,2007,293(6):113768-113771
[16]Wakasaki H,Koya D,Schoen FJ,et al.Targeted overexpression of protein kinase C beta 2 isoform in myocardium causes cardiomyopathy [J].Prod Natl Acad Sci USA,1997,94:9320-9325.
[17]Bowling N,Walsh RA,Song G,et al.Increased protein kinase C activity and expression of Ca2+-sensitive isoforms in the failing human heart[J].Circulation,1999,99(3):384-391.
[18] Ferreira JCB,Boer BN,Grinberg M,et al.Protein quality control disruption by PKC beta II in heart failure;rescue by the selective PKC betaⅡInhibitor,betaⅡV5-3[J].PLOS One,2012,7(3):e33175
[19]Palaniyandi SS,Batista Ferreira JC,Brum PC,et al.PKC beta 11 inhibition attenuates myocardial infarction induced heart failure and is associated with a reduction of fibrosis and proinflammatory responses[J],Journal of Cellular and Molecular Medicine,2011,15(8):1769-1777.
[20]Inagaki K,Iwanaga Y,Sarai N,et al.Tissue angiotensin II during progression or ventricular hypertrophy to heart failure in hypertensive rats;differential effects on PKC epsilon and PKC beta[J].J Mel Cell Cardiol,2002,34(10):1377-1385.
[21]孫宇田,劉聰聰,徐萌,等.黃芪對心肌梗死后大鼠心室重塑的改善作用及其對蛋白激酶C表達的影響[J].吉林大學學報:醫學版,2015,57(4):76.
[22]張英妮.阿霉素導致大鼠心肌鈣紊亂損傷及人參皂甙Rb1單體對其的保護作用[D].長春:東北師范大學,2008.
[23]楊競.白藜蘆醇抗糖尿病心肌病心肌纖維化作用及機制研究[D].遵義:遵義醫學院,2013.
[24]陳炬,張文斌,王敏,等.白屈菜紅堿對高糖培養的乳鼠心肌細胞形態和功能的影響[J].浙江醫學,2009,31(8):42.
[25]楊學偉,郭云良,崇卓,等.四逆湯(附子、干姜、甘草)對腎血管性高血壓大鼠血壓調節作用的實驗研究[J].中華高血壓雜志,2007,15(3):206-209.
[26]張艷,楊碩,龐敏,等.益氣活血復方對慢性心衰大鼠心肌組織AngⅡ及PKC的影響[J].中華中醫藥雜志,2008,23(11):999-1001.
[27]郭秋紅,彭雪梅,趙淑明,等.葶藶生脈方對心衰大鼠AngⅡ及其受體信號傳導的影響[J].中藥新藥與臨床藥理,2010,21(3):260-262.
[28]尚菊菊,李愛勇,楊洪志,等.參元丹藥理預適應對大鼠缺血再灌注心肌梗死面積、蛋白激酶C及熱休克蛋白70的影響[J].中華中醫藥雜志,2011,126(8):1730-1733.
[29]王峰.芪桂益脈靈對急性缺血再灌注大鼠心肌細胞蛋白激酶C的影響[D].哈爾濱:黑龍江中醫藥大學,2009.
[30]高玖鳴,宋昌旭,張軍,等.腺病毒介導的心肌蛋白激酶Cε基因轉移導致心肌損害[J].中國分子心臟病學雜志,2004,4(4):216-220.
[31]何華,高玖鳴,王文,等.心肌肥厚、肥厚-逆轉和慢性心力衰竭心肌中PKε信號復合物的蛋白質組學研究[J].中國醫藥,2009,4(9):655-658.
[32]周莉.燈盞花素的心腦血管藥理及臨床研究進展[J].中醫藥信息,2013,30(6):134-136.
[33]李鑫,董朝俠,蔡蘭英,等.中藥干預糖尿病鼠腎臟蛋白激酶C信號通路的研究進展[J].中國實驗方劑學雜志,2015,21(6):230-234.
R285
A
1004-745X(2016)12-2298-04
10.3969/j.issn.1004-745X.2016.12.027
2015-07-31)
國家自然科學基金項目(81273703)

