有氧運動通過激活PI3K(p110α)/Akt信號通路保護2型糖尿病小鼠心功能*
林延艷, 趙林雙, 劉 意
(廣州軍區武漢總醫院內分泌科,湖北 武漢 430070)
?
有氧運動通過激活PI3K(p110α)/Akt信號通路保護2型糖尿病小鼠心功能*
林延艷, 趙林雙△, 劉 意
(廣州軍區武漢總醫院內分泌科,湖北 武漢 430070)
目的: 探討高糖狀態下有氧運動對小鼠心功能障礙的作用及相關機制,為糖尿病心功能障礙的運動療法提供理論和實踐依據。方法: 將小鼠分成正常非運動組(NNC組)、正常運動組(ENC組)、糖尿病非運動組(NDM組)和糖尿病運動組(EDM組)。實驗結束后,評估小鼠的心臟功能,觀察心肌組織的病理改變、纖維化情況、ANP的mRNA表達、PI3K(p110α)及Akt的蛋白水平。結果: 超聲心動圖可見糖尿病小鼠心功能降低(P<0.05),運動干預后心功能逐漸恢復(P<0.05)。HE和Masson染色后光鏡下可見NDM組小鼠心肌結構極度紊亂,細胞排列不規整,纖維化程度增加,而EDM組心肌受損程度改善。與NNC組相比,糖尿病小鼠心肌組織中ANP的mRNA表達上調,PI3K(p110α)和Akt的蛋白水平受抑制(P<0.05),級聯失活。與NDM組相比,EDM組ANP的mRNA降低,PI3K(p110α)和Akt的蛋白水平升高(P<0.01)。結論: 糖尿病導致小鼠心肌損害,降低心功能;運動干預可能通過激活PI3K(p110α)/Akt信號通路,緩解高糖導致的心功能障礙,保護心肌細胞。
運動; 心功能; 糖尿病; 心肌
糖尿病(diabetic mellitus,DM)是一類發病機制復雜的疾病,在全球范圍內已成為導致死亡的第3大危險因素。流行病學研究發現,80%以上糖尿病患者死于心血管系統疾病,是非糖尿病人群心血管系統疾病病死率的2~3倍[1]。其中,糖尿病心肌損害是DM常見而嚴重的心血管并發癥,也是心臟疾病的獨立危險因素,已逐漸成為人類健康的重要威脅之一。在糖尿病心肌損害的保護措施中,除藥物干預外,規律性地運動在心肌保護作用中扮演重要的作用。作為DM的一個有效的心臟保護措施,運動能否改善DM誘導的心肌結構和功能損害及其發揮心肌保護作用的機制尚不明確。
在近10年的研究中,研究人員利用基因修飾等工具發現磷脂酰肌醇3-激酶(phosphatidylinositol 3-kinase,PI3K)的p110α/蛋白激酶B(protein kinase B,PKB,又稱Akt)信號通路在心肌細胞生長和生存中扮演的重要作用。PI3K(p110α)不但參與了胰島素及胰島素樣生長因子1(insulin-like growth factor-1,IGF-1)對心臟生長發育的調控,且在鼠類的病理性心肌模型中,PI3K(p110α)還能抑制胚胎基因的重新編碼,模擬運動訓練所帶來的益處,最終延長壽命;而表達顯性負效體PI3K(p110α)的小鼠壽命年限明顯縮短[2];PI3K(p110α)還與改善心臟能量物質供應、增強離體心臟心肌收縮力密切相關[3-5]。此外,PI3K(p110α)的下游Akt激活后也與細胞的各類調控反應相關,包括抑制凋亡,調控細胞增殖、代謝、肥大等[6-8]。但PI3K(p110α)/Akt是否參與運動的DM心肌保護作用目前尚未見到報道。本研究擬在構建糖尿病模型小鼠,通過探索糖尿病狀態下心功能的改變與PI3K(p110α)/Akt信號通路激活的相關性,以進一步了解運動影響心功能的分子機制。
材 料 和 方 法
1 實驗動物
5周齡SPF級C57BL/6小鼠購自武漢大學動物實驗中心,體重13~15 g,實驗動物合格編號為42000500006666。飼養環境為室溫20~24 ℃,相對濕度40%~60%,基礎飼料由實驗動物中心提供,自由攝食飲水,12 h交替照明。
2 主要試劑
鏈脲佐菌素(streptozotocin,STZ)購自Sigma;BCA蛋白定量試劑盒(碧云天生物技術有限公司);抗Akt抗體和抗p-Akt抗體(Cell Signaling Technology);兔抗PI3K(p110α)抗體(武漢三鷹生物技術有限公司);抗GAPDH抗體(杭州賢至生物有限公司);兔抗羊II抗和羊抗兔II抗(武漢博士德生物工程有限公司);TRIzol(Aidlab);cDNA第一鏈合成試劑盒(Vazyme)。PCR引物由武漢擎科生物有限公司合成;血糖儀及血糖試紙(Johnson & Johnson)。
3 主要方法
3.1 糖尿病小鼠模型的建立 將適應性喂養1周后的小鼠隨機分成正常對照(normal control,NC)組和DM模型組,NC組普通飼料喂養,DM組高糖高脂飼料喂養(普通飼料中加入10%蔗糖、10%豬油、2%膽固醇和0.15%膽酸鈉)。4周后,全部小鼠禁食10 h,DM組按照50 mg/kg劑量腹腔注射STZ溶液,連續5 d,同時NC組注射等量檸檬酸緩沖液。72 h后測尾尖血糖,10 d后行腹腔注射葡萄糖耐量實驗(intrape-ritoneal glucose tolerance test,IPGTT),造模成功標準為空腹血糖(fasting plasma glucose,FPG)≥7.0 mmol/L和(或)2 h 血糖(plasma glucose,PG)≥11.1 mmol/L。
3.2 實驗動物干預及分組 DM模型建立后,繼續8周高糖高脂喂養,再將NC組和DM組分為運動亞組和非運動亞組,即包括正常對照運動組(normal control exercise group,ENC;n=8)、正常非運動組(normal control non-exercise group,NNC;n=8)、糖尿病運動組(diabetic exercise group,EDM;n=10)和糖尿病非運動組(diabetic non-exercise group,NDM;n=10)。ENC和EDM組進行5周的無負重游泳干預。運動方案是Ploug等所用方法的改良版[9-10]:游泳訓練 每天1次,每周5 d,第1次15 min,以后每次增加15 min直至每天45 min,按照每天45 min運動量直至第2周結束,后3周每天運動60 min,一共5周。
3.3 小鼠體重、空腹血糖和糖耐量情況的監測 每周測定小鼠體重,每3周復測小鼠空腹血糖,開始運動干預后改為每周監測血糖。在最后一次運動結束后給各組小鼠做IPGTT。
3.4 心功能及血壓的測量 各組小鼠于DM誘導15周末,用1%戊巴比妥鈉50 mg/kg腹腔注射麻醉,仰臥固定,使用Vevo 1100心臟超聲診斷儀測定心臟的大小和功能,在心臟收縮和舒張過程中測定左室舒張末期容積(left ventricular end-diastolic volume,LVEDV)和左室收縮末期容積(left ventricular end-systolic volume,LVESV),比較左室射血分數(left ventricular ejection fraction,LVEF)及左室短軸縮短率(left ventricular shortening fraction,LVFS)以評價心臟收縮功能。處理動物前,清醒狀態下尾袖法給各組小鼠測量血壓。
3.5 樣本的收集及處理 最后一次游泳運動結束24 h后,給所有小鼠稱重,腹腔注射1%戊巴比妥鈉50 mg/kg麻醉,留取心臟標本,稱重,計算“心臟指數(HW/BW)=心臟重量(mg)/體重(g)”。部分心臟組織4%多聚甲醛固定,剩余心臟組織-70 ℃下保存。
3.6 心臟組織的病理結構觀察 取4%多聚甲醛固定的心臟組織,常規的梯度脫水、石蠟包埋、切片(5 μm),做常規HE、Masson染色,光鏡下觀察心臟組織形態病理學改變及纖維化程度。
3.7 實時熒光定量PCR實驗 提取小鼠心臟組織總RNA后經分光光度計行RNA定量和定性檢測。ANP引物的正義鏈為5’-CTGGGACCCCTCCGATAGAT-3’,反義鏈為5’-CACTCTGGGCTCCAATCCTG-3’;β-actin引物的正義鏈為5’-CACGATGGAGGGGCCGGACTCATC-3’,反義鏈為5’-TAAAGACCTCTATGCCAACACAGT-3’。PCR的擴增條件為94 ℃ 4 min; 94 ℃ 30 s, 56 ℃ 30 s, 72 ℃ 25 s, 30個循環;72 ℃ 5 min。擴增完成后60 ℃開始升溫作熔解曲線驗證擴增產物的特異性。反應完成后設定基線值和閾值,計算機分析得到循環閾值(Ct),基因相對表達量以2-ΔΔCt值計算分析。
3.8 Western blot法檢測蛋白表達 提取小鼠心臟組織總蛋白后BCA法測定總蛋白濃度。經過10%的SDS-PAGE分離,PVDF膜印跡,5%脫脂奶粉室溫下封閉2 h,加入抗GAPDH抗體(1∶1 000)、抗Akt抗體(1∶1 000)、抗p-Akt抗體(1∶1 000)和抗PI3K(p110α)抗體(1∶1 500),4 ℃孵育過夜。用封閉液稀釋相應的經辣根過氧化物酶(HRP)標記的 II 抗(1∶50 000) 37 ℃搖床孵育2 h。洗去多余Ⅱ抗,經ECL發光液發光、X光膠片壓片后顯影、定影。分析膠片灰度值,確定樣品中目的蛋白相對含量。
4 統計學處理
采用SPSS 20.0軟件進行數據分析,計量資料用均數±標準差(mean±SD)表示。組間比較采用單因素方差分析,如差異顯著,對該指標的均值進行SNK-q檢驗。以P<0.05為差異有統計學意義。
結 果
1 4組小鼠的體重、血糖情況
與NC組小鼠相比,DM組小鼠體重下降;與NNC組比較,ENC、NDM和EDM組的心臟指數增高。游泳干預后,EDM組小鼠的空腹血糖明顯低于NDM組,葡萄糖耐量也明顯改善,差異具有統計學顯著性(P<0.01);而NNC和ENC組的空腹血糖和葡萄糖耐量變化不大。這說明運動對正常小鼠血糖無影響,但在一定程度上可改善糖尿病小鼠空腹血糖、葡萄糖耐量情況,見圖1、表1。

Figure 1. The blood glucose levels of intraperitoneal glucose tolerance test (IPGTT) and the area under the curve. Mean±SD.n=4~5.*P<0.05vsNNC group;#P<0.05vsENC group;△P<0.05vsNDM group.
圖1 腹腔注射葡萄糖耐量實驗的血糖值及曲線下面積
表 1 運動前后小鼠空腹血糖的變化情況
Table 1. The changes of fasting blood glucose in the mice before and after exercise (mmol/L. Mean±SD)

TreatmentnBeforeexerciseAfterexerciseNNC46.52±0.396.30±0.59ENC46.82±0.485.77±0.59&NDM523.98±1.16?#26.25±4.14?#EDM523.43±2.55?#18.87±3.51?#△&
*P<0.05vsNNC group;#P<0.05vsENC group;△P<0.05vsNDM group;&P<0.05vsbefore exercise.
2 4組小鼠的血壓、心功能情況
無論是對于正常小鼠還是DM小鼠,運動均可以在一定程度上增強心肌收縮能力,改善心肌射血功能。與NNC組比較,未干預的DM小鼠心肌射血功能降低,LVEF和FS均下降,差異具有統計學顯著性(P<0.05)。在DM組中,運動干預的EDM亞組的LVEF和FS明顯高于未干預的NDM亞組(P<0.05)。NDM組的LVESV明顯高于ENC組(P<0.05),而各組的LVEDV變化較小,但差異無統計學顯著性。尾袖法測量各組小鼠血壓發現,NDM亞組的收縮壓、舒張壓均稍有降低,與ENC組比較,其收縮壓降低差異有統計學顯著性,而與其它組比較血壓變化的差異無統計學顯著性,見表2。
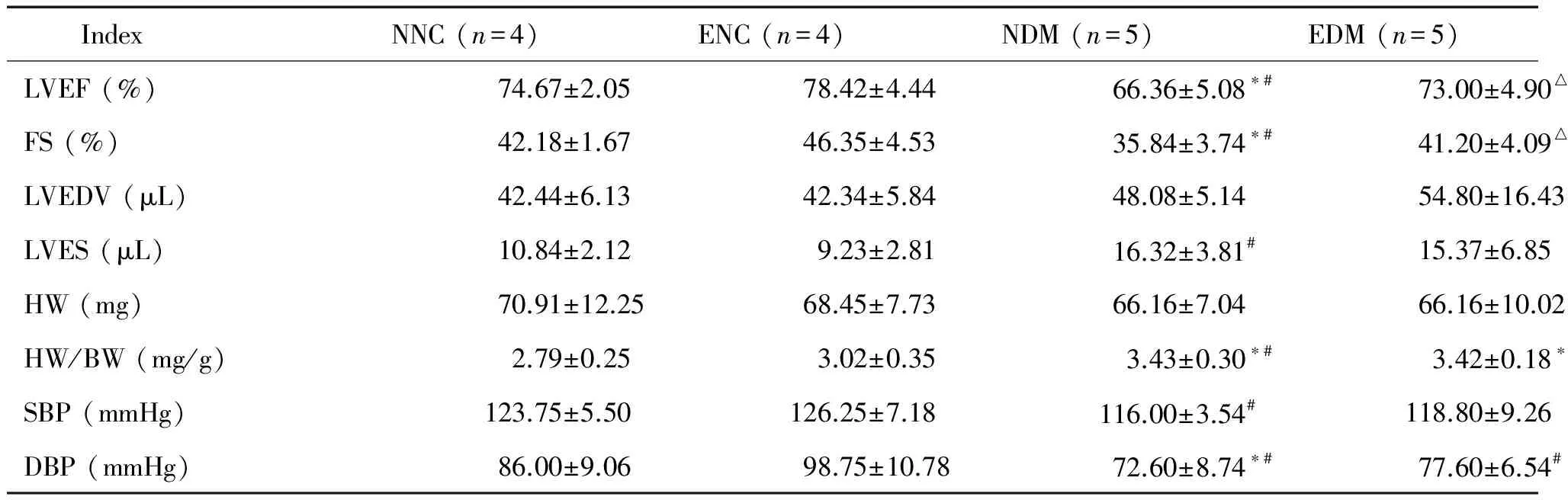
表2 各組小鼠心功能和血壓情況的比較
*P<0.05vsNNC group;#P<0.05vsENC group;△P<0.05vsNDM group.
3 心臟的病理學改變
HE染色可見NNC和ENC組小鼠的心肌細胞排列整齊,細胞核明顯,結構清晰,染色均勻。NDM組小鼠心肌結構極度紊亂,細胞排列十分不規整,心肌細胞間隙變大,連接不甚緊密,部分區域心肌斷裂,且心肌內纖維化程度增加。EDM組心肌形態結構較NDM組明顯改善,心肌細胞排列未見明顯紊亂,也未見明顯的肌纖維斷裂,細胞核形狀較規整,心肌結構趨向正常,心肌纖維化程度降低,見圖2A。Masson染色可見NNC和ENC組小鼠的心肌細胞核為深藍色,膠原纖維呈綠色,細胞間可見少量膠原纖維均勻分布。NDM組小鼠的心肌纖維化程度增加,運動干預后的EDM組心肌膠原纖維增生不甚明顯,走向較正常,見圖2B。

Figure 2. The pathological changes of the myocardial tissues under light microscope (×400).A: HE staining; B: Masson staining.
圖2 光鏡下心肌組織的病理學改變
4 運動對小鼠心肌內胚胎基因ANP mRNA表達的影響
與NNC和ENC組相比,NDM和EDM組心肌組織中胚胎基因ANP的mRNA表達上調(P<0.01),而該胚胎基因的表達在NNC和ENC組間的差異無統計學顯著性。這說明高糖可以誘導心肌組織中胚胎基因的表達,但是運動可以改善DM小鼠心肌組織中胚胎基因的表達,而運動對正常小鼠心肌內胚胎基因的表達無影響,見圖4。
5 運動對心肌內信號通路PI3K(p110α)/Akt蛋白表達的影響
如圖4結果顯示,T2DM顯著地降低PI3K(p110α)和磷酸化Akt的蛋白水平(P<0.01),而高糖對這些蛋白的抑制作用可以被運動所緩解,使得PI3K(p110α)和磷酸化Akt趨向正常組水平。這提示高糖狀態下,運動對心臟的保護作用可能部分與PI3K(p110α)/Akt信號通路激活相關。
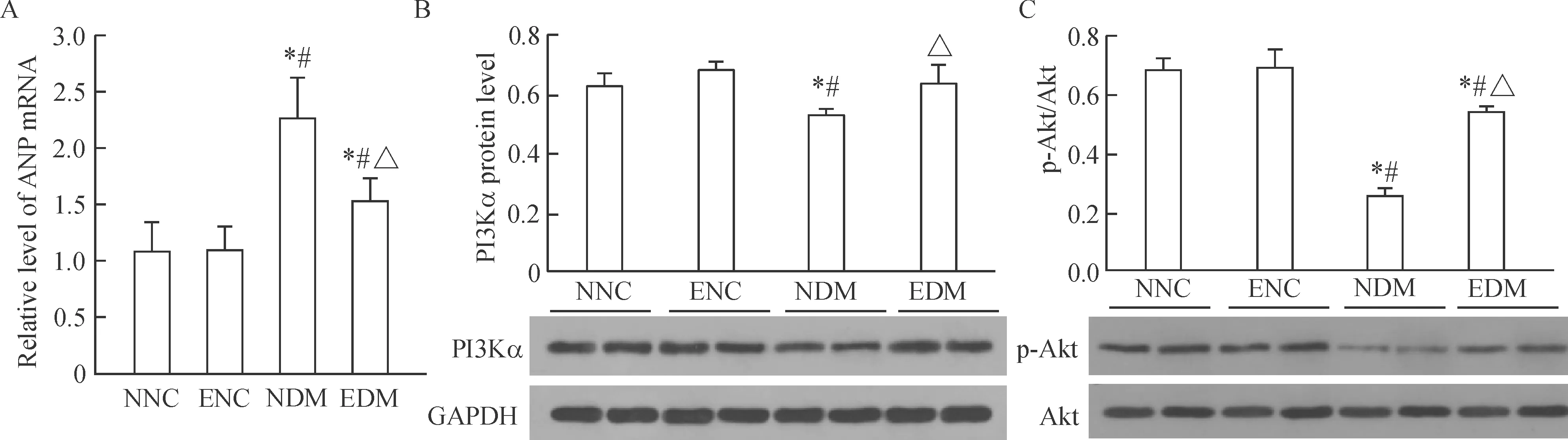
Figure 3. The mRNA expression of ANP (A) and the protein levels of PI3Kα/Akt (B, C) in the myocardium. Mean±SD.n=4~5.*P<0.05vsNNC group;#P<0.05vsENC group;△P<0.05vsNDM group.
圖3 心肌內ANP mRNA表達及PI3Kα/Akt蛋白水平的變化
討 論
本實驗通過構造糖尿病模型,發現運動改善糖尿病小鼠血糖、心功能及病理性損傷的作用可能與PI3K(p110α)/Akt信號通路激活相關。
長期以來,運動一直被視為DM藥物治療的有效輔助措施。近期研究發現,規律性地參加體育運動,可降低50%的心血管疾病發生風險[11]。即使對老年群體,運動仍是一個重要的非藥物治療策略[12-13]。因此,早期合理運動被視為預防心功能不全和心衰的重要措施之一。本實驗研究發現,運動不僅能在一定程度上降低DM小鼠空腹血糖和葡萄糖耐量,而且能改善糖尿病小鼠的心肌射血功能,減輕DM小鼠心肌病理性損害,保護高糖狀態下心肌細胞;但研究發現糖尿病小鼠血壓呈下降趨勢,考慮可能與受損的射血功能導致外周循環血量降低相關。眾所周知,長期的高血糖會導致心肌能量供應不足,心肌纖維化加重,心肌發生病理性重構,最終影響心臟的正常工作。運動作為DM的重要保護措施之一,其發揮心肌保護作用的機制涉及多個方面,包括改善能量代謝,抑制細胞凋亡、氧化應激損害、心肌纖維化等。但目前關于高糖狀態下,運動對心肌細胞保護作用的具體信號通路尚未統一。
PI3K(p110α)大量表達于心血管系統中,在心肌細胞生長和正常心功能的維護中發揮重要的作用。一方面,PI3K(p110α)可以促使心肌功能的正常發揮,當心肌過表達PI3K(p110α)或PI3K(p110α)上游信號受體IGF-1(IGF1R)時可促使心肌細胞增大或心臟生理性肥大;相反,當表達顯性負效體PI3K(p110α)或者敲除PI3K(p110α)的調控亞基p85后可導致心臟變小,并且能抵消IGF-1受體過表達所誘導的生理性肥大[14-15]。PI3K(p110α)過表達還可以促使冠狀動脈血管生成以保證心肌細胞氧氣和營養物質的順利供應[3],增強離體心臟的收縮功能[4];而當顯性負效體PI3K(p110α)過表達時則會降低心臟基本收縮能力[16]。另一方面,PI3K(p110α)還可以保護病理狀態下的心功能:在擴張性心肌病模型中,PI3K(p110α)還能通過模擬運動訓練,抑制胚胎基因的重新編碼,延長壽命;而表達顯性負效體PI3K(p110α)的小鼠則出現壽命年限縮短[2]。敲除PI3K(p110α)會加重因壓力負荷或心肌梗死導致的病理性的心肌損害,但PI3K(p110α)激活后可以緩解上述病理變化所導致的損害[2, 17]。此外,研究發現,PI3K(p110α)的下游Akt也控制各類調節反應,包括抑制凋亡,調控細胞增殖、代謝、肥大等[6-7]。簡而言之,PI3K(p110α)/Akt信號通路在生理性心肌生長中扮演重要角色,并且可以保護病理狀態下的心肌,改善心肌功能,延長壽命。
本研究發現,運動干預后的小鼠心肌組織中PI3K(p110α)表達和Akt磷酸化水平增強,PI3K(p110α)/Akt信號通路被激活;NDM組小鼠心肌內PI3K(p110α)表達及Akt磷酸化水平受抑制,而運動干預的EDM組小鼠心肌內PI3K(p110α)表達和Akt磷酸化水平得以改善。結合前人研究的成果,我們推測運動后的糖尿病小鼠心肌內PI3K(p110α)/Akt信號通路被激活,活化的PI3K(p110α)/Akt信號通路通過作用于其下游的磷酸化糖原合成激酶、內皮型一氧化氮合酶、哺乳動物雷帕霉素靶蛋白等,提高細胞生存率,保護高糖狀態下的心肌細胞[6, 18-19]。因此我們認為,運動對高糖狀態下小鼠心肌細胞的保護作用可能或至少部分是通過激活PI3K(p110α)/Akt信號通路實現的。當運動誘導PI3K(p110α)表達增強時,其下游的Akt也隨之被激活,再通過一系列的蛋白激活促進心肌細胞發生生理性肥大,調控代謝,增強心肌收縮力,從而保護病理狀態下的心肌細胞,改善心功能。運動這種保護糖尿病心肌功能、延緩糖尿病心肌損害發生發展的作用,在臨床上可以在一定程度上改善糖尿病患者生活質量,減輕經濟壓力,并且還能避免藥物治療帶來的或多或少的副作用。
總之,本實驗提示在運動保護DM心肌細胞的機制研究中,PI3K(p110α)/Akt信號通路的激活發揮關鍵的作用;該信號通路激活后可以降低高糖狀態導致的心肌損傷,增強心肌收縮能力,最終改善心功能,這為DM心肌損害的治療甚至逆轉心肌損害提供了新思路。
[1] Sowers JR, Epstein M, Frohlich ED. Diabetes, hypertension, and cardiovascular disease: an update[J]. Hypertension, 2001, 37(4):1053-1059.
[2] Mcmullen JR, Amirahmadi F, Woodcock EA, et al. Protective effects of exercise and phosphoinositide 3-kinase(p110α) signaling in dilated and hypertrophic cardiomyopathy[J]. Proc Natl Acad Sci U S A, 2007, 104(2):612-617.
[3] Bekhite MM, Finkensieper A, Binas S, et al. VEGF-mediated PI3K class IA and PKC signaling in cardiomyogenesis and vasculogenesis of mouse embryonic stem cells[J]. J Cell Sci, 2011, 124(Pt 11):1819-1830.
[4] Yano N, Tseng A, Zhao TC, et al. Temporally controlled overexpression of cardiac-specific PI3Kα induces enhanced myocardial contractility: a new transgenic model[J]. Am J Physiol Heart Circ Physiol, 2008, 295(4):H1690-H1694.
[5] 方 軍, 吳黎明, 陳良龍. RISK信號通路在心肌預處理及后處理中的作用[J]. 中國病理生理雜志, 2009, 25(10):2062-2067.
[6] Hanada M, Feng J, Hemmings BA. Structure, regulation and function of PKB/AKT: a major therapeutic target[J]. Biochim Biophys Acta, 2004, 1697(1-2):3-16.
[7] Brazil DP, Park J, Hemmings BA. PKB binding proteins: getting in on the Akt[J]. Cell, 2002, 111(3):293-303.
[8] 王華祖, 龔興國. 蛋白激酶B的研究進展[J]. 中國病理生理雜志, 2003, 19(11):84-89.
[9] Ploug T, Stallknecht BM, Pedersen O, et al. Effect of endurance training on glucose transport capacity and glucose transporter expression in rat skeletal muscle[J]. Am J Physiol, 1990, 259(6 Pt 1):E778-E786.
[10]尚畫雨, 夏 志, 張 丹, 等. 8周游泳運動對2型糖尿病大鼠周圍神經病變的影響[J]. 中國病理生理雜志, 2014, 30(4):719-724.
[11]Gomes CP, Kim TK, Wang K, et al. The implications on clinical diagnostics of using microRNA-based biomarkers in exercise[J]. Expert Rev Mol Diagn, 2015, 15(6):761-772.
[12]Oliveira J, Mesquita-Bastos J, Argel de Melo C, et al. Postaerobic exercise blood pressure reduction in very old persons with hypertension[J]. J Geriatr Phys Ther, 2016, 39(1):8-13.
[13]甄 潔, 李曉霞. 有氧運動抑制心梗后心力衰竭大鼠左室重塑及交感神經重塑[J]. 中國病理生理雜志, 2015, 31(6):973-979.
[14]Shioi T, Kang PM, Douglas PS, et al. The conserved phosphoinositide 3-kinase pathway determines heart size in mice[J]. EMBO J, 2000, 19(11):2537-2548.
[15]Mcmullen JR, Shioi T, Huang WY, et al. The insulin-like growth factor 1 receptor induces physiological heart growth via the phosphoinositide 3-kinase(p110α) pathway[J]. J Biol Chem, 2004, 279(6):4782-4793.
[16]Liang W, Oudit GY, Patel MM, et al. Role of phosphoinositide 3-kinase α, protein kinase C, and L-type Ca2+channels in mediating the complex actions of angiotensin II on mouse cardiac contractility[J]. Hypertension, 2010, 56(3):422-429.
[17]Lin RC, Weeks KL, Gao XM, et al. PI3K(p110α) protects against myocardial infarction-induced heart failure: identification of PI3K-regulated miRNA and mRNA[J]. Arterioscler Thromb Vasc Biol, 2010, 30(4):724-732.
[18]Oudit GY, Sun H, Kerfant BG, et al. The role of phosphoinositide-3 kinase and PTEN in cardiovascular physio-logy and disease[J]. J Mol Cell Cardiol, 2004, 37(2):449-471.
[19]Doble BW, Woodgett JR. GSK-3: tricks of the trade for a multi-tasking kinase[J]. J Cell Sci, 2003, 116(Pt 7):1175-1186.
(責任編輯: 林白霜, 羅 森)
Aerobic exercise protects cardiac function of T2DM mice by activation of PI3K (p110α)/Akt signaling pathway
LIN Yan-yan, ZHAO Lin-shuang, LIU Yi
(DepartmentofEndocrinology,WuhanGeneralHospitalofGuangzhouMilitaryCommand,Wuhan430070,China.E-mail:zls7111@aliyun.com)
AIM: To study the protective effect of aerobic exercise on cardiac dysfunction in mice and its mechanism, and to provide theoretical and practical basis for the exercise therapy of diabetic cardiac dysfunction.METHODS: The mice were divided into normal control non-exercise (NNC) group, normal control exercise (ENC) group, diabetic non-exercise (NDM) group and diabetic exercise (EDM) group. At the end of the experiment, the cardiac function was evaluated by echocardiography. The pathological changes of the myocardial tissues and the development of fibrosis were observed. The mRNA expression of ANP, and the protein levels of PI3K (p110α) and Akt were determined. RESULTS: The decrease in cardiac function of diabetic mice was observed, and the cardiac function recovered after exercise intervention (P<0.05). Under light microscope with HE and Masson staining, the myocardial structure in NDM group was in extreme disorder, cell arrangement was not neat, and the degree of fibrosis increased, but the myocardial damage was improved in ENC group. Compared with NNC group, the mRNA expression of ANP in the myocardium of diabetic mice was up-regulated (P<0.05). The protein levels of PI3K (p110α) and Akt were decreased (P<0.05), and the cascade was inactivated. Compared with NDM group, the mRNA expression of ANP was down-regulated and the protein levels of PI3K (p110α) and Akt were up-regulated in EDM group (P<0.05). CONCLUSION: Diabetes results in myocardial damage in mice, and reduces cardiac function. Exercise intervention alleviates the heart dysfunction induced by high glucose via activating PI3K(p110α)/Akt signaling pathway to protect the structure and function of the myocardium.
Exercise; Cardiac function; Diabetes mellitus; Myocardium
1000- 4718(2017)01- 0073- 06
2016- 05- 18
2016- 11- 09
湖北省自然科學基金資助項目(No. 2012FFB06807)
R363; R587.2
A
10.3969/j.issn.1000- 4718.2017.01.012
雜志網址: http://www.cjpp.net
△通訊作者 Tel: 027-50772198; E-mail: zls7111@aliyun.com

