刀鱭嗅覺受體基因MOR-51I2克隆、序列分析及組織表達
王曉梅朱國利唐文喬
(1. 上海海洋大學魚類研究室, 上海 201306; 2. 上海市海洋動物系統分類與進化重點實驗室, 上海 201306)
刀鱭嗅覺受體基因MOR-51I2克隆、序列分析及組織表達
王曉梅1,2朱國利1,2唐文喬1,2
(1. 上海海洋大學魚類研究室, 上海 201306; 2. 上海市海洋動物系統分類與進化重點實驗室, 上海 201306)
為研究刀鱭的嗅覺受體(Olfactory receptor, OR)是否參與其生殖洄游過程, 利用基因組步移技術, 從洄游型刀鱭(Coilia nasus)中克隆出嗅覺受體基因MOR-51I2的基因序列全長。該基因為單外顯子結構, 編碼區長為999 bp。在3′ UTR區域具有一段微衛星序列, 以(AC)n為重復單位, 并夾有若干T或G堿基, 且在不同生態型間具有明顯長度差異。MOR-51I2基因所編碼的蛋白具有7次疏水性α-螺旋的跨膜結構, 為G-蛋白偶聯受體。MOR-51I2基因與已報道的其他魚類的OR基因所編碼的氨基酸序列的同源性在51%以上, 其中與大西洋鯡(Clupea harengus)的OR51I2-like基因的同源性高達83%。經qRT-PCR分析顯示, 在定居型刀鱭中, MOR-51I2基因主要在嗅囊和性腺中表達, 在肝臟、鰓、肌肉微弱表達, 在心臟和眼睛中幾乎不表達。其中, 雌性嗅囊中的表達量約是雄性嗅囊中的2倍, 是精巢和卵巢中的80—100倍。在洄游型刀鱭中, 該基因在雄性嗅囊的表達量約是雌性嗅囊中的6倍。MOR-51I2基因在洄游型刀鱭的雌性嗅囊中的表達量約是定居型刀鱭的雌性嗅囊中的1/5, 而在洄游型刀鱭的雄性嗅囊中的表達量卻是定居型刀鱭的雄性嗅囊中的3倍。這些結果表明, MOR-51I2基因不但參與刀鱭的嗅覺功能, 而且可能參與了刀鱭的性腺發育及生殖洄游過程, 同時也可能與其生態型的分化相關。
刀鱭; 嗅覺受體基因; 組織表達; 生殖洄游; 生態型分化
刀鱭(Coilia nasus)是鯡形目(Clupeiformes)、鳀科(Engraulidae)的一種中小型魚類, 具有洄游和定居兩種生態型[1—4]。洄游型平時棲息于中國、日本和朝鮮半島的近海, 春季性成熟后進入河流的中、下游產卵, 孵化后的幼魚順流而下進入海中肥育。定居型主要分布于長江中下游干流及其附屬湖泊, 可在淡水中完成整個生活史[1,2,4]。在長江中,定居型刀鱭的資源量豐富, 是低值漁品。但洄游型刀鱭的種群數量卻呈急劇下降趨勢, 已成為長江流域最名貴的水產品之一。刀鱭的洄游型和定居型形態相近, 生殖洄游是區別兩者的主要表征之一。鑒別生態類型、闡明生殖洄游機制對保護和利用長江洄游型刀鱭這一珍貴漁業資源具有積極意義。已有學者嘗試用外部形態的多元分析[5—7]、“寄生蟲標記”[8,9]、耳石形態及元素成分[10—13]、肌肉同位素組分差異[14]以及某些基因差異[4,15]等鑒別刀鱭的不同生態類型, 但對刀鱭生殖洄游機制的研究才剛起步[16,17]。
魚類生殖洄游的嗅覺定向(Olfactory orientation)假說自20世紀50年代被提出以來[18], 嗅覺在美洲鰻(Anguilla rostrate)、紅大麻哈魚(Oncorhynchus nerka)、大西洋鮭(Pacific salmon)等過河口生殖洄游魚類的洄游中所起的重要作用已逐漸被證實[19—21]。魚類嗅覺依靠水中氣味分子如氨基酸、核苷酸、類固醇、前列腺素和膽汁酸等誘導作用于嗅覺受體蛋白而引起[16,22,23]。嗅覺受體主要在嗅覺上皮組織中表達, 氣味分子與嗅覺受體蛋白結合、識別并引發化學信號, 通過嗅神經傳送到神經中樞從而實現嗅覺識別[24], 嗅覺受體蛋白則由嗅覺受體基因所編碼[25—27]。已發現哺乳動物嗅覺受體有在進化上相互獨立的4個家族, 分別為主嗅覺受體(Main olfactory receptors, MORs)、犁鼻器受體(Vomeronasal receptors, VRs)、痕量胺相關受體(Trace-amine associated receptors, TAARs)和類甲酰肽受體蛋白(Formyl peptide receptor-like proteins)[28]。主嗅覺受體是數量最大的嗅覺受體基因亞家族, 最早發現于褐家鼠(Rattus norvegicus), 編碼區長度一般650 bp左右, 無內含子[29,30], 可識別水溶性氣味分子[26,29,31]。主嗅覺受體基因目前已在一些模式魚類, 如斑馬魚(Danio rerio)、紅鰭東方鲀(Takifugu rubripes)、綠斑河鲀(Tetraodon nigroviridis)、三刺魚(Gasterosteus aculeatus)、青鳉(Oryzias latipes)等[22,26,30,32,33]開展過研究, 但在非模式物種中研究尚少。在對多個刀鱭嗅囊轉錄組進行測序分析的基礎上, 我們已初步篩選出洄游型與定居型刀鱭差異表達的幾個MOR基因[16,22]。本研究克隆出其中的一個MOR基因, 分析了基因結構及在不同組織中的表達, 旨在弄清其在刀鱭兩個生態型中的序列差異, 為長江刀鱭生殖洄游的嗅覺定向機制和生態型演化研究提供一些線索。
1 材料與方法
1.1 樣本采集
實驗所用刀鱭定居型樣本為2014年3月采自江西鄱陽湖都昌水域, 洄游型樣本2014年5月采自長江靖江江段, 都是2齡、性腺發育Ⅲ期的個體, 標注為定居PY-1-PY-6, 洄游JJ-1-JJ-6。所有樣本都用定置刺網捕獲, 尚未死亡的個體立即包埋于-20℃醫用冰袋中, 使其失去知覺。在現場迅速用剪刀剖開腹部, 檢視性腺發育狀況, 對性腺發育Ⅲ期的個體進行實驗取樣[31]。定居型樣本取嗅囊、精巢、卵巢、肌肉、心臟、眼睛、胃壁、肝臟和腮等組織或器官, 洄游型樣本僅取嗅囊, 保存于液氮。返回實驗室以后, 根據刀鱭矢耳石重量與年齡的對應關系[10,13], 留用2齡個體作為實驗樣本。實驗開始前取出, 置-80℃保存備用。
1.2 刀鱭基因組DNA及總RNA的提取
利用動物組織基因組DNA小量提取試劑盒(上海萊楓生物科技有限公司)并按說明書提取洄游(JJ-1-JJ-6)、定居(PY-1-PY-6)刀鱭肌肉基因組DNA, 保存于-20℃冰箱。用EastepTM總RNA提取試劑盒(上海普洛麥格生物產品有限公司)提取定居型刀鱭組織或器官及洄游型刀鱭(雌/雄)嗅囊的總RNA, 進行3個重復。提取后的基因組DNA和總RNA用1%瓊脂糖凝膠電泳進行檢測, 判斷其完整性; Thermo Nandrop2000分光光度計測RNA A260/ A280值, 評價純度, 估測濃度大小。產物置于-80℃冰箱保存備用。
1.3 刀鱭cDNA文庫的建立
使用PrimeScriptTMII 1st Strand cDNA Synthesis Kit試劑盒及其方法(寶生物工程有限公司), 以Oligo dT Primer為引物對洄游型刀鱭嗅囊總RNA進行普通反轉錄, 獲得第一鏈cDNA, 為后續判斷MOR-51I2基因是否含有內含子做準備。使用PrimeScriptTMRT reagent Kit with gDNA Eraser (Perfect Real Time)試劑盒(同上), 以RT Primer Mix為引物獲得反轉錄cDNA, 為后續qRT-PCR反應做準備。產物保存于-20℃冰箱備用。
1.4 刀鱭MOR-51I2基因序列的獲取
依據本實驗室前期從洄游型刀鱭嗅囊cDNA文庫中獲得的MOR-51I2基因序列片段, 參照Genome Walking Kit試劑盒(寶生物工程有限公司)中對特異性引物的設計要求, 設計出獲取3′序列的特異性引物(3′-SP1、3′-SP2和3′-SP3, 表 1)和獲取5′序列的特異性引物(5′-SP1、5′-SP2和5′-SP3, 表 1)(引物均由上海生工生物工程股份有限公司合成)。優化反應體系和反應條件, 利用試劑盒中AP2簡并引物和特異性引物SP1/SP2/SP3進行3輪熱不對稱PCR反應。反應產物用1%瓊脂糖凝膠電泳檢測、切膠回收和克隆測序(序列均由上海邁浦生物科技有限公司測序)。最終獲得基因片段的側翼序列, DNAMAN 6.0軟件拼接后獲得目的基因序列。

表 1 引物序列Tab. 1 Primer sequences
1.5 刀鱭MOR-51I2基因開放閱讀框的獲取
(2)合理利用區塊鏈技術。區塊鏈技術是一種互聯網數據庫技術,其特點是去中心化、不可纂改性、公開透明,讓每個人均可參與數據庫記錄。區塊鏈技術憑借其去中心化的特點,能夠建立一個基于網絡的公共賬本,每一個區塊包含一次網絡交易,從而構建一個更加可靠的網絡系統,從根本上解決網絡交易中欺詐和“尋租”現象。因此,相關機構應合理利用區塊鏈技術,進一步降低當前電子支付存在的病毒侵襲、黑客攻擊、支付數據更改、資金無故流失等風險,健全信用體系,保障用戶權益。
利用NCBI網站(http://www.ncbi.nlm.nih.gov/)中Blastx工具, 對刀鱭MOR-51I2基因序列進行比對,尋找同源性最高的基因序列, 再用jellyfish軟件預測該基因的開放閱讀框區域。根據預測結果, 在MOR-51I2基因的開放閱讀框兩側設計特異性引物(ORF-R/ORF-F, 表 1), 進行基因序列的驗證, 判斷是否具有內含子并獲取基因的開放閱讀框。以洄游型刀鱭基因組DNA和嗅囊cDNA為模板, 進行PCR反應。反應體系: 模板<1 μg, ORF-R (10 μmol/L) 0.5 μL, ORF-F (10 μmol/L) 0.5 μL, 10×Taq Plus Buffer 2.5 μL, dNTP Mixture (2.5 mmol/L) 2 μL, Taq Plus DNA Polymerase (2.5 U/μL) 0.5 μL, 加ddH2O至25 μL。反應條件: 95℃ 5min; 95℃ 45s, 62℃45s, 72℃ 1min 30s, 30個循環; 72℃ 10min; 10℃保存。對PCR反應產物進行1%瓊脂糖凝膠電泳檢測,合格產物外送測序。為獲得具有完整開放閱讀框的MOR-51I2基因, 利用ORF-R/ORF-F引物對洄游和定居刀鱭基因組DNA進行PCR反應, 反應體系和反應條件同上。檢測后, 反應產物外送測序, 拼接后獲得目的片段。
1.6 刀鱭MOR-51I2基因序列分析
利用VecScreen(http://www.ncbi.nlm.nih.gov/ tools/vecscreen/)在線去除上述測序結果的載體, 用DNAMAN6.0軟件進行與引物的比對和拼接, Blastx軟件進行基因序列的預測翻譯及同源性分析。用Expasy網站(http://expasy.org/tools/)中的ProtParam工具(http://web.expasy.org/protparam/)分析蛋白質基本理化性質, ProtScale工具(http://ca.expasy. org/tools/protscale.html)分析蛋白質親疏水性, TMpred工具(http://www.ch.embnet.org/software/ TMPRED_form.html) 分析蛋白質跨膜區, Predict-Protein工具(http://www.predictprotein.org/)預測蛋白質二維結構, SWISS-MODEL ((http://swissmodel. expasy.org)在線預測蛋白質的三級結構。最后通過NCBI中Nucleotide blast工具下載同源DNA序列、Protein Blast下載同源蛋白序列, 利用ClustalX軟件進行序列比對, MEGA 6.0軟件構建Neighbor-joining系統發育樹。
1.7 刀鱭MOR-51I2基因的組織表達譜
用qRT-PCR反應分析MOR-51I2基因在定居型刀鱭嗅囊、精巢、卵巢、肌肉、心臟、眼球、胃壁、肝臟及鰓等10個組織或器官及洄游型刀鱭嗅囊的相對表達水平。在MOR-51I2基因編碼區內按熒光定量PCR反應的要求, 設計一對特異性引物QOR-R/QOR-F (表 1)。內參基因引物為GAPDHR/GAPDH-F (表 1), 采用SYBR?Premix Ex TaqTM(Tli RNaseH Plus)試劑盒和Bio-rad CFX Connet實時定量PCR儀, 進行PCR反應。反應體系: SYBR?Premix Ex TaqTM(Tli RNaseH Plus)(2×) 10 μL, 正反向引物(10 μmol/L)各0.4 μL, ROX Reference Dye (50×) 0.4 μL, cDNA模板(<100 ng) 2.0 μL, 滅菌蒸餾水6.8 μL, 共20 μL。以內參基因引物作陽性對照,滅菌蒸餾水作陰性對照, 每個組織和對照樣本均進行3個重復。反應條件: 95℃ 30s; 95℃ 5s, 60℃ 30s, 72℃ 32s, 40個循環; 并做溶解曲線。反應結束后獲得并導出各樣本的Ct (threshold cycle)值, 隨后采用2-ΔΔCt法[34]進行數據分析和表達差異性分析。
1.8 刀鱭MOR-51I2基因中微衛星序列分析
由于測序所得的MOR-51I2基因序列發現在非編碼區3′ UTR有一段微衛星重復序列, 因而依據微衛星片段兩側設計了引物(OR-R/OR-F, 表 1)。以洄游型和定居型刀鱭基因組DNA為模板, 進行PCR反應。反應體系: 模板<1 μg, OR-F (10 μmol/L) 0.5 μL, OR-R (10 μmol/L) 0.5 μL, 2×Taq Plus PCR MasterMix 12.5 μL, 加ddH2O至25 μL。反應條件: 95℃ 5min; 95℃ 45s, 63℃ 45s, 72℃ 30s, 30個循環; 72℃ 10min; 10℃保存。反應產物用1.5%瓊脂糖凝膠電泳檢測。
2 結果
2.1 刀鱭MOR-51I2的基因序列
2.2 刀鱭MOR-51I2的蛋白結構
經ProtParam和ProtScale在線分析, 發現刀鱭MOR-51I2基因序列所編碼的蛋白質序列, 其理化性質為: 氨基酸殘基332個、分子式為C1751H2724N430O443S21、相對分子質量為37560.7、理論pI值為9.45、正/負電荷殘基數為29和15、蛋白質序列的N端為起始密碼子所編碼的Met殘基、半衰期為30hours、不穩定系數(II)為31.27(<40, 表明此蛋白較穩定)以及總平均親水性(GRAVY)為0.648。經Predict Protein在線預測工具, 發現刀鱭MOR-51I2蛋白具有9個蛋白質綁定位點、6個DNA綁定位點、7個核苷酸綁定位點(圖 2)。功能區域主要集中在氨基酸序列的N端、TM5-TM6間非跨膜區以及羧基端。二級結構有55.72%為α-型螺旋、10.24% β-型螺旋以及34.04% β-型轉角, 并無二硫鍵結構。經SWISS-MODEL在線預測, 該蛋白質的三級結構具有7個α-型螺旋跨膜結構(圖 3)。
2.3 刀鱭MOR-51I2基因與其他物種相關基因的進化關系

圖 1 洄游型刀鱭(JJ-5) MOR-51I2基因的核苷酸序列和氨基酸序列Fig. 1 The sequence of nucleotide and amino acid of MOR-51I2 gene in the migratory C. nasus (JJ-5)“=”. 起始密碼子ATG、終止密碼子TAA (“*”); TM1-7. 7個跨膜域; “-”. 為微衛星序列, 長120 bp“=”. The initiation codon ATG, the termination codon TAA (“*”); TM1-7. Seven transmembrane regions; “-”. Microsatellite sequence, 120 bp
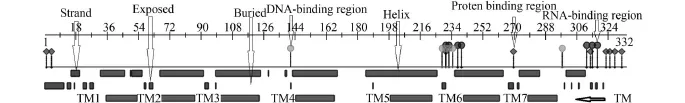
圖 2 MOR-51I2蛋白的功能區、二級結構類型和跨膜區Fig. 2 The protein function region, secondary structure type and transmembrane region of MOR-51I2 protein“Protein binding region”. 蛋白質綁定位點; “DNA binding region”. DNA綁定位點; “RNA binding region”. RNA綁定位點; “Helix”. α-型螺旋; “Strand”表示β-型螺旋; “Buried”. 鑲嵌于生物膜內片段; “Exposed”. 非鑲嵌于膜內的片段; “TM1-7”. 蛋白質的7個跨膜區域“Protein binding region”. Protein binding sites; “DNA binding region”. DNA binding sites; “RNA binding region”. RNA binding sites;“Helix”. α-helix; “Strand”. β-helix; “Buried”. The sequence that mosaiced in the biofilm; “Exposed”. The sequence that non-mosaiced in the biofilm; “TM1-7”. Seven transmembrane regions

圖 3 MOR-51I2蛋白的三級結構預測圖Fig. 3 The predicted three-dimensional structure of MOR-51I2 protein1—7表示蛋白質7個α-型螺旋跨膜結構1—7. Seven α-helix position

表 2 同源DNA序列Tab. 2 The homologous DNA sequences
利用NCBI中的nucleotide blast工具作在線預測, 發現刀鱭MOR-51I2基因序列與其他魚類同源基因的同源性在66%—85% (表 2)。同一物種選取其中1個同源性最高的核酸序列進行FASTA格式下載, 用MEGA6.0構建Neighbour-joining進化樹(圖 4)。可見, 基于核酸序列所構建的進化樹可分為兩大支, 其中刀鱭MOR-51I2基因與大西洋鯡(Clupea harengus) OR51I2-like基因、墨西哥脂鯉(Astyanax mexicanus) OR4K15-like基因及斑點雀鱔(Lepisosteus oculatus) OR4K15-like基因處于同一大分支, 序列之間的同源性較高, 分別為85%、76%和74%。但采用刀鱭MOR-51I2基因所編碼的氨基酸序列與其他魚類的同源嗅覺受體蛋白的氨基酸序列(表 3), 所構建的NJ進化樹(圖 5)與基于核酸序列所構建的進化樹(圖 4)有較大的差別。
2.4 刀鱭MOR-51I2基因的組織表達
利用特異性引物QOR-R和QOR-F對定居型刀鱭的10種組織或器官及洄游型刀鱭(雌/雄)的嗅囊進行實時熒光定量PCR反應, 得出各樣品的Ct值。以在胃壁中的表達量為參照值, 利用2-ΔΔCt法分析所得的結果見圖 6。可見, MOR-51I2基因在肌肉、心臟和眼睛中幾乎不表達; 在肝臟和鰓中的表達量也很低; 但在嗅囊和性腺中的表達量很高, 且嗅囊的表達量是性腺表達量的30—100倍。另外, 雌性嗅囊中的表達量約是雄性嗅囊的2倍, 而精巢中的表達量卻約是卵巢中的2倍。
用同樣方法對兩種生態型刀鱭嗅囊中的表達量進行分析比較(圖 7), 顯示MOR-51I2基因在洄游型雄性嗅囊中的表達量約是其雌性嗅囊中的6倍、定居型雄性嗅囊中的3倍, 但洄游型雌性嗅囊中的表達量卻僅是定居型雌性嗅囊中的1/5。
2.5 刀鱭MOR-51I2蛋白在兩個生態型間的差異性分析
通過特異引物ORF-R/ ORF-F, 對洄游型刀鱭(JJ-1-JJ-6)和定居型刀鱭(PY-1-PY-6)基因組DNA進行PCR擴增。獲得的DNA序列經DNAMAN軟件整理, jellyfish軟件預測翻譯的蛋白質序列。經比對發現, 兩個群體的MOR-51I2蛋白間的相似性為97.5%, 僅有若干氨基酸殘基的變化。
2.6 刀鱭MOR-51I2基因的微衛星在不同生態型間的差異性
用特異引物OR-F/OR-R對洄游型(JJ-1-JJ-10)和定居型刀鱭(PY-1-PY-10)進行PCR擴增, 經1.5%瓊脂糖凝膠電泳檢測(圖 8)并測序。結果表明, 定居型群體的微衛星片段長度長于洄游型群體, 但同一群體的不同個體間其長度也有一定的變化。分析顯示, 洄游型群體內的一致性為86.91%, 定居型群體內為93.29%, 兩個群體間僅82.66%。洄游型群體的微衛星組成平均為48.6(AC)、11.4(GC)、0.6(AG)、1.0(AA)及2.4(AT), 定居型群體則為57.0(AC)、12.6(GC)、1.8(AG)、1.0(AA)及4.4(AT), 可見定居型較洄游型多8.4組(AC)1.2組(GC)、1.2組(AG)和2.0組(AT)。
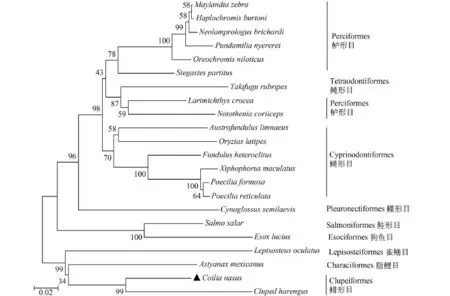
圖 4 刀鱭MOR-51I2核酸序列及其他魚類相關嗅覺受體基因序列的系統發育樹Fig. 4 The phylogenetic tree based on nucleotide sequence of MOR-51I2 in Coilia nasus and related olfactory receptor in other fishes節點處的數值為1000次bootstrap檢驗的支持率; 系統樹中刀鱭用▲標出; 下同The numbers at each node represent the popularity rating that was replicated after 1000 bootstrap iterations; ▲ in the figure represented C. nasus; the same applies below

表 3 同源蛋白序列Tab. 3 The homologous protein sequences
3 討論
3.1 MOR-51I2基因結構及其進化關系
本研究通過染色體步移技術獲得了一個刀鱭嗅覺受體基因, 經與NCBI比對, 發現該基因與大西洋鯡OR 51I2-like基因的同源性最高, 屬于主嗅覺受體基因家族。由于目前對該類基因尚未有統一的命名方式, 因此我們將其命名為MOR-51I2。該基因序列長1653 bp, 開放閱讀框區域長999 bp, 無內含子, 為單外顯子結構, 可編碼332個氨基酸殘基。所編碼的蛋白質有9個蛋白質綁定位點、6個DNA綁定位點和7個RNA綁定位點, 不含二硫鍵結構, 能夠形成7個疏水性α-型螺旋跨膜結構, 是典型的G蛋白偶聯受體。
核酸序列比較顯示, 刀鱭MOR-51I2基因與大西洋鯡OR51I2-like基因、墨西哥脂鯉OR4K15-like基因及斑點雀鱔OR4K15-like序列之間的同源性較高, 親緣關系較近, 這一結果基本符合魚類目一級階元的進化關系[35]。但刀鱭MOR-51I2基因所編碼的氨基酸序列與其他同源氨基酸序列構建的系統樹, 盡管與大西洋鯡及墨西哥脂鯉這一小分支上的親緣關系并沒有改變, 卻與斑點雀鱔的親緣關系發生了變化, 而進化上位于高等的紅麗魚卻單獨處于進化樹的基部位置。因此, 基于核酸序列所構建的系統樹可能更大程度地反映了物種之間的進化關系, 而基于氨基酸序列構建的系統樹可能更多地體現了該基因在功能上的趨同關系。從基因的結構和長度、編碼蛋白質的結構和性質看, 刀鱭MOR-51I2基因均與現有文獻報道的魚類MOR基因相符[30, 34]。
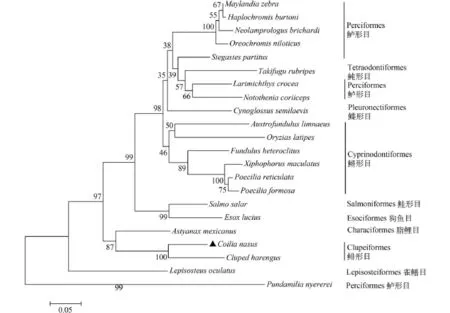
圖 5 刀鱭MOR-51I2氨基酸序列與其他魚類相關嗅覺受體蛋白的系統發育樹Fig. 5 The phylogenetic tree based on amino acid sequence of MOR-51I2 in C. nasus and related olfactory receptor in other fishes
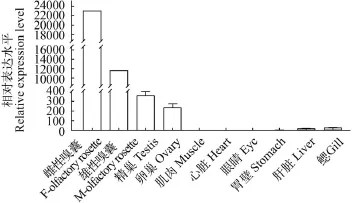
圖 6 MOR-51I2基因在定居型刀鱭組織中的表達差異(n=3)Fig. 6 The expression of MOR-51I2 in organs/tissues of the settlement C. nasus (n=3)
3.2 MOR-51I2基因的組織表達
實時熒光定量PCR反應顯示, MOR-51I2基因主要在嗅囊中表達, 在性腺中的表達量也很高, 而肌肉、心臟、眼睛、肝臟和鰓中幾乎不表達或表達量很低。但雌性嗅囊中的表達量要高出雄性嗅囊約2倍, 而精巢中的表達量是卵巢中的約2倍。這表明MOR-51I2基因不但與嗅覺功能有關, 也可能參與了刀鱭的性腺發育, 在雌雄個體間又存在著差異。
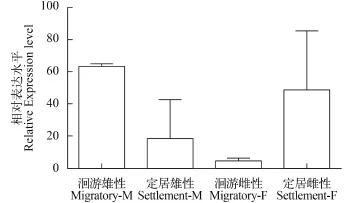
圖 7 MOR-51I2基因在不同生態型刀鱭嗅囊中的表達差異(n=3)Fig. 7 The expression of MOR-51I2 in rosettes of the different ecotypes of C. nasus (n=3)
進一步分析發現, MOR-51I2基因在洄游型雄性嗅囊中的表達量約是同一生態型雌性嗅囊表達量的6倍, 但定居型雌性嗅囊中的表達量卻約是同一生態型雄性嗅囊表達量的2.5倍。這預示著洄游型群體的雄性個體, 可能比雌性個體具有更強的識別水溶性氣味分子的能力。定居型則相反, 雌性識別水溶性氣味分子的能力可能明顯強于雄性。分析還發現, 雄性嗅囊中的表達量洄游型要明顯大于定居型, 而雌性則定居型要大于洄游型(圖 7)。這是否預示著, 洄游型刀鱭的雄性個體在溯河生殖洄游中起著主導作用, 而定居型刀鱭的雌性個體在尋找產卵場時起主導作用?還需要克隆更多的基因加以證實。
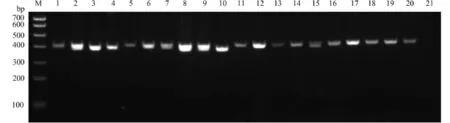
圖 8 刀鱭MOR-51I2基因中微衛星序列在不同生態型間的比較Fig. 8 Alignment of microsatellite sequence of olfactory receptor MOR-51I2 between the different ecotypes of C. nasusM代表Trans DNA MarkerⅠ; 泳道1—10代表洄游型刀鱭群體; 泳道11—20代表定居型刀鱭群體; 泳道21代表陰性對照(用ddH2O代替DNA模板)M. Trans DNA MarkerⅠ; 1—10. Migratory C. nasus; 11—20. Settlement C. nasus; 21. Negative control (ddH2O instead of DNA)
3.3 MOR-51I2基因的微衛星結構
此外, 在MOR-51I2基因緊鄰終止密碼子TAA的3′ UTR非編碼區中有一段微衛星序列, 其中以(AC)n最豐富, 具有長度多態性, 在定居型和洄游型群體間具有明顯的擴增差異帶。前者的微衛星條帶明顯多于后者, 微衛星平均長度前者也高于后者。微衛星側翼序列的突變和重復次數長度的變化, 包含著重要的物種進化信息[36,37]。本研究所顯示的MOR-51I2基因表達量差異、微衛星序列變化以及核酸和蛋白構建的系統樹差異, 是否與刀鱭定居型種群的形成和洄游習性的喪失相關, 還有待于進一步驗證。
[1]Fish Research Laboratory Institute of Hydrobiology, Chinese Academy of Sciences. Fishes of Yangtze River [M]. Beijing: Science Press. 1976, 21—26 [湖北水生生物研究所魚類研究室. 長江魚類. 北京: 科學出版社. 1976, 21—26]
[2]Yuan C M, Lin J B, Qin A L, et al. The taxonomy history and current situation of fishes on Chinese Coilia and talking several realizations of reconstruction old taxonomy of fishes [J]. Journal of Nanjing University (Natural Sciences), 1976, (2): 1—12 [袁傳宓, 林金榜, 秦安舲, 等. 關于我國鱭屬魚類分類的歷史和現狀-兼談改造舊魚類分類學的幾點體會. 南京大學學報(自然科學版), 1976, (2): 1—12]
[3]Cheng Q Q, Lu D R. PCR-RFLP analysis of cytochrome b gene does not support Coilia ectenes taihuensis being a subspecies of Coilia ectenes [J]. Journal of Genetics, 2005, 84(3): 307—310
[4]Tang W Q, Hu X L, Yang J Y. Species validities of Coilia brachygnathus and C. nasus taihuensis based on sequence variations of complete mtDNA control region [J]. Biodiversity Science, 2007, 15(3): 224—231 [唐文喬, 胡雪蓮, 楊金權. 從線粒體控制區全序列變異看短頜鱭和湖鱭的物種有效性. 生物多樣性, 2007, 15 (3): 224—231]
[5]Cheng Q Q, Han J D. Morphological variations and discriminant of two populations of Coilia ectenes [J]. Journal of Lake Science, 2004, 16(4): 356—364 [程起群, 韓金娣. 鱭屬兩種群的形態變異及綜合判別(英文). 湖泊科學, 2004, 16(4): 356—364]
[6]Cheng W X, Tang W Q. Some phenotypic varieties between different ecotypes of Coilia nasus in Yangtze River [J]. Chinese Journal of Zoology, 2011, 46(5): 33—40 [程萬秀, 唐文喬. 長江刀鱭不同生態型間的某些形態差異. 動物學雜志, 2011, 46(5): 33—40]
[7]Wang D T, Yang J, Jiang T, et al. A comparative study of the morphology of different geographical populations of Coilia nasus [J]. Journal of Fisheries of China, 2012, 36(1): 78—90 [王丹婷, 楊健, 姜濤, 等. 不同水域刀鱭形態的分析比較. 水產學報, 2012, 36(1): 78—90]
[8]Hsu W N, Sun C B, Tong Y R, et al. The biological indicator of the spawning migration of anchovy (Coilia ectenes Joroan et Seale) in Yangtze River [J]. Journal of Nanjing University (Natural Sciences), 1978, 3: 85—91 [徐艿南, 孫超白, 童遠瑞, 等. 長江流域刀鱭魚生殖洄游的“生物指標”. 南京大學學報:自然科學版, 1978, 3: 85—91]
[9]Li W X, Wang G T. Helminth communities in Coilia nasus from anadromous, freshwater and landlocked stocks [J]. Chinese Journal of Zoology, 2014, 49(2): 233—243 [李文祥, 王桂堂. 洄游型、淡水型和陸封型刀鱭的寄生蠕蟲群落結構. 動物學雜志, 2014, 49(2): 233—243]
[10]Guo H Y, Wei K, Tang W Q, et al. Sibling species discrimination for Chinese genus of Coilia fishes based on sagittal otolith morphology [J]. Acta Zootaxonomica Sinica, 2010, 35(1): 127—134 [郭弘藝, 魏凱, 唐文喬, 等.基于矢耳石形態特征的中國鱭屬魚類種類識別. 動物分類學報, 2010, 35(1):127—134]
[11]Yang J, Arai T, Liu H, et al. Reconstructing habitat use of Coilia mystus and Coilia ectenes of the Yangtze River estuary, and of Coilia ectenes of Taihu Lake, based on otolith strontium and calcium [J]. Journal of Fish Biology, 2006, 69(4): 1120—1135
[12]Jiang T, Zhou X Q, Liu H B, et al. Two microchemistry patterns in otoliths of Coilia nasus from Poyang Lake, China [J]. Journal of Fisheries of China, 2013, 37(2): 239—244 [姜濤, 周昕期, 劉洪波, 等. 鄱陽湖刀鱭耳石的兩種微化學特征. 水產學報, 2013, 37(2): 239—244]
[13]Li Y X, He W P, Liu J S, et al. Annulus validation and age and growth estimation of anadromous Coilia ectenes in the Yangtze estuary [J]. Acta Hydrobiologica Sinica, 2010, 34(4):787—793 [黎雨軒, 何文平, 劉家壽, 等. 長江口刀鱭耳石年輪確證和年齡與生長研究. 水生生物學報, 2010, 34(4): 787—793]
[14]Wang L, Tang W Q, Dong W X. The signatures of stable isotopes delta N-15 and delta C-13 in anadromous and non-anadromous Coilia nasus living in the Yangtze River, and the adjacent sea waters [J]. Journal of Ocean University of China, 2015, 14(6): 1053—1058
[15]He W P, Cheng F, Li Y X, et al. Molecular identification of Coilia ectenes and Coilia mystus and its application on larval species [J]. Acta Hydrobiologica Sinica, 2011, 35(4): 565—571 [何文平, 程飛, 黎雨軒, 等. 刀鱭和鳳鱭的分子鑒定及其在仔魚種類鑒定中的應用. 水生生物學報, 2011, 35(4): 565—571]
[16]Zhu G L, Wang L J, Tang W Q, et al. De novo transcriptomes of olfactory epithelium reveal the genes and pathways for spawning migration in Japanese grenadier anchovy (Coilia nasus) [J]. PLoS One, 2014, 9(8): e103832
[17]Zhu G L, Tang W Q, Wang L J, et al. Identification of a uniquely expanded V1R (ORA) gene family in the Japanese grenadier anchovy (Coilia nasus) [J]. DOI: 10.1007/s00227-016-2896-9
[18]Hasler A D, Wisby W J. Discrimination of stream odors by fishes and its relation to parent stream behavior [J]. The American Naturalist, 1951, 85(823): 223—238
[19]Barbin G P, Parker S J, McCleave J D. Olfactory clues play a critical role in the estuarine migration of silverphase American eels [J]. Environmental Biology of Fishes, 1998, 53(3): 283—291
[20]Hino H, Iwai T, Yamashita M, et al. Identification of an olfactory imprinting-related gene in the lacustrine sockeye salmon, Oncorhynchus nerka [J]. Aquaculture, 2007, 273(2—3): 200—208
[21]Dittman A H, Quinn T P. Homing in Pacific salmon: mechanisms and ecological basis [J]. Journal Experiment Biology, 1996, 199(Pt 1): 83—91
[22]Zhu G L, Tang W Q, Liu D. Research progress of olfactory receptor genes in fishes [J]. Journal of Fisheries of China, 2015, 39(6): 916—927 [朱國利, 唐文喬, 劉東. 魚類嗅覺受體基因研究進展. 水產學報, 2015, 39(6): 916—927]
[23]Lai X J, Hong W S, Zhang Q Y. Research progresses in fish olfactory system and sex pheromonal receptors [J]. Chinese Journal of Zoology, 2013, 48(2): 298—305 [賴曉健, 洪萬樹, 張其永. 魚類嗅覺系統和性信息素受體的研究進展. 動物學雜志, 2013, 48(2): 298—305]
[24]Hino H, Miles N G, Bandon H, et al. Molecular biological research on olfactory chemoreception in fishes [J]. Journal of Fish Biology, 2009, 75(5): 945—959
[25]Liu D, Zhang Z L, Zhao Y H, et al. Advancements in the morphological and physiological research on the olfactory organ of fishes [J]. Chinese Journal of Zoology, 2005, 40(6): 122—128 [劉東, 張振玲, 趙亞輝, 等. 魚類嗅覺器官的形態與生理研究進展. 動物學雜志, 2005, 40(6): 122—128]
[26]Niimura Y, Nei M. Evolutionary dynamics of olfactory receptor genes in fishes and tetrapods [J]. Proceedings of the National Academy of the Sciences, 2005, 102(17): 6039—6044
[27]Ngai J, Dowling M M, Buck L, et al. The family of genes encoding odorant receptors in the channel catfish [J]. Cell, 1993, 72(5): 657—666
[28]Zhou Y S, et al. Family structure and phylogenetic analysis of odorant receptor genes in the large yellow croaker (Larimichthys crocea) [J]. BMC Evolutionary Biology, 2011, 11(1717): 237
[29]Zhao H Q, Firestein S J. Vertebrate odorant receptors [J]. Cellular and Molecular Life Sciences, 1999, 56: 647—659
[30]Zhang X H, Firestein S. Genomics of olfactory receptors [J]. Results and Problems in Cell Differentiation, 2009, 47: 25—36
[31]Niimura Y. On the origin and evolution of vertebrate olfactory receptor genes: comparative genome analysis among 23 chordate species [J]. Genome Biology Evolution, 2009, 1: 34—44
[32]Alioto T S, Ngai J. The odorant receptor repertoire of teleost fish [J]. BMC Genomics, 2005, 6: 173
[33]Wellerdieck C, Oles M, Pott L, et al. Functional expression of odorant receptors of the zebrafish Danio rerio andof the nematode C-elegans in HEK293 cells [J]. Chemical Senses, 1997, 22(4): 467—476
[34]Livak K J, Schmittgen T D. Analysis of relative gene expression data using real-time quantitative PCR and the 2-??Ctmethod [J]. Methods, 2001, 25(4): 402—408
[35]Nelson J.S. Fishes of the World [M]. Wiley-Blackwell. 2006, 624
[36]Liu Z J, Jensen J W. Aquaculture has Great Expectations of the Genome Revolution [C]. In: Celebration of the 50 Years of DNA, A Commemorative Book for the discovery of the DNA structure by Francis Crick and James Watson. London: Cambridge. 2003, 50—52
[37]Zardoya R, Vollmer D M, Craddock C, et al. Evolutionary conservation of microsatellite flanking regions and their use in resolving the phylogeny of cichlid fishes (Pisces: Perciformes) [J]. Proceedings of the Royal Society B-biological Sciences, 1996, 263(1376): 1589—1598
CLONING, SEQUENCE ANALYSIS AND TISSUES EXPRESSION OF COILIA NASUS OLFACTORY RECEPTOR GENE MOR-51I2
WANG Xiao-Mei1,2, ZHU Guo-Li1,2and TANG Wen-Qiao1,2
(1. Laboratory of Fishes, Shanghai Ocean University, Shanghai 201306, China; 2. Shanghai Key Laboratory of Marine Animal Taxonomy and Evolution, Shanghai 201306, China)
Olfaction is an important tool for fish to perceive the external environment. To study the role of olfactory receptors in the spawning migration of Coilia nasus, the full-length sequence of olfactory receptor gene MOR-51I2 was cloned from the migratory C. nasus using genome walking technology. The MOR-51I2 gene was composed of a single exon with the open reading frame of 999 bp. The 3′ untranslated region of this gene had a microsatellite sequence formed by (AC)n inserted by several T and G. In addition, the microsatellite sequences in different ecotype of C. nasus had significant length difference. The MOR-51I2 was a G-protein-coupled receptor with seven hydrophobic alphahelical transmembrane structures. The MOR-51I2 protein shared homology (>51%) with known related olfactory receptors from other fishes and it reached 83% homology with the olfactory receptor 51I2-like protein in Clupea harengus. The MOR-51I2 gene was highly expressed in the female olfactory rosettes of the settlement population of C. nasus, which is two times compared with that in male olfactory rosettes and 80 to 100 times compared with that in testis and ovary. The MOR-51I2 gene was expressed weakly in liver and gills and was almost not detected in the muscle, heart and eye. The expression level of female olfactory rosettes was 5 times higher than that in male olfactory rosettes in the migratory population. The expression level in female olfactory rosettes of the settlement population was 5 times higher than that in female olfactory rosettes in the migratory population, while the expression level in the male olfactory rosettes of the migratory population was 2 times higher than that in male olfactory rosettes in the settlement population. These results suggest that MOR-51I2 gene may not only regulate the olfactory function of C. nasus, but also mediate gonad development, spawning migration, and ecological differentiation of C. nasus.
Coilia nasus; Olfactory receptor gene; Tissues expression difference; Spawning migration; Ecotype differentiation
Q344+.1
A
1000-3207(2017)01-0033-10
10.7541/2017.5
2016-01-12;
2016-05-28
公益性行業(農業)科研專項(201203065); 國家自然科學基金(31172407, 31472280); 高等學校博士學科點科研專項(2012 3104110006); 上海高校水產學高峰學科資助 [Supported by the Special Fund for Agro-Scientific Research in the Public Interest (201203065); the National Natural Science Foundation of China (31172407, 31472280); the Ministry of Education's Doctoral Discipline Foundation (20123104110006); Shanghai Universities First-class Disciplines Project of Fisheries]
王曉梅(1989—), 女, 安徽亳州人; 碩士; 主要從事魚類生殖洄游研究。E-mail: xmw0212@163.com
唐文喬, 教授, 博士生導師。E-mail: wqtang@shou.edu.cn

