白藜蘆醇對高脂脅迫團頭魴抗氧化能力、非特異免疫機能和抗病力的影響
閆亞楠 夏斯蕾 田紅艷 徐 超 賈二騰 劉文斌 張定東
(南京農業大學動物科技學院, 江蘇省水產動物營養重點實驗室, 南京 210095)
白藜蘆醇對高脂脅迫團頭魴抗氧化能力、非特異免疫機能和抗病力的影響
閆亞楠 夏斯蕾 田紅艷 徐 超 賈二騰 劉文斌 張定東
(南京農業大學動物科技學院, 江蘇省水產動物營養重點實驗室, 南京 210095)
為探討白藜蘆醇(RSV)對高脂脅迫團頭魴特定生長率、抗氧化能力、非特異免疫機能和抗病力的影響,試驗設計5組飼料: 正常脂組(脂肪水平5%)、高脂組(脂肪水平11%)以及在高脂組中分別添加0.04%、0.36%、1.08% RSV。養殖試驗持續10周, 在采樣結束后, 進行嗜水氣單胞菌攻毒試驗, 記錄攻毒后96h的成活率。結果表明: 團頭魴的特定生長率和日均采食量在添加1.08% RSV組出現最小值, 并顯著低于其他各組, 且團頭魴的飼料效率表現出相似趨勢。長期高脂飼喂可導致團頭魴血漿GSH含量顯著下降, 血漿MDA和NO含量顯著升高, 形成氧化應激。而長期氧化應激狀態, 可使團頭魴血漿溶菌酶活性和補體C3含量顯著降低, 肝臟中HSP70和HSP90應激調控基因表達上調, TNF-α炎癥反應基因表達也上調。添加0.04% RSV組顯著降低了血漿中SOD活性; 添加0.36%和1.08% RSV組顯著降低血漿MDA和NO含量, 顯著抑制了血漿SOD和CAT活性,且添加1.08% RSV組顯著增加了魚體血漿GSH含量。添加0.04%、0.36%和1.08%RSV組均顯著提高了團頭魴血漿補體C3含量和溶菌酶活性, 顯著下調了高脂脅迫團頭魴肝臟中HSP70、HSP90與TNF-α mRNA的表達量。嗜水氣單胞菌攻毒后團頭魴的成活率顯著受到RSV的影響, 并且在1.08% RSV添加組成活率最大。綜上結果表明, 團頭魴攝食高脂日糧之后, 機體處于氧化應激狀態, 導致魚體非特異免疫力和抗病力低下。而添加適宜劑量的RSV能夠改善機體這種氧化應激的狀態, 提高魚體的非特異免疫力和抗病力, 其中以1.08%的添加量最優。
白藜蘆醇; 高脂脅迫; 抗氧化; 非特異性免疫; 團頭魴
白藜蘆醇(Resveratrol, RSV), 是一種含有芪類結構的非黃酮類的多酚化合物, 分子式C14H12O3,結構為3,4,5-三羥基二苯乙烯(trans-3,4,5-Tri-hydroxystilbene), 廣泛存在于花生、葡萄、桑葚等種子植物中[1]。近年來, 國內外的學者對其藥理作用進行研究, 發現白藜蘆醇具有抗氧化、抗菌消炎、抗白血病、降脂和提高機體免疫力等功能。大量動物體內和體外試驗的研究都發現, RSV可以通過上調沉默信息調節因子1(Sirtuin1, SIRT1)的酶活性, 抑制SREBP下游基因的表達, 調節機體糖脂代謝, 并且RSV還能調節AMP依賴的蛋白激酶[Adenosine 5'-monophosphate (AMP)-activated protein kinase, AMPK]代謝調控因子的轉錄和表達, 進而調控動物體內的物質和能量代謝, 從而達到預防和治療一些代謝性疾病的作用[2,3]。
脂肪肝是由遺傳-環境-代謝應激相關因素導致的以肝細胞脂肪變性為主的一種代謝性疾病, 臨床上有酒精性脂肪肝和非酒精性脂肪肝(NAFLD)之分, 目前研究較多的是NAFLD, 其發生與胰島素抵抗(IR)密切相關, 因此糾正代謝紊亂對該病的治療有重要作用[4]。而隨著高密度水產養殖的發展, 飼料中脂肪含量過高、過度投喂、蛋能比失調等營養素原因造成養殖魚類營養性脂肪肝問題越來越突出。而肝臟作為魚類重要的代謝器官, 其損傷或病變將導致機體代謝機能紊亂和抗病力降低, 極易造成繼發傳染性疾病的暴發和肝膽綜合征的肆虐,嚴重威脅著集約化水產養殖業的持續健康發展[5]。
團頭魴(Megalobrama amblycephala), 俗稱武昌魚, 是我國養殖的主要經濟魚類之一, 生產中面臨嚴峻的脂肪肝問題。Lu等[6]研究表明, 長期攝食高脂日糧能夠誘導團頭魴產生肥胖和IR, 患上脂肪肝,可以為研究魚類脂肪肝的發生、發展、預防和治療機制提供較理想的動物模型。基于此, 本研究擬在團頭魴高脂日糧中添加RSV, 通過測定團頭魴抗氧化能力、非特異免疫機能和抗病力, 評估RSV作為添加劑, 應用于緩解高脂協迫以及預防和治療魚類脂肪肝的潛在作用, 以期為今后生產研究提供依據。
1 材料與方法
1.1 試驗設計和飼料配方
試驗飼料配方見表 1, 設計兩個對照組, 即正常脂組(Normal-fat diet, NFD; 脂肪水平5%)和高脂組(High-fat diet, HFD; 脂肪水平11%), 參考RSV在小鼠和大鼠上的研究[2,3], 本試驗在高脂日糧中以0.04%、0.36%、1.08%的梯度添加白藜蘆醇。白藜蘆醇(HPLC純度>98%)購自湖北巨勝科技有限公司。根據飼料配方將各個原料粉碎、稱重、充分混合均勻后, 加適量水, 使用小型飼料顆粒機制成粒徑2 mm水穩性良好的沉性顆粒料, 于通風處晾干后置于-20℃冰箱保存備用。
1.2 養殖試驗
養殖試驗在南京農業大學浦口基地戶外網箱進行, 試驗塘規格: 100 m×50 m (長×寬), 水深平均1.7 m。試驗幼魚購自江蘇廣陵長江系家魚原種場。馴化一周后, 選取規格整齊體格健壯的幼魚[初重: (28±0.10) g]320尾, 隨機分配到20個網箱(規格: 1.0 m×1.0 m×1.0 m)中, 每個網箱16尾, 投喂5組飼料, 每組設4個重復。戶外養殖期間, 每天定時投餌3次(7:30, 12:00和16:30), 飽食投喂, 養殖期為10周。試驗期間定期檢測水質: 水溫23—31℃, DO>5.0 mg/L, pH 7.0—7.5。

表 1 試驗飼料配方與營養水平Tab. 1 Formulation and proximate composition of the experimental diets
1.3 樣品采集及分析
養殖試驗結束后, 禁食24h以排空腸道內容物。使用MS-222(濃度100 mg/L; Sigma, 美國)麻醉,依次清點尾數并分箱稱重, 計算其特定生長率。每網箱隨機取4尾魚在冰袋上進行尾靜脈采血和肝臟樣本采集。血液采集后放入抗凝管(肝素鈉處理),于3000 g和4℃下離心10min, 吸取上清液標記分裝后存入-80℃冰箱保存備用。肝臟采集后用4℃預冷的生理鹽水沖洗干凈, 然后用濾紙吸干, 放入1 mL凍存管中用液氮速凍后置-80℃冰箱保存備用。
1.4 飼料常規營養成分分析
水分測定使用烘箱105℃烘至恒重, 粗蛋白使用瑞士Foss公司生產的半自動凱氏定氮儀, 粗灰分采取馬弗爐中550℃充分灼燒6h, 粗脂肪采用索氏抽提裝置進行測定7h, 能量采用通用熱彈能儀測定。
1.5 血漿免疫指標測定
血漿溶菌酶活性, 使用濁度比色法測定[7]; 血漿補體C3采用酶聯免疫吸附法測定; 總蛋白采用雙縮脲法測定; 血漿中白蛋白含量采用微量酶標儀法;血漿酸性磷酸酶(Acid phosphatase, ACP)含量采用磷酸苯二鈉法測定。以上試劑盒均購自南京建成生物科技有限公司。
血漿超氧化物歧化酶(Superoxide dismutase, SOD)采用氮藍四唑光化還原法測定, 過氧化氫化酶(Catalase, CAT)采用用H2O2還原法測定, 丙二醛(Malondialdehyde, MDA)采用硫代巴比妥比色法測定, 谷胱甘肽過氧化物酶(Glutathione peroxidase, GSH-PX)和谷胱甘肽還原酶(Glutathione reductase, GSH)采用酶偶聯連續監測法。以上試劑盒均購自南京建成生物科技有限公司。
1.6 嗜水氣單胞菌攻毒試驗
本試驗使用的嗜水氣單胞菌菌種(WJ2011BJ44)由中國水產科學研究院淡水漁業研究中心提供。在無菌條件下, 取-80℃保存菌種劃線接種在瓊脂固體平板培養基中, 恒溫箱28℃培養20h后, 挑取單獨菌落接種于5 mL肉湯液體培養基中, 28℃搖床恒溫過夜培養(180 r/min)。使用肉湯液體培養基將菌液按10倍系列濃度稀釋(1×106、1×107、1×108、1×109、1×1010CFU/mL), 通過在團頭魴腹部注射不同濃度梯度的嗜水氣單胞菌攻毒預試驗, 從而獲得該菌的半致死濃度為1×107CFU/mL。
在采樣結束后, 將室外網箱內每組剩余的實驗魚挪到室內循環系統內, 適應3d后, 每組魚腹腔注射稀釋好的菌液(1×107CFU/mL), 注射劑量為每100 g魚注射1 mL。注射結束后, 觀察統計實驗魚攻毒后6h、12h、24h、48h、72h、96h時的存活尾數。
1.7 肝臟熱休克蛋白70(HSP70)、熱休克蛋白90(HSP90)及腫瘤壞死因子α (TNF-α)基因表達的測定
肝臟總RNA提取: 取大約50—100 mg的團頭魴肝臟樣品, 放入含有1 mL RNA-iso Plus (Takara公司)的離心管中, 之后按照RNA-iso Plus試劑盒中說明書操作, 提取總RNA。最終獲得的樣品總RNA其OD260/OD280在1.8—2.0。
反轉錄: 按照Takara Prime Script?RT reageat Kit反轉錄試劑盒說明書進行操作, 所得cDNA保存于-20℃冰箱備用。
定量PCR: (1) 引物設計: 根據GenBank數據庫中的序列, 使用Primer Premier 5.0軟件設計內參基因β-actin[8,9]、熱休克蛋白70(HSP70)、熱休克蛋白90(HSP90)、腫瘤壞死因子α (TNF-α), 引物序列參見表 2, 引物由上海Invitrogen公司合成。 (2)實時熒光定量PCR反應: 根據SYBR?Premix Ex Taq TM II (TaKaRa公司)試劑盒說明書進行加樣上機, 結果采用2-??Ct方法分析。
1.8 數據統計分析
數據用SPSS 20.0進行統計分析, 兩個對照組采用獨立樣本T檢驗法分析, 高脂組和RSV添加組則采用單因素方差(One-Way ANOVA)中Duncan's多重比較法分析, 結果用平均數±標準誤來表示。使用Graph Pad Prism 5和Microsoft Excel 2010軟件進行圖形繪制。
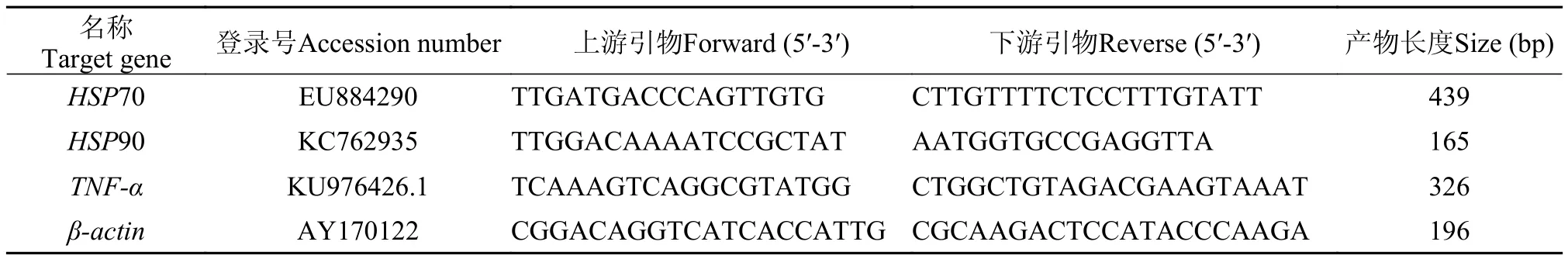
表 2 定量PCR引物序列Tab. 2 The primers used in quantitative real-time PCR
2 結果
2.1 RSV對投喂高脂日糧團頭魴特定生長率(SGR)的影響
如圖 1所示, NFD和HFD兩組的飼養期間成活率、SGR、日均采食量和飼料效率(FCR)均無顯著差異; 高脂組和高脂添加RSV組飼養期間成活率無顯著差異, 而1.08%RSV組的SGR和日均采食量均顯著低于其他各組, 且該組團頭魴的飼料效率也低于其他各組。
2.2 RSV對投喂高脂日糧團頭魴血漿抗氧化指標的影響
由圖 2可以得出, 與正常脂日糧相比, 投喂高脂日糧之后團頭魴血漿SOD、CAT、MDA和NO顯著提高, 而血漿GSH顯著降低。添加0.36% RSV和1.08% RSV之后, 血漿CAT、MDA和NO與高脂組相比顯著降低; 而血漿GSH僅在RSV1.08%添加水平顯著升高, 在0.04% RSV和0.36%RSV添加水平,血漿GSH雖然有所升高, 但無顯著差異; 添加0.04%—1.08%水平的RSV, 與高脂組相比, 可顯著降低血漿SOD。
2.3 RSV對投喂高脂日糧團頭魴血漿免疫指標的影響
從圖 3可以得出, 與正常脂日糧相比, 投喂高脂日糧之后, 團頭魴血漿白蛋白有所降低, 但無顯著差異, 但血漿補體C3、總蛋白、球蛋白、溶菌酶以及ACP都顯著降低。在添加RSV之后, 與高脂組相比, 不同添加量的RSV均顯著提高了血漿補體C3和溶菌酶含量; 血漿總蛋白、白蛋白、球蛋白以及ACP僅在HFD+0.04% RSV組顯著升高, 而其他各組相比高脂組均無顯著差異。
2.4 RSV對投喂高脂日糧團頭魴肝臟HSP70、HSP90及TNF-α mRNA表達量的影響
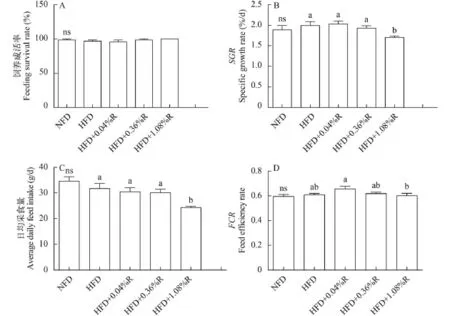
圖 1 RSV對投喂高脂日糧團頭魴飼養期間成活率、SGR、日均采食量和飼料效率(FCR)的影響Fig. 1 Effects of RSV supplementation on survival rate, SGR, average daily feed intake and feed efficiency rate of blunt snout bream fed high-fat diets高脂組和高脂添加RSV組中,a,b,c字母不同表示差異顯著(P<0.05); 正常脂與高脂組采用T-檢驗, *P<0.05, **P<0.01, ***P<0.001,nsP>0.05; 下同; 飼養成活率=100×(實驗末魚數量/實驗初魚數量), 特定生長率=100×ln(W末重/W初重)/t (養殖天數), 日均采食量=總采食量/飼養天數(d), 飼料效率=增重(g)/攝食量(g)Among HFD and HFD+RSV groups, mean values with different letters were significantly different (P<0.05); student's T-test analysis were used to explore the difference between NFD and HFD: *P<0.05, **P<0.01, ***P<0.001,nsP>0.05; the same applies below. Feeding survival rate=100×(the number of survival fish after feeding/ the number of fish before feeding), Specific growth rate, SGR=100×ln(Wfinalweight/Winitialweight)/t, Average daily feed intake=total feed intake/t (d), Feed efficiency rate=weight (g)/food intake (g)
由圖 4可以得出, 團頭魴肝臟HSP70、HSP90與TNF-α mRNA的表達量顯著受飼料中脂肪水平和RSV添加的影響。與正常脂日糧相比, 投喂高脂日糧之后團頭魴肝臟HSP70、HSP90與TNF-α mRNA的表達量顯著升高。在添加RSV之后, 與高脂組相比, 團頭魴肝臟HSP70、HSP90與TNF-α mRNA的表達量顯著下降。
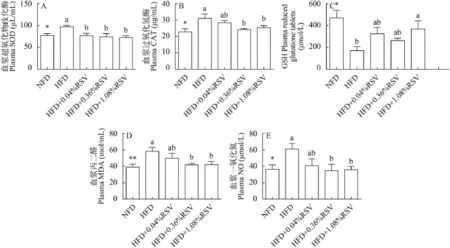
圖 2 RSV對投喂高脂日糧團頭魴血漿抗氧化指標的影響Fig. 2 Effects of RSV supplementation on plasma antioxidant capacity of blunt snout bream fed high-fat diets

圖 3 RSV對投喂高脂日糧團頭魴血漿免疫指標的影響Fig. 3 Effects of RSV supplementation on innate immunity of blunt snout bream fed high-fat diets
2.5 攻毒試驗累計死亡率
圖 5為團頭魴攻毒后96h成活率, 試驗結果表明: 飼料中脂肪水平可影響團頭魴的成活率, 正常脂組48h和72h成活率顯著高于高脂組, 96h時則無顯著差異; 團頭魴攻毒后的成活率又受RSV影響, RSV顯著提高了團頭魴48h和72h的成活率, 并且96h時1.08% RSV添加組的成活率最高, 顯著高于高脂組。
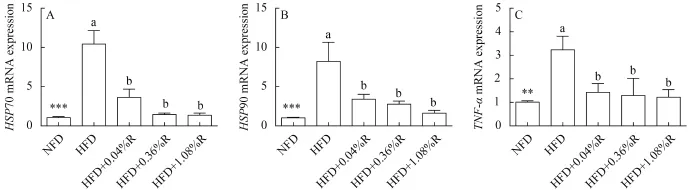
圖 4 團頭魴肝臟HSP70、HSP90與TNF-α mRNA相對表達量Fig. 4 Relative mRNA expression analysis of HSP70, HSP90 and TNF-α in the liver of blunt snout bream fed high-fat diets
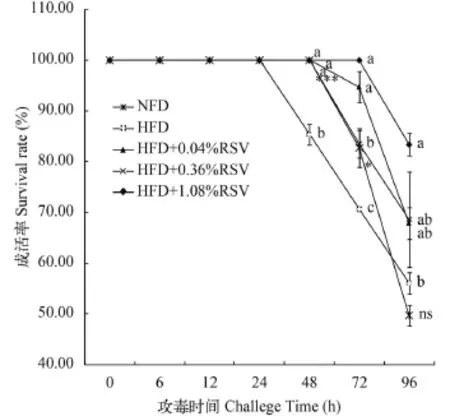
圖 5 嗜水氣單胞菌攻毒后96h的存活率(%)Fig. 5 Survival rates (%) of blunt snout bream after 96h of Aeromonas hydrophila challenge成活率(%)=(攻毒試驗結束存活魚數/攻毒試驗開始魚總數)× 100%Survival rate (%)=(the number of survival fish after infection/the number of fish before infection)×100%
3 討論
3.1 RSV對投喂高脂日糧團頭魴生長性能的影響
SGR是指生長率與生長天數的比值, 是衡量生長狀況的一個常用指標, 和增重率趨勢相同, 但又比增重率更加形象具體的反映動物的生長狀況, SGR越小, 代表每天的體重增長越慢[10]。 本試驗中, 1.08% RSV添加組的SGR顯著低于其他各組, 表明1.08%劑量的RSV能夠調控高脂脅迫下的團頭魴的體重, 這可能與RSV的降脂和攝食神經調節[11]作用有關。 許多研究表明, RSV能夠減少脂肪在一些組織和器官中過度沉積, 而其對動物體體重的調節受到RSV的劑量、試驗的動物種類和膳食結構等多種因素的影響[12,13]。本實驗室前期研究也證實了添加較高劑量的RSV可導致團頭魴體增重明顯下降, 其原因可能是: 一方面隨著RSV劑量的升高,肝臟脂肪和腹部脂肪含量呈下降趨勢, 且肝臟脂肪含量在RSV添加量為1.08%時顯著低于高脂組; 另一方面魚體內過多的RSV通過某種機制影響團頭魴采食, 減少餌料攝入。在本試驗中添加1.08%的RSV顯著影響團頭魴的日均采食量, 并且該組的飼料效率也顯著降低, 這可能與RSV對物質和能量代謝的調控作用有關[3]。上述因素導致了本試驗中1.08% RSV添加組團頭魴的SGR顯著低于其他各組。RSV能夠調節動物體的糖脂代謝, 調控相關基因的轉錄和表達[13,14], 并能影響采食量。在嚙齒動物上也有類似的研究結果, 并認為RSV能夠通過血腦屏障, 減少動物體的食物攝入[11,15]。因此, 在團頭魴高脂日糧中添加RSV既能緩解高脂脅迫又不影響生長性能的最低有效劑量, 仍需要我們進一步的研究。
3.2 RSV對投喂高脂日糧團頭魴抗氧化能力的影響
動物機體在新陳代謝過程中, 活性氧自由基的產生和消除保持著動態平衡[16]。而長期投喂高脂日糧會造成魚類的組織及細胞的線粒體膜超微結構發生改變, 導致線粒體膜通透性增大, 致使大量活性氧自由基(ROS)擴散到細胞的各個角落, 引起機體脂類、蛋白質、酶和DNA的氧化, 形成機體損傷[17]。而SOD可以催化活性氧(O2-)轉化為H2O2與O2, H2O2又可通過CAT和谷胱甘肽還原酶轉化為H2O, 從而保持了機體的氧化平衡, 減少了自由基對機體的傷害。MDA作為脂質過氧化的最終產物,具有細胞毒性, 會引起蛋白質、核酸等生命大分子的交聯聚合, 從而可以作為機體脂質過氧化的標志。在本研究中, 高脂組血漿SOD和CAT活性均顯著高于正常脂組, 可是其血漿中MDA的含量很高,血漿GSH含量卻很低, 說明高脂組魚體ROS的產生量遠遠大于機體自身的清除能力。而在添加RSV之后, 各組血漿兩種抗氧化酶的活性都有所降低,血漿MDA的含量顯著降低, 血漿GSH含量顯著升高, 說明魚體ROS的產生量未超出機體清除能力。在段勝紅[18]有關RSV對大鼠非酒精性脂肪肝的保護作用的研究發現RSV顯著降低模型組大鼠肝組織MDA含量, 同時在高妍等[19]有關烏克蘭鱗鯉的研究中發現當飼料中添加80—160 mg/kg RSV時,烏克蘭鱗鯉血漿MDA含量顯著降低。以上研究與本試驗結果一致, 說明RSV能夠提高動物機體的抗氧化能力, 抑制脂質過氧化反應。有研究表明, NO與氧化性肝損傷相關, 大量的NO則反而引起肝細胞損傷, 而適量的NO則對心血管起保護作用[20]。在本試驗中, 高脂組血漿NO含量顯著高于正常脂組, 而添加RSV之后血漿NO含量顯著降低, 該現象也表明RSV可減緩高脂脅迫誘導的肝臟損傷。在大鼠的研究中也得到相似的結果[21], 說明RSV可能通過降低iNOS活性及升高cNOS活性從而糾正了機體NO代謝的紊亂。TNF-α不僅是NAFLD的一個易感因子, 而且也是介導肝損傷的主要細胞因子之一,同時TNF-α及其誘導產生的一些細胞因子, 又可引起游離脂肪酸的增多, 從而進一步促進NAFLD的發展[22,23]。在本試驗中, 高脂組肝臟中TNF-α mRNA表達量顯著高于正常脂組, 表明高脂日糧可誘導團頭魴肝臟炎癥反應, 而添加RSV之后, 各試驗組中肝臟中TNF-α mRNA表達量均顯著低于高脂組, 說明RSV能夠減輕肝臟炎癥損傷。小鼠上也得到了類似的結果[24], 研究表明RSV在一定程度上能夠上調小鼠組織或細胞中SIRT1的表達, 進而調控炎癥因子及相關信號傳導通路, 從而抑制炎癥反應[25,26]。
3.3 RSV對投喂高脂日糧團頭魴免疫功能的影響
HSP70和HSP90均參與應激條件下的免疫應答反應, 其表達量在環境和生理的變化下都會隨之改變[27—28], 因此, HSP70和HSP90均是應激反應的重要指標。TNF-α也參與動物體內的免疫反應, 在許多病理狀態下產生增多, 調節機體免疫功能。高脂組團頭魴肝臟中HSP70、HSP90 和TNF-α mRNA表達量均顯著高于正常脂組, 表明試驗團頭魴已處于應激狀態中。而應激和免疫的關系密切相關, 長期的氧化應激或其他類型的應激反應都可能會損害機體的免疫器官, 降低機體的免疫功能[29,30]。ACP是魚類體內巨噬細胞溶酶體的標志性酶[31]。溶菌酶是魚類防護病原體入侵的重要非特異性免疫因子, 通過水解致病菌的黏多糖, 來達到抵抗外界細菌入侵的目的[32]。補體C3是血清中含量最高的補體成分, 參與機體抗微生物防御反應以及免疫調節,其水平是衡量動物機體體液免疫的重要標志[33]。血漿蛋白作為血漿的重要組成部分, 反映機體的健康狀況, 血漿蛋白的升高也與免疫力的增強有關,而在所有的蛋白組成中球蛋白是重要的組成成分,在免疫系統中發揮重要作用[34]。本試驗結果顯示高脂組團頭魴血漿ACP和溶菌酶活性以及補體C3、總蛋白和球蛋白含量均顯著低于正常脂組, 表明高脂組魚體受到氧化應激, 導致其非特異性免疫力下降, 并伴有肝臟損傷[29]。然而, RSV添加組團頭魴血漿補體C3含量和溶菌酶活性均顯著高于高脂組,表明RSV增強了高脂脅迫團頭魴的免疫功能。同時, 添加RSV之后團頭魴血漿總蛋白、白蛋白、球蛋白含量及ACP活性均高于高脂組, 這再次說明RSV可提高團頭魴的免疫力。類似的結果也發表在其他動物上。在酒劑中添加RSV經口灌胃, 能顯著增強小鼠細胞免疫、體液免疫和單核-巨噬細胞功能[35]; 在飼料中添加120 mg/kg的RSV可提高血鸚鵡溶菌酶活力[36]; 在日糧中添加0.1%至0.2% RSV有利于提高肉仔雞的免疫功能[37]。
3.4 RSV對投喂高脂日糧團頭魴抗病能力的影響
本試驗結果顯示, 添加適宜水平的RSV提高了團頭魴嗜水氣單胞菌感染之后的成活率, 成活率最高值出現在1.08%RSV組, 在日糧中添加0.04%和0.36%的RSV也提高了高脂脅迫下團頭魴的成活率。這與本試驗抗氧化和非特異免疫指標結果基本一致, 說明RSV通過提高高脂脅迫團頭魴魚體的抗氧化能力和免疫力, 提高了抗病力。RSV能通過阻礙生物膜的形成來降低細菌的耐藥性、阻礙細菌的毒性因子發揮作用, 并能抑制創傷弧菌的黏附及RTX毒素的產生, 來達到保護宿主細胞免受細菌感染引起的毒害和感染的目的[38—42], 推測RSV本身對嗜水氣單胞菌生長有抑制作用, 減弱該菌毒性。有文獻報道, RSV能通過Fiaf (快速誘導脂類因子)信號通路調節腸道菌群的組分, 改善小鼠高脂膳食引起的腸道菌群生態失調[38,43]。而腸道菌群調控下的腸黏膜系統調控動物的免疫與健康, 腸道是機體最大的免疫器官[44]。因此, 我們推測RSV通過調節團頭魴腸道菌群, 增強團頭魴腸道免疫力, 從而提高團頭魴的抗病力, 該機理有待我們后續研究進一步證明。
4 結論
綜上所述, 在高脂脅迫團頭魴的日糧中添加1.08%的RSV時能夠調控團頭魴的體重和日均攝食量, 能夠顯著提高團頭魴的抗氧化能力, 并且能夠提高團頭魴的非特異性免疫功能和抗病力。因此,在本試驗中團頭魴高脂日糧中RSV的適宜添加水平是1.08%。
[1]Park E J, Pezzuto J M. The pharmacology of resveratrol in animals and humans [J]. Biochimica Et Biophysica Acta, 2015, 1852(6): 1071—1113
[2]Smoliga J M, Baur J A, Hausenblas H A. Resveratrol and health & ndash; A comprehensive review of human clinical trials [J]. Molecular Nutrition & Food Research, 2011, 55(8):1129—1141
[3]Zhou B, Zhai Q W. Sirtuins in glucose and lipid metabolism [J]. Chinese Bulletin of Life Sciences, 2013, (2): 140—151 [周犇, 翟琦巍. Sirtuin蛋白家族和糖脂代謝.生命科學, 2013, (2): 140—151]
[4]Fan J G.Metabolic syndrome and fatty liver [R]. China Academic Journal Electronic Publishing House. 2005 [范建高. 代謝綜合征與脂肪肝. 全國脂肪性肝病專題研討會. 2005]
[5]Yang H K. Mechanism in tilapia's fatty liver pathological changes of lecithin, choline and inositol in the feed [D]. Thesis for Master of Science Guangxi University. 2012 [楊鴻昆. 卵磷脂、膽堿和肌醇在羅非魚脂肪肝病變中的作用機制. 碩士學位論文, 廣西大學. 2006]
[6]Lu K L, Xu W N, Li J Y, et al. Alterations of liver histology and blood biochemistry in blunt snout bream (Megalobrama amblycephala) fed high-fat diets [J]. Fisheries Science, 2013, (74): 1—11
[7]Wu X. Effects of four kinds of Chinese herbal polysaccharides on the growth performance, body composition, and part of physiological and biochemical indicator in yellow catfish (Pelteobagrus fulvidraco) [D]. Tianjin Agriculture University. 2011 [吳旋. 四種中草藥多糖對黃顙魚生長、體成分及部分生理生化指標的影響. 天津農學院. 2011]
[8]Zhao Y, Gul Y, Li S, et al. Cloning, identification and accurate normalization expression analysis of PPARa gene by GeNorm in Megalobrama amblycephala [J]. Fish & Shellfish Immunology, 2011, 31(3): 462—468
[9]Tang L,Xiang X, Jiang Y,et al. Identification and characterization of a novel Toll-like receptor 4 homologue in blunt snout bream, Megalobrama amblycephala [J]. Fish & Shellfish Immunology, 2016, 57: 25—34
[10]Tong X H, Ge B M, Wang H L, et al. Correlation between morphological traits and body weight of japanese flounder during different periods [J]. Hubei Agricultural Sciences, 2014, 53(4): 863—865 [佟雪紅, 葛寶明,王歡莉, 等. 牙鲆不同發育期形態性狀與體重相關性分析. 湖北農業科學, 2014, 53(4): 863—865]
[11]Kim Y, Keogh J B, Clifton P M. Polyphenols and glycemic control [J]. Nutrients, 2016, doi: 10.3390/nu801001
[12]Baur J A, Pearson K J, Price N L, et al. Resveratrol improves health and survival of mice on a highcalorie diet [J]. Nature, 2006, 444(7117): 337—342
[13]Rocha K K, Souza G A, Ebaid G X, et al. Resveratrol toxicity: effects on risk factors for atherosclerosis and hepatic oxidative stress in standard and high-fat diets [J]. Food & Chemical Toxicology an International Journal Published for the British Industrial Biological Research Association, 2009, 47(6): 1362—1367
[14]Rivera L, Morón R, Zarzuelo A, et al. Long-term resveratrol administration reduces metabolic disturbances and lowers blood pressure in obese Zucker rats [J]. Biochemical Pharmacology, 2009, 77(6): 1053—1063
[15]Sasaki T, Kitamura T. Roles of Foxo1 and Sirt1 in the central regulation of food intake [J]. Endocrine Journal, 2010, 57(11): 939—946
[16]Wan J J, Liu B, Ge X P, et al. Effects of dietary vitamin c on the non-specific immunity, three HSPs mRNA expression and disease resistance of juvenile Wuchang bream (Megalobrama amblycephala) [J]. Acta Hydrobiologica Sinica, 2014, 38(1): 10—18 [萬金娟, 劉波, 戈賢平, 等.日糧中不同水平維生素C對團頭魴幼魚免疫力的影響.水生生物學報, 2014, 38(1): 10—18]
[17]Tort L. Stress and immune modulation in fish [J]. Developmental & Comparative Immunology, 2011, 35(12): 1366—1375
[18]Duan S H. Effect of resveratro1 on protecting nonalcoholic fat liver in rates induced by high fat diet [J]. Chinese Medicine Modern Distance Education of China, 2009, 7(5): 127—128 [段勝紅. 白藜蘆醇對大鼠非酒精性脂肪肝的保護作用. 中國中醫藥現代遠程教育, 2009, 7(5): 127—128]
[19]Gao Y, Fang Z Z, Zhu G X, et al. Effects of different levels of resveratrol on parts of biochemical indices of Ukraine carp (Cyprinus carpio) [J]. Feed Industry, 2015, (2): 25—29 [高妍, 方珍珍, 朱國霞, 等. 不同水平白藜蘆醇對烏克蘭鱗鯉部分生化指標的影響. 飼料工業, 2015, (2): 25—29]
[20]Li W, Liu J, Bai J Y, et al. Progress on tumor necrosis Factor-α [J]. Progress in Veterinary Medicine, 2010, 31(12): 108—111 [李衛, 劉佳, 白家媛, 等. α腫瘤壞死因子的研究進展. 動物醫學進展, 2010, 31(12): 108—111]
[21]Zhu L X, Jin Z Y. Effects of piceid on blood lipid metabolism, nitric oxide and nitricoxide synthase in experimental hyperlipidemia rats [J]. Pharmacology and Clinics of Chinese Materia Medica, 2005, 21(3): 16—18 [朱立賢, 金征宇. 白藜蘆醇苷對高脂血癥大鼠血脂、一氧化氮及一氧化氮合酶的影響. 中藥藥理與臨床, 2005, 21(3):16—18]
[22]Sun H. The expression and significance of tumor necrosis factor α in liver of patients with nonalcoholic steato-hepatitis [D]. Hebei Medical University. 2009 [孫惠. 非酒精性脂肪性肝炎患者肝組織腫瘤壞死因子α的表達及其意義. 河北醫科大學. 2009]
[23]Valenti L, Fracanzani A L, Dong io vanni P, et al. Tumor necrosis factor alpha promoter polymor phisms and insulin resistance in nonalcoholic fatty liver disease [J]. Gastroenterology, 2002, 122(2): 274—280
[24]Andrade J M, Paraiso A F, de Oliveira M V, et al. Resveratrol attenuates hepatic steatosis in high-fat fed mice by decreasing lipogenesis and inflammation [J]. Nutrition, 2014, 30(7—8): 915—919
[25]Yoshizaki T, Milne J C, Imamura T, et al. SIRT1 exerts anti-inflammatory effects and improves insulin sensitivity in adipocytes [J]. Molecular & Cellular Biology, 2009, 29(5): 1363—1374
[26]Pfluger P T, Herranz D, Velasco-miguel S, et al. Sirt1 protects against high-fat diet-induced metabolic damage [J]. Proceedings of the National Academy of Sciences, 2008, 105(28): 9793—9788
[27]Kagawa N, Mugiya Y. Brain HSP70 mRNA expression is linked with plasma cortisol levels in goldfish (Carassius auratus) exposed to a potential predator [J]. Zoologicalence, 2002, 19: 735—740
[28]Fu D, Chen J, Zhang Y, et al. Cloning and expression of a heat shock protein (HSP) 90 gene in the haemocytes of Crassostrea hongkongensis under osmotic stress and bacterial challenge [J]. Fish & Shellfish Immunology, 2011, 31(1): 118—125
[29]Lu K L, Xu W N, Liu W B, et al. Association of Mitochondria dysfunction with Oxidative stress and Immune suppression in Blunt Snout Bream (Megalobrama amblycephala) fed a high-fat diet [J]. Journal of Aquatic Animal Health, 2014, (26): 100—112
[30]Tahmasebi-Kohyani A, Keyvanshokooh S, Nematollahi A, et al. Effects of dietary nucleotides supplementation on rainbow trout (Oncorhynchus mykiss) performance and acute stress response [J]. Fish Physiology and Biochemistry, 2012, 38(2): 431—440
[31]Jin S. Study on Physiological, Biochemical and Molecular Mechanism of enchanced Immunity ability by Chitosan in Ayu (Plecoglossus altivelis) [D]. Ningbo University. 2012 [金思. 殼聚糖提高香魚免疫力的生理生化及分子機理研究. 寧波大學. 2012]
[32]Wang M J, Liu D D, Qiao D, et al. The G-Type Lysozymes in Fish and Application in Fishes [R]. The China Society of Fisheries. 2013, 195—200 [王美娟, 劉丹丹,喬丹, 等. 魚類g型和c型溶菌酶及其在漁業生產上的應用. 中國水產學會魚病專業委員會學術研討會. 2013, 195—200]
[33]Holland M C H, Lambris J D. The complement system in teleosts [J]. Fish and Shellfish Immunology, 2002, 12(5): 399—420
[34]Magnadottir B. Immunological control of fish diseases [J]. Marine Biotechnology, 2010, 12(4): 361—379
[35]Zhou L Z, Yin J. Effect of resveratrol vina on immune function in mice [J]. Journal of Traditional Chinese Medicine University of Hunan, 2009, 29(1): 41—43 [周玲芝, 尹進. 白藜蘆醇酒劑對小鼠免疫功能影響的研究.湖南中醫藥大學學報, 2009, 29(1): 41—43]
[36]Cui P, Fan Z, Li J, et al. Effects of dietary resveratrol levels on biochemical parameters in liver of blood parrot Amphilophus labiatus♂×Cichlasoma synspilum♀ [J]. Journal of Dalian Ocean University, 2015, 30(2): 203—206 [崔培, 范澤, 李建, 等. 飼料中添加白藜蘆醇對血鸚鵡肝臟生化指標的影響. 大連海洋大學學報, 2015, 30(2): 203—206]
[37]Zhang C Y, Guo W J, Gong F, et al. Effects of dietary resveratrol on serum biochemical parameters and immune function in broilers [J]. Chinese Journal of Animal Science, 2010, 46(19): 51—53 [張彩云, 郭衛建, 龔芳,等. 白藜蘆醇對肉仔雞免疫性能及血清生化指標的影響. 中國畜牧雜志, 2010, 46(19): 51—53]
[38]Li P, Cheng X X. The effects of resveratrol on antibacterial and antiviral properties [J]. Chinese Journal of Microecology, 2014, 26(10): 1215—1219 [李萍, 程曉馨. 白藜蘆醇抗菌抗病毒作用的研究進展. 中國微生態學雜志, 2014, 26(10):1215—1219]
[39]Zhang R, Li Y J, Wang X. Recent development antibacterial effect of resveratrol [J]. Journal of Hebei Medical University, 2010, 31(9): 1151—1154 [張瑞, 李永軍, 王鑫. 白藜蘆醇抗菌作用的研究進展. 河北醫科大學學報, 2010, 31(9): 1151—1154]
[40]Kim J R, Mi H C, Oh D R, et al. Resveratrol modulates RTX toxin-induced cytotoxicity through interference in adhesion and toxin production [J]. European Journal Pharmacology, 2010, 642(1—3): 163—168
[41]Sambanthamoorthy K, Sloup R E, Parashar V, et al. Identification of small molecules thatantagonize diguanylatecyclase enzymes to inhibit biofilm formation [J]. Antimicrobial Agents & Chemotherapy, 2012, 56(10): 5202—5211
[42]Augustine N, Goelb A K, Sivakumarc K C, et al. Resveratrol-A potentialin-hibitor of biofilm formation in Vibrio cholera [J]. Phytomedicine International Journal of Phytotherapy & Phytopharmacology, 2014, 21(3): 286—289
[43]Qiao Y, Sun J, Xia S, et al. Effects of resveratrol on gut microbiota and fat storage in a mouse model with highfat-induced obesity [J]. Food Function, 2014, 5(6): 1241—1249
[44]Lei C L, Dong G Z. Regulation of intestinal mucosal immunity by intestinal flora in animals [J]. Chinese Journal of Animal Nutrition, 2012, 24(3): 416—422 [雷春龍, 董國忠. 腸道菌群對動物腸黏膜免疫的調控作用. 動物營養學報, 2012, 24(3): 416—422]
EFFECTS OF RESVERATROL SUPPLEMENTATION ON GROWTH PERFORMANCE, IMMUNITY, ANTIOXIDANT CAPABILITY AND DISEASE RESISTANCE OF BLUNT SNOUT BREAM FED HIGH-FAT DIET
YAN Ya-Nan, XIA Si-Lei, TIAN Hong-Yan, XU Chao, JIA Er-Teng, LIU Wen-Bin and ZHANG Ding-Dong
(Jiangsu Key Laboratory of Aquatic Animal Nutrition, College of Animal Science and Technology, Nanjing Agricultural University, Nanjing 210095, China)
This study was conducted to investigate the effects of Resveratrol (RSV) supplementation on specific growth rate (SGR), nonspecific immunity function, antioxidant capability and disease resistance of blunt snout bream fed highfat diet. This experiment was designed with five kinds of diets: a normal fat diet (NFD, 5% fat), a HFD (11% fat), and a HFD supplemented with 0.04%, 0.36%, and 1.08% RSV, respectively. At the end of 10-week feeding trial, fish were challenged by Aeromonas hydrophila at the concentration of 1×107CFU/mL, and the survival rate was recorded for the next 96h. The results showed that HFD supplemented with 1.08% RSV significantly reduced the SGR and average daily feed intake of blunt snout bream when compared to the other groups, the similar trend found in feed efficiency rate of blunt snout bream. In comparison with NFD, HFD significantly increased the levels of plasma MDA and NO, and decreased the level of plasma GSH in blunt snout bream. QRT-PCR results demonstrated that long-term HFD consumption induced the up-regulation of TNF-α, HSP70 and HSP90, which means HFD potently weaken antioxidant defenses in blunt snout bream. HFD supplemented with RSV at 0.04% significantly suppressed the activities of the plasma SOD. And yet, it not only significantly reduced the contents of plasma MDA and NO, but also significantly inhibited the activities of plasma SOD and CAT when HFD supplemented with 0.36% and 1.08% RSV. Besides, the plasma GSH content increased significantly when the fish fed HFD supplemented with 1.08% RSV. HFD supplemented with RSV at 0.04%, 0.36% and 1.08% all significantly increased plasma complement 3 content, enhanced lysozyme activities, and down-regulated the mRNA expressions of hepatic HSP70, HSP90 and TNF-α in blunt snout bream. After A. hydrophila challenge, the significant highest survival rate was observed in fish fed 1.08% RSV supplemented diet. In summary, when blunt snout bream was fed with high-fat diet for long time, the body was in a state of oxidative stress. And, the appropriate dose of RSV added could ameliorate the state of oxidative stress in the body, then the optimal dose of resveratrol was 1.08%.
Resveratrol; High-fat diet; Antioxidant ability; Non-specific immunity; Blunt snout bream
S965.1
A
1000-3207(2017)01-0155-10
10.7541/2017.20
2016-08-15;
2016-11-04
國家大宗淡水魚產業技術體系資金(CARS-49-20)資助 [Supported by the National Technology System for Conventional Freshwater Fish Industries (CARS-46-20)]
閆亞楠(1990—), 女, 河南商丘人; 碩士研究生; 主要研究方向為水產動物營養與飼料。E-mail: 2014105073@njau.edu.cn
張定東(1975—), 男, 博士, 副教授; 主要從事水產動物生理與營養、水產養殖生態的研究。E-mail: zdd_7597@njau.edu.cn

