長牡蠣精子超低溫冷凍后超微結構損傷研究
韓龍江劉清華許 飛溫海深李 軍
(1. 中國科學院海洋研究所, 中科院實驗海洋生物學重點實驗室,青島 266071; 2. 中國海洋大學, 青島 266009; 3. 海洋生態養殖技術國家地方聯合工程實驗室, 青島 266071; 4. 青島海洋科學與技術國家實驗室,
海洋生物學與生物技術功能實驗室 青島 266237)
長牡蠣精子超低溫冷凍后超微結構損傷研究
韓龍江1,2劉清華1,3,4許 飛1,3,4溫海深2李 軍1,3,4
(1. 中國科學院海洋研究所, 中科院實驗海洋生物學重點實驗室,青島 266071; 2. 中國海洋大學, 青島 266009; 3. 海洋生態養殖技術國家地方聯合工程實驗室, 青島 266071; 4. 青島海洋科學與技術國家實驗室,
海洋生物學與生物技術功能實驗室 青島 266237)
采用程序降溫儀分步降溫冷凍保存長牡蠣(Crassostrea gigas)精液, 并用掃描電鏡、透射電鏡研究了精子的超微結構損傷。超低溫冷凍保存后長牡蠣精子的運動率、受精率及孵化率與鮮精無顯著差異。鮮精中84.5%的精子形態結構正常, 凍精中73%的精子形態結構正常。形態結構正常的精子表現為頂體、質膜、線粒體與鞭毛結構完整、染色質形狀規則, 頂體、線粒體及中心粒結構正常, 鞭毛形態完整、微管結構清晰; 形態結構異常的精子表現為頂體脫落、解體, 精子頭部質膜膨脹、破裂、染色質腫脹、破裂、解體, 線粒體移位、脫落、膨脹, 嵴退化或消失, 鞭毛彎折、斷裂, 微管解聚。結果顯示, 以10% DMSO為抗凍保護劑, HBSS溶液為稀釋液, 1∶4的稀釋比例, 添加海藻糖, 采用分步降溫法冷凍保存, 對長牡蠣精子具有較好的抗凍保護作用, 合適的凍存方法可以有效的保護太平洋牡蠣精子冷凍過程中結構損傷。研究有助于長牡蠣種質資源的收集保存及應用。
長牡蠣; 精子; 掃描電鏡; 透射電鏡; 超微結構
檢測精子超低溫冷凍保存前后超微結構損傷已被應用于真鯛(Pagrosomus major)[1]、 中華鱘(Acipenser sinensis)[2]、大黃魚(Pseudosciaena crocea)[3]、太平洋牡蠣(Crassostrea gigas)[4]、 蝦夷扇貝(Patinopecten yessoensis)[5]、太平洋鱈(Gadus macrocephalus)[6]、香港巨牡蠣(Crassostrea hongkongensis)[7]等魚、貝類的精子質量檢測中。研究發現,精子超低溫冷凍保存不可避免的會造成其超微結構的損傷, 而精子超微結構的完整與否又直接與精子活力相聯系, 進而影響精子的受精能力。因此,研究精子超低溫冷凍保存前后超微結構損傷變化情況對于精子冷凍保存方法的改善具有重要意義。長牡蠣(Crassostrea gigas)主要分布于中國大陸、中國臺灣地區、韓國等, 常棲息在潮間帶及淺海的巖礁海底, 在我國養殖范圍十分廣泛, 經濟價值較高。最近一段時間, 隨著我國海水養殖業的不斷發展, 長牡蠣養殖規模呈不斷增大趨勢, 累代養殖與近親交配的加劇, 不可避免地造成了長牡蠣種質退化的現象, 開展長牡蠣精液的超低溫冷凍保存技術的研究具有重要意義[8,9]。有關長牡蠣精子的超低溫凍存的研究已有報道, 如李赟等[10]以滲透性抗凍保護劑超低溫凍存太平洋牡蠣精子, 復蘇后得到了較高的運動率, 并通過電子顯微鏡初步觀察了其超微結構的變化; Dong等[11,12]在以2%聚乙二醇(PEG)及兩種不同抗凍保護劑間的組合為抗凍劑冷凍保存太平洋牡蠣, 獲得了最高的運動率及受精率。但上述報道的降溫過程多以液氮面以上一定高度來控制, 穩定性差, 復溫解凍后精子運動率不高, 其精子超微架構損傷較為嚴重, 以程序降溫儀精準控制降溫程序超低溫冷凍保存長牡蠣精子, 并采用掃描電鏡和透射電鏡觀察其超微結構損傷的研究尚未見報道。本研究以無鈣HBSS為稀釋液, 10% DMSO為抗凍劑, 添加0.45 mol/L海藻糖, 程序降溫儀精準控制分步降溫超低溫冷凍保存長牡蠣精子, 采用掃描電鏡、透射電鏡技術研究了長牡蠣精子凍存前后超微結構損傷情況, 探索超低溫凍存及解凍過程對長牡蠣精子損傷情況, 以期為長牡蠣精子超低溫凍存技術的改進及凍精質量的評價提供參考。
1 材料與方法
1.1 實驗材料
實驗所用的長牡蠣由中國科學院海洋研究所海洋貝類增養殖與生物技術實驗室提供, 提前一周暫養于水族樓循環水系統的水族箱中, 暫養期間水溫控制在16—18℃, 每天上午10時換水一次, 實驗時選擇性腺飽滿的雄性長牡蠣(殼高8.8—10.5 cm,殼寬6.1—7.0 cm)通過人工解剖取精液, 解剖過程中盡量避免性腺組織的混入, 紗網過濾后放入50 mL離心管里, 顯微鏡觀察精子活力良好(運動率≥80%)置于4℃冰箱中用作精子超低溫冷凍保存。
1.2 實驗方法
精子的超低溫凍存及解凍將精液稀釋液即無鈣HBSS溶液[13]與抗凍劑DMSO混合配制成抗凍液(DMSO占10%), 長牡蠣精液和抗凍液按1∶4比例加入到1.8 mL凍存管中, 并添加0.45 mol/L的海藻糖, 輕輕上下顛倒數次使其充分混勻后置于4℃的冰箱中預冷20min。在此期間, 打開程序降溫儀,設定好降溫程序(0℃開始, -15℃/min降溫至-60℃,停留120s后以-20℃/min降溫至-150℃, 停留300s),待程序降溫儀運行穩定后, 迅速將預冷過的凍存管裝入程序降溫儀中, 開始降溫。程序運行結束后,采用37℃水浴鍋水浴解凍, 解凍期間用鑷子輕輕搖晃凍存管使其受熱均勻, 解凍后檢測凍精活力。
鮮精與凍精的活力測定按劉清華等[14]的方法檢測新鮮精液和解凍復蘇后精子活力, 具體操作為: 載玻片上滴加40 μL混有5% BSA的新鮮過濾滅菌海水, 采用滅菌后的牙簽輕輕沾取少量精液與其混勻, 置于顯微鏡下, 通過計算機輔助精液分析系統(Computer-assisted sperm analysis, CASA)采集6個視野的視頻圖像, 統計運動率, 精液運動率為一個視野內快速運動精子數目占全部精子數目的百分比。實驗設3個重復。
受精率和孵化率的測定分別取鮮精、冷凍保存解凍精子與新鮮解剖的長牡蠣卵子人工授精, 測定其受精率和孵化率[15], 實驗設3個重復。
鮮精與凍精的超微結構觀察掃描電鏡(Scanning electron microscope, SEM)觀察: 電鏡制片與觀察在青島大學醫學院完成, 具體操作為: 取鮮精與剛解凍的精液, 用新鮮配制的電鏡緩沖液配成2.5%的戊二醛避光條件下固定1d (4℃), 采用磷酸緩沖液(0.2 mol/L, pH=7.4)漂洗數次后用1%新鮮配制的鋨酸溶液4℃固定2h, 經梯度酒精脫水后采用醋酸異戊脂置換, 最后離子鍍膜制成成片, 采用日本電子株式會社(JEOL公司)的JSM-840型掃描電鏡下觀察、拍照。
透射電鏡(Transmission electron microscopy, TEM)觀察: 取鮮精與凍融精液, 用新鮮配制的電鏡緩沖液配成的2.5%的戊二醛(0.2 mol/L, pH=7.4)避光條件下進行前固定, 然后用1%新鮮配制的鋨酸溶液4℃固定2h, 依次采用不同梯度酒精脫水, Epon-812滲透包埋, 超薄切片機切片, 醋酸鈾和檸檬酸鉛雙重染色后制成成片, 置于透射電子顯微鏡(日立H-7000)下觀察、拍照。
1.3 數據處理
數據采用SPSS17.0進行處理, 并對數據進行單因素方差分析(ANOVA), 顯著性水平檢驗采用Duncan氏比較分析, 所有結果均以平均值±標準差的形式進行表示, P<0.05表示差異顯著。
2 結果
2.1 長牡蠣鮮精及凍精的運動率、受精率和孵化率
鮮精和解凍后長牡蠣精子運動率、受精率和孵化率結果見表 1。結果表明, 鮮精與解凍后精子的活力相比差異不顯著(P>0.05)。
2.2 長牡蠣鮮精及凍精的超微結構
掃描電子顯微鏡觀察結果表明, 鮮精中形態結構異常的精子占全部精子數量的15.5%, 形態結構正常的精子占全部精子占84.5%; 解凍后精子中形態結構異常的精子占全部精子數量的27%, 形態結構正常的精子占全部精子的73%。

表 1 長牡蠣鮮精及凍精的運動率、受精率及孵化率 (n=3, X± SD)Tab. 1 Motility, fertilization rate and hatching rate of fresh sperm and frozen-thawed sperm of Crassostrea gigas (n=3, X±SD)
長牡蠣精子冷凍前后掃描電鏡超微結構
由圖 1可知, 長牡蠣精子超微結構主要由頭部和尾部兩部分組成, 精子全長約32 μm, 頸部不明顯。頭部呈近似圓形, 前端有一突出結構為頂體, 頭部下方線粒體緊鄰頭部很清晰, 呈圓形, 4個緊密排列,圍繞在鞭毛周圍, 精子的鞭毛細長, 近頭部較粗遠端漸細, 主段均勻, 尾端逐漸變細。
超低溫冷凍保存解凍后對長牡蠣精子超微結構的損傷主要表現在鞭毛脫落、彎折(圖 2A), 頂體直接消失, 質膜皺縮, 鞭毛脫落(圖 2B); 線粒體變形、腫脹, 移位脫落, 頭部表面膜凹凸不平(圖 2C)精子頭部細胞膜破損凹陷, 質膜間斷破裂、脫落,線粒體外膜膨脹、破裂, 內容物流出, 尾部鞭毛腫脹(圖 2D)。
長牡蠣精子冷凍前后透射電鏡超微結構
由圖 3可知, 長牡蠣精子超微結構主要由頭部和尾部組成。頭部結構主要包含頂體、亞頂體腔、染色質、囊泡、中心體及線粒體等結構, 鞭毛由質膜及微管組成(圖 3A、圖 3B), 頭部的主要部分由染色質組成, 中心體由近端中心粒和遠端中心粒垂直排列構成, 近端中心粒靠近染色質, 遠端中心粒靠近鞭毛向后延伸出軸絲, 兩中心粒呈垂直排列, 囊泡鑲嵌于染色質中(圖 3B), 4個線粒體呈環形排列,內有大量致密嵴狀結構, 中心粒位于4個線粒體中間(圖 3C), 精子尾部為細長的鞭毛結構, 呈現典型的“9+2”微管軸絲結構, 外面包有質膜結構, 軸絲由雙連體和中央微管組成, 9組雙連體微管均勻分布在外面, 一組中央微管位于中間, 二聯體微管致密,結構清晰可辨(圖 3D)。電鏡觀察顯示, 鮮精形態結構正常的精子表現為染色質結構完整、無破裂變形現象, 質膜無膨脹破裂, 中心粒結構正常, 線粒體形態完整、嵴較發達, 鞭毛結構完整、清晰(圖 3)。
透射電鏡形態結構異常的精子表現在質膜、核內部結構、線粒體、染色質和鞭毛等結構。超低溫冷凍對部分長牡販精子造成了嚴重的影響, 具體表現為頭部染色質的破裂變形, 核變形、核內空泡增多, 甚至整體分解, 質膜破裂消失, 頭部頂體處質膜破損, 頭部核質膜破損缺失, 核膜間斷或局部破裂、脫落, 裙皺增多且膜的連續性遭到破壞, 線粒體腫脹、大小不一(圖 4A), 頂體結構受損傷、變松散、解體, 質膜腫脹, 頭部質膜與內部間隙加大,線粒體破裂變形, 鞘外質膜缺損, 線粒體膜不完整,內部嵴結構損傷、疏松, 球形的線粒體缺失、結構松散甚至脫落, 內容物流出, 尾部斷裂及中心粒結構消失等(圖 4B), 長牡蠣頭部頂體內含多種酶類,對于精子入卵具有重要作用, 頂體結構的損傷會對精子功能產生一定的影響。在超低溫冷凍過程中發現的頂體結構的損傷甚至缺失, 表明超低溫冷凍過程一定程度上會對對精子產生損傷, 進而影響其生理功能。超微結構觀察發現, 超低溫冷凍過程對長牡蠣精子頭部造成的損傷主要表現在頂體松散、變形, 染色質缺失, 核頂變形、染色質側面出現凹陷, 核表面不均勾, 內部結構彌散, 線粒體部分或全部脫落消失(圖 4C), 冷凍對精子尾部損傷主要表現為: 精子尾部腫脹變形, 形狀不規則, 變形嚴重, 二聯微管解聚、彌散(圖 4D)。
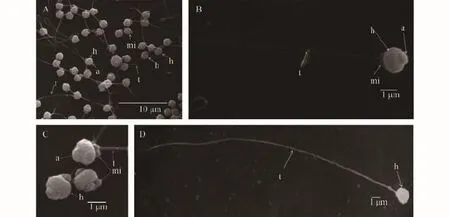
圖 1 長牡蠣鮮精掃描電鏡觀察Fig. 1 The ultrastructure of fresh spermatozoa of Crassostrea gigas by SEMA. 鮮精整體掃描電鏡照片; B、D. 單個精子掃描電鏡圖, 示精子頭部近似圓形, 頂體位于頭部前方, 部分線粒體整齊排列, 鞭毛細長; C. 示精子頭部結構, 頂體、頭部、線粒體及鞭毛依次排列; h: 頭; t: 鞭毛; a: 頂體; mi: 線粒體A. Fresh sperm of SEM; B, D. Single sperm of SEM, The sperm head approximate circular, acrosome located in the front of head, Some mitochondria ranked neatly, flagella slender; C. The structure of sperm head, head, acrosome mitochondria and flagella lined. h: head; t: flagellum; a: acrosome; mi: mitochondria
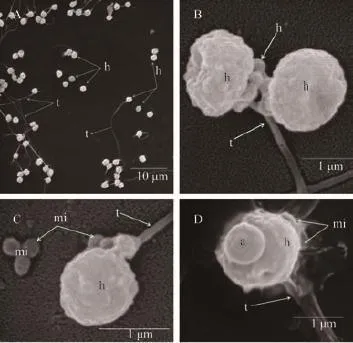
圖 2 長牡蠣凍精掃描電鏡觀察Fig. 2 The ultrastructure of cryopreserved spermatozoa of Crassostrea gigas by SEMA. 凍精整體掃描電鏡照片, 示鞭毛脫落、折斷; B. 兩個精子掃描電鏡圖, 示頭部頂體脫落, 質膜皺縮變形; C、D. 單個精子掃描電鏡圖, 示部分線粒體脫落、破損, 質膜皺縮, 胞膜凍裂, 細胞液外流; h: 頭; a: 頂體; t: 鞭毛; mi: 線粒體A. The whole frozen sperm of SEM, flagellum fall off, bend; B. Two frozen sperm of SEM, acrosome fall off head, plasmalemma collapse; C, D. Single frozen sperm of SEM, some of mitochon dria fall off, damaged, plasmalemma plasmolysis, cell membrane frost cleft, cytosol outflow; h: head; a: acrosome; t: flagellum; mi: mitochondria
3 討論
3.1 長牡蠣精子超微結構特點
電子顯微鏡觀察長牡蠣精子冷凍前后的形態和超微結構發現, 長牡蠣精子主要由頭部、中段和尾部組成。頭部近似圓形, 與大多數魚類和貝類精子相似[11,16]。頭部頂端有頂體, 向后依次為亞頂體腔、染色質、線粒體、中心粒和鞭毛。精子中段不明顯, 由4個線粒體圍繞中心粒組成, 與香港牡蠣等精子的超微結構相似[7]。超微結構觀察發現, 牡蠣精子尾部鞭毛結構細長, 其長度與幾種常見貝類精子長度基本相似, 但與鳥類、魚類和哺乳類精子鞭毛長度相差較大[17,18]。鞭毛軸絲呈典型的“9+2”結構, 與香港巨牡蠣、皺紋盤鮑(Haliotis discus hannai)和蝦夷扇貝等精子相同[5,7,19], 解凍后精子中有一定比例的精子形態結構發生了不同程度的損傷,主要損傷表現為頂體全部或部分消失, 染色質破裂損傷, 甚至整體分解, 核變形、質膜破裂損傷, 線粒體結構彌散, 內嵴結構破裂, 膜內物質外流, 嵴疏松變形, 甚至脫落。鞭毛腫脹、彎折, 精子鞭毛中間位置膨脹、斷裂, 二聯微管解聚等。掃描電鏡和透射電鏡能從精子超微結構的變化程度來表示超低溫冷凍前后精子結構上的變化。長牡蠣精子凍融后超微結構觀察發現部分精子頂體結構破裂甚至缺失、精子細胞膜腫脹甚至破裂; 線粒體破裂, 體內嵴結構變形, 膜結構破損腫脹變形, 內容物流出;鞭毛彎折、斷裂[18]。與其他海洋動物精子超低溫冷凍過程中超微結構的損傷基本一致。
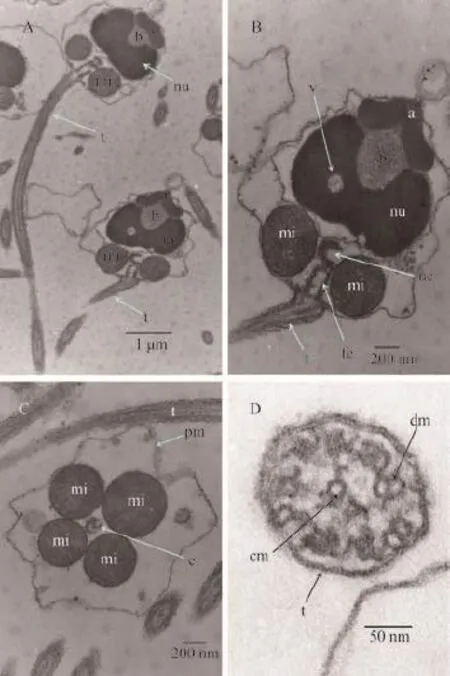
圖 3 長牡蠣鮮精透射電鏡觀察Fig. 3 The ultrastructure of fresh spermatozoa of Crassostrea gigas by TEMA. 鮮精縱切, 示單個精子整體縱切; B. 鮮精頭部縱切, 示鮮精頭部超微結構; C. 鮮精橫切, 示線粒體超微結構; D. 鮮精鞭毛橫切, 示鞭毛典型“9+2”結構; a: 頂體; b: 亞頂體腔; c: 中心體; t:鞭毛; cm:中央微管; dm: 雙連體; pm: 質膜; mi: 線粒體; nu: 核A. Fresh sperm rip cutting; B. Fresh sperm head rip cutting, show ultrastructure; C. Fresh sperm rip cutting, show mitochondria ultrastructure; D. Fresh sperm flagellum crosscut, show “9+2”structure. a: acrosome; b: cavity; c: centrosome; t: flagellum; cm: central microtubules; dm: double conjoined; pm: plasma membrane; mi: mitochondria; nu: nucleus
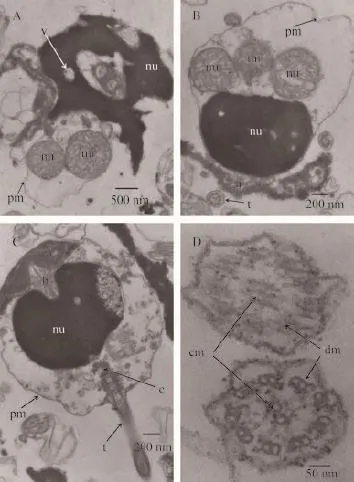
圖 4 長牡蠣凍精透射電鏡觀察Fig. 4 The ultrastructure of fresh spermatozoa of Crassostrea gigas by TEMA. 凍精縱切, 示胞膜破裂, 染色質破損、變形, 鞭毛脫落; B. 凍精斜切, 示質膜腫脹, 頂體解體, 線粒體損傷; C. 鮮精縱切, 示線粒體脫落, 染色質破損; D. 凍精鞭毛橫切, 下部鞭毛示精子典型“9+2”, 上部鞭毛示微管解聚, 膜皺縮變形; a: 頂體; b: 亞頂體腔; c: 中心體; t: 鞭毛; cm: 中央微管; dm: 雙連體; pm: 質膜; mi: 線粒體; nu: 核A. Frozen sperm rip cutting show membrane rupture, chromatin damaged, flagellum fall off; B. Frozen sperm bevel, show plasma membrane swollen, disintegration of acrosome, mitochondria damage; C. Frozen sperm rip cutting, show mitochondrial loss, chromatin damaged; D. Frozen sperm flagellum crosscut, show“9+2” structure. a: acrosome; b: cavity; c: centrosome; t: flagellum; cm: central microtubules; dm: double conjoined; pm: plasma membrane; mi: mitochondria; nu: nucleus
3.2 精子結構損傷與精子功能之間的關系
一般認為, 凍精結構改變的主要原因是細胞內冰晶造成的損傷[20,21]。雖然抗凍保護劑對精子超低溫冷凍過程具有一定的保護作用, 在一定程度上能夠有效避免精子超微結構的損傷, 但仍有部分精不可避免的會發生結構上的變化, 影響其生理功能,最終體現為影響精卵識別與受精[22]。在實驗過程中發現精子超微結構的變化主要有: 精子內部染色質的變化, 如染色質彌散或腫脹[23,24]; 細胞器的損傷, 如線粒體消失、破損或內嵴損傷[25]; 精子質膜的變化, 如破裂、消失或腫脹; 鞭毛結構的損傷, 如鞭毛腫脹、軸絲斷裂、微管解聚等[26]。牡蠣精子的向前運動主要是由尾部鞭毛的擺動完成, 而精子鞭毛完成這一功能是由線粒體來提供能量的, 線粒體是大多數動物細胞主要的的供能細胞器。超微結構觀察發現, 解凍后精子中有部分精子線粒體受損傷, 其生理功能降低甚至喪失, 表現為精子活力下降甚至完全失活, 長牡蠣精子線粒體及鞭毛是精子完成運動功能主要結構, 它們的損傷不可避免地會造成精子功能的下降, 進而影響精子入卵[27]。精子內部存在眾多由膜包被而成的細胞器, 發揮著重要的生理功能, 由于精子內部膜結構主要有磷脂雙分子層和鑲嵌在其中的蛋白質組成, 其結構的不穩定性也決定了其對外界溫度變化比較敏感, 加之冷凍、復溫過程中冰晶的產生, 致使其在超低溫冷凍保存過程中極易受到損傷, 精子冷凍及復溫過程中細胞膜的損傷, 破壞了精子正常的生理結構, 不可避免地造成精子功能的紊亂。與之相反的, 精子的非膜性結構和細胞核染色質等結構在超低溫冷凍過程中抗凍能力較強。目前大部分精子超低溫冷凍保存研究, 不同學者在研究不同物種精子凍存過程中采用了不同的凍存方法, 但超低溫凍存過程對精子超微結構損傷主要集中在精子相對脆弱的膜系統上[28]。章龍珍等[29]在鱘魚精子超低溫凍存研究中發現, 超低溫凍存對精子超微結構的損傷主要集中在精子細胞膜結構的破損, 從而改變了精子細胞內部特有的相對穩定的內環境, 精子細胞膜上膜脂發生晶格化的一種現象, 影響了精子細胞的功能,最終影響了精子活力, 致使其受精能力的下降。程順等[3]以Cortland溶液為稀釋液, 10% DMSO為抗凍劑冷凍大黃魚精子過程中發現, 大黃魚精子超低溫冷凍及水浴復溫過程中, 鞭毛軸絲內結構并未發生明顯改變, 精子冷凍保存過程并未對軸絲結構產生大的影響。張蓮蕾等[1]對真鯛精子冷凍的研究中發現, 復蘇后的凍融精子中, 超微結構觀察發現70%以上的精子具有相對完整的線粒體結構和完整且均勻的精子細胞膜結構, 剩余精子細胞不同程度上存在結構的變化和損傷, 并指出真鯛精子超微結構的受損, 尤其是相關功能蛋白結構的變化時導致精子活力及生理機能變化的重要原因。李赟等[10]以10% DMSO為抗凍劑, 采用距液氮面以上不同高度的方法控制降溫速率冷凍保存太平洋牡蠣精子,并采用電子顯微鏡觀察其超微結構損傷情況, 研究表明, 在解凍后的精子中有一部分超微結構發生了不同程度的變化, 超低溫冷凍和升溫解凍, 對牡蠣部分精子的膜結構損傷嚴重, 導致精子活力和受精能力下降。超低溫冷凍保存也會對鞭毛造成一些不可逆的傷害, 破壞了許多功能蛋白的作用, 對精子尾部的損傷造成軸絲結構破壞, 從引起精子運動功能的喪失, 線粒體和鞭毛在精子運動過程中主要起著供能和提供向前動力的作用, 線粒體通過消耗精子細胞內部的ATP為鞭毛擺動提供能量, 鞭毛擺動給精子提供了一種向前的動力[30]。研究表明, 大部分魚類精子在性腺中是不運動的, 只有當精子收到外界(滲透壓、離子、蛋白質)的刺激后, 精子才能激活, 鞭毛開始擺動并提供一種向前的動力[31]。于海濤等[32]以10% DMSO為抗凍劑, 分段冷凍法保存紅鰭東方鲀[Fugu rubripes (Temminck et Schlegel)]精子, 電鏡觀察發現鞭毛斷裂或被膜膨脹脫落, 導致了精子活力下降。因此在精子超低溫冷凍保存過程中, 我們多選擇那些毒性低、滲透性較好的抗凍保護劑來保護精子凍存過程中的損傷[33,34]。韓龍江等[6]在超低溫冷凍太平洋鱈精子時發現, 超低溫冷凍及復溫過程對精子鞭毛結構的損傷多集中于精子鞭毛中段, 并指出這可能是因為鞭毛中段特殊結構造成的, 膜結構的脆弱使其在冷凍過程中更易受到損傷。朱豪磊等[7]在香港牡蠣精子冷凍過程中發現, 精子膜的損傷對保存精子的活力影響很大,精子超微結構異常主要表現為精子細胞膜及核膜的破損腫脹, 線粒體缺失或破損, 鞭毛彎折、斷裂甚至脫落, 染色質彌散解體等, 與本研究觀察到的的長牡蠣精子超微結構冷凍損傷情況基本一致。
4 小結
本研究表明長牡蠣精子冷凍保存前后運動率差異不顯著, 其受精能力亦無顯著差異, 解凍后長牡蠣精子超微結構形態正常的占84.5%, 說明以10% DMSO作為抗凍保護劑, 添加海藻糖HBSS作為稀釋液, 對長牡蠣精子超低溫冷凍保存具有較好的保護作用。實驗組凍融后精子受精率、孵化率高于鮮精。我們猜測一方面可能是由于在精子冷凍過程中, 質量差的精子被凍死, 質量好的精子存活了下來, 存活下來的優質精子提高了精子的受精率及孵化率。另一方面, 在長牡蠣受精實驗中我們還發現, 過多或者過少的精子圍繞在卵子周圍均對卵子的受精及孵化產生一定的影響, 鮮精精子密度不可避免的會高于凍精。因此, 在本實驗中, 可能由于活力差、運動速率慢的精子死亡, 存活下來的精子質量提高及圍繞在卵子周圍精子數量更加適合卵子的受精導致了精子受精率、孵化率略高于鮮精, 但二者之間差異不顯著。電子顯微鏡技術,可以用于探索長牡蠣精子超低溫保存及復溫過程中冷凍損傷情況, 有助于篩選更加有效的精子凍存方法, 推動精子超低溫冷凍損傷機理的研究。今后可以采用流式細胞儀、單細胞凝膠電泳及高效色譜技術繼續深入分析長牡蠣精子冷凍前后膜結構、染色質及細胞內各生化成分的變化, 以便探討超低溫凍存精子細胞性結構損傷的機制。
[1]Chen Y K. The effect of cryopreservation on sperm quality of red seabream (Pagrus major) [D]. Thesis for Master of Science. Institute of Oceanology, Chinese Academy of Sciences. 2010 [陳亞坤. 超低溫保存對真鯛(Pagrus major)精子質量的影響. 中國科學院海洋研究所. 2010]
[2]Li P. Cryopreservation and ultrastructure of Acipenser sinensis gray [D]. Huazhong Agricultural University. 2007 [厲萍. 中華鱘精子結構特征及其精液超低溫冷凍保存技術研究. 華中農業大學. 2007]
[3]Cheng S, Yan J Q, Zhu J Q, et al. Vitality and ultrastructure observation of fresm and cryopreservated sperm in Pseudosciaena crocea [J]. Oceanologia et Limnologia Sinica, 2013, 44(1): 56—61 [程順, 閆家強, 竺俊全, 等.大黃魚(Pseudosciaena crocea)精子冷凍前后的活力及超微結構變化. 海洋與湖沼, 2013, 44(1): 56—61]
[4]Adams S L, Roberts R D, Webb S C, et al. Cryopreservation of sperm of the Pacific oyster (Crassostrea gigas): development of a practical method for commercial spat production [J]. Aquaculture, 2004, 242(1—4): 271—282
[5]Yang P M, Yang A G, Liu Z H, et al. Ultrastructure and cryodamage studies of Patinopecten yessoensis sperm by electron microscopy [J]. Marine Fishery Research, 2008, 29(1): 98—102 [楊培民, 楊愛國, 劉志鴻, 等. 蝦夷扇貝精子形態結構和超低溫冷凍損傷的電鏡觀察. 海洋水產研究, 2008, 29(1): 98—102]
[6]Han L J, Liu Q H, Yu D D, et al. Cryopreservation and ultrastructure of Gadus macrocephalus sperm [J]. Oceanologia et Limnologia Sinica, 2014, 45(4): 789—797 [韓龍江, 劉清華, 于道德, 等. 太平洋鱈(Gadus macrocephalus)精液超低溫冷凍方法的建立及精子超微結構分析.海洋與湖沼, 2014, 45(4): 789—797]
[7]Zhu H L. Study on the sperm of Crassostrea hongkongensis using cold-store technology [D]. Guangxi University. 2013 [香港牡蠣精子冷凍保存的研究. 廣西大學. 2013]
[8]Yang H, Hu E, Cuevas-Uribe R, et al. High-throughput sperm cryopreservation of eastern oyster Crassostrea virginica [J]. Aquaculture, 2012, 344(3):223-230.
[9]Vitiello V, Carlino P A, Del Prete F, et al. Effects of cooling and freezing on the motility of Ostrea edulis (L., 1758) spermatozoa after thawing. [J]. Cryobiology, 2011, 63(2):118—124.
[10]Li Y, He G Z. The morphological and ultrastructural variation of pacific oyster Crassostrea gigas (Thunberg) sperm after cryopreservation [J]. Journal of Ocean University of Qingdao (Natural Science), 2002, (4): 526-532 [李赟, 賀桂珍. 超低溫保存存前后太平洋牡蠣精子Crassostrea gigas (Thunberg)超微結構觀察. 青島海洋大學學報(自然科學版), 2002, (4): 526—532]
[11]Dong Q, Huang C, Eudeline B, et al. Systematic factor optimization for cryopreservation of shipped sperm samples of diploid Pacific Oysters, Crassostrea gigas [J]. Cryobiology, 2005, 51(2): 176—197
[12]Dong Q, Huang C, Eudeline B, et al. Systematic factor optimization for sperm cryopreservation of tetraploid Pacific oysters, Crassostrea gigas [J]. Theriogenology, 2006, 66(2): 387—403
[13]Hanks J H. Hanks' balanced salt solution and pH control [J]. Methods in Cell Science, 1975, 1(1): 3—4
[14]Liu Q, Li J, Zhang S, et al. An efficient methodology for cryopreservation of spermatozoa of red seabream, Pagrus major, with 2-mL Cryovials [J]. Journal of the World Aquaculture Society, 2006, 37(3): 289—297
[15]Teng S S. The study of Crassostrea gigas crossbreeding [D]. Ocean University of China. 2009 [滕爽爽. 長牡蠣雜交育種的研究. 中國海洋大學. 2009]
[16]Wang M F, Bin C Y, Dou W, et al. The detection and evaluation and evaluation on the sperm quality of mollusk: the evaluation of sperm survival rate of pinctada maternalI stained by eosin y and typan blue [J]. Acta Hydrobiologica Sinica, 2013, 32(5): 803—809 [王梅芳, 賓承勇, 豆偉, 等. 貝類精子質量檢測與評價方法研究I: 染色法檢測馬氏珠母貝精子的存活率的研究. 水生生物學報, 2013, 32(5): 803—809]
[17]Vidal A H, Batista A M, Silva E C B D, et al. Soybean lecithin-based extender as an alternative for goat sperm cryopreservation [J]. Small Ruminant Research, 2013, 109(1): 47—51
[18]Babiak I, Ciereszko A, Litvak M. Semen characteristics and their ability to predict sperm cryopreservation potential of Atlantic cod, Gadus morhua L [J]. Theriogenology, 2011, 75(7): 1290—1300
[19]Hassan M M, Qin J G, Li X. Sperm cryopreservation in oysters: A review of its current status and potentials for future application in aquaculture [J]. Aquaculture, 2015, 438(1): 24—32
[20]Tiersch T R, Yang H, Jenkins J A, et al. Sperm cryopreservation in fish and shellfish [J]. Society of Reproduction & Fertility Supplement, 2007, 65: 493—508
[21]Chen D H, Li Y D, Jia Z L, et al. Cryopreservation of Eriocheir sinensis sperms (In vitro) with different cryoprotective solutions and prefreezing time [J]. Acta Hydrobiologica Sinica, 2008, 32(4): 579—585 [陳東華, 李艷東, 賈林芝, 等. 冷凍保護劑及預冷時間對河蟹精子體外冷凍保存的影響. 水生生物學報, 2008, 32(4): 579—585]
[22]Dai T, Zhao E, Lu G, et al. Sperm cryopreservation of yellow drum Nibea albiflora: A special emphasis on postthaw sperm quality [J]. Aquaculture, 2012, s 368—369(1): 82—88
[23]Shi Y X, Cheng S, Zhu J Q, et al. Sperm cryopreservation and enzyme activity detection in Lateolabrax maculates [J]. Acta Hydrobiologica Sinica, 2015, 39(6): 1241—1247 [史應學, 程順, 竺俊全, 等. 中國花鱸精子的超低溫冷凍保存及酶活性檢測. 水生生物學報, 2015, 39(6): 1241—1247]
[24]Dreanno C, Fauvel C, Cosson J, et al. Cryopreservation of sperm in marine fish [J]. Aquaculture Research, 2000, 31(3): 231—243
[25]Yao Z, Crim L W, Richardson G F, et al. Motility, fertility and ultrastructural changes of ocean pout (Macrozoarces americanus L.) sperm after cryopreservation [J]. Aquaculture, 2000, 181(3): 361—375
[26]Wang X G, Luo J, Yin S W, et al. Investigation of spermatozoa motility of Epinephelus malabaricus and comparison of the spermatozoa ultrastructure before and after ultra-low temperature freeze [J]. Marine Science, 2013, 37(2): 70—75 [王小剛, 駱劍, 尹紹武, 等. 點帶石斑魚的精子活力及超低溫冷凍前后精子超微結構的比較. 海洋科學, 2013, 37(2): 70—75]
[27]Cabrita E, Engrola S, Concei??o L E C, et al. Successful cryopreservation of sperm from sex-reversed dusky grouper, Epinephelus marginatus [J]. Aquaculture, 2009, 287(1—2): 152—157
[28]Pérez-Cerezales S, Martínez-Páramo S, Cabrita E, et al. Evaluation of oxidative DNA damage promoted by storage in sperm from sex-reversed rainbow trout [J]. Theriogenology, 2009, 71(4): 605—613
[29]Zhang L Z, Liu P, Zhuang P, et al. Observing on cryodamage of spermatozoa of Siberian sturgeon (Acipenser b. baerii) [J]. Journal of Fisheries of China, 2008, 32(4): 558—565 [章龍珍, 劉鵬, 莊平, 等. 超低溫冷凍對西伯利亞鱘精子形態結構損傷的觀察. 水產學報, 2008, 32(4): 558—565]
[30]Kudo S, Linhart O, Billard R. Ultrastructural studies of sperm penetration in the egg of the European catfish, Silurus glanis [J]. Aquatic Living Resources, 1994, 7(2):93—98
[31]Kopeika J, Kopeika E, Zhang T, et al. Effect of DNA repair inhibitor (3-aminobenzamide) on genetic stability of loach (Misgurnus fossilis) embryos derived from cryopreserved sperm [J]. Theriogenology, 2004, 61(9): 1661—1673
[32]Yu H T, Zhang X M, Chen C, et al. Changes in ultrastructures of Takifugu rubripes spermatozoa before and after cryopreservation [J]. Marine Science, 2007, 31(2): 17—19 [于海濤, 張秀梅, 陳超, 等. 紅鰭東方鲀精子超低溫保存前后的超微結構觀察. 海洋科學, 2007, 31(2): 17—19]
[33]Peng L Y, Xiao Y M, Liu Y. Effect of cryopreservation and short-term storage of Chinese giant salamander sperm [J]. Acta Hydrobiologica Sinica. 2011, 35(2): 325—332 [彭亮躍, 肖亞梅, 劉筠. 低溫和超低溫保存對中國大鯢成熟精子的影響. 水生生物學報, 2011, 35(2): 325—332]
[34]Liu Y, Li X. Successful oocyte cryopreservation in the blue mussel Mytilus galloprovincialis [J]. Aquaculture, 2015, 438: 55—58
STUDY ON ULTRASTRUCTURE OBSERVATION OF FRESH AND CRYOPRESERVATED SPERM IN CRASSOSTREA GIGAS
HAN Long-Jiang1,2, LIU Qing-Hua1,3,4, XU Fei1,3,4, WEN Hai-Shen2and LI Jun1,3,4
(1. Key Laboratory of Experimental Marine Biology, Institute of Oceanology, Chinese Academy of Sciences, Qingdao 266071, China; 2. College of Fisheries, Ocean University of China, Qingdao 266009, China; 3. National & Local Joint Engineering Laboratory of Ecological Mariculture, Qingdao 266071, China; 4. Laboratory for Marine Biology and Biotechnology, Qingdao National Laboratory for Marine Science and Technology, Qingdao 266237, China)
A step-wise cooling schemes was employed to cryopreserve Crassostrea gigas sperm, and the sperm ultrastructure was observed by scanning electron microscopy and transmission electron microscopy. The results showed that there were no significant differences between frozen-thawed sperm and fresh sperm in the motility, fertilization rate and hatching rate. Both the fresh sperm and cryopreserved sperm had ultrastructural damages. The normal rates of the fresh and cryopreservated sperms were 84.5% and 73%, respectively. The cryopreserved sperm without damage had normal morphology in the plasma membrane, mitochondria and nuclear, the acrosome, and centriole, and the mitochondrion obtained integrity with well-developed cristae. The sperm cryodamages with damages had swelled or disrupted plasma and nuclear membrane, partially damaged nucleus and swelled, dislocated or disarticulated mitochondrion with degenerated or vanished cristae. The results showed that HBSS with at 1∶4 dilution trehalose and 10% DMSO is the best condition for extender and cryoprotecant and for protecting the frozen-thawed C. gigas sperm, which will benefit the preservation of C. gigas and application of sperm cryopreservation skills.
Crassostrea gigas; Sperm; Cryopreservation; Vitality; Ultrastructure
S917
A
1000-3207(2017)01-0220-08
10.7541/2017.28
2016-02-19;
2016-06-21
國家高技術研究發展計劃(863計劃)項目(2012AA10A402); 海洋經濟創新發展區域示范項目(12PYY001SF08); 國家重點基礎研究發展計劃(973計劃)項目(2010CB126401); 鰲山科技創新計劃(2015ASKJ02,2015ASKJ02-03-03)水產種質資源平臺運行服務項目; 中國科學院青促會項目資助 [Supported by the National High Technology Research and Development Program of China (863 Program) No (2012AA10A4020); Regional Demonstration Project of Marine Economic Innovation and Development (12PYY001SF08); National Basic Research Program of China (2010CB126401); Qingdao National Laboratory for Marine Science and Technology (No.2015ASKJ02, 2015ASKJ02-03-03); Aquatic Germplasm Resources Platform Running Services; Youth Innovation Promotion Association CAS]
韓龍江(1989—), 男, 山東濰坊人; 理學碩士; 主要從事海洋動物種質資源保藏與海水魚類繁殖生理研究。E-mail: hanlong jiang1989@163.com; 劉清華為并列第一作者
溫海深, wenhaishen@ouc.edu.cn; 李軍, 研究員, 主要從事魚類繁育研究。E-mail: junli@qdio.ac.cn

