間充質(zhì)干細(xì)胞多模態(tài)示蹤方法的應(yīng)用
吳 春,姜在波,朱康順,黃明聲,關(guān)守海,李征然,錢結(jié)勝,李名安,單 鴻
(中山大學(xué)附屬第三醫(yī)院放射科 介入放射學(xué)研究所,廣東 廣州 510630)
間充質(zhì)干細(xì)胞多模態(tài)示蹤方法的應(yīng)用
吳 春,姜在波,朱康順,黃明聲,關(guān)守海,李征然,錢結(jié)勝,李名安,單 鴻*
(中山大學(xué)附屬第三醫(yī)院放射科 介入放射學(xué)研究所,廣東 廣州 510630)
目的 合成具備MR顯像和基因傳輸功能的納米載體,探討載體對(duì)間充質(zhì)干細(xì)胞(MSCs)的基因傳輸功能及其聯(lián)合生物發(fā)光成像(BLI)和MRI對(duì)MSCs雙模態(tài)示蹤的能力。方法 合成三元共聚物聚乙二醇-聚天冬氨酸(聚乙烯亞胺)-超順磁性氧化鐵納米顆粒載體(PAI/SPION);利用凝膠阻滯實(shí)驗(yàn)分析載體攜帶質(zhì)粒(pDNA)的能力;電位及粒度測(cè)定儀測(cè)量載體復(fù)合pDNA后的粒徑和電位;采用大鼠股骨骨髓分離培養(yǎng)MSCs;采用流式細(xì)胞儀、激光共聚焦顯微鏡評(píng)估PAI/SPION/pDNA對(duì)MSCs的基因轉(zhuǎn)染效率;聯(lián)合BLI和MRI雙模態(tài)示蹤MSCs。結(jié)果 成功合成了載體PAI/SPION。氨基與質(zhì)粒磷酸根的摩爾比(N/P)=3.0時(shí),PAI/SPION可完全復(fù)合pDNA。N/P=12時(shí),粒徑趨于穩(wěn)定,為(74.8±8.1)nm,電位為(12.2±1.5)mV,載體對(duì)MSCs的基因轉(zhuǎn)染率為(71.2±2.3)%。激光共聚焦顯微鏡下,胞漿內(nèi)可見大量表征PAI/SPION的綠色熒光和表征pDNA的紅色熒光,且MSCs生物發(fā)光強(qiáng)度最高,T2*WI標(biāo)準(zhǔn)化信號(hào)強(qiáng)度最低。結(jié)論 本研究成功合成了MRI可視的基因傳輸載體PAI/SPION;載體可高效傳輸pDNA至大鼠MSCs,且可成功聯(lián)合BLI和MRI雙模態(tài)示蹤MSCs。
間充質(zhì)干細(xì)胞;基因;生物發(fā)光;磁共振成像
多種致病因素均可導(dǎo)致急、慢性肝功能損傷,間充質(zhì)干細(xì)胞(mesenchymal stem cells, MSCs)移植為治療肝損傷提供了新途徑[1-2]。已有研究[3-5]報(bào)道,干細(xì)胞移植有助于肝損傷的修復(fù)和再生。但由于缺乏有效的干細(xì)胞活體示蹤技術(shù),干細(xì)胞移植的臨床應(yīng)用受到了限制,因此研制實(shí)時(shí)、無創(chuàng)的干細(xì)胞示蹤成像技術(shù)非常重要。本研究利用合成的具備基因傳輸功能和MRI顯像功能的三元共聚物載體(PAI/SPION),對(duì)MSCs基因傳輸及聯(lián)合生物發(fā)光成像(bioluminescence imaging, BLI)和MRI雙模態(tài)示蹤MSCs進(jìn)行研究。
1 材料與方法
1.1 主要實(shí)驗(yàn)儀器與材料 聚乙二醇-聚天冬氨酸(胱胺二鹽酸-丁二酸酐)[mPEG-b-PAsp(DMEA-SA),中山大學(xué)化工學(xué)院提供];水溶性Fe3O4納米顆粒(WSPION,中山大學(xué)化工學(xué)院提供);端氨基線性聚乙烯亞胺(lPEI-NH2,中山大學(xué)化工學(xué)院提供);質(zhì)粒pDNA(pCMV-Luciferase2-mKate2,中山大學(xué)附屬第三醫(yī)院分子影像實(shí)驗(yàn)室提供);低糖DMEM培養(yǎng)基(Gibco公司);熒光染料Oregen Green 488(Molecular Probes公司);胎牛血清(Gibco公司);熒光染料popo-3(Molecular Probes公司);電泳凝膠成像分析儀(Alpha Innotech公司);90Plus-Zeta電位及粒度測(cè)定儀(BI-MAS公司);流式細(xì)胞儀(BD公司);激光共聚焦顯微鏡(Zeiss公司);GE 1.5T MRI掃描儀;活體成像系統(tǒng)(Caliper Life Science公司)。
1.2 實(shí)驗(yàn)動(dòng)物 取6周齡雌性SD大鼠3只,體質(zhì)量80~90 g,由中山大學(xué)動(dòng)物中心提供,批號(hào)為SYXK(粵)2012-0081,并通過中山大學(xué)實(shí)驗(yàn)動(dòng)物倫理委員會(huì)許可。
1.3 納米載體PAI/SPION的合成 ①將1.52 g lPEI-NH2溶解于20 ml乙二胺四乙酸中,再加入1.2 eq三乙胺,室溫下反應(yīng)30 min。②將1.07 gm PEG-b-PBLAsp(DMEA-SA)溶解于20 ml乙二胺四乙酸中,再加入0.4 g N-羥基琥珀酰亞胺,反應(yīng)溶液水浴至18℃,加入0.72 g二環(huán)己基碳二亞胺,充入氬氣,將反應(yīng)溶液密封。③1 h后,再緩慢加入配制好的lPEI-NH2溶液,18℃水浴反應(yīng)1 h,然后置于室溫下24 h。④過濾去除沉淀物,將濾液用去離子水透析,以去除有機(jī)溶劑和過量的lPEI-NH2,凍干后獲得終產(chǎn)物聚乙二醇-聚天冬氨酸(聚乙烯亞胺)[mPEG-b-PAsp(-g-ss-PEI)],即PAI。⑤將100 mg PAI溶解于5 ml去離子水中,然后加入40 mg WSPION,于室溫下攪拌48 h,用450 nm濾過膜去除較大的聚合物顆粒。⑥反應(yīng)產(chǎn)物經(jīng)去離子水離心超濾,再用220 nm濾過膜過濾后,得到終產(chǎn)物PAI/SPION溶液,置于4℃恒溫環(huán)境中保存。
1.4 凝膠阻滯實(shí)驗(yàn) ①質(zhì)粒pDNA(pCMV-Luciferase2-mKate2)含有熒光素酶表達(dá)基因和紅色熒光蛋白表達(dá)基因。按照載體氨基與質(zhì)粒磷酸根的摩爾比(ratio of nitrogen to phosphorus, N/P;1.5、2.0、2.5、3.0、3.5)配制不同類型的PAI/SPION/pDNA復(fù)合物溶液。取1 μg pDNA與相應(yīng)量載體PAI/SPION溶液混勻,室溫靜置復(fù)合30 min。②取0.3 g瓊脂糖加入30 ml TAE緩沖液,微波爐加熱至瓊脂糖完全溶解,將溶液倒入插有梳子的平板,加1.5 μl溴化乙錠溶液,室溫下靜置30 min待瓊脂糖溶液凝固。③瓊脂糖溶液完全凝固后拔出梳子,將上述復(fù)合好的體系和未經(jīng)載體復(fù)合的pDNA加入上樣孔,恒壓100 V電泳45 min后,置于紫外線燈下觀察電泳條帶。
1.5 粒徑和電位測(cè)量 ①按照不同的N/P比(6、8、10、12、14、16)配制不同的PAI/SPION/pDNA復(fù)合物溶液,取1 μg pDNA和相應(yīng)質(zhì)量載體溶液混勻,室溫靜置復(fù)合30 min。②將復(fù)合好的體系PAI/SPION/pDNA和未復(fù)合質(zhì)粒的載體PAI/SPION溶液各取50 μl置入比色杯中,利用90 Plus-Zeta電位及粒度測(cè)定儀分別測(cè)量其粒徑和電位,入射激發(fā)光波長(zhǎng)λ=532 nm,入射角θ=90°,測(cè)量5次取其平均值。
1.6 MSCs的分離和培養(yǎng) ①將6周齡雌性SD大鼠脫頸處死,于無菌條件下將大鼠股骨分離并浸泡入低糖DMEM培養(yǎng)基(10%胎牛血清,1%青/鏈霉素)[6]。②離斷大鼠股骨干,用26號(hào)針將低糖DMEM培養(yǎng)基沿股骨干斷端注入骨髓腔內(nèi)沖洗骨髓組織,獲取骨髓組織混懸液。③骨髓組織混懸液離心分離20 min后,用低糖DMEM培養(yǎng)基重懸沉淀物,置入培養(yǎng)皿內(nèi)于恒溫培養(yǎng)箱中培養(yǎng)。④24 h后,去除未貼壁細(xì)胞,每隔3天更換培養(yǎng)基,當(dāng)細(xì)胞貼壁率達(dá)到70%時(shí),用胰酶消化分離細(xì)胞,按1∶3比率稀釋傳代。第4代MSCs用于本實(shí)驗(yàn)研究。
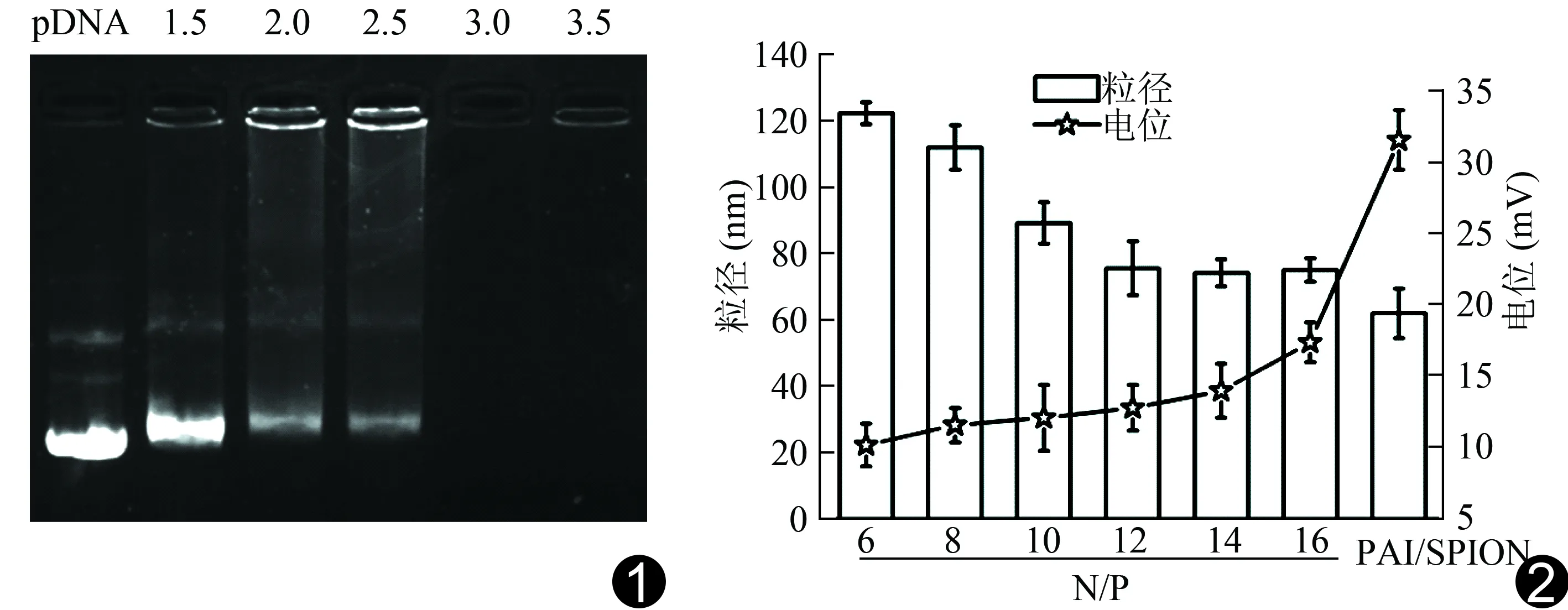
圖1 不同N/P比pDNA被載體PAI/SPION負(fù)載后在瓊脂糖凝膠中電泳圖 圖2 不同N/P比條件下PAI/SPION/pDNA的電位和粒徑圖
1.7 MSCs吸收分析 熒光染料popo-3標(biāo)記的pDNA(紅色熒光)被用來觀察細(xì)胞對(duì)質(zhì)粒的吸收。①在激光共聚焦皿內(nèi)種入MSCs,每孔的細(xì)胞數(shù)量約為1 000個(gè)。②用Oregon Green 488熒光染料標(biāo)記PAI/SPION(綠色熒光),用popo-3熒光染料標(biāo)記pDNA(紅色熒光)[7],每個(gè)細(xì)胞培養(yǎng)皿內(nèi)pDNA用量為4 μg,按照N/P=12制備復(fù)合物PAI/SPION/pDNA。③將復(fù)合物PAI/SPION/pDNA加入細(xì)胞培養(yǎng)皿,于恒溫培養(yǎng)箱孵育1 h。④在細(xì)胞培養(yǎng)皿中加入DNA染色劑DAPI(1 mg/ml),孵育15 min后在激光共聚焦顯微鏡下觀察并實(shí)時(shí)記錄。
1.8 MSCs轉(zhuǎn)染分析 ①在6孔板內(nèi)種入MSCs,每孔的細(xì)胞數(shù)量約為2×105個(gè)。②每孔細(xì)胞培養(yǎng)基中pDNA用量為4 μg,按照不同的N/P比(8、10、12、14、16)分別配制復(fù)合物PAI/SPION/pDNA。③將配制好的不同復(fù)合物體系分別加入細(xì)胞培養(yǎng)孔,在恒溫培養(yǎng)箱中孵育48 h。④消化、分離細(xì)胞并重懸在300 μl PBS溶液中,采用流式細(xì)胞儀檢測(cè)紅色熒光蛋白陽性細(xì)胞數(shù)量評(píng)估復(fù)合物的MSCs基因轉(zhuǎn)染效率。未進(jìn)行轉(zhuǎn)染的MSCs作為空白對(duì)照組。采用WinMDI 2.9軟件分析流式細(xì)胞儀檢測(cè)數(shù)據(jù)。
1.9 MSCs的BLI MSCs中報(bào)告基因表達(dá)程度 利用生物發(fā)光成像進(jìn)行評(píng)估。①在48孔板內(nèi)種入MSCs,每孔的細(xì)胞數(shù)量約為6×104個(gè)。②按照不同的N/P比(8、10、12、14、16)分別配制復(fù)合物PAI/SPION/pDNA,每孔細(xì)胞培養(yǎng)基中pDNA用量為 2 μg。③將配制好的不同復(fù)合物體系分別加入細(xì)胞培養(yǎng)孔,在恒溫培養(yǎng)箱中孵育48 h。④室溫下將熒光素酶底物(30 μg)加入細(xì)胞培養(yǎng)孔,利用活體成像系統(tǒng)觀察MSCs的BLI并實(shí)時(shí)記錄,定量分析不同處理組細(xì)胞的生物發(fā)光強(qiáng)度,以photos/sec/cm2/steradian(sr)為生物發(fā)光強(qiáng)度單位。未轉(zhuǎn)染的MSCs作為對(duì)照組。
1.10 MSCs的MR掃描 利用MR評(píng)估MSCs對(duì)PAI/SPION/pDNA的吸收能力。掃描前準(zhǔn)備:①在6孔板內(nèi)種入MSCs,每孔細(xì)胞數(shù)量約為2×105個(gè);②按照不同的N/P比(8、10、12、14、16)配制復(fù)合物PAI/SPION/pDNA,每孔細(xì)胞培養(yǎng)基中pDNA用量設(shè)為4 μg;③將不同復(fù)合物分別加入細(xì)胞培養(yǎng)孔,恒溫培養(yǎng)箱內(nèi)孵育1 h;④稱取0.4 g明膠置入10 ml雙蒸水中,制備4%明膠溶液備用;⑤使用胰酶消化分離干細(xì)胞,用300 μl PBS溶液重懸MSCs,置入小離心管;⑥干細(xì)胞懸液與等體積的4%明膠溶液混合,置入96孔板。
MR掃描:采用GE Signa Excite Ⅱ 1.5T MR掃描儀,8通道頭部線圈,對(duì)MSCs懸液進(jìn)行T2*WI。掃描參數(shù):TR 450 ms,TE 15ms,翻轉(zhuǎn)角15°,F(xiàn)OV 200 mm×200 mm,矩陣320×192,層厚1.0 mm,層間距1.0 mm。ROI設(shè)置為30 mm2,測(cè)量細(xì)胞懸液 T2*WI信號(hào)強(qiáng)度。各處理組MSCs懸液MR信號(hào)強(qiáng)度除以對(duì)照組MSCs懸液MR信號(hào)強(qiáng)度,獲得標(biāo)準(zhǔn)化信號(hào)強(qiáng)度百分率。未進(jìn)行轉(zhuǎn)染的細(xì)胞作為對(duì)照組。
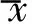
2 結(jié)果
2.1 凝膠阻滯 pDNA條帶的強(qiáng)度隨N/P比的增加而逐漸減弱,當(dāng)N/P比達(dá)3.0時(shí),游離的pDNA條帶完全消失(圖1),裸pDNA為對(duì)照組。提示在N/P比達(dá)3.0時(shí),載體PAI/SPION可以完全負(fù)載pDNA。
2.2 電位和粒徑 PAI/SPION的電位與粒徑分別為(+31.3±2.3)mV、(61.2±6.5)nm。隨著N/P比增加,復(fù)合物PAI/SPION/pDNA的電位逐漸上升,粒徑逐漸下降,在N/P=12時(shí),復(fù)合物電位達(dá)(12.2±1.5)mV;粒徑趨于穩(wěn)定,為(74.8±8.1)nm,見圖2。
2.3MSCS復(fù)合物吸收分析結(jié)果 激光共聚焦顯微鏡下見MSCs形態(tài)大而扁平,與PAI/SPION/pDNA(N/P=12)孵育的MSCs中呈現(xiàn)出高強(qiáng)度的pDNA紅色熒光和PAI/SPION綠色熒光(圖3),表明PAI/SPION/pDNA可被MSCs大量吸收。
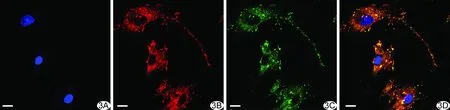
圖3 與N/P=12的復(fù)合物PAI/SPION/pDNA共同孵育MSCs的激光共聚焦圖像 A.MSCs細(xì)胞核呈藍(lán)色熒光; B.pDNA呈紅色熒光;C.PAI/SPION呈綠色熒光; D.復(fù)合圖像呈黃色熒光 (×630;比例尺:50 μm)
2.4MSCs基因轉(zhuǎn)染評(píng)估 N/P比不同,其相應(yīng)的MSCs基因轉(zhuǎn)染效率也不同。在N/P=12時(shí),與PAI/SPION/pDNA共同孵育的MSCs基因轉(zhuǎn)染效率最高,為(71.2±2.3)%。N/P=8、10、14、16時(shí),其轉(zhuǎn)染效率與N/P=12時(shí)比較差異均有統(tǒng)計(jì)學(xué)意義(P均<0.05),見圖4。
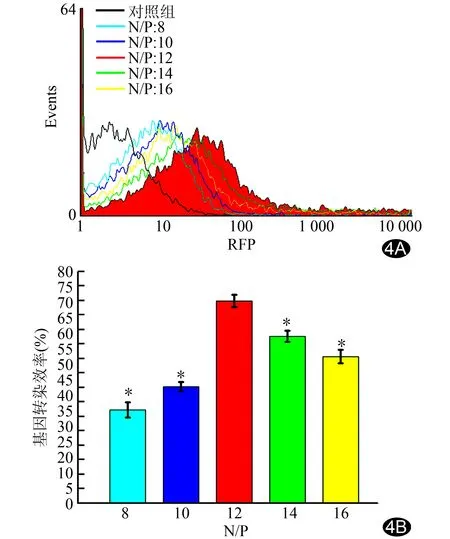
圖4 不同N/P比復(fù)合物PAI/SPION/pDNA對(duì)MSCs的流式分析圖(A)及基因轉(zhuǎn)染效率(B) N/P=12時(shí),MSCs基因轉(zhuǎn)染效率最高,為(71.2±2.3)%(n=3;*:與N/P=12時(shí)復(fù)合物PAI/SPION/pDNA共同孵育MSCs基因轉(zhuǎn)染效率比較,P<0.05)
2.5 MSCs的BLI 在與不同N/P比復(fù)合物共同孵育后,與N/P=12的PAI/SPION/pDNA共同孵育的MSCs生物發(fā)光強(qiáng)度值最高,與其他N/P比組間比較差異均有統(tǒng)計(jì)學(xué)意義(P均<0.05),見圖5,即當(dāng)N/P=12時(shí),PAI/SPION能高效的傳輸pDNA至MSCs內(nèi),并且在MSCs內(nèi)生成豐富的熒光素酶。
2.6 MSCs的MRI 在N/P=12時(shí),MSCs于T2*WI呈現(xiàn)出顯著的陰性成像效果(即變暗征象,圖6A),標(biāo)準(zhǔn)化MR信號(hào)強(qiáng)度值最低,為(37.2±4.1)%,與其他N/P比組間比較差異有統(tǒng)計(jì)學(xué)意義(P<0.05,圖6B)。即N/P=12時(shí),MSCs吸收復(fù)合物PAI/SPION/pDNA的效率最高。
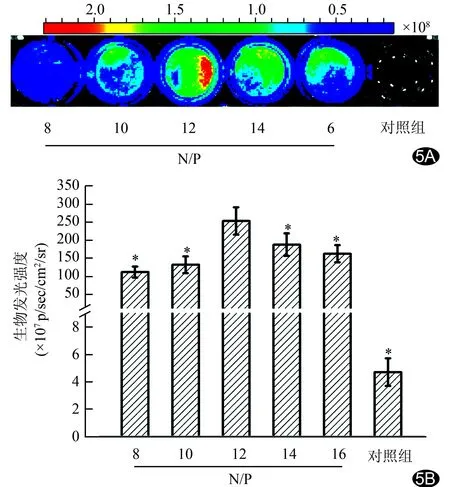
圖5 MSCs的BLI A.與不同N/P比復(fù)合物共同孵育后MSCs的生物發(fā)光圖像; B.與不同N/P比復(fù)合物共同孵育后MSCs生物發(fā)光強(qiáng)度值的定量分析(n=3;*:與N/P=12時(shí)復(fù)合物PAI/SPION/pDNA共同孵育MSCs的生物發(fā)光強(qiáng)度比較,P<0.05)
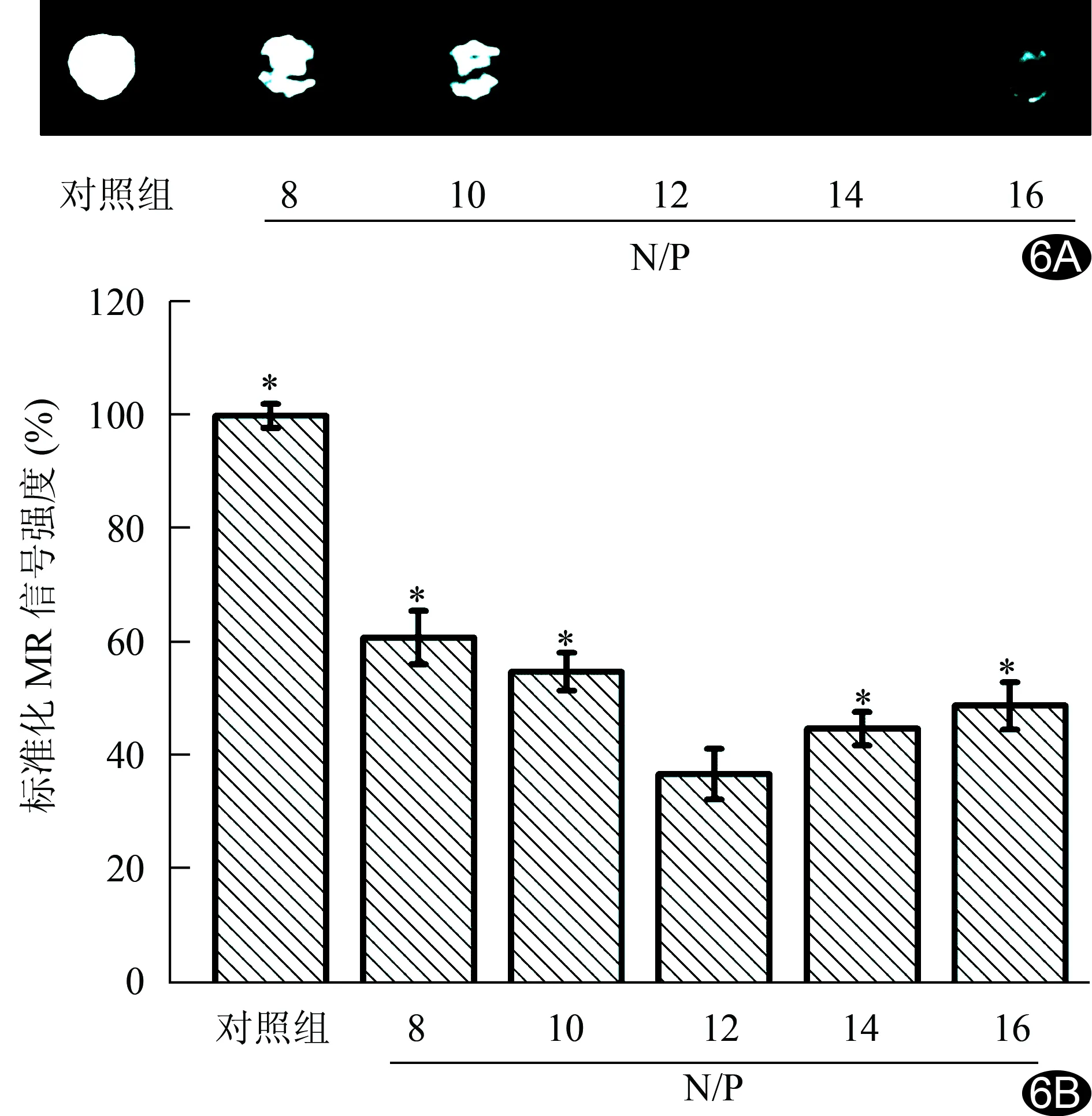
圖6 MSCs的MRI成像 A.與不同N/P比復(fù)合物共同孵育后MSCs的T2*WI圖像; B.與不同N/P比復(fù)合物共同孵育后MSCs的標(biāo)準(zhǔn)化T2*WI信號(hào)強(qiáng)度(n=5;*:與N/P=12的復(fù)合物PAI/SPION/pDNA比較P<0.05;未經(jīng)復(fù)合物轉(zhuǎn)染的MSCs為對(duì)照組)
3 討論
研發(fā)高效、非侵襲性的活體成像技術(shù)示蹤MSCs對(duì)細(xì)胞移植醫(yī)學(xué)的發(fā)展非常重要。本研究合成了新型的MRI可視化非病毒基因傳輸載體PAI/SPION,將兼有紅色熒光蛋白和熒光素酶蛋白報(bào)告基因的質(zhì)粒傳輸至MSCs內(nèi),MSCs被熒光素酶和SPION標(biāo)記,為聯(lián)合生物發(fā)光成像和MRI對(duì)MSCs的雙模態(tài)示蹤提供了可能。
本研究采用瓊脂糖凝膠電泳實(shí)驗(yàn)評(píng)估載體PAI/SPION負(fù)載pDNA的能力。裸pDNA具有負(fù)電荷,可在電場(chǎng)中移動(dòng)。而帶正電荷的載體利用正、負(fù)電荷間的相互作用吸引pDNA,從而限制其在電場(chǎng)中的位移。實(shí)驗(yàn)結(jié)果顯示N/P=3.0時(shí),具有正電荷的載體PAI/SPION可完全中和質(zhì)粒所具有的負(fù)電荷,為PAI/SPION傳輸質(zhì)粒進(jìn)入細(xì)胞提供了基礎(chǔ)。研究[8-9]表明小的粒徑和適當(dāng)?shù)娜蹶栃噪娢挥欣诩?xì)胞對(duì)納米顆粒復(fù)合物的吸收。小粒徑有利于加強(qiáng)細(xì)胞對(duì)復(fù)合物納米顆粒的內(nèi)吞作用,而過高的陽性電位會(huì)導(dǎo)致較高的細(xì)胞毒性[10]。本研究中,當(dāng)N/P=12時(shí),復(fù)合物PAI/SPION/pDNA的粒徑趨向穩(wěn)定,約(74.8±8.1)nm,電位約(12.2±1.5)mV。為選擇復(fù)合物最佳粒徑值和電位值用于細(xì)胞基因轉(zhuǎn)染,本研究進(jìn)一步評(píng)估不同N/P比時(shí)形成的復(fù)合物PAI/SPION/pDNA對(duì)MSCs的基因傳輸能力。筆者從大鼠股骨骨髓內(nèi)成功分離、培養(yǎng)MSCs,在激光共聚焦顯微鏡下,與PAI/SPION/pDNA(N/P=12時(shí))共同孵育的MSCs胞漿內(nèi)呈現(xiàn)出較強(qiáng)的表征PAI/SPION的綠色熒光和表征pDNA的紅色熒光,流式細(xì)胞儀定量分析進(jìn)一步確認(rèn)N/P=12時(shí),PAI/SPION傳輸pDNA至MSCs的效率最高,以上均表明當(dāng)N/P=12時(shí),PAI/SPION/pDNA具備合適的粒徑和電位,可傳輸更多的質(zhì)粒至MSCs。
當(dāng)兼有紅色熒光蛋白和熒光素酶蛋白報(bào)告基因的質(zhì)粒被載體PAI/SPION傳輸至MSCs后,熒光素酶蛋白在細(xì)胞內(nèi)大量表達(dá)。熒光素酶可催化熒光素酶底物產(chǎn)生光子,所產(chǎn)生的光子可被活體成像系統(tǒng)俘獲并進(jìn)行定量分析[11]。生物發(fā)光成像時(shí),當(dāng)N/P=12,與PAI/SPION/pDNA共同孵育的MSCs中生物發(fā)光強(qiáng)度值最高,為活體監(jiān)控移植入體內(nèi)的MSCs的生存、遷移、分布提供了基礎(chǔ)[12]。研究[13]證實(shí)MRI可有效的探測(cè)標(biāo)記磁性可視對(duì)比劑的細(xì)胞,作為最敏感的超順磁性MRI對(duì)比劑,SPION被廣泛用于標(biāo)記MSCs的相關(guān)研究。本研究顯示N/P=12時(shí),與復(fù)合物PAI/SPION/pDNA共同孵育的MSCs T2*WI信號(hào)強(qiáng)度最低,當(dāng)SPION從移植的MSCs內(nèi)排出后,SPION會(huì)被體內(nèi)網(wǎng)狀內(nèi)皮系統(tǒng)選擇性吸收并參與體內(nèi)血紅蛋白的代謝過程[14]。
BLI和MRI均具備無創(chuàng)、可重復(fù)追蹤體內(nèi)移植干細(xì)胞的功能。BLI具有無輻射、高敏感度、可進(jìn)行定量/定性分析并判斷移植細(xì)胞生存狀態(tài)的優(yōu)點(diǎn),但BLI空間分辨率差,且因光子穿透性差而只適用于小動(dòng)物實(shí)驗(yàn)研究;MRI具備良好的空間分辨率,且成像不受組織深度影響,但其判斷移植細(xì)胞生存狀態(tài)的能力相對(duì)較低。
總之,本研究合成的新型載體可將熒光素酶報(bào)告基因和SPION高效轉(zhuǎn)入MSCs,熒光素酶在MSCs內(nèi)大量表達(dá),可利用BLI和MRI雙模態(tài)示蹤MSCs,聯(lián)合兩種成像模式優(yōu)點(diǎn),并且載體PAI/SPION對(duì)MSCs有良好的基因轉(zhuǎn)染效率,在以MSCs為基礎(chǔ)的再生醫(yī)學(xué)和基因治療方面有廣闊應(yīng)用前景。
[1] Jang YO, Kim YJ, Baik SK, et al. Histological improvement following administration of autologous bone marrow-derived mesenchymal stem cells for alcoholic cirrhosis: A pilot study. Liver Int, 2014,34(1):33-41.
[2] 賴麗莎,陳俊偉,朱康順,等.聯(lián)合運(yùn)用骨髓間充質(zhì)干細(xì)胞與促肝細(xì)胞生長(zhǎng)素治療大鼠急性肝衰竭.中國(guó)醫(yī)學(xué)影像技術(shù),2012,28(12):2127-2131.
[3] Li DL, He XH, Zhang SA, et al. Bone marrow-derived mesenchymal stem cells promote hepatic regeneration after partial hepatectomy in rats. Pathobiology, 2013,80(5):228-234.
[4] Seki T, Yokoyama Y, Nagasaki H, et al. Adipose tissue-derived mesenchymal stem cell transplantation promotes hepatic regeneration after hepatic ischemia-reperfusion and subsequent hepatectomy in rats. J Surg Res, 2012,178(1):63-70.
[5] Zhang Y, Cai W, Huang Q, et al. Mesenchymal stem cells alleviate bacteria-induced liver injury in mice by inducing regulatory dendritic cells. Hepatology, 2014,59(2):671-682.
[6] Pang P, Wu C, Gong F, et al. Nanovector for gene transfection and MR imaging of mesenchymal stem cells. J Biomed Nanotechnol, 2015,11(4):644-656.
[7] Chen G, Chen W, Wu Z, et al. MRI-visible polymeric vector bearing CD3 single chain antibody for gene delivery to T cells for immunosuppression. Biomaterials, 2009,30(10):1962-1970.
[8] Green JJ, Chiu E, Leshchiner ES, et al. Electrostatic ligand coatings of nanoparticles enable ligand-specific gene delivery to human primary cells. Nano Lett, 2007,7(4):874-879.
[9] Dai J, Zou S, Pei Y, et al. Polyethylenimine-grafted copolymer of poly (l-lysine) and poly (ethylene glycol) for gene delivery. Biomaterials, 2011,32(6):1694-1705.
[10] Carrabino S, Di Gioia S, Copreni E, et al. Serum albumin enhances polyethylenimine-mediated gene delivery to human respiratory epithelial cells. J Gene Med, 2005,7(12):1555-1564.
[11] 劉靜靜,胡曉俊,李征然,等.Luciferase2/mKate2雙報(bào)告基因?qū)π∈蠊撬栝g充質(zhì)干細(xì)胞的標(biāo)記及活體光學(xué)成像研究.中山大學(xué)學(xué)報(bào)(醫(yī)學(xué)科學(xué)版),2014,35(3):334-339.
[12] 李征然,唐文杰,李丹,等.人永生化骨髓間充質(zhì)干細(xì)胞移植后在肝損傷裸鼠體內(nèi)的活體光學(xué)示蹤.實(shí)用醫(yī)學(xué)雜志,2014,30(10):1552-1555.
[13] Naseroleslami M, Parivar K, Khoei S, et al. Magnetic resonance imaging of human-derived amniotic membrane stem cells using PEGylated superparamagnetic iron oxide nanoparticles. Cell J, 2016,18(3):332-339.
[14] Wang YX, Hussain SM, Krestin GP. Superparamagnetic iron oxide contrast agents: Physicochemical characteristics and applications in MR imaging. Eur Radiol, 2001,11(11):2319-2331.
Application in multimodality tracking of mesenchymal stem cells
WUChun,JIANGZaibo,ZHUKangshun,HUANGMingsheng,GUANShouhai,LIZhengran,QIANJiesheng,LIMing'an,SHANHong*
(DepartmentofRadiology,theThirdAffiliatedHospital,InsituteofInterventionalRadiology,SunYat-senUniversity,Guangzhou510630,China)
Objective To synthesize MRI-visible gene transfer nanocarrier and to assess the gene delivery ability of nanocarrier to mesenchymal stem cells (MSCs) and monitored the MSCs using bioluminescence imaging (BLI) and MRI. Methods The terpolymer nanocarrier poly (ethylene glycol)-block-poly (L-aspartic acid)-grafted polyethylenimine functionalized with superparamagnetic iron oxide nanoparticles (PAI/SPION) was synthesized. The degree of binding between PAI/SPION and pDNA was determined with agarose gel electrophoresis. The Zeta potential and particle size of polymer vectors were measured with a Zeta-Plus instrument. MSCs were isolated and cultured from the femurs of the rats. The gene transfection efficiency of PAI/SPION/pDNA to MSCs was evaluated by flow cytometry and laser confocal microcopy. And the BLI and MRI were combined to monitor MSCs. Results PAI/SPION vectors were synthesized successfully. PAI/SPION could condense pDNA entirely at a nitrogen of non-viral vector/phosphorus of plasmid (N/P) ratio of 3.0. The particle size of PAI/SPION/pDNA attained a constant size of (74.8±8.1)nm at a N/P ratio of 12, and the Zeta potential reached (12.2±1.5)mV, the transfection efficiency of PAI/SPION/pDNA to MSCs was (71.2±2.3)%. The MSCs showed significantly stronger PAI/SPION (green) and pDNA (red) fluorescence under the laser confocal microcopy, the bioluminescence light intensity of the MSCs attained the highest values and the normalized MR T2*WI signal intensity attained the lowest values. Conclusion The study successfully synthesizes an MRI-visible non-viral gene vector PAI/SPION, which possesses a higher transfection efficiency in transferring pDNA into MSCs and can dually monitor the MSCs using BLI and MRI.
Mesenchymal stromal cells; Genes; Bioluminescence; Magnetic resonance imaging
廣東省自然科學(xué)基金博士啟動(dòng)項(xiàng)目(2015A030310171)。
吳春(1975—),男,河南鄭州人,博士,主治醫(yī)師。研究方向:分子影像學(xué)。E-mail: chunwu@aliyun.com
單鴻,中山大學(xué)附屬第三醫(yī)院放射科 介入放射學(xué)研究所,510630。E-mail: shanhong@mail.sysu.edu.cn
2016-07-14
2016-10-12
實(shí)驗(yàn)研究
10.13929/j.1003-3289.201607066
R329.2; R445.2
A
1003-3289(2017)02-0171-06

