誤診為腦內(nèi)炎性肉芽腫的多形性黃色星形細(xì)胞瘤1例報(bào)道及文獻(xiàn)復(fù)習(xí)
李文森,李劍劍,洪新雨,關(guān) 毅
(吉林大學(xué)第一醫(yī)院 神經(jīng)腫瘤外科,吉林 長(zhǎng)春130021)
*通訊作者
誤診為腦內(nèi)炎性肉芽腫的多形性黃色星形細(xì)胞瘤1例報(bào)道及文獻(xiàn)復(fù)習(xí)
李文森,李劍劍,洪新雨,關(guān) 毅*
(吉林大學(xué)第一醫(yī)院 神經(jīng)腫瘤外科,吉林 長(zhǎng)春130021)
多形性黃色星形細(xì)胞瘤(pleomorphic xanthoastrocytoma,PXA)是一種非常少見(jiàn)的顱內(nèi)原發(fā)腫瘤,發(fā)生率占星形細(xì)胞瘤1%左右,以往觀點(diǎn)認(rèn)為PXA是趨于良性的腫瘤,手術(shù)全切預(yù)后較好[1,2]。近年來(lái)研究發(fā)現(xiàn),部分PXA術(shù)后具有復(fù)發(fā)、轉(zhuǎn)移、間變等惡性組織學(xué)特點(diǎn),因此2007年WHO將PXA定為Ⅱ級(jí),將伴有間變特征的PXA定為Ⅲ級(jí)[3]。由于PXA發(fā)生率較低,對(duì)于其臨床特點(diǎn)和影像學(xué)了解不多,臨床上常將其誤診為血管網(wǎng)狀細(xì)胞瘤、腦膜瘤等其它腫瘤[4],因此盡快提高對(duì)PXA認(rèn)識(shí),早期診斷治療,對(duì)患者預(yù)后起著至關(guān)重要的作用。日前我們收治1例青年男性病人,長(zhǎng)期被診斷為“腦內(nèi)炎性肉芽腫”,術(shù)后病理證實(shí)為PXA(Ⅱ級(jí)),現(xiàn)結(jié)合國(guó)內(nèi)外文獻(xiàn)對(duì)PXA的臨床特點(diǎn)和容易誤診的原因進(jìn)行分析。
1 臨床資料
患者22歲,男性。2008年因癲癇大發(fā)作,行頭部MRI檢查見(jiàn)右頂葉稍長(zhǎng)T1長(zhǎng)T2信號(hào)影,FLAIR呈稍高信號(hào)影,邊界清楚,病灶呈不均勻強(qiáng)化,直徑約0.5 cm,周圍水腫不明顯,中線結(jié)構(gòu)無(wú)移位。發(fā)病后在北京和長(zhǎng)春多家三甲醫(yī)院均診斷為“腦內(nèi)炎性肉芽腫”,建議抗炎和抗癲癇治療(具體不詳)。近7年未規(guī)律服用抗癲癇和抗炎藥物。每年癲癇大發(fā)作3至4次,于2015年4月來(lái)我院就診,考慮腦內(nèi)炎性肉芽腫可能性大,建議頭孢吡肟1.0 g/次,每日2次靜點(diǎn),規(guī)范抗炎治療2個(gè)月后復(fù)查頭MRI,病灶未縮小(圖1),決定行手術(shù)治療。病程中無(wú)明顯感染病史。查體和化驗(yàn)檢查無(wú)陽(yáng)性表現(xiàn)。入院后行24小時(shí)視頻腦電圖監(jiān)測(cè)提示腦內(nèi)考慮多發(fā)癲癇灶,給予德巴金1 000 mg/日口服。
入院后在神經(jīng)導(dǎo)航下行手術(shù)治療,術(shù)中見(jiàn)腫瘤呈灰白色、實(shí)性、質(zhì)軟,邊界清楚。術(shù)中行皮層腦電監(jiān)測(cè),確認(rèn)病變周邊存在癲癇波,顯微鏡下將病變?nèi)壳谐T俅涡行g(shù)中皮層腦電監(jiān)測(cè),約10分鐘后癲癇波逐漸消退。術(shù)后給予抗炎、抗癲癇等對(duì)癥治療。
術(shù)后病理回報(bào):右側(cè)頂葉多形性黃色星形細(xì)胞瘤(PXA),WHO分級(jí):II級(jí)。免疫組化結(jié)果:GFAP(+),S-100(+),CD34(部分+),Ki-67(+2%)。
術(shù)后14個(gè)月復(fù)查頭部MRI,未見(jiàn)腫瘤復(fù)發(fā);24小時(shí)視頻腦電監(jiān)測(cè)示仍有癲癇波存在,德巴金用量同術(shù)前,術(shù)后病人未有癲癇發(fā)作,癲癇得到有效控制。
2 討論
PXA由Kepes等人發(fā)現(xiàn)并認(rèn)為腫瘤是起源于腦表軟膜下星形細(xì)胞的一種特殊類型的星形細(xì)胞瘤,于1979年正式命名為多形性黃色星形細(xì)胞瘤[1]。PXA最初被認(rèn)為是趨于良性腫瘤,手術(shù)全切效果好,長(zhǎng)期生存率較高,九十年代初WHO曾將其定為Ⅰ級(jí)。近十余年,研究發(fā)現(xiàn)部分腫瘤術(shù)后可復(fù)發(fā),具有侵襲、轉(zhuǎn)移等特點(diǎn),甚至可轉(zhuǎn)化為膠質(zhì)母細(xì)胞瘤,放化療效果不佳,最終2007年WHO將它定為Ⅱ級(jí)(PXA)和Ⅲ級(jí)(間變性PXA)。這改變了我們對(duì)PXA的認(rèn)識(shí),并逐漸引起人們的重視。而其影像學(xué)特點(diǎn),在臨床上常常容易被誤診為其它顱內(nèi)腫瘤。
發(fā)病年齡和部位 據(jù)報(bào)道,PXA主要好發(fā)于兒童和青少年,發(fā)病平均年齡26歲左右,男女無(wú)明顯性別差異[5]。PXA大多為單發(fā),可能由于腫瘤起源于軟膜下星形細(xì)胞,因此大多數(shù)腫瘤部位表淺,其中近半數(shù)發(fā)生在顳葉[2],其次發(fā)生在頂葉、枕葉等部位,發(fā)生于小腦半球、松體果區(qū)、脊髓等處少見(jiàn)[6]。
臨床特征和MRI影像學(xué)表現(xiàn) 大部分病人發(fā)病緩慢,病程較長(zhǎng),提示該病趨于良性。可能與PXA發(fā)生于腦表軟膜下和顳葉有關(guān),絕大數(shù)病人主要癥狀表現(xiàn)為反復(fù)發(fā)作性癲癇,部分病人即使手術(shù)切除腫瘤,癲癇也很難有效控制。隨著腫瘤大小、部位不同,還可表現(xiàn)為高顱壓和其他局灶性神經(jīng)癥狀。
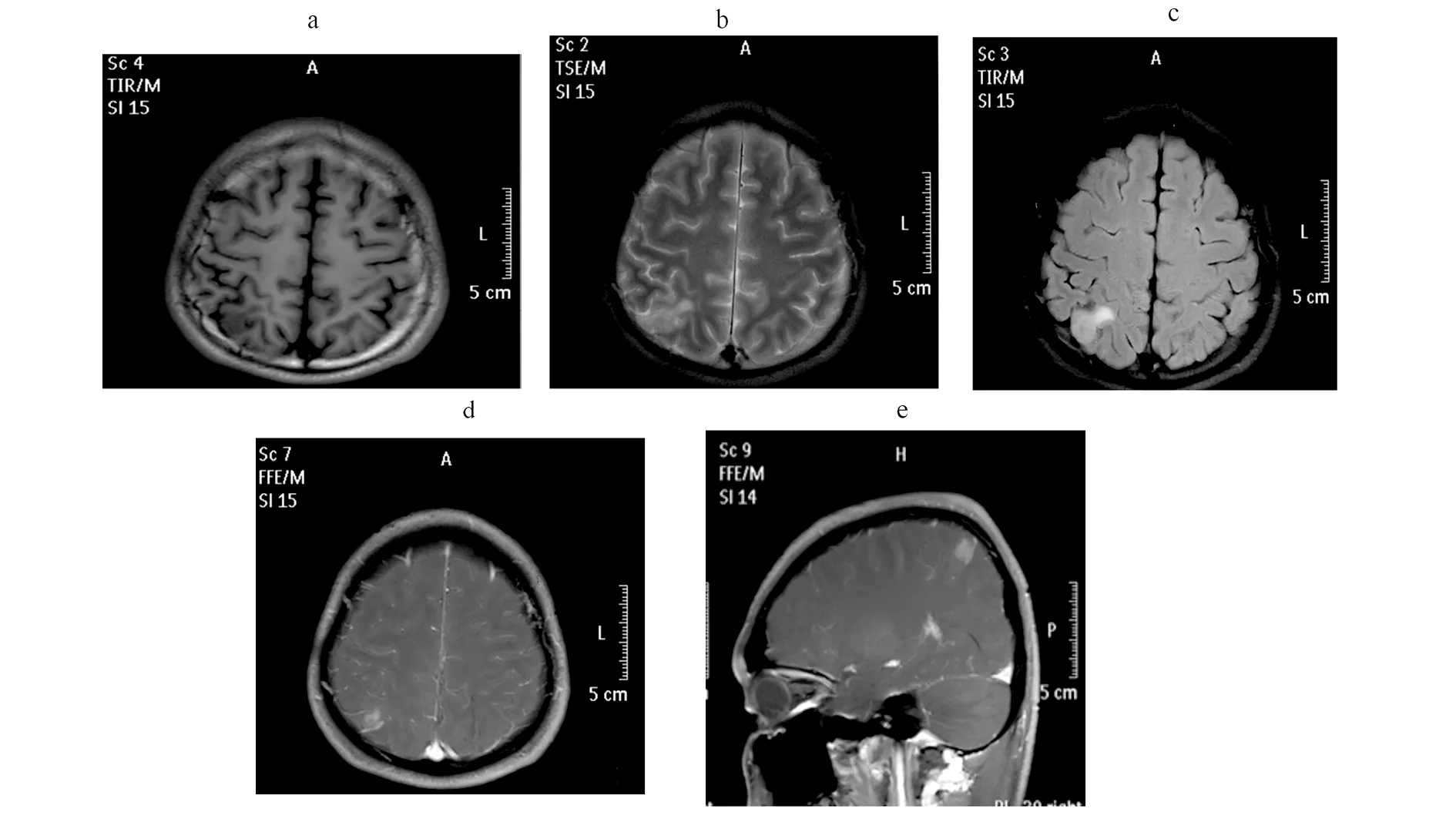
右頂葉腦表見(jiàn)稍長(zhǎng)T1長(zhǎng)T2信號(hào)影(a,b),FLAIR呈稍高信號(hào)影(c),邊界清,病灶明顯強(qiáng)化,直徑約0.5 cm,周圍水腫不明顯(d,e)。
2011年Yu等人將PXA分為三型,即實(shí)性型、大囊伴壁結(jié)節(jié)型和囊實(shí)混合型[7]。實(shí)性型指病變表現(xiàn)為實(shí)性結(jié)節(jié),伴或不伴囊腔,實(shí)性部分占病變總體積50%以上。MRI平掃病變邊界較清,腫瘤實(shí)性部分和壁結(jié)節(jié)T1W1呈等信號(hào)或稍低信號(hào)影,T2W1呈等信號(hào)或稍高信號(hào)影;囊壁T1W1和T2W1均為等信號(hào);囊性部分T1W1為低信號(hào),T2W1為高信號(hào)。實(shí)性部分和壁結(jié)節(jié)呈不均勻強(qiáng)化,囊壁強(qiáng)化不明顯或不強(qiáng)化,病變周邊多為輕度水腫[8]。有的腫瘤伴有腦膜強(qiáng)化,易于腦膜瘤相混淆[3]。國(guó)內(nèi)學(xué)者也有利用磁共振波譜成像(MRS),對(duì)PXA病變進(jìn)行檢查的報(bào)道,Cho/NAA比值<2,提示腫瘤趨于良性病變,目前國(guó)內(nèi)外資料較少,還有待進(jìn)一步研究,未來(lái)MRS對(duì)鑒別PXA良惡性程度應(yīng)有較大幫助[9]。
病理學(xué)和免疫組化表現(xiàn) 病理組織鏡下見(jiàn)多核巨細(xì)胞、梭形細(xì)胞、肥胖細(xì)胞和泡沫樣細(xì)胞混合組成。伴有星形細(xì)胞增生和血管周圍淋巴細(xì)胞浸潤(rùn),細(xì)胞間充滿豐富的網(wǎng)狀纖維,核分裂像無(wú)或少,定義為WHO Ⅱ級(jí)。當(dāng)腫瘤細(xì)胞核分裂像≥5個(gè)/10HP或/和伴有細(xì)胞壞死、明顯的細(xì)胞間變時(shí),定義為間變性PXA(Ⅲ級(jí))[10]。
幾乎全部PXA免疫組化染色神經(jīng)膠質(zhì)纖維酸性蛋白(GFAP)呈陽(yáng)性,證明其來(lái)源于星形細(xì)胞,這也是最具特征性組織學(xué)表現(xiàn)。GFAP陽(yáng)性是重要診斷依據(jù)之一,并有助于與其他腫瘤相鑒別。其次CD34表達(dá)與PXA惡性程度有關(guān),在良性PXA標(biāo)本中CD34陽(yáng)性率高達(dá)84%,而在間變性PXA中CD34陽(yáng)性率僅為44%,因此CD34可初步鑒別良性和間變性PXA,S-100被證明也與本病高度相關(guān)[11]。
治療 治療以手術(shù)為主,腫瘤全切預(yù)后較好。研究發(fā)現(xiàn),腫瘤全切的患者中有85%生存期超過(guò)15年,大部分切除者則只有50%生存期超過(guò)15年[6]。另外Giannini等人對(duì)71例PXA病例研究證實(shí),腫瘤全切的病人長(zhǎng)期生存率較高,5年生存率為81%,10年生存率為70%;5年無(wú)復(fù)發(fā)生存率為72%,10年無(wú)復(fù)發(fā)生存率可達(dá)61%,且腫瘤切除范圍與無(wú)復(fù)發(fā)生存率有直接關(guān)系[2]。
研究表明,有15% -20%PXA可復(fù)發(fā)或間變,具有高度侵襲性,甚至可轉(zhuǎn)變?yōu)槟z質(zhì)母細(xì)胞瘤[10,12]。最新研究發(fā)現(xiàn),在組織學(xué)、免疫組化、分子和臨床特征方面,上皮樣膠質(zhì)母細(xì)胞瘤和PXA密切相關(guān)或他們實(shí)為同一類型腫瘤,這也許可以解釋部分PXA具有復(fù)發(fā)、轉(zhuǎn)移等生物學(xué)行為[13]。復(fù)發(fā)不伴有轉(zhuǎn)移者,仍建議積極手術(shù)治療;復(fù)發(fā)伴有轉(zhuǎn)移者,特別是伴有廣泛轉(zhuǎn)移灶者,則治療非常棘手,手術(shù)很難將這些病灶完全切除。PXA術(shù)后是否需要放化療、目前還存在爭(zhēng)議。Koga等對(duì)一例播散性PXA病人采取立體定向放射治療,患者生存期延長(zhǎng)至66個(gè)月[10]。Lubansu等對(duì)一例復(fù)發(fā)伴有轉(zhuǎn)移的患者,采用硫替派、卡鉑和替莫唑胺聯(lián)合化療,26個(gè)月后復(fù)查病灶無(wú)明顯進(jìn)展[14]。截止目前,雖然個(gè)別病例取得了較好的治療效果,整體來(lái)說(shuō)復(fù)發(fā)特別是伴有轉(zhuǎn)移病灶的病人,放化療效果并不確切,多數(shù)預(yù)后不良。
由于PXA較特殊的臨床和影像學(xué)表現(xiàn),同時(shí)發(fā)病率低,很容易被誤診為其他腫瘤。PXA術(shù)前多被診斷為胚胎發(fā)育不良性腫瘤、血管網(wǎng)狀細(xì)胞瘤等腫瘤,甚至個(gè)別PXA位置表淺,伴有腦膜尾征而被診斷為腦膜瘤[3]。
本病例術(shù)前長(zhǎng)達(dá)數(shù)年,被多家大醫(yī)院均診斷為“腦內(nèi)炎性肉芽腫”。腦內(nèi)炎性肉芽腫,多為隱匿性感染局限后,局部炎性組織包裹,膠質(zhì)纖維增生而形成境界明顯的結(jié)節(jié)狀病灶。臨床上直徑2 cm以下微型肉芽腫主要為細(xì)菌性,個(gè)別為寄生蟲性或結(jié)核性。癲癇為主要癥狀,MRI掃描呈長(zhǎng)T1、長(zhǎng)T2信號(hào),病灶邊界清楚,強(qiáng)化明顯,形狀多為類圓形。治療以抗炎、抗癲癇治療為主,治療后病變不消退、癲癇難以控制者,考慮手術(shù)治療。
我們反思本病例誤診原因,總結(jié)出以下幾條經(jīng)驗(yàn):①腦內(nèi)炎性肉芽腫即使抗炎治療無(wú)效,也不要輕易考慮病變?yōu)榻Y(jié)核性或寄生蟲性肉芽腫,應(yīng)高度懷疑可能為腫瘤,特別是PXA的可能;②特別是病變位于腦表軟膜下的考慮為腦內(nèi)炎性肉芽腫的病人,規(guī)律抗炎治療后病變無(wú)明顯消退者,應(yīng)盡快手術(shù)治療,盡早明確病理,以免延誤治療時(shí)機(jī)。目前實(shí)性PXA術(shù)前誤診為腦內(nèi)炎性肉芽腫的病例國(guó)內(nèi)外還未見(jiàn)報(bào)道。雖然研究表明實(shí)性PXA較其他兩型PXA具有惡性程度低、預(yù)后好等特點(diǎn),但不積極手術(shù)治療,實(shí)性PXA有進(jìn)一步發(fā)展為惡性、間變PXA的可能[5]。因此充分了解、認(rèn)識(shí)和重視本病,在臨床工作中具有重要意義。
綜上所述,PXA總體來(lái)說(shuō)是趨于良性腫瘤,手術(shù)全切預(yù)后好,但近年來(lái)隨著病例報(bào)道逐漸增多,發(fā)現(xiàn)有15% -20% PXA可復(fù)發(fā)或間變,治療效果不佳,預(yù)后差。實(shí)際臨床工作中,PXA常常被誤診為其它腫瘤或病變,需引起高度重視。結(jié)合臨床和影像學(xué)特點(diǎn),對(duì)高度懷疑PXA的病人,盡早手術(shù)治療,明確病理,以免延誤最佳治療時(shí)機(jī)。
[1]Kepes JJ,Rubinstein LJ,Eng LF.Pleomorphic xanthoastrocytoma:A distinctive meningocerebral glioma of young subjects with relatively favorable prognosis.A study of 12 cases[J].Cancer,1979,44(5):1839.
[2]Giannini C,Scheithauer BW,Butget PC,et al.Pleomorphic xanthoastrocytoma:What do we really know about it?[J].Cancer,1999,85(9):2033.
[3]Louis DN,Ohgaki H,Wiestler OD,et al.The 2007 WHO Classificationof Tumours of the Central Nervous System[J].Acta Neuropathol,2007,114 (2):97.
[4]徐 露,成官迅,李學(xué)農(nóng).顱內(nèi)多形性黃色星形細(xì)胞瘤的MRI表現(xiàn)及誤診分析[J].中國(guó)醫(yī)學(xué)影像技術(shù),2015,31(2):201.
[5]韋程綱,譚潔瑩,劉國(guó)順,等.非典型多形性黃色星形細(xì)胞瘤的MRI及病理表現(xiàn)[J].放射學(xué)實(shí)踐,2015,30(1):21.
[6]沈 軍,程宏偉.多形性黃色星形細(xì)胞瘤的臨床研究進(jìn)展[J].國(guó)際神經(jīng)病學(xué)神經(jīng)外科學(xué)雜志,2011,38(3):245.
[7]Yu S,He L,Zhuang X,et al.Pleomorphic xanthoastrocytoma:MR imaging findings in 19 patients[J].Acta Radiol,2011,52(2):223.
[8]韋程綱,龔艷媚,劉國(guó)順,等.23例腦部多形性黃色星形細(xì)胞瘤的MRI分型對(duì)比研究[J].臨床放射學(xué)雜志,2015,34(2):173.
[9]張 蕊,彭曉剛,崔麗華,等.磁共振在多形性黃色星形細(xì)胞瘤診斷中的價(jià)值[J].腫瘤學(xué)雜志,2015,21 (2):157.
[10]Koga T,Morita A,Maruyama K,et a1.Long-tetm control of disseminated pleomorphic xanthoastrocytoma with anaplastic features by means of stereotactic irradiation[J].Neuro Oncol,2009,11(4):446.
[11]Matsumoto K,Suzuki SO,Fukui M,et a1.Accumulation of MDM2 in pleomorphic xanthoastrocytomas[J].Pathol Int,2004,54(6):387.
[12]Perry A,Giannini C,Scheithauer BW,et al.Composite pleomorphic xanthoastrocytoma and ganglioglioma:report of four cases and review of the literature[J].Am J Surg Pathol,1997,21(7):763.
[13]Alexandrescu S,Korshunov A,Lai SH,et al.Epithelioid glioblastomas and anaplastic epithelioid pleomorphic xanthoastrocytomas-same entity or first cousins?[J].Brain Pathol,2016,26(2):215.
[14]Lubansu A,Rorive S,David P,et al.Cerebral anaplastic pleomorphic xanthoastrocytoma with meningeal dissemination at first presentation[J].Childs Nerv Syst,2004,20(2):119.
1007-4287(2017)03-0529-03
2016-09-17)

